准东煤中钠高温形态的化学动力学模拟
2017-10-17季杰强程乐鸣刘炎泉王勤辉骆仲泱
季杰强, 程乐鸣, 刘炎泉, 王勤辉, 骆仲泱
(浙江大学 热能工程研究所,能源清洁利用国家重点实验室,杭州 310027)
准东煤中钠高温形态的化学动力学模拟
季杰强, 程乐鸣, 刘炎泉, 王勤辉, 骆仲泱
(浙江大学 热能工程研究所,能源清洁利用国家重点实验室,杭州 310027)
采用化学动力学软件Chemkin对碱金属含量高的准东煤在燃烧过程中气相钠的高温形态分布进行模拟计算,将模型计算结果与文献中的试验结果进行对比,研究了温度、过量空气系数α和压力对碱金属钠在高温下形态分布的影响,并对含钠气相产物进行了敏感性分析. 结果表明:计算结果与试验结果一致,验证了该模型的正确性;温度对含钠气相产物的转化有很大影响;当α<1时,含钠气相产物的组分分布受α的影响较大;压力对含钠气相产物物质的量分数的影响较小.
准东煤; 钠形态; 化学动力学; 敏感性; 模拟
Abstract: Chemical kinetics software Chemkin was applied to perform analog calculation on morphology distribution of gas-phase sodium at high temperatures in Zhundong coal with high alkali content during combustion process, and the calculation results were subsequently compared with reference data, so as to study the effects of following factors on the distribution of high-temperature morphology of alkali sodium, such as the temperature, excess air coefficient (α) and pressure, etc., and to analyze the sensitivity of relevant products. Results show that the calculation results agree well with actual measurements, proving the model to be correct; temperature significantly influences the conversion of sodium-containing gas-phase products; the component distribution of sodium-containing gas-phase products is remarkably influenced byαin the case ofα<1, which is slightly influenced by pressure.
Key words: Zhundong coal; sodium morphology; chemical kinetics; sensitivity; simulation
准东煤田发现于2005年,其蕴含的煤炭资源非常丰富,预测储量可达3.9×1011t[1],占新疆煤炭储量(2.19×1012t)的17%~18%,占全国煤炭储量(5×1012~6×1012t)的7%~8%. 准东煤的煤质较好,水分和挥发分含量较高,灰分和硫含量较低,应用前景非常广阔. 然而研究表明,准东煤中钠、钾等碱金属含量偏高,国内传统用煤中钠的质量分数一般在1%~2%(以灰分计),而准东煤中钠的质量分数一般在5%以上(以灰分计).燃用含高碱金属和碱土金属的煤会出现结渣、沾污、积灰和腐蚀等各种问题,严重影响锅炉的正常运行. Wang等[2]认为准东煤在燃烧过程中析出的碱金属和碱土金属化合物(NaCl、Na2SO4、CaSO4和K2SO4)[3]先在受热面附近沉积,随后部分硅铝酸盐被初始沉积层捕获,这是沾污形成的主要原因. 因此,研究准东煤这类典型的高钠煤中气相碱金属的析出规律及高温形态分布具有重要意义.
由于气相碱金属在线测量比较困难,因此针对气相碱金属在高温下形态分布的试验研究很少. Bläsing等[4]采用分子束质谱仪对烟气进行在线测量后发现,58NaCl+的析出量与硫、氯元素的质量比呈负相关,同时也与铝和硅的总含量呈负相关. Bläsing等[5]研究了水蒸气对煤气化过程中碱金属等无机物析出的影响,发现加入水蒸气将导致23Na+、39K+/39NaO+、56KOH+、58NaCl+和74KCl+的释放量增加. Oleschko等[6]采用分子束质谱仪分析了6种无烟煤在燃烧过程中气相碱金属的释放情况,结果表明随着温度从800 ℃升至1 200 ℃,NaCl的释放量减少,KCl的释放量增加;增大压力导致NaCl的释放量减少. 然而,上述试验研究还存在一些不足:(1)具有相同质荷比的物质无法区分,如40NaOH+与40Ar+、39K+与39NaO+;(2)含量较低的碱金属化合物信号易受环境噪音影响而难以测定,如142Na2SO4+等.这些都会影响测量结果的准确性,因此通常需要结合模拟结果对碱金属高温形态的变化规律进行完善.
谭力[7]采用FactSage研究了稻草秸秆燃烧过程中燃烧温度、炉内压力、过量空气系数、燃料中的硫元素含量和氯元素含量等因素对碱金属迁移的影响. 陈安和等[8]采用FactSage计算了秸秆、树皮、木屑、废木和橄榄渣5种生物质在热解条件下氯及碱金属元素的分布和迁移特性. Wei等[9]采用FactSage研究了过量空气系数和压力对秸秆燃烧过程中氯及碱金属释放行为的影响. 目前,热力学计算均基于以下前提:(1)不研究过程的速率,即忽略停留时间这个因素;(2)仅研究系统的平衡状态,忽略反应机理. 对于炉内燃烧或气化过程,停留时间对碱金属析出的影响很大. 另外,由于炉内复杂的物理化学反应,系统难以达到或者维持在平衡状态,因此热力学计算存在一定的局限性. 化学动力学研究的是化学过程的速率及化学反应机理,可有效弥补热力学计算的不足,更接近炉内真实状况. 但目前的资料显示,几乎没有应用化学动力学研究气相碱金属在高温下分布的相关报道.虽然Takuwa等[10]基于Chemkin软件模拟了在H2、O2和NaOH混合系统中燃烧时含钠气相产物的转化过程,但并未考虑HCl及SO2的影响. 化学动力学是研究化学反应机理的有效途径,针对准东煤燃烧过程中气相碱金属的高温形态分布,笔者采用化学动力学软件Chemkin Pro计算并分析了温度、压力及过量空气系数对含钠气相产物的影响,通过分析各基元反应了解反应产物随各影响因素变化的原因.
1 气相化学组分的化学动力学模型
1.1 煤样参数
以含高碱金属的准东煤为计算对象,其工业分析、元素分析及灰分分析如表1和表2所示,其中氯元素质量分数的测定采用GB/T 3558—1996 《煤中氯的测定方法》.
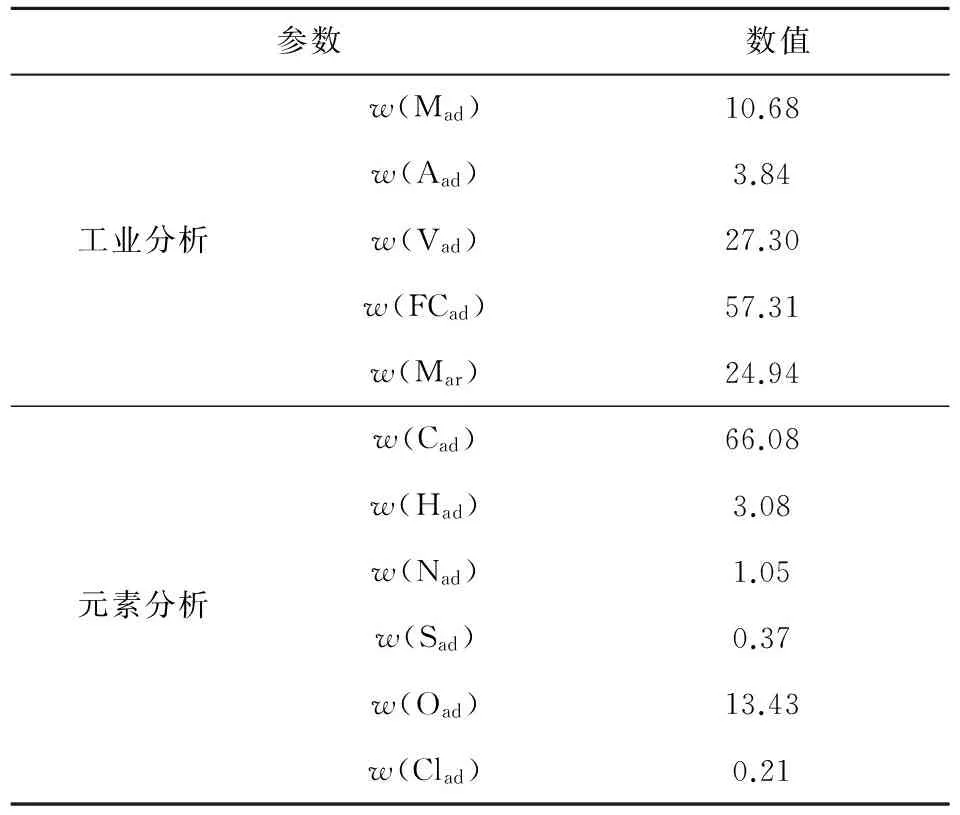
表1 准东煤的工业分析和元素分析

表2 准东煤灰分分析
1.2 化学动力学模型
基元反应的速率常数k为依赖于温度的Arrehenius形式:
k=A·Tβexp[-E/(RT)]
(1)
式中:k为速率常数,s-1;A为指前因子;T为温度,K;β为指数;E为活化能,J/mol;R为气体常数,取8.314 J/(mol·K).
计算模型选用PSR(Perfect stirred reactor),即物料以稳定的流量进入反应器后,瞬间就在整个反应器内分散均匀并与反应器内原存留的物料完全混合,因此反应物转化为生成物的速率由化学反应速率控制,而不是由混合过程控制.
基于涉及C、H、O、N元素的GADM98详细化学反应机理[11],同时考虑了Glarborg等[12-13]提出的S、Cl、K、Na元素的详细化学反应机理,建立了Na高温形态分布的化学动力学模型.该模型涉及的主要元素和化合物如表3所示,模型中考虑了139步反应. 计算中使用的热力学数据来自于Chemkin自带的therm.dat文件、NIST(National Institute of Standards and Technology)数据库和NASA(National Aeronautics and Space Administration)发表的热力学数据[14].

表3 化学动力学模型中包含的组分
1.3 参数设置
根据表1和表2中准东煤的分析数据,初始组分分2部分输入计算,C、H、O、N、S元素折算为理论烟气含量输入,Cl、K、Na元素按以下形式输入计算.
煤中的钠以4种形态存在:无机钠、羧酸盐形式的有机钠、配位形式的有机钠和不可溶钠[15]. 在该煤样中,上述4种钠的质量分数依次为61%、11%、4%和24%[16]. 刘大海等[15]认为以NaCl晶体和水合离子形式存在的无机钠都以NaCl的形式释放,有机钠以钠原子的形式释放,而不可溶钠在加热过程中不挥发,故钠元素以NaCl(61%w(Natotal))和钠原子(15%w(Natotal))的形式输入. 煤中的钾也以4种形态存在,其中水溶性钾、醋酸铵溶钾、盐酸溶钾和不可溶钾的质量分数依次为29%、8%、5%和58%[16],钾的析出形式与钠相似[17],故钾元素以KCl(29%w(Ktotal))和钾原子(13%w(Ktotal))的形式输入. 对于氯,除了以碱金属氯化物的形式析出外,还会以HCl的形式析出[18].可通过NaCl和KCl的含量来确定与碱金属结合的氯含量(NaCl:43.0%w(Cltotal);KCl:1.6%w(Cltotal)),剩余的即为以HCl(55.4%w(Cltotal))形态存在的氯,故氯有NaCl、KCl和HCl 3部分输入.
此外,该模型中未将硅、铝、钙等包括在内.虽然这些元素对气相碱金属的析出有一定影响,但该化学动力学计算主要研究的是气相碱金属与不同化合物间的相互转化,且含硅、铝、钙矿物对碱金属吸附的化学动力学机理尚不明确,因此该模型暂时不考虑以上几种元素. 计算中变量的控制如表4所示.

表4 计算中的参数设置
1.4 敏感性分析
敏感性分析是一种能够深入直观地分析组分、基元反应和反应条件等因素对系统反应参数敏感程度的方法. 总体敏感性分析用于机理简化,局部敏感性分析用于研究详细机理的化学动力学特性. 局部敏感性分析的正交表达式[19]如下:

(2)


2 结果及讨论
2.1 Chemkin计算结果与试验结果对比
由于气相碱金属在线测量比较困难,故研究者大多给出了气相碱金属的定性或半定量分析.在与Dleschko等[6]试验条件相同工况下(T=1 473 K,压力p=100 kPa、300 kPa和900 kPa)进行Chemkin计算.为了验证该模型的可靠性,将模型计算结果与试验结果进行对比,如图1所示,其中左边纵坐标为计算所得产物的物质的量分数,右边纵坐标为质谱仪得出的峰面积数据,其数值大小与产物的物质的量分数成正比. 由图1可知,随着压力升高,NaCl、HCl和SO2的物质的量分数都减少,计算结果与试验结果相符,验证了该模型的正确性.
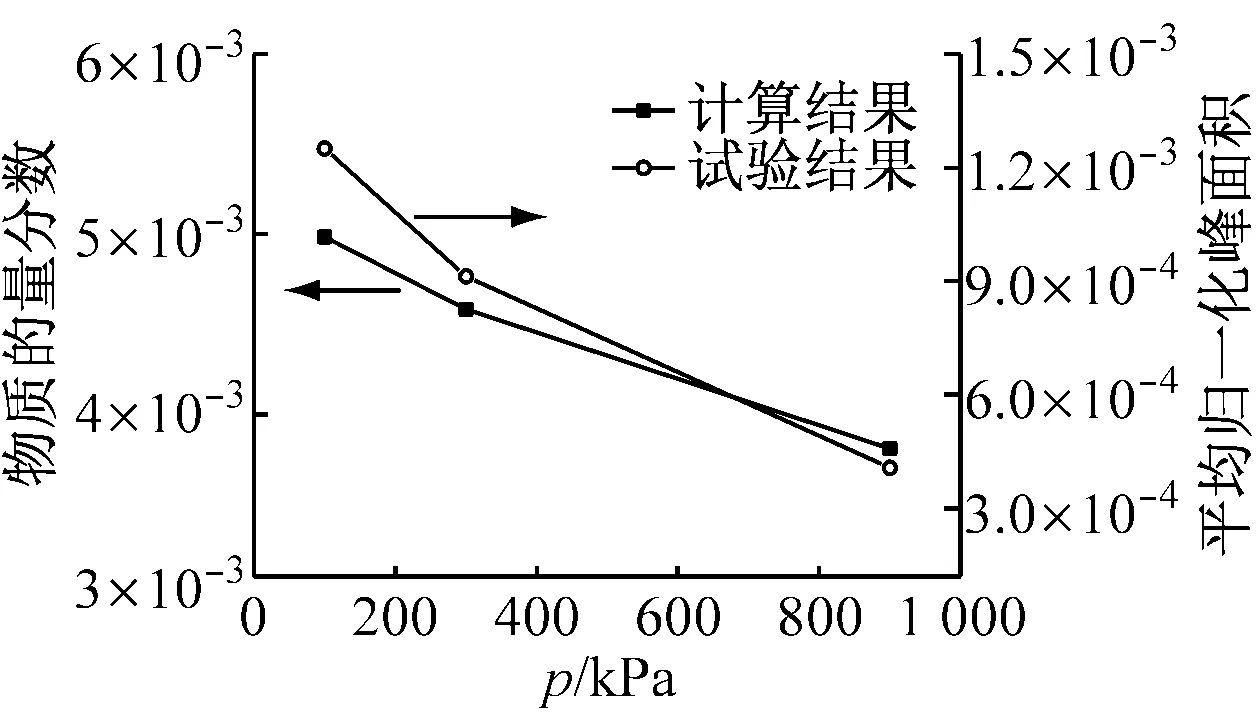
(a) NaCl
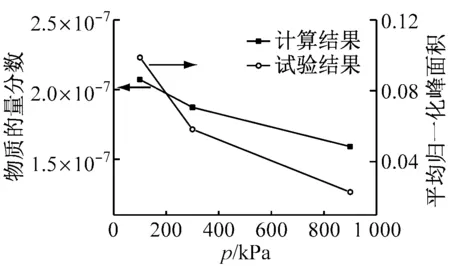
(b) HCl

(c) SO2
2.2 含钠气相产物的物质的量分数与停留时间的关系
图2给出了含钠气相产物的物质的量分数随停留时间(t)的变化,图中列出了主要的反应产物,忽略了低物质的量分数的产物,如NaOH和Na2SO4等. 由图 2可知,反应初期NaCl(g)的物质的量分数约为60%,其他几种钠化合物的物质的量分数很少,这与初始加入的组分有关;随着停留时间延长,NaCl(g)的物质的量分数继续增加,成为主要的产物;当停留时间达到10-3s时,各产物的物质的量分数基本保持不变,在此状态下钠主要以NaCl(g)形态存在,其物质的量分数约为70%.
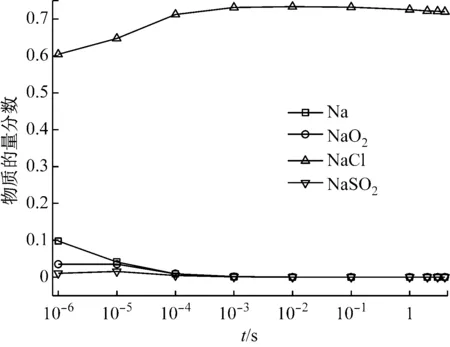
图2 含钠气相产物的物质的量分数随停留时间的变化
由此可见,在给定的烟气流量下,反应进行10-3s以后,各产物物质的量分数基本处于稳定值,可以认为停留时间达到10-3s后,反应达到了平衡.
2.3 含钠气相产物的物质的量分数与温度的关系
图3给出了含钠气相产物的物质的量分数随温度的变化.由图3可知,各产物的物质的量分数随温度的变化主要经历以下过程:
(1)温度低于1 200 K时,产物以NaCl(g)和(NaCl)2(g)为主;在温度升至1 300 K的过程中,(NaCl)2(g)的物质的量分数逐渐减少,而NaCl(g)的物质的量分数则逐渐增加,并在1 300 K左右达到最大值75%,此过程中(NaCl)2(g)逐渐向NaCl(g)转化. 对于该过程,刘敬等[16]认为,从1 000 K左右开始,准东煤中的钠主要以NaCl(g)的形式析出,部分以中间体(NaCl)2(g)的形式析出,且(NaCl)2(g)在1 273 K后消失,这与图3的结果相近.
(2)温度高于1 400 K后,NaCl(g)的物质的量分数逐渐减少,在1 900 K时减至60%左右;与此同时,NaOH(g)和Na(g)的物质的量分数逐渐增加,在1 900 K时分别达到12%和3%,此时部分NaCl(g)转化成NaOH(g)和Na(g). 对于此过程,Bläsing等[5]认为在高温下特别是还原性气氛下,NaCl(g)会分解生成Na(g),但是Na(g)不稳定,一部分Na(g)会与H2O(g)反应生成NaOH(g);此外,碱金属氯化物也会直接转化成氢氧化物[16].
(3)由图3(b)可知, 产物中以硫酸盐形式存在的钠的物质的量分数在0.3%以下.这主要是由于该煤样中氯的物质的量分数比钠的物质的量分数高(Cl、Na摩尔比为1.4∶1),根据Kim等[20]的研究结果可知,氯的物质的量分数直接影响NaCl的析出,NaCl的析出量随氯质量分数的增加而增多. 另外,在1 200 K左右,NaHSO4(g)和Na2SO4(g)的物质的量分数都达到了峰值.
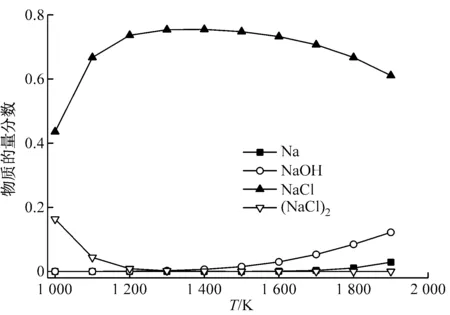
(a) 高物质的量分数产物

(b) 低物质的量分数产物
选取图3中的NaCl和Na2SO4作为分析对象,对NaCl在1 100 K和1 900 K温度下进行敏感性分析,对Na2SO4在1 200 K温度下进行敏感性分析,结果如图4所示.在图4(a)中,反应(3)的敏感性系数的绝对值较大,且为正值,这将促进NaCl的生成;反应(4)对NaCl的生成起抑制作用,但其敏感性系数的绝对值较小,故在1 100 K下,NaCl(g)的生成反应占据主导,NaCl(g)的物质的量分数增加,这与图3(a)中NaCl(g)在1 100 K左右的变化规律相符.
NaO2+HCl=NaCl+HO2
(3)
NaCl+NaCl=(NaCl)2
(4)
在图4(b)中,对NaCl生成影响较大的是反应(4)和反应(5). 与反应(4)相比,反应(6)的敏感性系数的绝对值更大,即对NaCl的抑制作用更强.因此,在1 900 K时,NaCl(g)的物质的量分数比1 100 K时少. 根据反应(6),NaCl(g)将转化为NaOH(g),NaCl(g)的物质的量分数减少,而NaOH(g)的物质的量分数增加,这与图3(a)的转化规律相符,也与刘敬等[16]的结论一致.
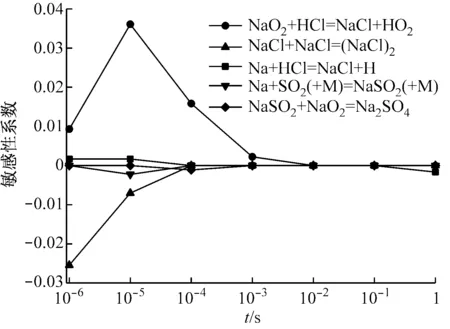
(a) 1 100 K

(b) 1 900 K

(c) 1 200 K
Na+HCl=NaCl+H
(5)
NaCl+H2O=NaOH+HCl
(6)
在图4(c)中,主要是反应(7)和反应(8)促进Na2SO4物质的量分数增加.在815 ℃下燃烧时,大部分有机钠以钠原子形式释放[15],此时生成的钠接触到SO2便会发生反应生成Na2SO4. 这一结论与Bläsing等[4]的结论有所不同,Bläsing[4]认为Na2SO4是由NaCl直接转化而来的,发生的反应见式(9).
Na+SO2(+M)=NaSO2(+M)
(7)
NaSO2+NaO2=Na2SO4
(8)
4NaCl+2H2O+2SO2+O2=2Na2SO4+4HCl
(9)
2.4 含钠气相产物的物质的量分数与过量空气系数的关系
图5给出了NaCl(g)、NaOH(g)和Na(g)的物质的量分数与过量空气系数α和温度的关系. 由图5可知,温度高于1 100 K时,α对NaCl(g)、NaOH(g)和Na(g)的物质的量分数的影响才有所体现;当α≥1时,即在氧化性气氛下,Na(g)、NaCl(g)和NaOH(g)的物质的量分数的差异不大;当α<1时,随着α增大,NaCl(g)和NaOH(g)的物质的量分数逐渐增加,Na(g)的物质的量分数逐渐减少. 这与Wei等[9]的热力学计算结果相近,Wei等[9]认为与燃烧过程相比,气化过程(即α<1)对碱金属析出的影响更大,而随过量空气系数α增大,Na(g)的物质的量分数减少及NaOH(g)的物质的量分数增加的主要原因是发生了如下反应:

(b) NaOH
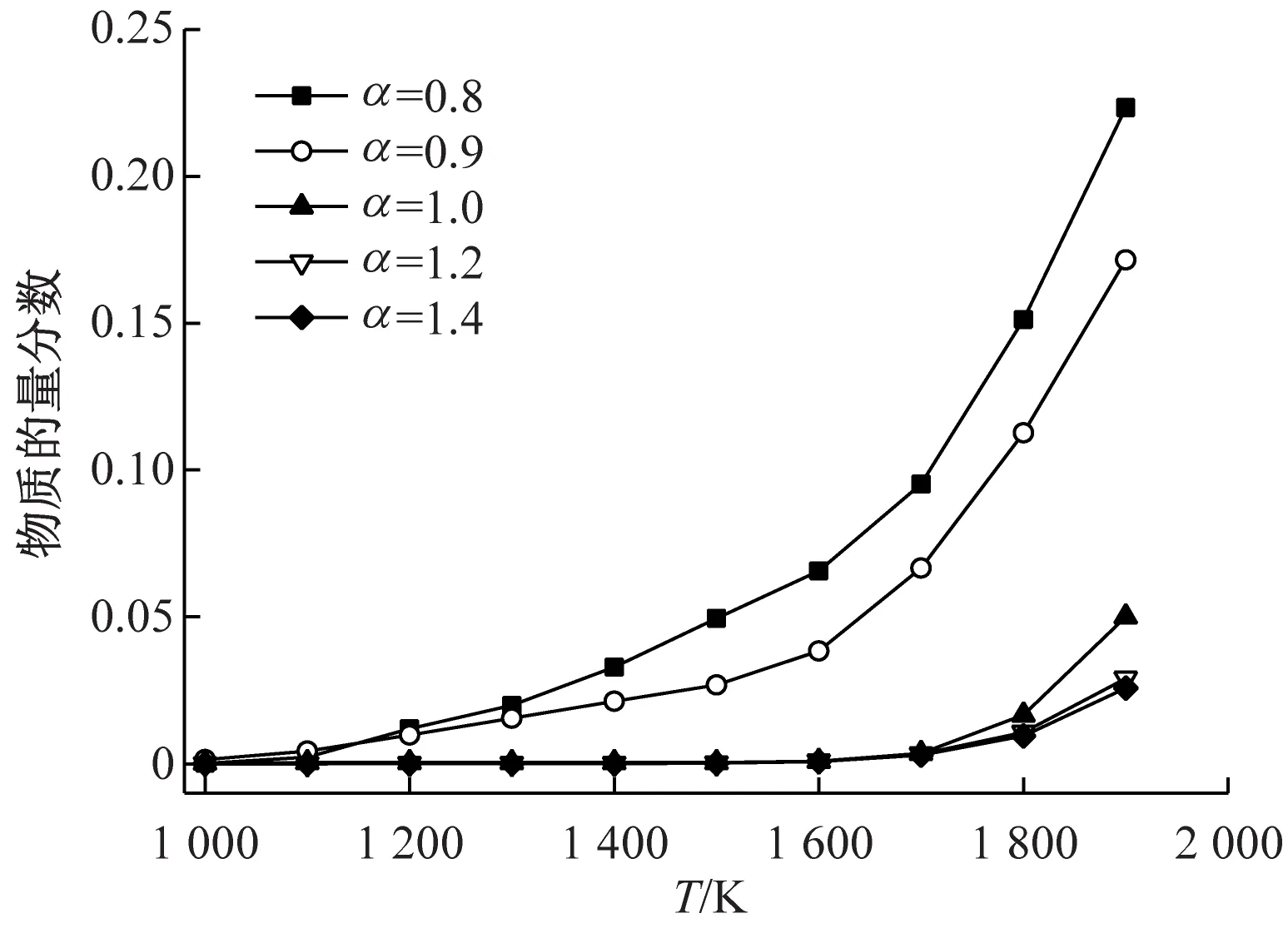
(c) Na

(10)
由图4(b)可知,温度较高时,反应(5)会促进NaCl(g)的生成;在氧化性气氛下,氢原子被快速氧化,致使该反应的平衡右移,NaCl(g)的物质的量分数增加;而在还原性气氛下,随着α减小,该反应的作用减弱,NaCl(g)的物质的量分数减少,Na(g)的物质的量分数增加,这与图5(a)和图5(c)的变化规律相符.
在1 900 K下NaOH的敏感性分析结果如图6所示. NaOH的熔点为323 ℃,沸点为1 388 ℃,加热至分解时产生Na2O. 由图6可知,在1 900 K下,影响NaOH生成的主要是反应(6)、反应(11)和反应(12).高温下,反应(6)促进了NaCl的消耗以及NaOH物质的量分数的增加,即高温下NaCl向NaOH转化. 在氧化性气氛下,O2的存在以及氢的消耗会促进反应(11)和反应(12)中NaOH和NaO的生成;在还原性气氛下,NaOH的生成将受到抑制,随着α减小,NaOH(g)的物质的量分数逐渐减少,Na(g)的物质的量分数逐渐增加,这与图5(b)的变化规律相符.
Na+H2O=NaOH+H
(11)
Na+O2=NaO+O
(12)

图6 1 900 K下NaOH的敏感性分析结果
2.5 含钠气相产物物质的量分数与压力的关系
图7给出了Na(g)、NaCl(g)和NaOH(g)的物质的量分数与压力的关系. 由图7可知,当温度高于1 500 K时,Na(g)和NaOH(g)的物质的量分数随压力的升高而略有减少;当温度低于1 300 K时,NaCl(g)的物质的量分数受压力的影响较大,并随压力的升高而减少;当温度高于1 300 K时,NaCl(g)的物质的量分数随压力升高而略有增加. Bläsing等[21]和Oleschko等[6]的试验结果也表明升高压力会减少NaCl(g)的物质的量分数,Wei等[9]的热力学计算结果表明压力升高会导致NaCl(g)和NaOH(g)的物质的量分数减少.
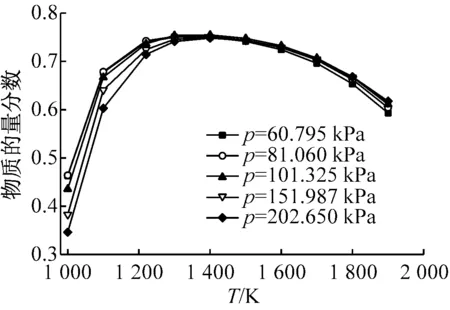
(a) NaCl
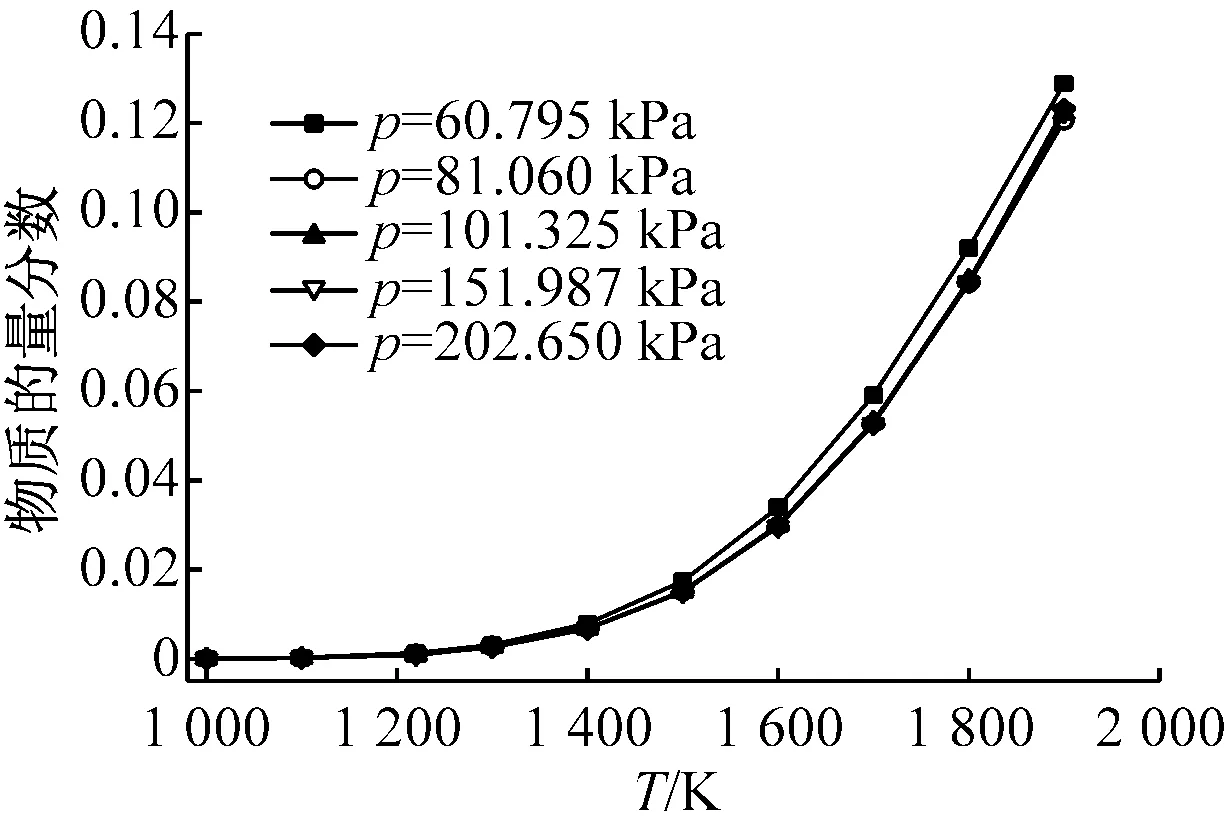
(b) NaOH

(c) Na
总体来看,压力主要影响较低温度下NaCl(g)的物质的量分数,其主要原因在于:温度低于1 300 K时,NaCl(g)与(NaCl)2(g)相互转化,从化学反应平衡角度来看,升高压力使反应(4)的平衡右移,即NaCl(g)的物质的量分数减少.
气相碱金属析出后会与Al2O3、SiO2等氧化物反应.研究表明,NaCl和Na2SO4是参与反应的主要化合物,主要发生反应(13)~反应(16),生成的二硅酸钠(Na2Si2O5)及钠长石(Na2Al2Si6O16)的熔点分别为874 ℃和1 100 ℃,这些低温共熔体易加剧炉内沾污、结渣,因此可根据上述结论选取合适的工况,控制气相碱金属化合物的含量,从而达到减少锅炉沾污、结渣的目的.
2NaCl+2SiO2+H2O=Na2Si2O5+2HCl
(13)
2NaCl+Al2O3+6SiO2+H2O=Na2Al2Si6O16+2HCl
(14)
2Na2SO4+6SiO2=2Na2O·6SiO2+2SO2+O2
(15)
Na2SO4+Al2O3·2SiO2=Na2O·Al2O3·2SiO2+SO3
(16)
3 结 论
(1)对比试验结果与化学动力学模型计算结果可知,两者的变化趋势相符,验证了该模型的准确性.
(2)计算结果表明,含钠气相产物随温度的变化主要经历以下过程:温度低于1 200 K时,产物以NaCl(g)和(NaCl)2(g)为主;在温度升至1 300 K过程中,(NaCl)2(g)逐渐转化为NaCl(g);当温度高于1 400 K后,NaCl(g)逐渐转化为NaOH(g)和Na(g). 硫酸盐形式的含钠气相产物的物质的量分数很少,NaHSO4(g)和Na2SO4(g)的物质的量分数均在1 200 K达到峰值.
(3)温度高于1 100 K时,过量空气系数α对含钠气相产物的影响较明显:当α≥1时,Na(g)、NaCl(g)和NaOH(g)的物质的量分数基本不受α的影响;当α<1时,随着α增大,Na(g)的物质的量分数逐渐减少,NaCl(g)和NaOH(g)的物质的量分数逐渐增加.
(4)压力对含钠气相产物的影响不大,当温度高于1 500 K时,随着压力生高,Na(g)和NaOH(g)的物质的量分数有所减少;当温度低于1 300 K时,NaCl(g)的物质的量分数随着压力升高而减少;当温度高于1 300 K时,NaCl(g)的物质的量分数随着压力升高而略有增加.
(5)不同碱金属化合物的物理性质不同,与其他氧化物生成低温共熔体的能力也不同,故可根据以上结论选取合适的工况,控制气相碱金属化合物的组成,从而达到减少锅炉沾污、结渣的目的.
[1] 崔育奎, 张翔, 乌晓江. 配煤对新疆准东高碱煤沾污结渣特性的影响[J].动力工程学报, 2105, 35(5): 361-365.
CUI Yukui, ZHANG Xiang, WU Xiaojiang. The effect of coal blending ratio on slagging/fouling characteristics of Zhundong Xinjiang high-alkali coal[J].JournalofChineseSocietyofPowerEngineering, 2015, 35(5): 361-365.
[2] WANG X B, XU Z X, WEI B, et al. The ash deposition mechanism in boilers burning Zhundong coal with high contents of sodium and calcium: A study from ash evaporating to condensing[J].AppliedThermalEngineering, 2015, 80: 150-159.
[3] 代百乾, 乌晓江, 张忠孝. 高碱煤燃烧过程中灰中主要元素的迁移规律[J].动力工程学报, 2014, 34(6): 438-442.
DAI Baiqian, WU Xiaojiang, ZHANG Zhongxiao. Transition behavior of main elements in fly ash during high alkali coal combustion[J].JournalofChineseSocietyofPowerEngineering, 2014, 34(6): 438-442.
[6] OLESCHKO H, MÜLLER M. Influence of coal composition and operating conditions on the release of alkali species during combustion of hard coal[J].Energy&Fuels, 2007, 21(6): 3240-3248.
[7] 谭力. 生物质燃烧过程中碱金属迁移及结渣特性的研究[D]. 北京: 华北电力大学, 2014.
[8] 陈安和, 杨学民, 林伟刚. 生物质热解和气化过程中Cl及碱金属逸出行为的化学热力学平衡分析[J].燃料化学学报, 2007, 35(5): 539-547.
CHEN Anhe, YANG Xuemin, LIN Weigang. Release characteristics of chlorine and alkali metals during pyrolysis and gasification of biomass by thermodynamical equilibrium analysis[J].JournalofFuelChemistryandTechnology, 2007, 35(5): 539-547.
[9] WEI X L, SCHNELL U, HEIN K R G. Behaviour of gaseous chlorine and alkali metals during biomass thermal utilisation[J].Fuel, 2004, 84(7/8): 841-848.
[10] TAKUWA T, NARUSE I. Detailed kinetic and control of alkali metal compounds during coal combustion[J].FuelProcessTechnology, 2007, 88(11/12): 1029-1034.
[11] GLARBORG P, ALZUETA M U, JOHANSEN K D, et al. Kinetic modeling of hydrocarbon/nitric oxide interactions in a flow reactor[J].CombustionandFlame, 1998, 115(1/2): 1-27.
[12] GLARBORG P, MARSHALL P. Mechanism and modeling of the formation of gaseous alkali sulfates[J].CombustionandFlame, 2005, 141(1/2): 22-39.
[13] HINDIYARTI L, FRANDSEN F, LIVBJERG H, et al. An exploratory study of alkali sulfate aerosol formation during biomass combustion[J].Fuel, 2008, 87(8/9): 1591-1600.
[14] MCBRIDE B J, ZEHE M J, GORDON S. NASA glenn coefficients for calculating thermodynamic properties of individual species[R]. Cleveland, Ohio: Glenn Research Center, 2002.
[15] 刘大海, 张守玉, 涂圣康, 等. 五彩湾煤中钠在燃烧过程中的迁移释放规律[J].化工进展, 2015, 24(3): 705-709.
LIU Dahai, ZHANG Shouyu, TU Shengkang, et al. Modes of occurrence and transformation of alkali metals in Zhundong coal during combustion[J].ChemicalIndustryandEngineeringProgress, 2015, 24(3): 705-709.
[16] 刘敬, 王智化, 项飞鹏, 等. 准东煤中碱金属的赋存形式及其在燃烧过程中的迁移规律实验研究[J].燃料化学学报, 2014, 42(3): 316-322.
LIU Jing, WANG Zhihua, XIANG Feipeng, et al. Experimental study on the occurrence of alkali metal of Zhundong coal and its migration during combustion[J].JournalofFuelChemistryandTechnology, 2014, 42(3): 316-322.
[17] JOHANSEN J M, JAKOBSEN J G, FRANDSEN F J, et al. Release of K, Cl, and S during pyrolysis and combustion of high-chlorine biomass[J].Energy&Fuels, 2011, 25(11): 4961-4971.
[18] LI G Y, WANG C A, YAN Y, et al. Release and transformation of sodium during combustion of Zhundong coals[J].JournaloftheEnergyInstitute, 2016, 89(1): 48-56.
[19] 徐莹. 气体再燃化学动力学分析及机理简化研究[D]. 哈尔滨: 哈尔滨工业大学, 2010.
[20] KIM S S, KANG Y S, LEE H D, et al. Release of potassium and sodium species during combustion of various rank coals, biomass, sludge and peats[J].JournalofIndustrialandEngineeringChemistry, 2012, 18(6): 2199-2203.
Chemical Kinetics Simulation on High-temperature Morphology of Alkali Sodium in Zhundong Coal
JIJieqiang,CHENGLeming,LIUYanquan,WANGQinhui,LUOZhongyang
(State Key Laboratory of Clean Energy Utilization, Institute for Thermal Power Engineering, Zhejiang University, Hangzhou 310027, China)
2016-10-17
2016-11-03
国家科技支撑计划资助项目(2015BAA04B02-09)
季杰强(1991-),男,浙江金华人,博士研究生,主要从事准东煤沾污结渣方面的研究. 程乐鸣(通信作者),男,教授,博士,电话(Tel.):0571-87953208;E-mail:lemingc@zju.edu.cn.
1674-7607(2017)10-0780-08
TF536
A
470.30
