微胶囊释放机制概述
2017-10-16张小军
马 涛,孙 哲,张小军*
(1.中农立华生物科技股份有限公司,北京 100052;2.滨州市农业局,山东滨州 256600)
◆专论与综述◆
微胶囊释放机制概述
马 涛1,孙 哲2,张小军1*
(1.中农立华生物科技股份有限公司,北京 100052;2.滨州市农业局,山东滨州 256600)
控制释放在保护药物免受内在或外界条件的影响,提高药物有效利用率,延长持效期等方面起了重要作用。微囊化是控制释放的一种有效途径,微囊化技术多种多样,微囊化所用壁材也不尽相同,伴随的微胶囊释放机制亦各不相同。文中对几种微胶囊控释机制进行了详细论述,以期对探索高功效、智能化微囊化技术提供参考依据。
微囊化;控制释放;释放机制;综述
Abstract:The controlled release played a critical role in protecting the drug from being damaged by internal or external factors,improving effective availability and prolonging lasting period.The microcapsulation is an effective way to control release.The microcapsulation technology is varied,and the wall materials are also different,so the release mechanisms must be different.In this paper,several kinds of controlled release mechanism of microcapsules were discussed in detail.It had a great significance on exploring high efficiency,intelligence and release-controlled microcapsulation technology.
Key words:microcapsulation;controlled release;release mechanism;review
控制释放系统的设计目的主要包括:1)保护敏感有效成分,减少外界环境因素对其的影响[1];2)延缓芯材释放,延长持效期[2];3)降低对作物、环境等的毒害[3];4)减少用药次数,提高药物有效利用率等。因此,药物释放在药物传导系统设计过程中是一个不可忽略的关键点。微囊化在药物释放领域是一个比较新颖的概念。通过近些年来科学家的不断探索和实践,微囊化技术已逐渐发展成熟。众所周知,微囊化技术一般是指利用一种较薄的、不同特性的材料将固体或液体微小颗粒包覆起来,以达到控制释放的技术[4]。目前微囊化技术在化工、食品、医药、精油等领域得到广泛的开发与应用,但在农药领域的应用还不够广泛。由于生产条件的局限性和使用环境的复杂性,农药微囊化技术大部分还只是在实验室中进行,而且微胶囊工业化放大技术目前掌握的人数较少,并没有在行业中普及。随着微囊化技术的进步,近几年来已不断有农药微胶囊商品化,如吡虫啉、毒死蜱、高效氯氰菊酯等[5]。然而我国对农药微胶囊的研究尚处于制备过程,对最为关键的释放过程未进行系统的研究,而且随着国家肥药双减政策深入实施,重点着眼于制备过程已不能满足人们对省力化、智能化、高功效剂型的需求。
本文就近年来国内外微胶囊化不同的释放机制进行了详细综述,探讨了不同释放机制的特性。此外,根据研究人员多年从事微囊化技术研究的实践经验,先对微囊化的技术方法进行简短概述,然后结合目前农药微胶囊的登记现状,探讨了国内农药微胶囊有待解决的问题,旨在促进农药微囊化技术的发展。
1 微胶囊制备方法
目前,农药微胶囊(如图1)常用的制备方法有原位聚合法[6]和界面聚合法[7],另外还有喷雾干燥法[8]、包结络合法[9]、超临界流体法[10]、溶剂挥发法[11]、相分离法[12]、锐孔-凝固浴法[13]等,近年来也有学者探索提出了微流体技术[14]和配位聚合技术[15]等微囊化新技术。常用的壁材主要有脲醛树脂、密胺树脂、聚脲、聚氨酯等。由于所需囊壁材料和药物类型不同,释放机理也各式各样。
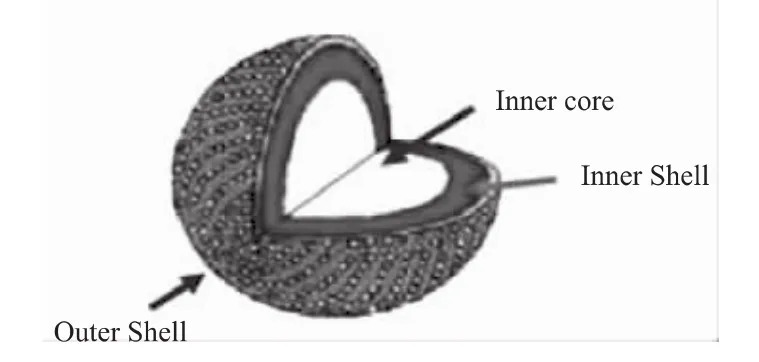
图1 微胶囊结构简图
2 微胶囊释放机制
药物微囊化后,一般要求药物能定时定量从微胶囊中释放,以达到防治的目的[16]。由于微胶囊材料和药物类型的不同,药物的释放动态主要取决于药物本身在介质中的溶解性、溶剂的扩散能力、聚合物的溶胀、囊壁材料的降解以及外界因素,如触碰、光、pH等[17]。微胶囊释放机制主要包括以下4种:扩散-控制释放、溶解-控制释放、降解-控制释放和刺激-控制释放。
2.1 扩散释放
这是一种常见的释放方式,一般采用界面聚合法和原位聚合法制备的微胶囊的释放机制主要为扩散控制释放。微胶囊被当做一种存储的容器,当与均一溶液接触时,溶剂分子通过微胶囊上的孔隙或通道进入囊内将药物溶解,然后通过溶剂分子的不断运动将药物从囊内搬运到囊外,从而达到扩散释放的目的[18]。这种释放根据所包裹药物的溶解度不同分为连续和不连续释放。囊内药物溶解较快,这种释放系统属于不连续释放系统(如图2)。此种释放,遵循一级释放动力学模型[19-20]。当药物从囊内扩散后,囊内药物浓度降低,从而使得扩散速率随着时间呈指数性降低。如果囊内药物具有较低的溶解度,则开始只有一部分扩散出来,后面会缓慢释放直到囊内药物完全溶解,此释放系统为连续释放(如图3)。该释放符合零级释放动力学模型[19-20]。总之,扩散释放机制主要取决于以下因素:溶剂对药物的溶解速率和溶剂渗透进入囊壁的速率、药物溶液逃离微胶囊的速率。
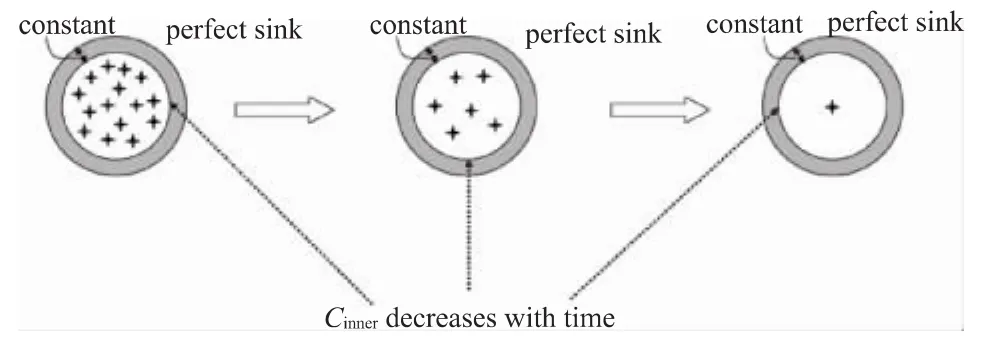
图2 微胶囊不连续释放系统

图3 微胶囊连续释放系统
在零级释放模型中,药物释放动态还需考虑初始载药量。受微胶囊初始载药量与微胶囊囊壁厚度的影响,释放系统的初始释放状态可能会存在2种情况[19]。一是初始释放呈现一种“突释”现象。大量的药物在贮存期间可能已扩散到囊壁材料中,当该释放系统暴露于释放介质中时,就会有个较高的释放速率,即“突释”。二是初始释放呈现低释放速率现象。该现象与“突释”相反,药物被包裹后几乎不会渗透进入壁材,因此,最初的浓度一般会低于稳定状态的浓度,即产生低速释放现象。
2.2 溶解释放
溶解释放过程属于物理化学过程[21]。在此释放机制中,当聚合物囊壁在释放介质中可溶时,药物的释放速率由聚合物囊壁的溶解速率决定[22]。囊壁厚度越大,囊壁在释放介质中的溶解度越小,药物释放越慢。
2.3 囊壁侵蚀和降解控制释放机制
目前最常见的可降解微胶囊壁材主要为聚乳酸或乳酸与羟基乙酸聚合物。易侵蚀系统最重要的特点是释放机制和侵蚀动态。侵蚀产物必须无毒且可回收。侵蚀释放方式有2种:本体溶蚀和表面侵蚀。
单体系聚合物的侵蚀发生在释放介质中,特别是水,极易攻击聚合物的共价键。对于水解不稳定的化学键,水的存在是侵蚀速率的重要决定因素。键的水解也可以由酸或碱催化,这种情况下侵蚀速率将取决于本地质子供体和受体的浓度。
当水侵入聚合物时水解反应迅速发生。在这种情况下,水存在于微胶囊体系周围,链断裂过程能够发生在囊体任何地方。开始时水解作用可能会很慢,尤其是聚合链过长,最初的链断裂反而使得聚合链具有足够的流动性和迁移性,并形成晶体,不利于水解反应的继续,然而水解反应达一定程度后,整个过程将加速。本体溶蚀释放特点如图4所示。第1阶段(a)药物链接到微胶囊释放体系的表面;第2阶段(b)为潜在释放阶段,小部分聚合物开始降解,但药物依然被包覆;第3阶段(c)聚合物分解,药物得到迅速释放。

图4 本体溶蚀致药物释放示意图
当微胶囊与水接触时,表面侵蚀反应发生。表面侵蚀较缓慢,水解反应则较快。例如聚酐类聚合物是一种具有一定疏水性的材料,为防止发生水解反应,不稳定的化学键被埋藏在聚合物内层,因此伴随着水解反应的进行,离微胶囊表面较近的药物首先缓慢释放。侵蚀释放过程如图5所示。被包覆的药物随着囊壁材料的侵蚀而缓慢释放,囊壁聚合物的侵蚀由表及里,粒径也逐渐减小,最终导致所有药物的释放[23]。

图5 表面侵蚀释放机制示意图
侵蚀和降解释放过程只是理想条件下的简单过程,现实情况下释放过程比较复杂,单纯的本体溶蚀和表面侵蚀很少存在。微胶囊释放机制还跟所包裹药物的性质有关。周训卿等[24]以可生物降解的壳聚糖(CS)和DL-丙交酯为原料,合成了可降解的壳聚糖-聚乳酸接枝共聚物(CS-co-PLA),并以此为壁材制备嘧菌酯微胶囊,嘧菌酯被包裹在共聚物的疏水内核中,释放速率较慢。为了提高凝胶微球的缓释性能,向飞等[25]以啶虫脒为模型药物,采用层层组装(LBL)方法,制得了海藻酸钠与壳聚糖交替包覆的具有多层膜结构的凝胶微球。由于海藻酸钠/壳聚糖聚电解质膜间主要靠静电作用吸附在一起,其较强的溶胀性能和疏松的层层结构相对于钙离子交联的微球具有更强的吸水作用,所以随膜层数的增加,微球的溶胀度增大,膜层越容易从微球表面脱落,进而控制药物释放。
2.4 触发诱导释放机制
刺激反应式微胶囊在药物释放、香料释放、食品保鲜、自修复材料中应用较广泛。目前有多种刺激途径可以用于微胶囊药物的释放。触发诱导释放的刺激因子主要有化学、生物、光、热、磁和电等[26]。图6介绍了几种在农药领域有潜在应用价值的触发诱导释放机制。

图6 微胶囊的刺激释放机制
2.4.1 化学诱导释放机制
利用化学方法控制微胶囊释放是通过触发囊壁上的某些化学键来引发一系列反应,从而控制释放过程。化学诱导大体上分为2类:1)pH变化;2)硫键的还原反应。这里重点描述pH诱导释放。许多反应都是由酸或碱催化完成的,例如聚丙烯酸盐类吸水剂具有强吸水性的同时,也对溶液中质子浓度的变化具有一定的响应能力,因而可以制成质子敏感型水凝胶。当溶液呈中性或弱碱性时,聚合物链水化后呈伸展状态,孔道关闭;当溶液呈强酸性(pH值≤2)时,由于聚电解质链收缩,孔道自动打开,处于开放状态。依据该原理,人们可以设计制作智能水凝胶微球,应用在缓释药物及生化医药方面。Hoffman[27]对其应用已进行了全面综述。目前pH刺激响应微胶囊主要用于医学领域。pH刺激响应性药物释放体系特别适合口服药物的控制释放,即利用人体消化道各环节pH值的不同,控制药物在特定的部位释放。pH刺激响应性药物释放系统采用对pH值有响应性的凝胶材料做为药物包埋基质,利用凝胶在不同pH值下溶胀度、渗透性能的不同,来控制药物的释放[28]。Schwarte等[29]用聚乙二醇和聚甲基丙烯酸N,N-二乙基氨基乙酯制得一种新型接枝阳离子型水凝胶。这种水凝胶显示出非常强的pH敏感性,pH值较高时溶胀比高达25倍,可用于7-(β-羟丙基)茶碱、维生素B12、荧光黄异硫氰酸盐-葡聚糖的释放。Abbaspourrad等[30]用微流体技术制备了pH刺激响应微胶囊(如图7)。随着pH值的增大,所包裹物质的释放速率随之增加。

图7 pH响应微胶囊释放过程示意图
诱导释放要求施用环境比较特定,目的性较强,目前在农药领域研究甚少。在农药生产中可以根据各种农药本身的性质和所施用环境的酸碱度来决定某些农药制剂的加工形式。
2.4.2 生物刺激释放机制
生物学特性和生物分子都能够刺激微胶囊释放芯材物质。从文献角度可以将生物刺激释放方式分为2类:一是生物的生命活动产生刺激,破坏了囊壁从而导致释放。陆一匡等[31]应用界面聚合法制备了用于防治光肩星天牛和黄斑星天牛的触破式氯氰菊酯微胶囊剂。此触破式微胶囊受外界压力作用而破裂,并释放有效成分。实践证明该微胶囊剂不仅对天牛击倒快、药效高,而且具有持效期长的优点。二是通过生物分子如酶类对囊壁的降解促使芯材物质释放。此类型目前在医药领域应用较多,依靠人体内各种消化酶来溶解囊壁,进而使囊内药物释放。例如,酯酶催化酯水解反应,糖苷酶催化糖苷键水解,肽酶催化蛋白质水解生成氨基酸,还原酶催化氢化反应等。
2.4.3 热刺激释放机制
温度变化也可以引发微胶囊的释放。温度的变化引起微胶囊囊壁的熔化,导致相变,从饱满水合状态转变成干瘪失水状态,相变使囊壁产生孔隙,进而使药物释放。温度的增加可以使聚合物解体或者分解,导致芯材释放。除了直接加热外,其他的光、电、磁也可以引起温度变化,进而导致释放。本文主要关注直接加热达到释放的机制。Sun等[32]选择微流体技术,采用复乳化法制备了单分散性微胶囊,该微胶囊随着外界温度的升高,囊壁熔化,芯材释放,释放过程如图8。所制备微胶囊以石蜡为壁材,以甲苯胺蓝为芯材,当温度升高到45℃时,囊壁开始熔化(2),使得芯材与熔化壁材融合(3),再经过几分钟的持续加热,芯材全部释放。

图8 热响应微胶囊的热释放示意图
2.4.4 光刺激释放机制
光刺激控释系统目前已有较多应用,纳米粒子和发色基团能够在一定波长范围内吸收光,而且吸收截面可以调整为单光子或多光子吸收。光刺激释放的原理主要是体积相转变。从相转变机理角度可以将它分为2种。一种是所用壁材聚合物含有光活性基团,如偶氮苯、螺苯并吡喃、三苯甲烷等[33]。这些活性基团受到光照后,构型发生变化或形成带电荷的基团,导致聚合物分子链的构象或亲疏水性发生变化,进而改变聚合物的结构(如图9A、图9B),引起控释体系发生体积相转变,实现药物在胶束中的包载和释放[34]。比如,偶氮苯基团是由2个苯环通过偶氮键(-N=N-)连接起来的光活性基团,存在顺式和反式2种异构体[35-37]。当受到特定波长紫外光照射时,偶氮苯基团的反式异构体会转变为顺式异构体;当受到蓝光照射时,顺式异构体可转变为反式异构体。如果偶氮苯基团位于形成控释体系的聚合物分子主链上,其顺-反异构体的转化会导致聚合物分子链的构象发生明显变化,从而引起控释体系发生体积相转变,进而导致药物释放。2004年,Wang等[38]首次将光敏感性基团引入聚合物胶束的结构中,获得了一种在可见光和紫外光作用下可控自组装和自解离的BCPM。

图9 光刺激响应性缓释系统
另一种光刺激响应性缓释系统(如图9C)是由贵金属纳米粒子和温度刺激响应性聚合物材料形成的复合体系。当这类控释体系受到光照时,其中的贵金属纳米粒子如银纳米粒子或金纳米粒子等可以将光能转化成热能,导致温度高于其中温度刺激响应性聚合物,发生体积相转变。后面的释放机制同热刺激释放机制。此类释放机制由于用到银纳米粒子和金纳米粒子等贵金属,成本比较昂贵,在医药领域应用较多,在农药领域应用较少。但由于丰富的紫外线资源,第1种光敏式微胶囊有望在农药领域得到广泛的开发与应用。
3 农药微囊化方面存在的问题
虽然农药微胶囊概念在行业内由来已久,但诸多因素限制了农药微胶囊由理论向实践的转化。总体来说,农药微囊化技术的发展需要克服诸多难点。常见的问题有:农药微胶囊化技术仍然停留在探索阶段,没有一套成熟的技术理论作为指导;农药种类繁多,性质各不相同,微囊化技术多样,很难探索出一种既简单又适用的方法;对农药微胶囊的释放机制研究太少,应以所需农药微胶囊的释放机制去指导微囊化技术的探索;微囊化要求较高,工业化生产难以准确控制[39];目前工业化产品的工艺方法比较单一,仅限于原位聚合法和界面聚合法等;另外,由于微囊化成本较高,企业对该技术的投入较少,重视度不够。
4 结语
本文对几种控释策略及释放机制进行了详细叙述,强调了几种释放机制在控释系统中的重要作用。当设计开发控释系统时,重要的是识别或理解该系统的控释机制。通常情况下并不是一种控释机制在起主导作用,有可能在每个阶段均有一种控释机制。因此,了解各种控释机制,以所需要的控释机制去指导控释系统的设计才是达到控释效果的最佳途径。药物控制释放确实在一定程度上增加了药物的实际价值,但不可否认控制释放产品的开发花费较大。并不是所有的药物都需要制成控释制剂,其中易降解、毒性较高或对特定环境有影响的药物需要加工成控释制剂。随着对控释机制理解加深和控释技术的发展,将会有越来越多合适的药物开发成控释制剂。
[1]Hadwiger L A,Mcbride PO.Low-Level Copper Plus Chitosan Applications Provide Protection Against Late Blight of Potato[J/OL].(2006-04-06)[2017-06-01].http://www.plantmanagementnetwork.org/pub/php/research/2006/chitosan/.
[2]Green J M,Beestman G B.Recently Patented and Commercialized Formulation and Adjuvant Technology [J].Crop Protection,2007,26(3):320-327.
[3]Sutter S C,Buera M P,Elizalde B E.Beta-Carotene Encapsulation in a Mannitol Matrix as Affected by Divalent Cations and Phosphate Anion [J].International Journal of Pharmaceutics,2007,332(1/2):45-54.
[4]Agnihotri N,Mishra R,Goda C,et al.Microencapsulation—A Novel Approach in Drug Delivery:A Review[J].Indo Global Journal of Pharmaceutical Sciences,2012,2(1):1-20.
[5]陈列忠,陈建明,赵敏,等.毒死蜱·高效氯氰菊酯的微胶囊化及其对蛴螬的防治效果[J].农药学学报,2009,11(4):487-492.
[6]周一万,冯俊涛,张兴.冬青油微囊悬浮剂的制备及其杀蚜活性研究[J].农药学学报,2013,15(2):228-233.
[7]傅桂华,钟滨,陈建宇,等.界面聚合法制备农药微胶囊剂的研究[J].农药,2005,44(2):66-68.
[8]孙厚良.喷雾干燥法制备微胶囊工艺研究[J].化工时刊,2005,19(10):16-19.
[9]颜铭池,许英梅,安晓雯,等.包结络合法制备香精微胶囊的研究[J].日用化学品科学,2006,29(4):19-21.
[10]乔吉超,胡小玲,管萍.超临界流体技术制备微胶囊的研究进展[J].现代化工,2007,27(增刊1):122-125.
[11]孟锐,杨代斌,李晓刚,等.乳化溶剂挥发法制备放线菌酮微胶囊剂[J].农药,2009,48(12):886-888;891.
[12]田春华,冀志霞,吴广涛,等.苏云金芽胞杆菌聚γ-谷氨酸-明胶微胶囊剂制备及其抗逆性 [J].应用与环境生物学报,2009,15(3):367-370.
[13]曹德勇.毒死蜱的微胶囊化[D].天津:天津大学,2006.
[14]蒋东.微胶囊的研制与应用进展 [J].天津药学,2012,24(2):62-65.
[15]孟锐,李晓刚,刘双清,等.基于聚碳酸亚丙酯载体的农药微胶囊制备与表征[J].功能材料,2012,43(22):3143-3147.
[16]何玉军.浅析药物微囊化的制备及释放机制 [J].按摩与康复医学,2011(8):35-35.
[17]严敖金,张灿峰,柳富国,等.触破式微胶囊加工工艺及初步应用[J].南京林业大学学报:自然科学版,1999,23(1):65-68.
[18]Krishna S A,Jyothika M.A Review on Microcapsules[J].CIBTech Journal of Pharmaceutical Sciences,2015,4(2):26-33.
[19]Siepmann J,Siegel R A,Rathbone M J.Fundamentals and Applications of Controlled Release Drug Delivery [M].New York:Springer,2012:127-152.
[20]Siepmann J,Siepmann F.Modeling of Diffusion Controlled Drug Delivery[J].Journal of Controlled Release,2012,161(2):351-362.
[21]陆彬.微型胶囊中药物的释放特性 [J].华西药学杂志,1986(1):34-39.
[22]Gunder W,Lippold B H,Lippold B C.Release of Drugs from Ethyl Cellulose Microcapsules(Diffusion Pellets)with Pore Formers and Pore Fusion [J].European Journal of Pharmaceutical Sciences,1995,3(4):203-214.
[23]罗华丽,鲁在君.壳聚糖作为药物载体的缓释机理的研究进展[J].天中学刊,2006,21(2):38-40.
[24]周训卿,曹立冬,刘亚静,等.嘧菌酯微囊的制备及其性能表征[J].农药学学报,2014,16(2):213-219.
[25]向飞,颜慧琼,陈秀琼,等.海藻酸钠/壳聚糖层层裹覆凝胶微球的缓释性能[J].化工新型材料,2016,44(2):165-168.
[26]Esser-kahn A P,Odom S A,Sottos N R,et al.Triggered Release from Polymer Capsules [J].Macromolecules,2011,44(14):5539-5553.
[27]Hoffman A S.“Intelligent”Polymers in Medicine and Biotechnology[J].Artificial Organs,1995,19(5):458-467.
[28]张玉翠,王斌,庄善学,等.智能给药系统研究进展——化学刺激响应性药物释放系统[J].甘肃联合大学学报:自然科学版,2006,20(4):9-11.
[29]Schwarte L M,Peppas N A.Novel Poly(ethylene glycol)-grafted,Cationic Hydrogels:Preparation,Characterization and Diffusive Properties[J].Polymer,1998,39(24):6057-6066.
[30]Abbaspourrad A,Datta S S,Weitz D A.Controlling Release from pH-Responsive Microcapsules [J].Langmuir the Acs Journal of Surfaces&Colloids,2013,29(41):12697-12702.
[31]陆一匡,张灿峰,王小平.触破式微胶囊剂(绿色威雷)的研制及应用[J].现代农药,2001(3):11-13.
[32]Sun B J,Shum H C,Holtze C,et al.Microfluidic Melt Emulsification for Encapsulation and Release of Actives[J].ACS Applied Materials&Interfaces,2010,2(12):3411-3416.
[33]Lee H,Wu W,Oh J K,et al.Light-Induced Reversible Formation of Polymeric Micelles [J].Angewandte Chemie,2007,46(14):2453-2457.
[34]Alvarez Lorenzo C,Bromberg L,Concheiro A.Light-Sensitive Intelligent Drug Delivery Systems[J].Photochemistry&Photobiology,2009,85(4):848-860.
[35]Cui L,Tong X,Yan X,et al.Photoactive Thermoplastic Elastomers of Azobenzene-Containing Triblock Copolymers Prepared Through Atom Transfer Radical Polymerization [J].Macromolecules,2004,37(19):7097-7104.
[36]Tong X,Wang G,Soldera A,et al.How Can Azobenzene Block Copolymer Vesicles be Dissociated and Reformed by Light?[J].The Journal of Physical ChemistryB,2005,109(43):20281-20287.
[37]王东瑞,王晓工.偶氮嵌段共聚物合成,自组装与光响应性[J].化工学报,2010,61(7):1713-1719.
[38]Wang G,Tong X,Zhao Y.Preparation of Azobenzene-Containing Amphiphilic Diblock Copolymers for Light-Responsive Micellar Aggregates[J].Macromolecules,2004,37(24):8911-8917.
[39]白文营,马兰可,金晓阳,等.滴丁·乙-脲醛微囊悬浮剂的制备与表征[J].广州化工,2014,42(10):104-105.
(责任编辑:顾林玲)
澳大利亚2017/18年高粱种植面积将增长54.4%
据澳大利亚农业资源经济科学局(ABARES)预计,2017/18年澳大利亚夏季高粱种植面积同比增长54.4%,至59.6万hm2。
ABARES指出,在过去的一年,棉花生产的预期收益过高,从而导致高粱种植面积处于历史较低水平。夏季作物种植面积将比上年增长2.6%,至140万hm2。棉花种植面积预计下降22.8%,至43万hm2。这主要归因于旱地棉花种植面积的下降,其降幅预计达73%,种植面积至5.6万hm2。然而,由于灌溉水丰足,棉花种植预期收益上升,灌溉田棉花种植面积预计将增长7%,至37.4万hm2。同样,充足的灌溉用水有望促进澳大利亚水稻种植,水稻种植面积预计将增长5%,至8.4万hm2。
(陈晨译自《AGROW》)
A Review of Microcapsule Release Mechanism
MA Tao1,SUN Zhe2,ZHANG Xiao-jun1*
(1.Sino-Agri Leading Biosciences Co.,Ltd.,Beijing 100052,China;2.Binzhou Agricultural Bureau,Shandong Binzhou 256600,China)
TQ 450.1
A
10.3969/j.issn.1671-5284.2017.05.001
2017-06-22
马涛(1989—),男,河北省沧州市人,硕士研究生,主要从事农药剂型研发。E-mail:matao_lh@sino-agri-sal.com
张小军(1977—),男,山西省交口县人,博士,高级工程师,主要从事农药剂型研发及使用技术研究。E-mail:zhangxj369@sina.com
