基于普鲁士蓝/二氧化钛纳米管修饰碳糊电极的 电流传感器检测偏二甲肼的研究
2017-10-15任向红胡莉军
任向红, 董 超, 胡莉军
(火箭军工程大学五系,陕西西安 710025)
偏二甲肼(UDMH)是广泛使用的火箭燃料[1],也可应用于聚合物、农药、医药和化疗药物的合成[2]。但它是一种有毒挥发性液体,可以通过口、皮肤或呼吸道进入人体,UDMH为致癌物质(可能致癌)[3]。目前,测定UDMH的分析方法有荧光法[4]、气相色谱法[5]、流动注射分光光度法[6]、分光光度法[7]等。然而,这些方法有各种缺点,比如操作复杂、灵敏度不足或缺乏便携仪器等。
普鲁士蓝(PB)是一种多核过渡金属氰化物,具有电致变色性质[8]、光物理特性、磁性[9]和潜在的电分析性能以及类沸石结构,这些特性有良好的催化性能[10 - 11],已经被用于H2O2和葡萄糖等的电催化氧化方面。TiO2是钛的最常见化合物,具有化学惰性、良好的生物兼容性、较强的氧化能力,以及抗化学腐蚀和光腐蚀的能力。其中,TiO2纳米管(TNTs)具有较大的比表面积和较高的吸附能力,有良好的选择性,具有新颖的光电转换效率和光催化性能。由于TNTs独特的物理化学性质,将其作为PB的载体,将会有更好的催化活性。在本研究中,对比普鲁士蓝修饰碳糊电极(PB/CPE)检测特点,基于PB/TNTs/CPE的电化学传感器被用于检测UDMH溶液,并考察了具体影响因素。
1 实验部分
1.1 仪器与试剂
CHI1200B型电化学工作站(上海辰华有限公司);采用三电极体系:修饰碳糊电极作为工作电极(直径3 mm,深度2 mm)(上海楚兮实业有限公司),232型甘汞电极作为参比电极,213型铂电极作为对电极(上海罗素科技有限公司)。pHB-5型pH计(杭州奥利龙仪器有限公司);JEM-200CX型透射电子显微镜(TEM)(日本,JEOL公司);BS210S型电子天平(北京赛多利斯仪器系统有限公司)。
石墨粉、液体石蜡、KCl、HCl、NaOH、FeCl3和K4Fe(CN)6,均购自天津天力化学试剂有限公司;TiO2粉末购自天津化学试剂有限公司;5%Nafion溶液购自美国杜邦公司。试剂纯度均为分析纯,电解质溶液为0.1 mol·L-1KCl,所有溶液用去离子水配备。
偏二甲肼(UDMH)溶液(含量>98%)来自航天推进剂库存样品。
1.2 实验方法
电化学实验采用三电极体系,操作软件为CHI通用电化学分析软件,方法为循环伏安法(CV)和计时电流法(CA)。对PB/TNTs/CPE进行电化学表征,研究扫速、pH值的影响,以及得出UDMH检测的线性范围等均使用CV法;考察电流响应灵敏度使用CA法。
1.3 PB及TNTs的合成
根据化学反应方程式:3K4[Fe(CN)6]+4FeCl3→Fe4[Fe(CN)6]3+12KCl合成PB。具体方法:30 mL K4[Fe(CN)6]溶液快速加入到相同浓度的40 mL FeCl3溶液中,立即形成PB,过滤,收集所得蓝色沉淀,再将沉淀物置于烘箱中在80 ℃下烘干,然后用玛瑙研钵研磨,便得到PB纳米颗粒。
采用水热法合成TNTs。称取1.5 g TiO2,溶于32 mL 10 mol·L-1的NaOH溶液中,充分搅拌形成白色的糊状混合物。将混合物加入到聚四氟乙烯反应釜中,置于130 ℃的烘箱中反应24 h。空气中自然冷却后,将合成的白色沉淀物用大量水和稀HCl不断洗涤,直至其pH值约为7,并在80 ℃下烘干,得到的白色固体用玛瑙研钵充分研磨,得到均质的白色粉末,备用。
1.4 PB/TNTs复合材料及化学修饰碳糊电极的制备
PB/TNTs复合材料的制备:取0.4 g TNTs加入到40 mL FeCl3溶液中,于室温下搅拌30 min后,再将30 mL K4[Fe(CN)6]溶液慢慢滴入到以上混合物中,搅拌30 min;得到的蓝色混合物用抽滤装置进行反复抽滤,以除去没有被吸附的蓝色PB分子,直至上清液为无色。最后将蓝色沉淀物于烘箱中80 ℃下烘干,用玛瑙研钵对所得固体进行研磨,便得到PB/TNTs复合材料。
修饰碳糊电极的制备:将PB/TNTs(0.01 g)与石墨粉(0.45 g)和石蜡油(0.3 mL)混合35 min,得到均匀碳糊。然后将碳糊注入电极的末端管孔内(直径3 mm、深度2 mm)。由铜棒连接到内孔管的碳糊,制备得到PB/TNTs/CPE。PB/CPE采用制备好的PB(0.01 g)与石墨粉(0.45 g)和石蜡油(0.3 mL)混合35 min,其余同上。
2 结果与讨论
2.1 PB纳米粒子和PB/TNTs复合材料的特征
图1为PB纳米粒子和PB/TNTs复合材料的透射电镜(TEM)图像。从图1a可见,PB纳米粒子有很强的凝聚性,附着程度比较高,而且单个粒子分散的尺寸不足50 nm。TNTs有较大的比表面积和较强的吸附能力,从图1b可以看出TNTs可以作为PB粒子的载体。另外从图1a可以看出PB粒子的立方体特性,这种形貌能够提供比球形粒子更强的催化性。

图1 PB纳米粒子(a)和PB/TNTs复合材料(b)的透射电子显微镜(TEM)图Fig.1 TEM images of PB nanoparticles(a) and PB/TNTs composites(b)
2.2 化学修饰电极的电化学表征
图2显示了阳极和阴极电流与扫速以及与扫速平方根的线性关系。可见扫速在10~100 mV·s-1区间内峰电流与扫速线性相关。从结果可以得出,PB含量的降低是一个吸附控制的过程,在扫速高于100 mV·s-1的情况下,相对于v1/2的Ip值是线性的,表明是一个扩散控制过程,有文献报道了类似结果[12 - 16]。
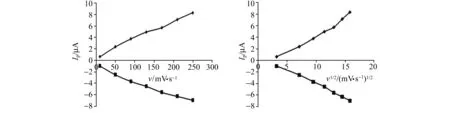
图2 阳极和阴极峰电流与相应的扫速和扫速率平方根的关系Fig.2 Plots of anodic and cathodic peak currents vs.scan rate and its square root
2.3 UDMH在三种不同碳糊电极上的电化学行为
从图3A中的曲线a可以看出,在单纯的CPE上,UDMH的氧化需要较高的正电位,从而出现了无规则的阳极反应曲线,反应过程与电解动力学相关。相比之下,从图3B中曲线c和图3C中曲线e可以看出,UDMH的氧化均发生在很低的正电位,伴随着产生阴极峰电流和阳极峰电流。但是对比PB/CPE,虽然PB/TNTs/CPE所得的峰电流更小,但是从总体的电流变化范围可以看出,TNTs作为PB的载体时,能够增强电子转移的效率和速率,从而使PB的催化活性得到增强,检测的灵敏度更高。另一方面,对比图3B中曲线d和图3C中曲线f可以看出,PB/CPE氧化峰的电位要大于PB/TNTs/CPE,也说明了TNTs使电子转移的效率增强。
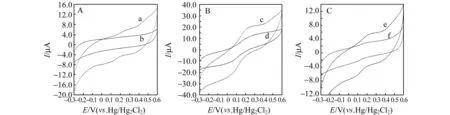
图3 碳糊电极(A)、PB修饰碳糊电极(B)和PB/TNTs修饰碳糊电极(C)的循环伏安图Fig.3 Cyclic voltammograms for CPE(A),PB/CPE(B) and PB/TNTs/CPE(C)(b),(d) and (f) are in 0.1 mol·L-1 KCl solution;(a),(c) and (e) are in 0.1 mol·L-1 KCl solution containing 10 mg·L-1 UDMH.
2.4 扫描速率的影响
由图4A可以得出峰电流Ip与扫描速率的平方根v1/2呈线性关系,可知UDMH的氧化过程本身是受扩散控制的,同Andrieux和Saveant描述的情况相同[17],整体不可逆的电子转移传递系数α可以从图4B得出,根据以下方程式计算:Ep=b/2log(v)+k,其中,b为塔菲尔斜率,Ep对logv的点的截距是恒定的。因此,b=2(0.059/αn),为64 mV(图4B),α=1.84,而用同样的方法计算的PB修饰碳糊电极的α=0.30,结果表明UDMH的电催化氧化速率决定于单电子转移的具体过程,而且PB/TNTs/CPE的电子传递系数要高于PB/CPE。
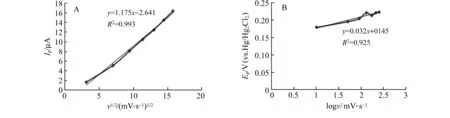
图4 (A)阳极峰电流与v1/2的线性关系曲线;(B)塔菲尔曲线Fig.4 (A) Plot of anodic peak currents against the square root of scan rate;(B) Tafel plot
2.5 pH值的影响
通过添加少量的稀HCl或NaOH溶液,调节0.1 mol·L-1KCl溶液的pH值在1.3~9.3的范围内变化,对比研究pH值对UDMH在PB/TNTs/CPE和PB/CPE上的电化学响应的影响。图5显示了峰电流和pH值之间的关系。从图中可以观察到,随着pH值的增大,PB/TNTs/CPE的峰电流响应一直增加,而PB/CPE在中性溶液中峰电流的响应最大,两者不同的原因一方面是由于UDMH为弱碱性,在酸性环境中生成盐。另一方面是由于在碱性溶液(pH>8)中PB由氢氧根离子分解,但是PB/TNTs/CPE中PB由TNTs负载,分离相对较少,而且PB粒子不在电极表面,很少脱落,分解反应并且可逆。因此,PB/TNTs/CPE在碱性溶液中使用时峰电流响应会随pH的增大而增加。
2.6 线性范围和检测限
图6为PB/TNTs/CPE在含不同浓度的UDMH的KCl溶液中的循环伏安图(扫速100 mV·s-1),在0.3~100 mg·L-1范围内,UDMH的浓度和峰电流有较好的线性关系,回归方程为:y=0.063x+7.925(R2=0.974),检测限为2.6×10-5g·L-1,低于PB/CPE的检测限4.6×10-5g·L-1。
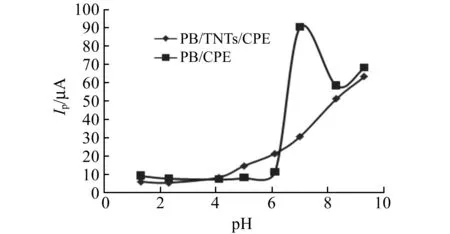
图5 pH值在1.3~9.3的范围内PB/CPE和PB/TNTs/CPE在60 mg·L-1偏二甲肼存在时的响应Fig.5 The corresponding change of oxidation peak current of PB/TNTs/CPE and PB/CPE in KCl solution containing 60 mg·L-1 UDMH at pH value of 1.3-9.3
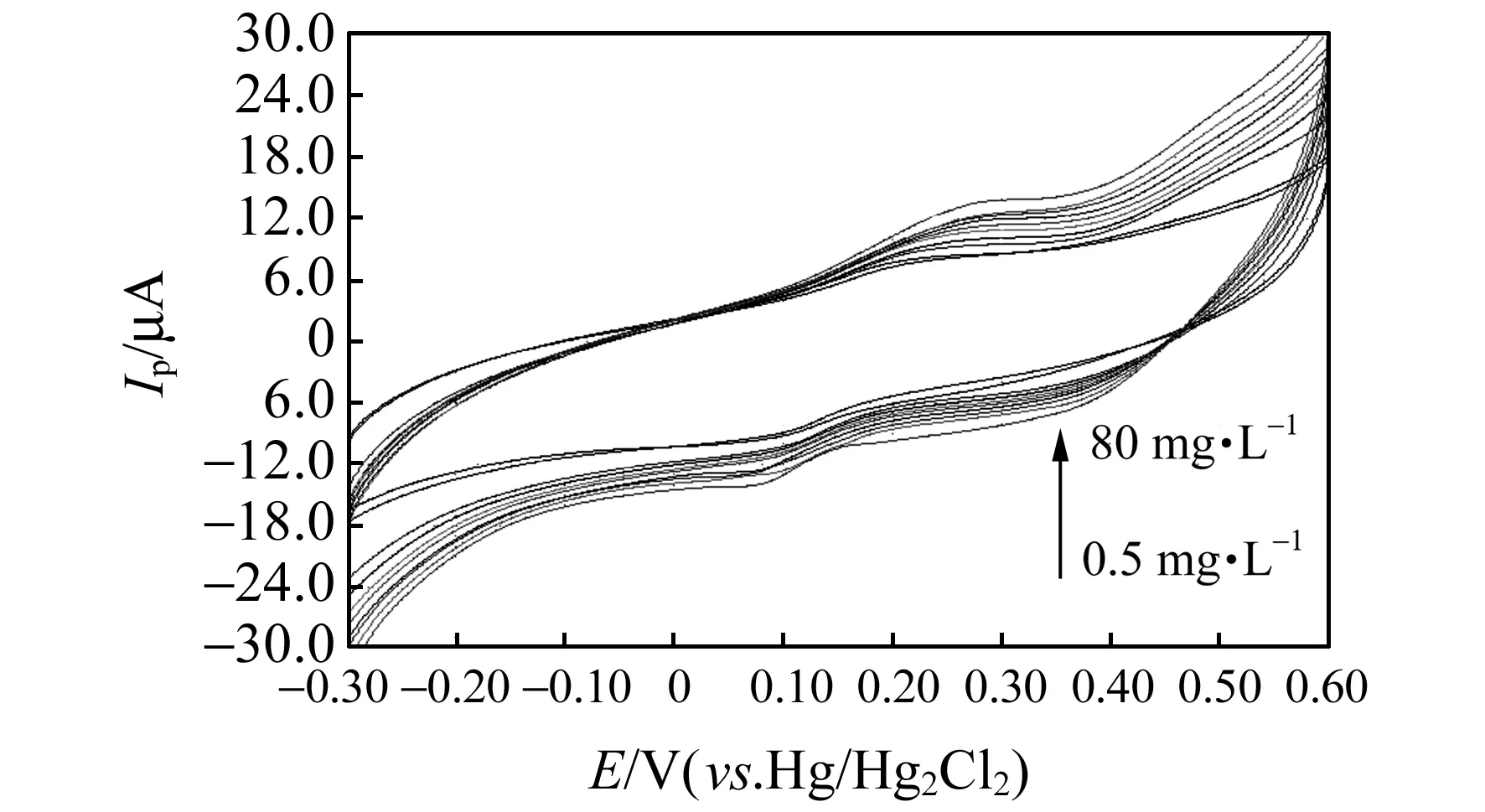
图6 PB/TNTs/CPE在不同浓度的偏二甲肼溶液中的循环伏安图Fig.6 Cyclic voltammograms of PB/TNTs/CPE at different concentration of UDMH
2.7 电极电流响应灵敏度
图7是两个目标电极的时间-电流响应曲线。从图中可以看出,电极都有较好的灵敏度,PB/TNTs/CPE的灵敏度要显著高于PB/CPE,这与TNTs可以增加电子转移效率有关。
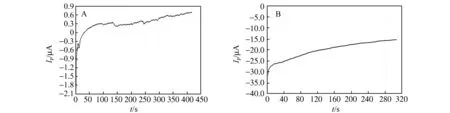
图7 (A)PB/CPE在0.1 mol·L-1KCl溶液中连续滴加40 mg·L-1UDMH时的计时-电流曲线[16];(B)PB/TNTs/CPE在40 mg·L-1的UDMH中连续滴加0.1 mol·L-1 KCl时的计时-电流曲线Fig.7 (A) Amperometric response of PB/CPE for successive addition of 40 mg·L-1 UDMH into 0.1 mol·L-1 KCl solution;(B) Amperometric response of PB/TNTs/CPE for successive addition of 0.1 mol·L-1KCl solution into 40 mg·L-1 UDMH
2.8 干扰实验
当UDMH浓度为10 mg·L-1时,考察了潜在的干扰物质(测量误差小于3%),实验结果见表1。

表1 在最优条件下一些外界离子对10 mg·L-1的UDMH测定的影响Table 1 Effect of some foreign ions on the determination of 10 mg·L-1 UDMH under optimal conditions
Note:the max permissible molar concentration ratio is the ratio of the molar concentration of external ions and UDMH.
2.9 实际水样中UDMH的测定
采用标准加入法,在雨水和自来水水样中分别加入不同浓度的UDMH,制备两种不同的水样,用PB/TNTs/CPE在上述实验条件下进行分析检测,结果见表2。回收率在82.5%到92%之间,表明该方法基本适用于来自不同基体的实际样品分析。

表2 水样中UDMH的测定结果Table 2 The measurement results of UDMH in water samples
3 结论
基于PB/TNTs/CPE的电流传感器可以用于UDMH溶液的测定。结果表明,对比PB/CPE,PB/TNTs/CPE的优势明显,在碱性溶液中和有干扰离子时更加稳定、灵敏度更高、有相对较宽的检测范围和较低的检测限。
