聚乙烯醇增敏藏红T为探针的共振瑞利散射法 测定阴离子表面活性剂
2017-10-15马彩娟钟卫烨张伟爱
马彩娟, 钟卫烨, 张伟爱, 白 研*
(广东药科大学公共卫生学院,广东广州 510310)
阴离子型表面活性剂具有良好的乳化、发泡、渗透、去污和分散性能,尤其是十二烷基苯磺酸钠(SDBS)在日常生活和工农业生产中使用较为广泛[1]。然而,含有SDBS等阴离子表面活性剂的工业废水和生活废水大量排入水体,将严重影响水质,甚至造成水生生物死亡。亚甲蓝分光光度法[2]为检测水体中的阴离子表面活性剂的国家标准方法(GB/T7494-1987),但其前处理操作繁琐,且萃取用的氯仿为有毒溶剂。目前,测定环境中阴离子表面活性剂较为普遍的方法是高效液相色谱法[3]、分光光度法[4 - 5]和流动注射分析法[6 - 7]。共振瑞利散射(RRS)法是近年发展起来的一种新的分析技术,可用于痕量金属[8]、药物[9]、蛋白质[10]及阴离子表面活性剂[11]的研究和测定,该方法操作简便、快速且灵敏度较高。
藏红T(Safranine T,ST)是一种具有吩嗪结构的碱性染料,具有大共轭结构,在弱酸性条件下可电离出阳离子,曾作为荧光探针[12]用于阴离子表面活性剂的测定。聚乙烯醇(PVA)分子链上含有大量羟基使其具有较强的亲水性、成膜性,可用作分散剂和胶体保护剂。本文研究了在PVA存在下,SDBS与ST形成离子缔合物的光谱特性、适宜的反应条件和影响因素,建立了一种测定阴离子表面活性剂的RRS新方法。该方法灵敏度高,稳定性和选择性好,可用于环境水样中阴离子表面活性剂的测定。
1 实验部分
1.1 主要仪器与试剂
F-2500型荧光分光光度计,UV-3010型紫外分光光度计(日本,日立公司);pHS-3C型精密酸度计(上海虹益仪器仪表有限公司);CP124C型电子天平(上海奥豪斯有限公司)。所用玻璃仪器均以5%HNO3浸泡24 h以上,再以三次蒸馏水冲洗干净、备用。
0.50 g/L SDBS标准储备溶液:准确称取SDBS(Aladdin公司)0.050 g,溶于水并定容于100 mL容量瓶中,SDBS工作液为20.00 μg/mL,临用前配制。1.0×10-3mol/L的ST溶液:准确称取0.088 g ST(Sigma公司),溶于水中,定容于250 mL容量瓶中。1%PVA溶液:准确称取1.0 g PVA(天津市百世化工有限公司,平均聚合度为1750±50)于100 mL容量瓶中,以水定容至刻度后,超声1 h,混匀,备用。柠檬酸-柠檬酸钠缓冲溶液:由0.1 mol/L柠檬酸与0.2 mol/L柠檬酸钠溶液按不同比例配制而成。实验所用试剂均为优级纯或分析纯,实验用水均为三次蒸馏水。
1.2 实验方法
于10 mL比色管中,依次加入pH=4.0的柠檬酸-柠檬酸钠缓冲溶液1.00 mL,适量SDBS工作液或者样品测试液,ST溶液0.50 mL,PVA溶液0.20 mL,以水稀释至刻度,于荧光分光光度计上,以λex=λem进行同步扫描,记录RRS光谱,再于λ=340 nm处,分别记录各测试液的共振瑞利散射强度IRRS和试剂空白的共振瑞利散射强度I0,计算ΔI=IRRS-I0。
2 结果与讨论
2.1 共振瑞利散射光谱

图1 ST-SDBS-PVA体系的RRS光谱Fig.1 RRS spectra of ST-SDBS-PVA system A:1.cST:0.5×10-4 mol/L,cPVA:0.02%;2.cSDBS:2.5 μg/mL;3 - 7.cST:0.5×10-4 mol/L,cPVA:0.02%,cSDBS:1.0,2.0,3.0,4.0,5.0 μg/mL.B.1.cST:0.5×10-4 mol/L;2.cST:0.5×10-4 mol/L,cSDBS:1.0 μg/mL.C.The calibration curve of ST-SDBS-PVA system.
采用F-2500型荧光分光光度计,分别对柠檬酸-柠檬酸钠缓冲溶液中不同体系以λex=λem进行同步扫描,得到RRS光谱图。由图1可知,ST-PVA(图1A曲线1)、SDBS(图1A曲线2)及ST(图1B曲线1)本身的RRS强度较弱(由于响应值较弱,前两条曲线几乎重合)。但在弱酸性条件下,SDBS与ST可通过静电引力和疏水作用力结合形成离子缔合物,引起RRS强度增强,且在571 nm处有新的RRS峰产生(图1B曲线2)。在此基础上加入PVA后,PVA可在一定时间内稳定吸附于ST-SDBS缔合物表面,形成吸附层使分子团体积增大,使RRS强度明显增强,同时聚合物分子团与水溶液的亲和性较好,阻止了微粒间的聚集,使体系在溶液中的稳定性增强[13](图1A曲线3~7)。体系的最大RRS峰位于340 nm处,在一定浓度范围内,RRS强度随着SDBS浓度的增加呈线性增加趋势,线性关系良好(图1C)。
2.2 实验条件优化

图2 pH对RRS强度的影响Fig.2 Effect of pH on RRS intensity cST:0.5×10-4 mol/L;cPVA:0.02%;cSPBS:3.0 μg/mL.
2.2.1缓冲体系及pH分别试验了柠檬酸-柠檬酸钠、NaH2PO4-柠檬酸、B-R、HAc-NaAc四种缓冲溶液对体系RRS的影响。结果表明,体系在柠檬酸-柠檬酸钠缓冲溶液中ΔI最大,当用柠檬酸-柠檬酸钠作为缓冲介质时,pH值对RRS的影响见图2,结果表明最佳pH值范围是3.0~5.0,实验选定pH为4.0,且通过实验得出缓冲溶液的最佳用量为1.00 mL。
2.2.2ST加入量考察了ST加入量对RRS强度的影响。当ST浓度为0.3×10-4~1.0×10-4mol/L时,ΔI达到最大。当ST用量过多或过少均会导致ΔI值降低。当ST用量过少,体系反应不完全,RRS强度降低;当ST用量过多,过量的染料分子易在溶液中发生自聚集现象,不利于其与SDBS的缔合作用,从而导致RRS强度降低。故实验选用ST浓度为0.5×10-4mol/L。
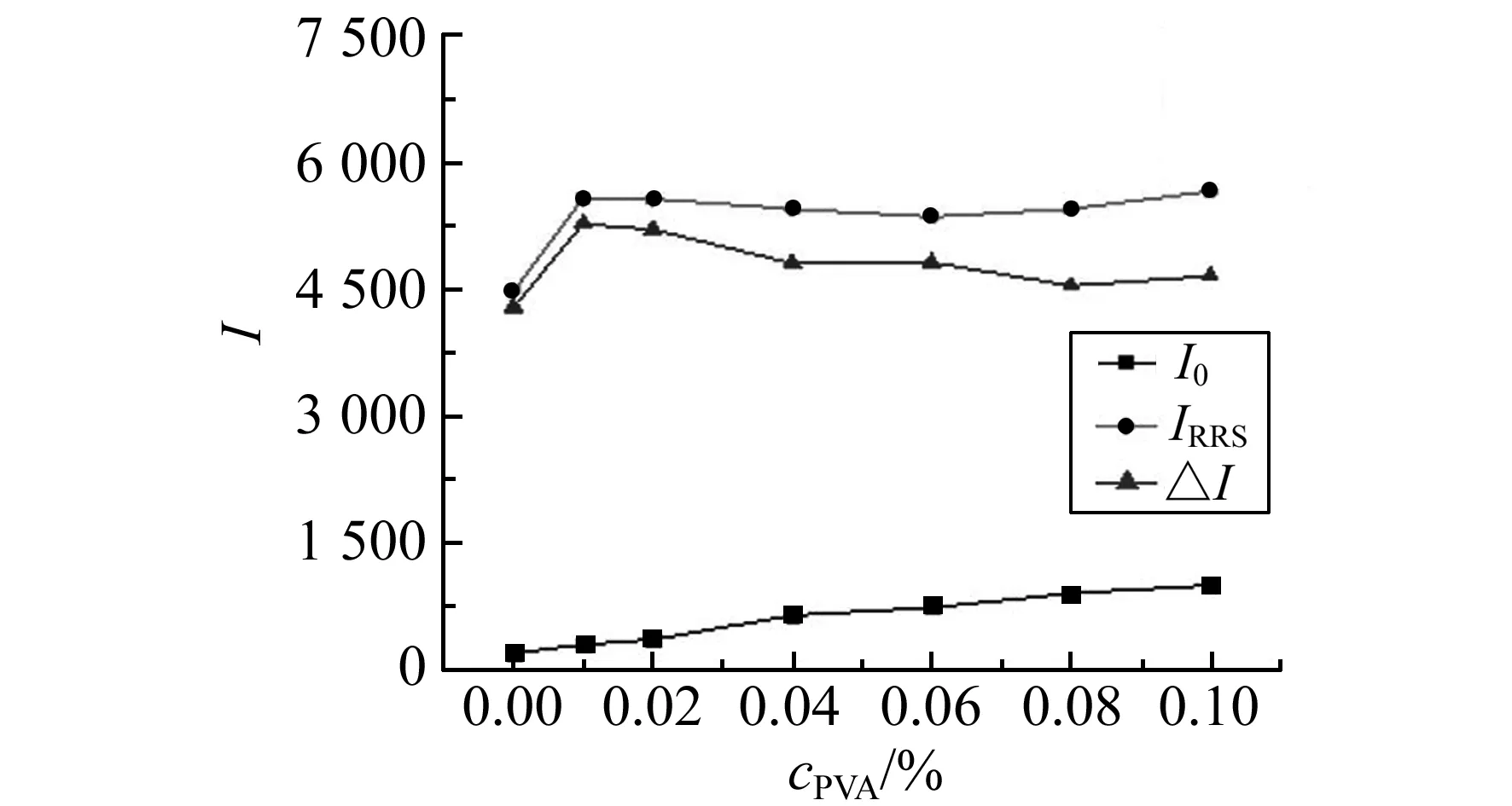
图3 聚乙烯醇用量的影响Fig.3 Effect of PVA concentration on RRS intensity cST:0.5×10-4 mol/L;cSDBS:3.0 μg/mL.
2.2.3表面活性剂的选择及用量考察了PVA,吐温20和吐温80三种表面活性剂对体系RRS的影响。结果发现,加入吐温20或吐温80,体系的RRS值均降低,仅PVA对ST-SDBS体系具有显著增敏效果,且体系稳定性提高。进一步考察了PVA用量的影响,见图3。当在体系中加入一定量PVA时,RRS值明显增大。实验选用PVA浓度为0.02%时,即PVA(1%)的用量为0.20 mL。
2.2.4温度与反应时间实验表明,温度对该反应的影响较大,随着温度的升高,ΔI下降,反映出SDBS与ST的缔合为放热过程,因而反应应在室温下进行。实验还考察了体系的反应速度及稳定时间,该体系在5 min内反应完全,90 min内ΔI保持相对稳定。
2.2.5离子强度的影响实验中用NaCl(0~0.2 mol/L)考察了离子强度对该体系RRS值的影响。结果表明,当NaCl浓度在0~0.05 mol/L时,ΔI逐渐降低;当NaCl浓度为0.05~0.20 mol/L时,ΔI保持相对稳定。在实验条件下,带负电荷的SDBS与带正电荷的ST通过静电引力和疏水作用结合,当体系中引入NaCl时,由于Na+和Cl-的加入,使SDBS与ST之间静电作用减弱,干扰SDBS-ST缔合物的形成,ΔI降低。但是,随着离子强度的增加,大分子疏水作用也逐渐增大[14],有利于SDBS与ST的缔合,因此,体系的ΔI保持相对稳定。
2.2.6试剂加入顺序的影响实验考察了试剂加入顺序对体系的共振瑞利散射强度的影响。实验表明,加入顺序按缓冲液+SDBS+ST+PVA时ΔI最大,即先加入缓冲溶液,为体系提供一个利于反应的弱酸性条件,使SDBS与ST结合形成离子缔合物,再加入PVA与前两者结合,形成三元复合物。也可推断PVA大分子在ST-SDBS缔合物表面形成吸附层,分子团体积增大,灵敏度提升。因而选择该加入顺序进行后续实验。
2.3 线性关系与检出限
在最佳实验条件下,测定不同浓度SDBS时的ΔI,并绘制标准曲线。结果表明:在0.15~5.0 μg/mL浓度范围内,ΔI与SDBS浓度c呈良好线性关系,线性方程为:ΔI=1824.2c-192.18(c:μg/mL),相关系数R2=0.9969,检出限为8.6 ng/mL。因而,构建的RRS新方法操作简便、快速,成本较低,适于痕量阴离子表面活性剂的测定。
2.4 方法的选择性
按实验方法考察了环境水体中常见金属离子对SDBS测定结果的影响,计算产生约≤±5%相对误差(RE)时加入各共存物质的浓度结果,见表1。通过抗干扰实验得出,0.5 mL的Na2EDTA(0.01 mol/L)可以掩蔽10倍Fe3+、Hg2+、Pb2+、Cd2+,5倍Al3+、Ba2+、Zn2+、Mn2+的干扰。Ca2+的干扰可加入草酸形成难溶物质后,过滤去除。
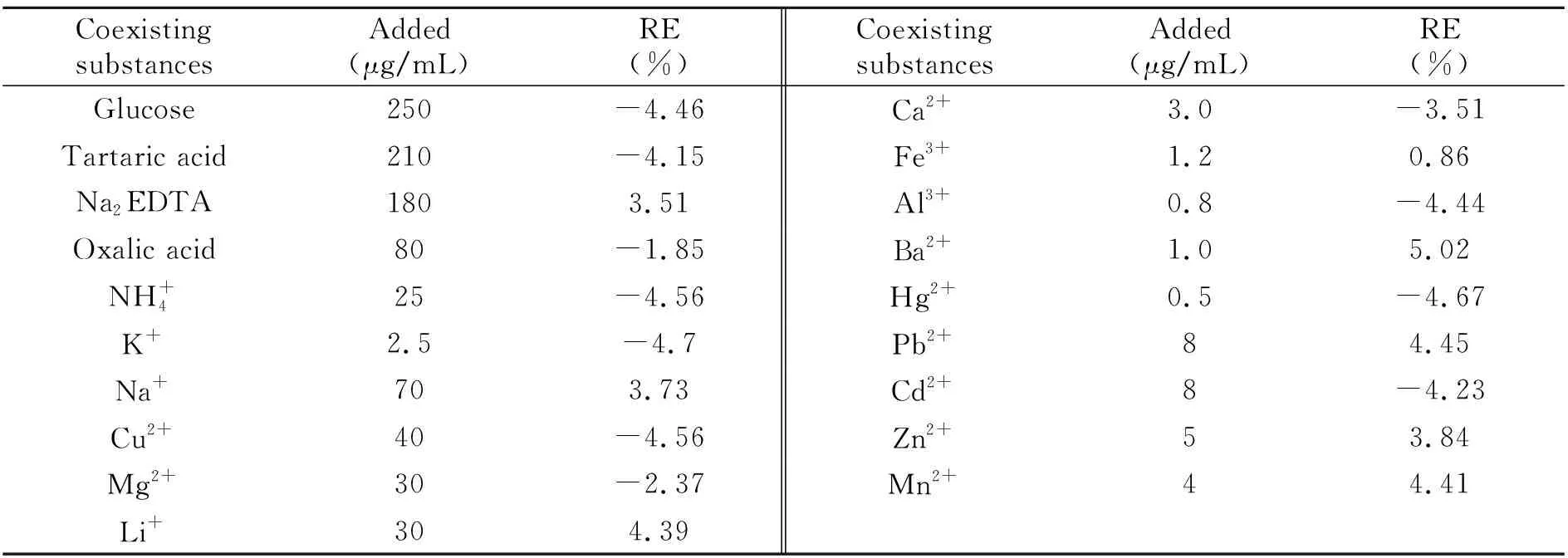
表1 共存离子的影响(SDBS 2.00 μg/mL)Table 1 Effects of coexistent substances
2.5 实际样品分析
2.5.1样品的预处理用采水装置分别于广州A码头污染点及其下游50 m、下游150 m取得水样,过滤除去不溶杂质,然后分别准确吸取50.00 mL水样,用柠檬酸调pH至4.0,再加入1.00 mL草酸(1 000 μg/mL)溶液,摇匀并静置30 min后过滤,以水定容至100 mL,作为样品测试液。
2.5.2样品含量的测定于10 mL比色管中,按先后顺序加入pH=4.0的柠檬酸-柠檬酸钠缓冲液1.00 mL,一定体积的SDBS标准溶液或样品测试液,ST溶液0.50 mL,PVA溶液0.20 mL,0.50 mL Na2EDTA(0.01 mol/L)溶液。由于实际样品中离子强度均较大,为消除因样品与标准溶液之间离子强度的差异给测定结果带来的误差,在制备标准系列时,需向各标准管中另外加入0.10 mol/L NaCl溶液,再用水稀释至刻度,摇匀,各平行三份。于F-2500型荧光分光光度计上测定各管的共振瑞利散射强度,并计算各样品测试液中阴离子表面活性剂含量。根据样品测试液含量(表2),计算得出广州A码头污染点及其下游50 m、下游150 m的SDBS平均含量分别为0.790、0.500、0.120 μg/mL,相对标准偏差(RSD)分别为1.46%、1.22%、1.89%。同时,对样品进行加标回收率试验,平均回收率为94.1%~95.7%,RSD为0.95%~1.50%。测定结果与国家标准方法亚甲蓝分光光度法对照,通过SPSS22.0的T检验法分析表明,本法结果与国家标准方法测定结果差异无统计学意义(α=0.05)。

表2 回收率实验Table 2 Recovery test of samples
3 机理分析
3.1 体系散射光增强的原因分析
共振瑞利散射具有瑞利散射和电子吸收光谱的双重特性,灵敏度与选择性都有所提高[15]。该体系共振瑞利散射峰位于吸收带上,因此瑞利散射能够吸收光能而产生再散射,即产生一种散射增强效应[16]。其次,SDBS与ST均有良好的水溶性,当带负电的SDBS与带正电的ST结合后,两者电荷被中和,失去亲水性,离子缔合物的疏水芳基骨架与水相之间易形成疏水界面,使散射强度增大。又由于具有大共轭分子结构的染料ST与SDBS通过静电引力结合后,电荷间的束缚作用以及分子体积的增大,限制了染料分子中芳基的转动,增加了分子的平面性和刚性,也使散射强度增强。
3.2 PVA的增敏、增稳机制
PVA的加入对体系的灵敏度有很大的提升,原因在于PVA可认为是支链上带有仲醇结构的长链线性大分子化合物,在一定浓度下可形成三维立体的空间结构,使ST-SDBS缔合物处于其空间结构中,分子团稳定性提高。另一方面,PVA支链上的活性氢可与ST-SDBS缔合物的氮原子形成氢键,在缔合物表面形成稳定的吸附层,使分子团体积增大,根据共振瑞利散射公式[17],体系的分子团体积增加,共振瑞利散射强度增强。同时,PVA支链的羟基结构与水介质有良好的亲和性,此支链结构在水溶液中形成空间位垒,阻止微粒的聚集,提高体系的稳定性。
4 结论
建立了以ST为探针,PVA为增敏剂的测定阴离子表面活性剂的共振瑞利散射法。该方法操作简便、灵敏度高,线性范围宽,样品测定结果与国家标准方法亚甲蓝分光光度法相比较差异无统计学意义,且避免了标准方法中使用氯仿多次萃取可能带来的误差以及对环境的二次污染,更有利于应用普及。
