水分胁迫下黄瓜叶片光响应过程的模拟*
2017-10-13张曼义1杨再强1侯梦媛1
张曼义1,杨再强1,2**,侯梦媛1
水分胁迫下黄瓜叶片光响应过程的模拟
张曼义,杨再强,侯梦媛
(1.南京信息工程大学灾害预报预警与评估协同创新中心,南京 210044;2.南京信息工程大学江苏省农业气象重点实验室,南京210044)
以黄瓜品种“博新525”(Boxin525)为试材,设置4个土壤水分处理,即正常灌溉CK(土壤相对湿度为70%~80%)、轻度胁迫T1(土壤相对湿度为60%~70%)、中度胁迫T2(土壤相对湿度为50%~60%)、重度胁迫T3(土壤相对湿度为35%~45%),利用LI-6400便携式光合仪测定不同水分处理下黄瓜叶片的光响应曲线,采用直角双曲线、非直角双曲线、指数和叶子飘等4种光响应模型对黄瓜叶片光响应过程进行模拟,运用统计方法进行模拟效果评价,以探讨水分胁迫对黄瓜叶片光响应过程的影响。结果表明:(1)水分胁迫导致黄瓜叶片净光合速率(Pn)下降,当光合有效辐射PAR(photosynthetically active radiation)为800µmol·m·s时,T1、T2和T3处理叶片Pn分别比CK下降17.92%、26.49%和50.00%。实测与模拟的光响应曲线对水分胁迫的响应趋势一致,随着胁迫程度增加,Pn-PAR曲线变化幅度减小。(2)水分胁迫显著影响黄瓜叶片的光响应曲线参数。4种模型模拟的叶片初始量子效率均随胁迫加重呈先升高后降低的变化趋势;叶片暗呼吸速率以T2处理最高;4种模型计算的T1、T2和T3处理叶片光饱和点平均值较CK分别下降24.28%、31.99%和38.33%,叶片最大净光合速率平均值分别降低23.88%、33.19%和55.78%。(3)CK处理的黄瓜叶片光响应曲线模拟值偏离程度及光响应曲线参数的平均相对误差均最低,水分胁迫降低了黄瓜叶片光响应曲线的模拟效果。(4)4种模型模拟效果以叶子飘模型最佳,其后依次为指数模型、非直角双曲线模型、直角双曲线模型。研究认为水分胁迫显著影响黄瓜叶片的光响应过程,降低黄瓜叶片的光合能力。
黄瓜;光合作用;水分胁迫;光响应模型;光响应参数
黄瓜(L.)是中国主要蔬菜之一,属葫芦科植物,喜温喜湿,不耐旱涝。近年来,中国黄瓜栽培发展迅速,种植面积已达125.3万hm。黄瓜植株和果实对水分需求量大,且对水分供给要求较为苛刻。水分过多造成空气湿度过高,容易导致植株发生病害,水分过少抑制植株生长。光合作用是自然界最重要的碳素同化作用,地球上一切构建生命结构的物质和维持生命活动所消耗的能量,绝大部分来自于这一过程。因此,研究水分胁迫下黄瓜光合作用的光响应过程,对于了解黄瓜光合特性与土壤水分间的关系,以及黄瓜生育期间的水分管理具有重要意义。
近年来,国内外关于水分胁迫对植物光合特性的影响已有一些报道。Zhang等研究发现水分胁迫影响百合光响应曲线的变化幅度,净光合速率随胁迫加重而降低。Liu等研究发现水分胁迫降低冬小麦净光合速率,但轻度胁迫提高小麦的水分利用效率。郭春芳等研究发现水分胁迫导致植物最大净光合速率、表观量子效率和光饱和点显著降低,光补偿点和暗呼吸速率升高。胡宏远等研究表明,水分胁迫导致赤霞珠葡萄净光合速率、蒸腾速率、胞间CO浓度和气孔导度呈下降趋势。
目前,国内外学者建立了许多光响应模型来模拟植物的光响应过程,如直角双曲线模型、非直角双曲线模型、指数模型和叶子飘模型等。关于光响应过程的模拟研究多集中于林木和大田作物等,现有研究对蔬菜的光响应过程模拟研究鲜有报道。因蔬菜存在生长周期短、采收期长的特点,与林木和大田作物的遗传特性不同,因此,本研究通过温室水分控制试验,采用直角双曲线模型、非直角双曲线模型、指数模型和叶子飘模型对水分胁迫下黄瓜叶片的光响应过程进行模拟,旨在为黄瓜的水分管理、高产优质栽培提供科学依据。
1 材料与方法
1.1 试验设计
试验于2016年4-6月在南京信息工程大学Venlo型温室(30.04°N,116.78°E)进行。试验温室顶高5.0m,肩高4.5m,宽9.6m,长30.0m,南北走向。供试土壤为中壤土,容重1.32g·cm,pH7.4,有机质18.4g·kg,全氮0.79g·kg,全磷0.75g·kg,田间持水量为32.45%(体积含水量)。试材为黄瓜品种“博新525”,于2月28日营养钵内育苗,正常管理浇水,选取长势一致的三叶一心黄瓜幼苗,定植于温室水泥池苗床中(长8m,宽1m),缓苗一周后开始水分胁迫试验。试验设置4个土壤水分处理:正常灌溉CK(土壤相对湿度为70%~80%)、轻度胁迫T1(土壤相对湿度为60%~70%)、中度胁迫T2(土壤相对湿度为50%~60%)、重度胁迫T3(土壤相对湿度为35%~45%)。试验期间,用置于土壤内15cm深度处的土壤水分传感器(ECH2O,Decagon Devices Inc.,USA)实时监测土壤体积水分含量及水势,测量数据用EM50数据采集器(EM50,Decagon Devices Inc.,USA)自动采集并存储,采集频率为60s一次,存储每30min的平均值。按照设定的处理目标,每天计算各处理所需灌溉的水量,用滴灌设备进行灌溉。试验采用随机区组设计,每个处理3次重复,共12个小区,小区间用塑料薄膜隔开防止渗漏。黄瓜苗定植行距30cm,株距40cm,每小区定植5株苗,每个处理15株。每小区每两周施用复合肥4g(N:P:K= 10:9:8)。
1.2 光响应曲线测定
于成熟期从每个处理的3个小区内分别选取1株健康植株,于晴天上午9:00-11:00用便携式光合作用测量系统(LI-6400,LI-COR Biosciences,USA)测量黄瓜植株倒数第5-7位成熟叶片。利用光合作用测量系统的人工光源控制叶室内光合有效辐射(PAR)分别为0、50、100、150、200、400、600、800、1000、1200、1500、1800μmol·m·s,在每个光强水平下测量并记录光合速率及相关要素数值,测量期间叶室内空气温度在25±1℃范围内,大气CO浓度在380±5μmol·mol范围内。叶片在每个PAR水平下适应120s,并进行3次重复读数。根据实测点绘制Pn-PAR光响应曲线,并估算相应的暗呼吸速率(Rd)、光补偿点(LCP)、光饱和点(LSP)、最大净光合速率(Pmax)和表观量子效率(α)。
1.3 不同处理15cm土层土壤水分动态
试验期间不同处理土壤水分动态如图1所示。由图可见,试验期间不同处理土壤水势、体积含水量呈波动性变化,但均在设置水平范围内,随着胁迫加重,土壤水势和体积含水量逐渐降低。
1.4 数据处理与分析方法
1.4.1 数据处理
利用Excel2010进行制图,采用SPSS21.0软件进行光响应曲线的非线性回归分析、单因素方差分析和Duncan法(α=0.05)多重比较。
1.4.2 光响应曲线模拟模型
(1)直角双曲线模型
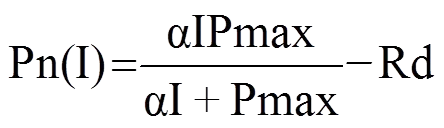
式中,Pn(I)为净光合速率(µmol·m·s),I为光合有效辐射(µmol·m·s),Pmax为最大净光合速率(µmol·m·s),Rd为暗呼吸速率(µmol·m·s),α为初始量子效率(µmol·mol)。若模型模拟较好,则用式(2)计算光补偿点LCP(µmol·m·s)。
(2)
因式(1)无极值,故用y=Pmax与弱光下(PAR≤200μmol·m·s)的线性方程的交点作为光饱和点LSP(µmol·m·s)。
(2)非直角双曲线模型

式中,θ为光响应曲线的凸度。0<θ≤1,其它参数意义同式(1)。若模型模拟较好,则用式(4)计算LCP。即
(4)
因式(3)无极值,故用y=Pmax与弱光下(PAR≤200μmol·m·s)的线性方程的交点作为光饱和点LSP。
(3)指数模型

(6)
式中,计算LSP时,假设LSP对应的Pn为0.9Pmax,其它参数意义同式(1)。
(4)叶子飘模型

(8)
(9)

式中,α、β、γ为系数,其它参数含义同式(1)。
1.4.3 模拟效果评价
利用均方根误差RMSE(Root Mean Squared error)、相对误差RE对模拟值与实测值间的符合度进行分析,RMSE、RE值越小,表明模拟值与实测值间的偏差越小,模型模拟效果越好。

式中,P为净光合速率实测值(μmol·m·s);为净光合速率模拟值(μmol·m·s);n为样本容量;i为模拟值和实测值的样本序号。
(12)
式中,y为光响应曲线参数实测值;为光响应曲线参数模拟值;n为样本容量。
2 结果与分析
2.1 水分胁迫下黄瓜叶片净光合速率的光响应过程
由图2可见,水分胁迫下黄瓜叶片净光合速率(Pn)对光强的响应趋势与正常灌溉条件下(CK)表现一致,即当光合有效辐射(PAR)≤200µmol·m·s时,Pn随PAR的增加呈线性增加,当PAR>200µmol·m·s时,Pn随PAR的增加幅度减缓,并逐渐趋于平稳。但是,从曲线的变化幅度看,水分胁迫条件下与CK有明显区别,且不同胁迫程度下也有显著差异。具体表现为,在光合有效辐射较低区域,CK处理中叶片Pn增加速度最快、幅度最大,达到最大值时对应的PAR值(即光饱和点)最高,在1500µmol·m·s附近;轻度胁迫处理(T1)的黄瓜光饱和点接近CK但曲线总体低于CK,中重度胁迫处理(T2、T3)中Pn达到最大值时PAR值则相对较低,当PAR>800µmol·m·s时Pn即达到了最大值,并开始出现光抑制现象。在同一PAR水平下,Pn随胁迫加重而降低。当PAR=800µmol·m·s时,T1、T2和T3处理Pn分别比CK下降了17.92%、26.49%和50.00%。说明水分胁迫处理显著影响了黄瓜叶片Pn的光响应过程,且胁迫程度越重,Pn随PAR变化幅度越小。
注:短线表示均方差。下同
Note: The short bar is mean square error. The same as below
2.2 水分胁迫下黄瓜叶片光响应过程的模拟
4种模型对水分胁迫下黄瓜叶片光响应过程的模拟如图3所示,由图可见,水分胁迫下黄瓜叶片光响应模拟曲线与CK处理基本一致,各处理光响应模拟曲线均随PAR增加呈先迅速后缓慢增加,与实测光响应曲线的变化趋势基本一致。从曲线变化幅度来看,水分胁迫下光响应模拟曲线与CK处理有显著差异。PAR较低时,CK处理叶片Pn随PAR上升速度最快,胁迫处理叶片Pn上升速度随胁迫加重逐渐降低。说明水分胁迫显著影响黄瓜叶片光响应过程的模拟,随着胁迫加重,Pn模拟值随PAR变化幅度减小。
2.3 水分胁迫下黄瓜叶片光响应曲线参数模拟
4种模型对水分胁迫下黄瓜叶片光响应曲线参数的模拟如表1所示。由表可见,与CK处理相比,4种模型叶片初始量子效率(α)随胁迫加重呈先升高后降低的趋势。T1、T2处理下4种模型得出的α均高于CK,T3处理下除直角双曲线模型得出的α高于CK外,其它均低于CK。不同模型得出的叶片光补偿点(LCP)对水分胁迫的响应情况不同。非直角双曲线和叶子飘模型得出的LCP在T1处理下低于CK,而在T2、T3处理下高于CK;直角双曲线模型得出的LCP在T1、T3处理下较CK分别下降14.64%、15.66%,而在T2处理下与CK无显著差异;指数模型得出的LCP在T1处理下与CK无明显差异,但在T2、T3处理下较CK升高37.36%、14.80%。4种模型得出的叶片暗呼吸速率(Rd)对水分胁迫的响应一致,均为T2处理的Rd最高,T1、T3处理的Rd较CK有不同程度的升高或下降。4种模型得出的叶片光饱和点(LSP)在水分胁迫处理下均有不同程度降低。从4种模型的平均值来看,T1、T2和T3处理叶片LSP较CK分别下降24.28%、31.99%和38.33%。随胁迫程度加重,4种模型得出的最大净光合速率(Pmax)均逐渐降低,T1、T2和T3处理叶片Pmax较CK分别降低23.88%、33.19%和55.78%。
综合4种模型来看,水分胁迫下叶片α随胁迫加重先升高后降低;不同模型下各处理叶片LCP变化不同;中度胁迫处理下叶片Rd最高;不同模型叶片LSP、Pmax随胁迫加重均有不同程度降低。

表1 各处理黄瓜叶片光响应参数模拟值与实测值的比较
注:“-”表示无数据,标注的数据为约数。下同。
Note: “-” indicates no data,noted data are approximate number. The same as below. α: initial quantum efficiency; LCP: light compensation point; Rd: dark respiration rate; LSP: light saturation point; Pmax: maximum net photosynthetic rate.
2.4 水分胁迫下黄瓜叶片光响应曲线模拟效果评价
利用光响应模拟曲线的均方根误差(RMSE)、决定系数(R)及光响应参数实测值与模拟值的相对误差(RE)对各模型模拟效果进行定量评价。由图4可见,不同处理Pn模拟值偏离程度不同。整体来看,CK处理Pn模拟值偏离程度较低,而胁迫处理Pn模拟值仅在Pn处于低值区时,与实测值符合较好。随着实测值的增加,Pn模拟值偏离程度逐渐升高。由表2可见,各处理下4种模型的R较高,均在0.9以上。其中CK处理下模型的R平均值最接近1,为0.9986;而胁迫处理下模型的R平均值低于CK,T1、T2和T3处理下模型的R平均值分别为0.9951、0.9888和0.9894。不同处理下模型的RMSE平均值不同。其中,CK处理下模型的RMSE平均值最小,为0.3152;随着胁迫加重,各胁迫处理下模型RMSE平均值分别为0.4571、0.5784和0.3671。
由表3可见,就不同模型中光响应参数的平均相对误差(MRE)来看,CK处理下光响应参数的MRE最低,在直角双曲线、非直角双曲线、指数和叶子飘模型中依次为0.359、0.276、0.131和0.109。T1、T2和T3处理光响应参数MRE较CK分别升高45.02%、83.49%和16.47%。从单个光响应参数MRE来看,指数模型下叶片光补偿点(LCP)的MRE最低,为0.220。其中T1、T2处理叶片LCP的RE较CK分别降低42.42%、9.52%;T3处理叶片LCP的RE较CK高32.90%。非直角双曲线模型下叶片暗呼吸速率(Rd)的MRE最低,为0.054。T1处理叶片Rd的RE较CK升高22.44%,T2处理叶片Rd的RE是CK的2.47倍,T3处理叶片Rd的RE较CK降低13.16%。叶子飘模型下光饱和点(LSP)和最大净光合速率(Pmax)的MRE最低,分别为0.199、0.008。CK处理叶片LSP的RE为0.154,T1处理叶片LSP的RE较CK降低37.01%,T2、T3处理叶片LSP的RE较CK分别升高72.73%、82.47%。CK处理叶片Pmax的RE为0.006,T1处理叶片Pmax的RE是CK处理的2.17倍,T2处理叶片Pmax的RE较CK升高16.67%,T3处理叶片Pmax的RE较CK降低16.67%。此外,综合比较,叶子飘模型的平均RMSE最低,直角双曲线、非直角双曲线、指数和叶子飘模型所有参数MRE分别为0.382、0.322、0.166和0.149。模型模拟效果以叶子飘模型最佳,其次分别为指数模型、非直角双曲线模型、直角双曲线模型。

表2 各处理黄瓜叶片不同光响应模型的决定系数和均方根误差

表3 各处理黄瓜叶片光响应参数模拟值与实测值的相对误差
Note: RE: relative error; MRE: mean relative error.
综上来看,水分胁迫降低了4种模型对黄瓜叶片光响应曲线的模拟效果,4种模型下CK处理叶片光响应曲线的模拟效果最好。模型模拟效果以叶子飘模型最佳,其后依次为指数模型、非直角双曲线模型、直角双曲线模型。
3 结论与讨论
光合作用是植物生长发育的基础,光响应曲线的测定及模拟是研究植物光合作用的重要手段之一。本研究利用4种模型对水分胁迫下黄瓜叶片的光响应过程进行模拟,光响应模拟曲线的走势和变化幅度与实测光响应曲线基本一致。本研究中,水分胁迫下黄瓜叶片的光响应过程与正常灌溉条件下(CK)变化一致,净光合速率(Pn)随光合有效辐射(PAR)呈先迅速后缓慢增加。各处理光响应曲线变化幅度不同,随着胁迫加重,Pn随PAR变化幅度减小,在同一PAR水平下,Pn随胁迫加重而降低。这与前人研究结果基本一致。
通过光响应曲线获得的初始量子效率、光补偿点、光饱和点、暗呼吸速率和最大净光合速率等光响应曲线参数对于判定植物的光合能力有着重要意义。初始量子效率(α)代表光响应曲线的初始斜率,此外,也有学者提出用表观量子效率来表征植物利用光能的能力。实际计算中常用植物在光补偿点(LCP)的量子效率来表示。本研究认为,4种模型下黄瓜叶片α随胁迫加重呈先升高后降低的趋势,其原因是适当的水分胁迫有利于提高光能利用率,但水分胁迫过重,会导致叶片α下降,光能利用率降低。而陆燕元等研究认为随水分胁迫加剧,甘薯对光能的利用效率逐渐降低,这可能是因为作物种类不同。不同模型对黄瓜叶片LCP模拟结果不同,徐梦莎等研究表明,随着胁迫加重,杏LCP逐渐增加。可能是由于随着水分胁迫加重,植物生物膜结构受损伤,细胞膜脂化作用加重,导致植物对弱光的利用能力下降。而李强等研究表明,随着胁迫加重,荻的LCP持续下降,这反映了不同植物对光环境的适应力不同。本研究中叶片暗呼吸速率Rd以T2处理下最高,其它处理叶片较CK有不同程度的升高和下降,这说明中度胁迫提高了黄瓜叶片的暗呼吸速率。本研究中,水分胁迫下黄瓜叶片光饱和点(LSP)、最大净光合速率(Pmax)均有不同程度降低,这与众多学者研究一致,说明水分胁迫导致黄瓜叶片利用强光的能力降低,这是因为水分胁迫破坏了RUBP羧化酶活性,降低了电子传递效率,从而影响黄瓜叶片碳同化过程。
本研究采用均方根误差(RMSE)、决定系数(R)和相对误差(RE)来评价光响应曲线的模拟效果。结果表明,CK处理下叶片光响应曲线模拟效果最好,水分胁迫下光响应曲线模拟的R降低,RMSE和RE值升高。非直角双曲线模型得出的Rd平均相对误差(MRE)最小,这与鲁肃等研究结果一致。本研究中指数模型计算的LCP平均相对误差最小,而刘泽彬等研究发现叶子飘模型对叶片LCP的模拟效果最好,于艳梅等则认为非直角双曲线模型对叶片LCP的模拟效果最好,这可能是因为不同植物对光响应模型的适应性不同。本研究中,叶片LSP、Pmax利用叶子飘模型模拟效果最佳,这与众多学者的研究结果一致。
本研究表明水分胁迫会导致黄瓜叶片光响应曲线变化幅度减小,并显著影响光响应曲线参数。直角双曲线模型、非直角双曲线模型、指数模型和叶子飘模型对CK处理叶片光响应曲线的模拟效果均优于水分胁迫处理。本文只考虑了土壤水分对黄瓜叶片光响应过程的影响,但由于土壤水分不同,土壤蒸发和植株蒸腾必然会有差异,导致土壤温度发生变化,本研究没有考虑土壤温度对叶片光响应过程的影响,今后需要在控制环境下进一步开展研究。此外,本研究结果仅为定性结论,要量化水分胁迫对黄瓜光响应曲线的影响,并使之模型化,尚需设置更多的水分处理进行进一步的试验研究。但本研究结果为明确不同土壤水分水平下黄瓜光合作用对光强的响应特性,并在此基础上开展水分调控提供了参考,也为下一步定量模拟水分胁迫对黄瓜生长的影响奠定了基础。
[1]李建伟.黄瓜栽培新技术[M].北京:中国农业出版社,2004.
Li J W.New technology of cucumber cultivation[M].Beijing: China Agriculture Press,2004.(in Chinese)
采用SPSS 19.0统计学软件,对10个变量指标(年龄、性别、肿瘤直径、血管包裹程度、病理分级、肿瘤形态、手术切除程度、肿瘤质地、是否脑干水肿及术前KPS评分)与肿瘤复发是否相关进行单因素分析,将具有统计学意义的因素作为自变量,以是否复发作为因变量,采用Pearsonχ2检验进行非条件Logistic回归分析。P<0.05为差异具有统计学意义。
[2]田婧,郭世荣.黄瓜的高温胁迫伤害及其耐热性研究进展[J].中国蔬菜,2012,18:43-52.
Tian J,Guo S R.Research progress on high-temperature stress injury and heat tolerance of cucumber[J].China Vegetables, 2012,18:43-52.(in Chinese)
[3] 张立军,梁宗锁.植物生理学[M].北京:科学出版社,2007.
Zhang L J,Liang Z S.Plant physiology[M].Beijing:Science Press,2007.(in Chinese)
[4] Elfadl M A,Luukkanen O.Field studies on the ecological strategies of Prosopies juliflora in a dryland ecosystem Ⅰ:a leaf gas exchange approach[J].Journal of Arid Environments, 2006,66(1):1-15.
[5] Rahmati M,Davarynejad G H,GénaRd M,et al.Peach water relations,gas exchange,growth and shoot mortality under water deficit in semi-arid weather conditions[J].Plos One, 2015,10(4):1-19.
Zhang Y Z,Li H D, Li X,et al.Effects of light intensity and water stress on leaf photosynthetic characteristics of ginger[J]. Acta Horticulturae Sinica,2013,40(11):2255-2262.(in Chinese)
[7] Zhang Y J,Xie Z K,Wang Y J,et al.Effect of water stress on leaf photosynthesis, chlorophyll content,and growth of oriental Lily[J].Russian Journal of Plant Physiology,2011, 58(5):844-850.
[8] Liu E K,Mei X R,Yan C R,et al.Effects of water stress on photosynthetic characteristics,dry matter translocation and WUE in two winter wheat genotypes[J].Agricultural Water Management,2016,167:75-85.
[9] 郭春芳,孙云,张木清.土壤水分胁迫对茶树光合作用-光响应特性的影响[J].中国生态农业学报,2008,16(6):1413-1418.
Guo C F,Sun Y,Zhang M Q.Effects of soil water stress on photosynthetic light response curve of tea plant()[J].Chinese Journal of Eco-Agriculture,2008,16(6): 1413-1418.(in Chinese)
[10] 林琭,汤昀,张纪涛,等.不同水势对黄瓜花后叶片气体交换及叶绿素荧光参数的影响[J].应用生态学报,2005,26(7): 2030-2040.
Lin L,Tang J,Zhang J T,et al.Effects of different water potentials on leaf gas exchange and chlorophyll fluorescence parameters of cucumber during post-flowering growth stage[J].Chinese Journal of Applied Ecology,2015,26(7): 2030-2040.(in Chinese)
[11] 胡宏远,王振平.水分胁迫对赤霞珠葡萄光合特性的影响[J].节水灌溉,2016,2:18-22.
Hu H Y,Wang Z P.The effects of water stress on photosynthetic characteristics of Cabernet Sauvignon[J]. Water Saving Irrigation,2016,2:18-22.(in Chinese)
[12] 滕振宁,方宝华,刘洋,等.镉对不同品种水稻光合作用的影响[J].中国农业气象,2016,37(5):538-544.
Teng Z N,Fang B H,Liu Y,et al.Effects of Cd on photosynthesis of different rice varieties[J].Chines Journal of Agrometeorology,2016,37(5):538-544.(in Chinese)
[13] Retkute R,Unna S,Smith R,et al.Exploiting heterogeneous environments:does photosynthetic acclimation optimise carbon gain in uctuating light[J].Journal of Experimental Botany,2015,66(9):2437-2447.
[14] Xu J Z,Yu Y M,Peng S Z,et al.A modified nonrectangular hyperbola equation for photosynthetic light-response curves of leaves with different nitrogen status[J].Photosynthetica, 2014,52(1):117-123.
[15] Zheng Y,Zhao Z,Zhou J J,et al.Evaluations of different leaf and canopy photosynthesis models:a case study with black locust() plantations on a Loess Plateau[J].Pakistan Journal of Botany,2012,44(2):531-539.
[16] Ye Z P.A new model for relationship between irradiance and the rate of photosynthesis in[J].Photosynthetica, 2007,45:637-640.
[17] Xia J H,Zhang G C,Zhang S Y,et al.Photosynthetic and water use characteristics in three natural secondary shrubs on Shell Islands,Shandong,China[J].Plant Biosystems, 2014,148(1): 109-117.
[18] 郎莹,张光灿,张征坤,等.不同土壤水分下山杏光合作用光响应过程及其模拟[J].生态学报,2011,31(16):4499-4508.
Lang Y,Zhang G C,Zhang Z K,et al.Light response of photosynthesis and its simulation in leaves ofL.under different soil water conditions[J].Acta Ecologica Sinca,2011,31(16):4499-4508.(in Chinese)
[19] 徐俊增,彭世彰,魏征,等.不同供氮水平及水分调控条件下水稻光合作用光响应特征[J].农业工程学报,2012,28(2): 72-76.
Xu J Z,Peng S Z,Wei Z,et al.Characteristics of rice leaf photosynthetic light response curve with different water and nitrogen regulation[J].Transactions of the CSAE,2012,28(2): 72-76.(in Chinese)
[20] 李永秀,张富存,杨再强.光合作用模型在长江下游冬麦区的适用性研究[J].中国农业气象,2011,32(4):588-592.
Li Y X,Zhang F C,Yang Z Q.Applicability of different models for winter wheat in the lower Yangtze River[J]. Chinese Journal of Agrometeorology,2011,32(4):588-592.(in Chinese)
[21] 冷寒冰,秦俊,叶康,等.不同光照环境下荷花叶片光合光响应模型比较[J].应用生态学报,2014,25(10):2855-2860.
Leng H B,Qin J,Ye K,et al.Comparison of light response models of photosynthesis inleaves under different light conditions[J].Chinese Journal of Applied Ecology,2014,25(10):2855-2860.(in Chinese)
[22] 叶子飘,于强.一个光合作用光响应新模型与传统模型的比较[J].沈阳农业大学学报,2007,38(6):771-775.
Ye Z P,Yu Q.Comparison of a new model of light response of photosynthesis with traditional models[J].Journal of Shenyang Agricultural University,2007,38(6):771-775.(in Chinese)
[23] 王海珍,韩路,徐雅丽,等.干旱胁迫下胡杨光合光响应过程模拟与模型比较[J].生态学报,2017,37(7):1-10.
Wang H Z,Han L,Xu Y L,et al.Simulated photosynthesis responses of populus euphratica during drought stress using light-response models[J].Acta Ecologica Sinca,2017,37(7): 1-10.(in Chinese)
[24] 赵丽,贺玉晓,魏雅丽,等.干热河谷区土壤水分胁迫下扭黄茅光合作用光响应过程及其模拟[J].中国农学通报,2016, 32(17):115-121.
Zhao L,He Y X,Wei Y L,et al.Light response characteristics of photosynthesis ofand its simulation under soil water stress in dry-hot walley[J].Chinese Agricultural Science Bulletin,2016,32(17):115-121.(in Chinese)
[25] 陈卫英,陈真勇,罗辅燕,等.光响应曲线的指数改进模型与常用模型比较[J].植物生态学报,2012,36(12):1277-1285.
Chen W Y,Chen Z Y,Luo F Y,et al.Comparison between modified exponential model and common models of light-response curve[J].Chinese Journal of Plant Ecology, 2012,36(12):1277-1285.(in Chinese)
[26] 王荣荣,夏江宝,杨吉华,等.贝壳砂生境干旱胁迫下杠柳叶片光合光响应模型比较[J].植物生态学报,2013,37(2):111-121.
Wang R R,Xia J B,Yang J H,et al.Comparison of light response models of photosynthesis in leaves ofunder drought stress in sand habitat formed from seashells[J].Chinese Journal of Plant Ecology,2013,37(2): 111-121.(in Chinese)
[27] 陆燕元,马焕成,李昊民,等.土壤干旱对转基因甘薯光合曲线的响应[J].生态学报,2015,35(7):2155-2160.
Lu Y Y,Ma H C,Li H M,et al.Light response characteristics of photosynthetic of transgenic sweet potato under drought stress[J].Acta Ecologica Sinica,2015,35(7):2155-2160.(in Chinese)
[28] 徐梦莎,李芳东,朱高浦,等.水分胁迫对仁用杏苗期光合生理和生物量积累的影响[J].热带作物学报,2016,37(4):700-708.
Xu M S,Li F D,Zhu G P,et al.The responses of photosynthetic physiology and biomass accumulation of sweet kernel-apricot() seedling to soil water stress[J].Chinese Journal of Tropical Crops,2016, 37(4):700-708.(in Chinese)
[29] 张曼义,杨再强,侯梦媛.土壤水分胁迫对设施黄瓜叶片光合及抗氧化酶系统的影响[J].中国农业气象,2016,38(1): 21-30.
Zhang M Y,Yang Z Q,Hou M Y.Effects of soil water stress on photosynthetic characteristics and antioxidant enzyme system of cucumber leaves in greenhouse[J].Chinese Journal of Agrometeorology,2016,38(1):21-30.(in Chinese)
[30] 李强,王非,何淼,等.土壤水分胁迫对荻光合生理特性的影响[J].草业科学,2013,30(7):1031-1035.
Li Q,Wang F,He M,et al.Effects of soil water stress on photosynthetic characteristics of[J].Pratacultural Science,2013,30(7):1031-1035.(in Chinese)
[31] 云文丽,侯琼,王海梅,等.不同土壤水分对向日葵光合光响应的影响[J].应用气象学报,2014,25(4):476-482.
Yun W L,Hou Q,Wang H M,et al.Effects of different soil moistures on photosynthetic characteristics of sunflower[J]. Joural of Applied Meteorological Science,2014, 25(4):476- 482.(in Chinese)
[32] 李泽,谭晓风,卢锟,等.干旱胁迫对两种油桐幼苗生长、气体交换及叶绿素荧光参数的影响[J].生态学报,2017,37(5): 1-10.
Li Z,Tan X F,Lu K,et al.Influence of drought stress on the growth,leaf gas exchange and chlorophyll fluorescence in two varieties of tung tree seedlings[J].Acta Ecologica Sinica,2017,37(5):1-10.(in Chinese)
[33] 鲁肃,张宇清,吴斌,等.水分胁迫下油蒿光合光响应过程及其模拟[J].北京林业大学学报,2014,36(1):55-61.
Lu S,Zhang Y Q,Wu B,et al.Simulation of photosynthesis- light response process inunder water stress[J].Journal of Beijing Forestry University,2014,36(1): 55-61.(in Chinese)
[34] 刘泽彬,程瑞梅,肖文发,等.不同淹水时间下中华蚊母树光响应特征及其模型比较[J].应用生态学报,2015,26(4): 1083-1090.
Liu Z B,Cheng R M,Xiao W F,et al.Light response characteristics of photosynthesis and model comparison ofin different flooding durations[J].Chinese Journal of Applied Ecology,2015,26(4):1083-1090.(in Chinese)
[35] 于艳梅,徐俊增,彭世彰,等.不同水分条件下水稻光合作用的光响应模型的比较[J].节水灌溉,2012,10:30-32.
Yu Y M,Xu J Z,Peng S Z,et al.Evaluation of photosynthesis light response model for rice leaf under different water conditions[J].Water Saving Irrigation,2012,10:30-32.(in Chinese)
[36] Fang L D,Zhang S Y,Zhang G C,et al.Application of five light-response models in the photosynthesis of×cv.‘
[37] Zu Y G,Wei X X,Yu J H,et al.Response in the physiology and biochemistry of Korean pine () under supplementary UV-B radiation[J].Photosynthetica,2011, 49(3):448-458.
Simulation of Light Response of Photosynthesis ofL. Leaves under Water Stress
ZHANG Man-yi, YANG Zai-qiang, HOU Meng-yuan
(1. Collaborative Innovation Center on Forecast and Evaluation of Meteorological Disasters, Nanjing University of Information Science & Technology, Nanjing 210044, China; 2. Jiangsu Key Laboratory of Agricultural meteorology, Nanjing University of Information Science & Technology, Nanjing 210044)
ForL. (cv.), four different soil moisture levels were designed, which were normal irrigation (CK, soil relative humidity was 70%-80%), light water stress (T1, soil relative humidity was 60%-70%), moderate water stress (T2, soil relative humidity was 50%-60%) and severe water stress (T3, soil relative humidity was 35%-45%), respectively. Light response curves of cucumber leaves were measured under each treatment using LI-6400 portable photosynthesis system. Four different models (i.e. rectangular hyperbola, non-rectangular hyperbola, exponential and Ye Z P model) were applied to simulate light response curves of cucumber leaves, and the simulation effects were evaluated by statistics methods. Based on the experimental data and simulation results, the effect of water stress on light response curves of cucumber was discussed. The results indicated that water stress caused decline of net photosynthetic rate (Pn), at a PAR (photosynthetically active radiation) level of 800µmol·m·s, Pn decreased by 17.92%, 26.49% and 50.00% under T1, T2 and T3 treatments, respectively, compared with CK. The simulated light response curves showed a similar trend with the measured ones in response to water stress, and the variation amplitude of Pn-PAR curve decreased as water stress aggravated. Water stress affected light response curve parameters of cucumber leaves significantly. The initial quantum efficiency of cucumber leaves derived from the four mentioned models all increased at first and dropped afterwards with the aggravation of water stress, and the dark respiration rate was the highest under T2 treatment. Compared to CK, the average light saturation point calculated by four models decreased by 24.28%, 31.99% and 38.33%, respectively, under T1, T2 and T3, and the average maximum net photosynthetic rate declined by 23.88%, 33.19% and 55.78%, respectively, under T1, T2 and T3. The deviation degree of simulated light response curve and mean relative error of light response parameters achieved the lowest under CK, and the simulation effects of light response curve were weakened by water stress. The Ye Z P model performed best in simulation of the light response curve, next was the exponential model, the non-rectangular model, and the rectangular hyperbola model was the least effective one. The study indicated water stress significantly influenced light response of photosynthesis of cucumber leaves, and reduced photosynthetic capacity of leaves.
Cucumber; Photosynthesis; Water stress; Light response model; Light response parameters
10.3969/j.issn.1000-6362.2017.10.003
张曼义,杨再强,侯梦媛.水分胁迫下黄瓜叶片光响应过程的模拟[J].中国农业气象,2017,38(10):644-654
2017-02-23
。E-mail:yzq@nuist.edu.cn
国家自然科学基金面上项目(41775104);国家公益性行业(气象)科研专项(GYHY201506001-6)
张曼义(1994-),女,硕士生,主要研究方向为设施农业气象。E-mail:915192963@qq.com
