数字化实验与化学教学的融合
——以探究乙醇与钠反应的定量实验为例
2017-10-09杨晓洁
杨晓洁 程 萍
(1南京师范大学教师教育学院 江苏南京 210097;2安徽蚌埠第九中学 安徽蚌埠 233000)
数字化实验与化学教学的融合
——以探究乙醇与钠反应的定量实验为例
杨晓洁1.2程 萍1
(1南京师范大学教师教育学院 江苏南京 210097;2安徽蚌埠第九中学 安徽蚌埠 233000)
随着计算机技术和传感技术的发展,数字化实验已经成为化学课堂有力的教学助手。文章以乙醇与钠的反应为例,将定性实验与数字化定量探究实验结合,采用转化率处理数据,让学生在心理上形成学习化学独特的四重表征,并培养学生的证据意识和推理能力。
乙醇;钠;数字化;转化率;表征
随着课程改革的不断深入,转变教学理念,改变教学模式,培养学生的化学核心素养,适应现代化教学的需求是高中化学课堂教学一直关注的问题。化学是一门以实验为基础的学科,因此在高中化学课堂教学中,不仅要重视实验教学,更要重视实验的课堂教学。教学实验与技术的发展和进步是密切相关的,随着计算机技术和传感技术的发展,数字化手持技术已经成为化学课堂有力的教学助手。如何充分发挥数字化实验的技术优势,将其成为提高学生化学核心素养有利的工具,是一个值得深思与探讨的问题。本文主要阐述在课堂教学中从乙醇与钠反应的定性实验,乙醇的球棍模型引发疑问探究乙醇的真实结构,进而合理使用数字化手持技术“探究乙醇与钠反应的定量实验”,并采用转化率处理数据。
一、乙醇与钠反应的数字化实验
1.实验仪器和药品
依据任红艳等人[1](2010)所设计的“利用手持技术改进测定乙醇分子结构实验”,结合本校的实际情况,此次教学实验,所使用到的仪器和药品有铁架台(带铁圈)、石棉网、1 mL注射器、250 mL圆底烧瓶、酒精灯、无水乙醇(已蒸馏)、金属钠、气压传感器、采集器、电脑。

图1 实验仪器和药品

图2 实验装置图
2.实验步骤
(1)在注射器中充入0.2mL无水乙醇,按图中所示组好装置,在洁净干燥的圆底烧瓶中加入约0.3g金属钠,塞上装有注射器和气压传感器的塞子。
(2)点击“开始”采集数据,通过注射器向250 mL圆底烧瓶中一次性注入0.2mL无水乙醇。
(3)当反应进行缓慢时(反应产生的蜡状乙醇钠会包裹在钠块表面,阻止反应的继续进行),用酒精灯加热大约15s,以溶解包裹在钠块表面的乙醇钠,反应继续进行。
(4)待反应停止,烧瓶完全冷却以后,点击“停止”,结束数据的采集。
(5)重复实验若干次,取三次或四次曲线求氢气产生的气压平均值。
(6)已知乙醇的密度为ρ=0.7894 g/mL,用水测法测烧瓶的体积,通过理想气体状态方程式:PV=nRT(式中P是压力;V是体积;n是气体物质的量;T是热力学温度,它和摄氏温度t的关系为T=t+273,R=8.31J·mol-1·K-1),计算得到反应产生氢气的物质的量,再求得乙醇与钠之间的物质的量之比,进而确定乙醇的结构。
二、基于数字化实验的乙醇与钠反应的课堂教学设计
1.教学内容分析
乙醇是鲁科版必修二第三章第三节的教学内容,在教材中对于这部分内容是这样呈现的:
【实验一】向试管里注入约2mL无水乙醇,再放入一小块金属钠,观察发生的现象,检验生成的气体。
乙醇能与金属钠反应生成乙醇钠并放出氢气。

可以看出,在鲁科版的教材中对于这部分内容描述是比较粗略的,相关知识点也是直接呈现的方式。但笔者认为乙醇是学生在学习有机化合物阶段所接触到的第一种含氧衍生物,在课堂中针对乙醇的结构进行深入的探究,将对学生学习有机化合物“结构决定性质”这一学科核心思想产生深刻的影响。
2.学情分析
高中阶段学生的思维主要表现为从形式逻辑思维逐步向辩证逻辑思维发展过渡,已经能够进行理论思维。随着理论思维的发展,高中生对化学实验中的各种现象的因果关系解释越来越感兴趣。高中阶段的化学实验,多以定性实验为主,定量实验不多,因此学生定量的观念和意识较为缺乏。而数字化实验突破了感性观察和只注重定性分析的局限性,直观地呈现化学实验数据的变化,从而帮助学生更深入地理解化学反应的本质和规律。本校配备了中学教学能使用到的各种传感器,在以前的化学课堂和课外活动的教学过程中,学生使用过二氧化碳传感器、pH传感器、电导率传感器等,因此学生对数字化实验并不陌生。学生的心理现状和学习经验为本节课的推进起了支撑作用。
3.教学目标
知识与技能:
(2)加深理解有机化合物“结构决定性质”的核心思想。
过程与方法:
(1)学生亲自进行实验的设计,认识数字化实验的特点。
(2)通过数字化实验结果的分析,在“宏观—微观—符号—曲线”之间建立联系。
情感态度与价值观:
(1)在实验设计和数据处理中,体会化学实验的科学性,激发探究热情。
(2)在探究过程中培养一丝不苟、实事求是的科学态度。
4.教学过程
赛努奇人物画收藏趣味倾向的形成与赛努奇本人以及整个欧洲所具有的西方文化基因与背景密切相关,他们对中国绘画所体现的中国文化、历史内容更感兴趣,收藏的趣味正是以“他者”的眼光来观照中国文化的结果。绘画在西方汉学家与收藏家的眼中更多的是历史文化的窗口,满足他们对异域异质文化的向往与探求之心。就赛努奇所藏人物画所反映的趣味来看,其所体现的情节性和东方文化的内涵,正是西方以同构的方式来了解和认识中国文化的表现。
(1)教学流程图
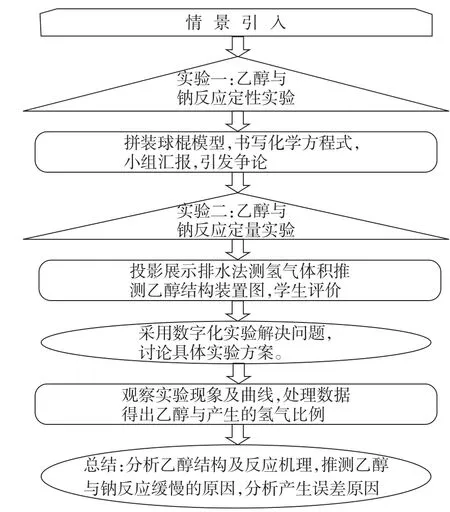
图3 教学流程图
依据实验一的宏观描述,引发问题探究乙醇的真实结构,依据实验二的曲线表征处理数据得到乙醇和氢气之间的比例,推理得到乙醇的微观结构及反应机理,进而使用化学语言表征反应过程,从而在学生心理上形成学习化学独特的四重表征。
(2)教学的具体过程如下:
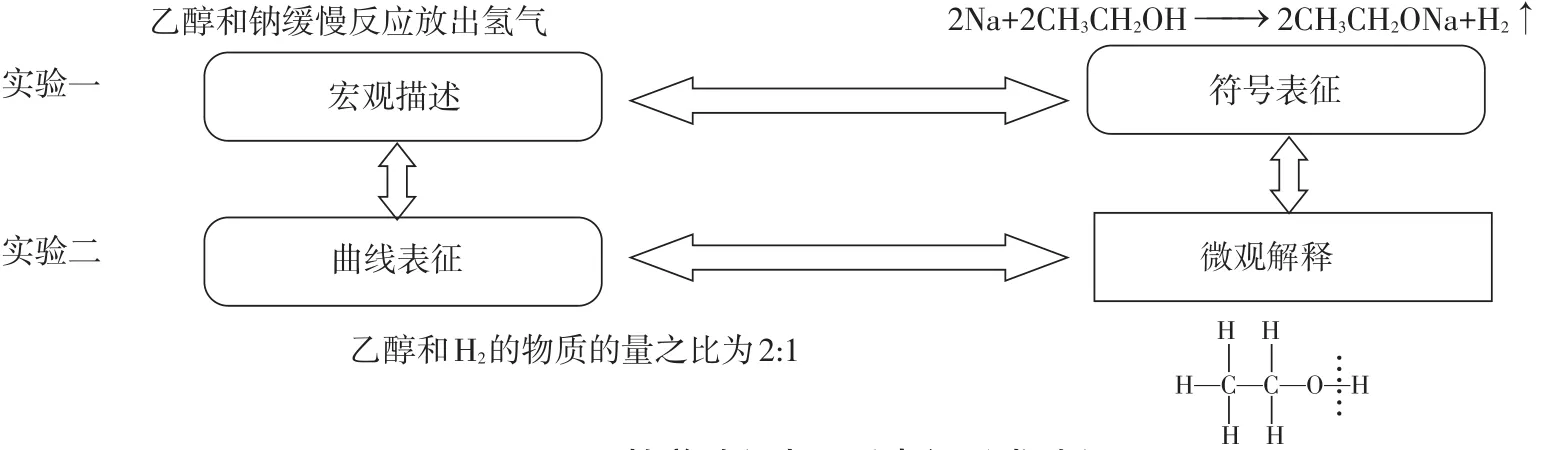
图4 教学过程中四重表征形成过程
(1)情景引入,分组实验
从试剂瓶中取出一试管的无色透明液体,让学生猜测是什么,通过观察有同学说是水,有的同学猜测是乙醇。教师说:“乙醇似水,是否与水性质相似?”。而学生对于水的化学性质中,印象最深的要数水与钠的反应。学生分组亲自动手对这个实验进行操作。具体过程如下:向青霉素瓶中加入少量无水乙醇。再取一小块钠放入青霉素瓶中,将尖嘴玻璃管的大头朝下插入乙醇中,并使之罩住钠块。钠块与乙醇反应产生的气体从玻璃管上口排出。不用验纯(尖嘴管内的少量空气可很快被生成的氢气排出),直接在尖嘴玻璃管的上口点燃气体。此时可用干燥洁净的小烧杯罩在火焰上方,结合使用澄清石灰水,以检验燃烧产物为水,从而确定生成的气体是氢气。

图5 乙醇与钠反应的定性实验
(2)拼装模型,引发质疑
通过此定性实验,学生发现乙醇和水都能与钠反应产生氢气,但乙醇的反应比水的反应明显要缓慢得多,这是什么原因呢?同学们知道结构是决定性质的,通过乙醇的分子式,利用老师事先给准备好的球棍模型,小组内的同学们拼装起乙醇可能的结构,并按照所拼装的结构推测反应过程,书写相应的化学方程式。
在进行汇报的时候,小组间的同学们起了很大的争执,不同的小组拼装出来的结构不同,所得到方程式也不同。
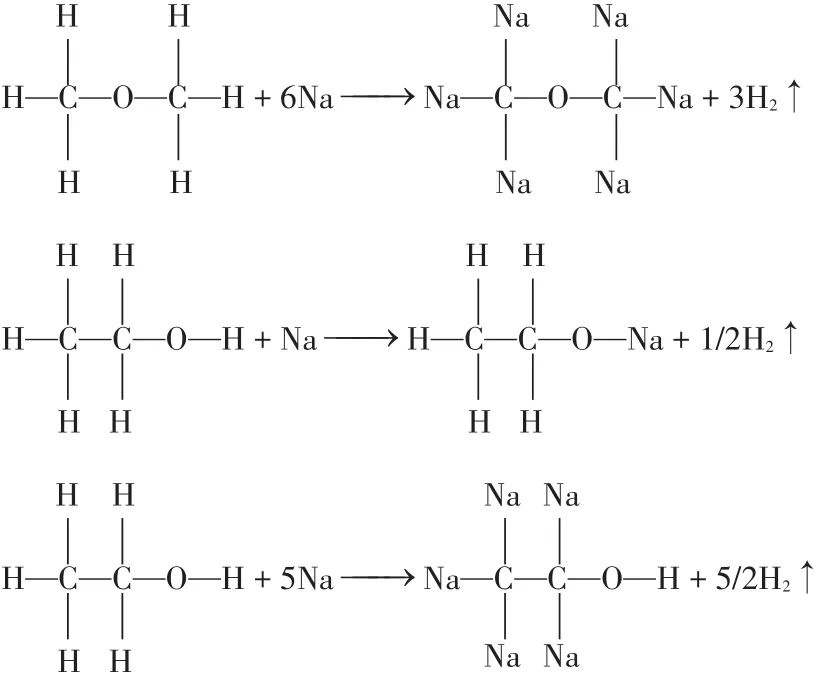
猜想一:乙醇是两个甲基通过氧原子连接的结构,在反应的过程中断裂的是C-H键,1分子的乙醇可以产生3分子的氢气,乙醇与氢气之间的物质的量之比为1:3。化学方程式如下:

图A
猜想二:乙醇是一个乙基和一个羟基所组成,在反应的过程中断裂的是O-H键,2分子的乙醇可以产生1分子的氢气,乙醇与氢气之间的物质的量之比为2:1。化学方程式如下:
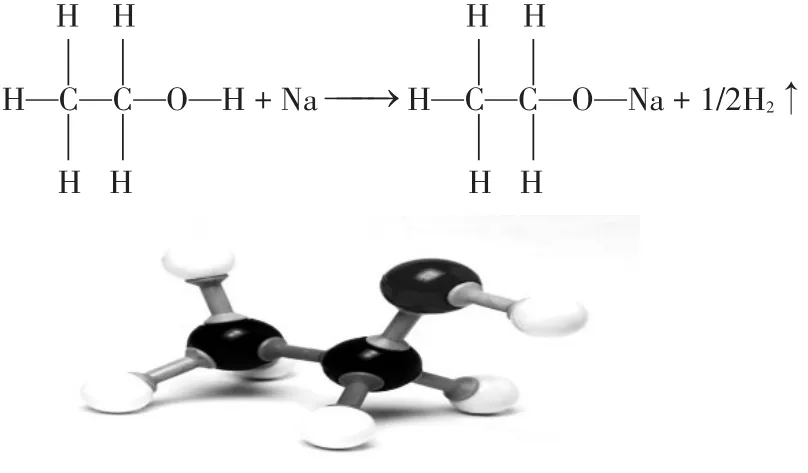
图B
猜想三:乙醇是一个乙基和一个羟基所组成,与猜想二不同的是在反应的过程中断裂的是C-H键,2分子的乙醇可以产生5分子的氢气,乙醇与氢气之间的物质的量之比为2∶5。化学方程式如下:
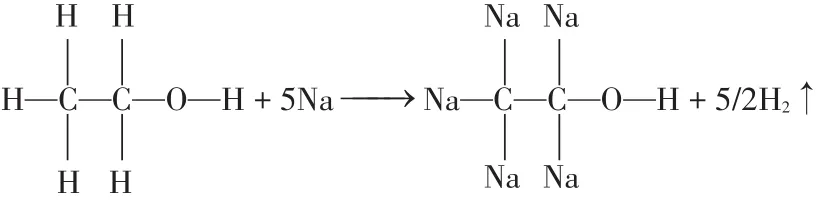
那么,乙醇的结构究竟是怎样的,在反应的过程中断裂的是哪些化学键,而乙醇与钠的反应为什么比水的缓慢?
为了解决这些问题,让学生设计实验方案。同学们认为可以利用传统仪器通过排水法测定乙醇与钠反应所产生氢气体积来确定乙醇的结构。学生展示小组内的实验设计图。教师给予评价。
展示在以前的课本和习题中利用传统仪器设计的实验装置(详见图甲、图乙)。
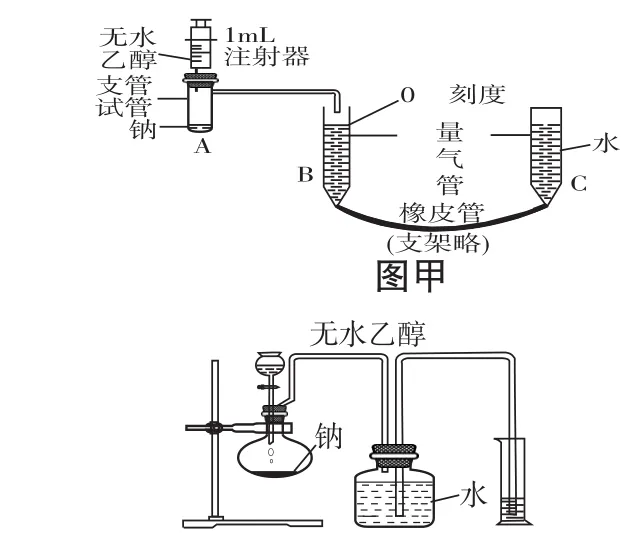
图乙
在对其原理进行了简单的说明后,同学们感觉到,排水法装置操作复杂,实验误差大。那么,可否使用手持技术来解决这个问题呢?
(3)讨论实验方案,选择实验仪器
展示学校所配备的手持技术实验传感器,同学们一致选择了气压传感器,认为气压传感器可以测定在密闭容器中反应所产生氢气的压强,此时再给学生提供理想气体状态方程,明确氢气的压强和其物质的量之间的关系。
(4)进行实验操作,得到曲线,计算结果得出乙醇与氢气的物质的量之比。
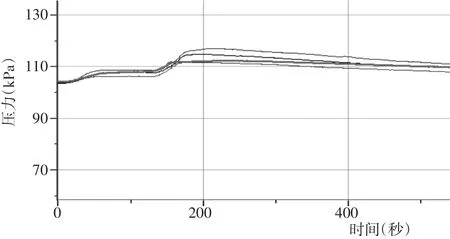
图6 测定乙醇分子结构实验压强变化曲线
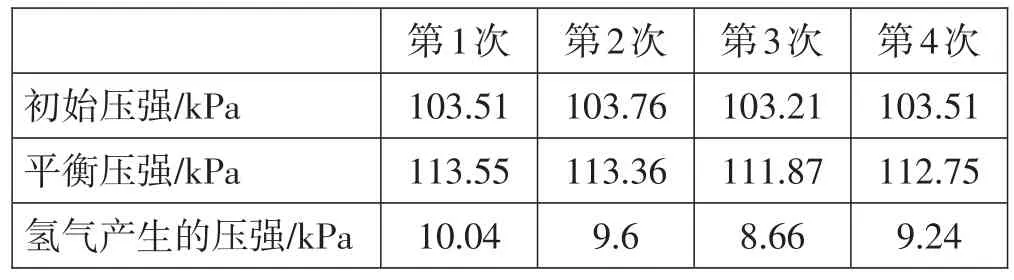
表1 测定乙醇分子结构实验数据处理表
乙醇定量0.2mL,密度为ρ=0.7894 g/mL,室内温度为15℃,学生用水测法测烧瓶的体积V=360mL,取四次合理的实验数据计算出氢气产生压强的平均值为9.385kPa,在课堂中,依据实验数据计算出来乙醇与氢气之间的物质的量之比约为2.43。在任红艳老师等[1]所做的实验中,计算出来的数据是2.05,本人做了多次实验,发现利用本校所使用的手持技术传感器,很难达到这个精确度。对于上述实验数据,很多学生出现错误判断,无法把结论和乙醇的真实结构联系起来,但是采用以下计算损失率的方式很好地解决了这个问题,学生轻松地得出了乙醇的结构和反应原理。

乙醇用量是0.00343mol,学生通过实验数据得到氢气物质的量为0.00141mol,如果反应按照第一个化学反应进行理论数据为n(H2)=0.01029mol,损失率为86.3%;如果按照第二个反应过程进行理论数据为n(H2)=0.001715mol,损失率为17.78%;如果按照第三个反应过程进行理论数据为n(H2)=0.008575mol,损失率为83.56%。学生亲眼看到了这个反应的进行,大部分乙醇被钠消耗,就算是因为加热和放热,乙醇易挥发等因素,损失率也不可能达到83%以上,因此很容易得出损失率在17.78%是合理的,进而判断出乙醇的构型和反应过程所断裂的化学键。
(5)交流实验结果,从宏观描述到微观辨析
此时所有的问题都迎刃而解,同学们争先恐后地回答小组讨论的结果。
学生1:依据实验数据可以推出1 mol乙醇分子里有1 mol氢原子可以被取代,因此可以确定乙醇与钠反应断裂的是O—H,而不是C—H键,乙醇的结构为(Ⅰ),而不是(Ⅱ),而乙醇之所以能像水一样和钠反应是因为它和水的结构类似都存在羟基。
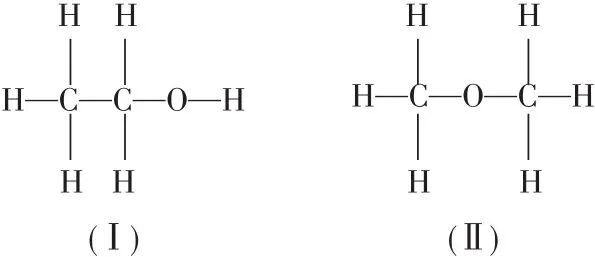
学生2:乙醇与钠的反应比水缓慢是由结构所决定的,乙醇的羟基直接连接的是烷基,正因为烷基的存在,导致氢氧键活性减弱。
最后让学生分析,我们使用数字化仪器,为什么还会产生实验误差?
学生3:由于乙醇与钠的反应是一个放热反应,而乙醇容易挥发,因此误差不可避免。为了减少误差,我们必须等到反应结束,烧瓶完全冷却以后再分析数据。
三、本教学设计的特点与教学反思
1.对本数字化实验的反思
本节课在课堂中使用数字化仪器仍然出现了误差较大的问题,其主要原因是因为本来反应使用的乙醇量就很少(只有0.2mL),而此反应是放热反应,且在反应的过程中有加热操作,反应所得到的乙醇钠会消耗附着一定的乙醇(互溶),所以乙醇的损失是不可忽略的,因此,虽然传感器的灵敏度高,最后得到的数据也是有误差的。由此,给予我们的启示是,真实的定量实验对反应条件的控制要求极高,而且一定会出现误差,如何合理减小误差本身就是实验探究的一个重要部分。
利用压强传感器进行乙醇和钠反应的定量实验对学生来说是一个很好的体验,明显提高了学生的积极性,由于气压传感器能实时准确地展现压强的变化,给学生一种感受现代化技术的强烈冲击,而且通过实验定量分析有机物的教学过程,颠覆了一向填鸭式的教学方式,因此学生也表现出了极大的兴趣,并思考相应的问题。比如在课堂中我们只做了一组实验,其它数据都是老师课前做实验所得的数据,在没有计算出合理的结果时,就有学生有这样的疑问,是不是因为老师做实验时和本节课上课时的温度是不同的,导致实验误差,这说明此实验的进行触发了学生新的思考。学生通过整个教学课堂初步体验科学家探索物质世界的过程,通过操作、思考、讨论、分析误差等活动拓展学生的视野,增强学生分析问题的能力,特别有利于学生进行探索式学习。
2.利用数字化实验帮助学生形成四重表征
数字化实验通过先进的实验设备实时、直观性地展现在化学变化的过程中有关数据的变化,可以完成从定性到定量双重的实验指标。在实验探究过程中,学生通过对一系列宏观现象以及数字化实验数据的分析,在“宏观—微观—符号—曲线”之间建立联系,在心理上形成了化学学习的独特的四重表征。
3.将定性实验与定量实验结合,培养学生的证据意识和推理能力
化学的定性实验是研究物质包含哪些成分和性质,化学的定量实验是测定物质所含各种成分的数量,从定性到定量,反映的是从现象到本质的规律,是科学发展的必然。可以说,没有对化学实验的定量研究就没有化学科学的产生与发展,因此重视和加强定量意识的教学很有必要。本节课从定性实验到定量实验的探究,不仅能提高学生的定量意识,而且能加强学生获取证据、基于证据推理的意识和能力。在探究过程中,鼓励学生从问题和假设出发,确定探究目的、设计探究方案,通过观察、实验收集证据,并基于事实和证据来推测、确定乙醇的结构,让学生充分认识证据在探究中的重要性。
4.实验教学的设计与创新,促进教师自身的专业化成长
实验是化学的灵魂,而实验的核心是设计最合理的实验方案。不仅学生需要在探究中成长,教师更要促进自身的专业化成长。教师应充分利用身边的教学资源,从传统实验仪器、微型实验仪器、手持技术仪器中寻找合适的仪器和操作,让化学实验教学更简约、更易操作、现象更明显、课堂教学更高效。而在设计、改进实验教学的过程中,如何引导学生利用实验现象和数据得出正确结论,引导学生采用不同的方式去解决问题,老师也经历了深思熟虑的过程,提升了自身探究科学本质的能力。
[1] 任红艳,洪湘琼.利用手持技术改进测定乙醇分子结构实验[J].化学教育,2010(4):71
[2] 凌崇忠,刘观赞.乙醇与钠反应实验的简易安全设计[J].化学教育,2010(7):66
[3] 马宏佳,汪学英主编.化学教学论[M],南京:南京大学出版社,2014(7):168

1008-0546(2017)10-0080-05
G633.8
B
10.3969/j.issn.1008-0546.2017.10.026
