科学知识是变化的
——以高中阶段“氧化还原反应”教学为例
2017-10-09王冬顾晔
王 冬 顾 晔
(江宁高级中学 江苏南京 211100)
科学知识是变化的
——以高中阶段“氧化还原反应”教学为例
王 冬 顾 晔
(江宁高级中学 江苏南京 211100)
“科学知识是变化的”是科学的本质的基本特征之一,结合化学史阐述了氧化还原反应的知识进阶,指出概念教学中的知识进阶不是对之前概念建构的完全否定,新的现象和发现对现行理论或概念提出挑战正是符合科学本质的。
科学的本质;氧化还原反应;科学史
IB课程在最近一次课程修订中,理化生三门学科均提出一个共同的主旨,即“科学的本质”,具体设计理念是,在关注学科知识的同时,将科学的本质充分整合到课程中去。
科学的本质是一个涉及哲学、社会学和科学史等多个方面的复杂的概念,而其包含的特征却能让我们对之有真切的认识:如“科学知识是变化的”,笔者尝试以氧化还原反应的概念进阶(图1)谈谈“科学知识是变化的”这一特征。
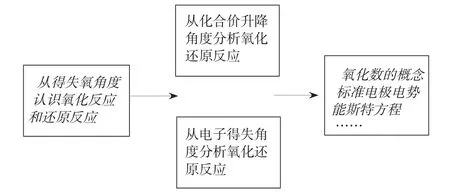
图1 氧化还原反应概念的进阶
以上氧化还原反应的概念进阶图中,未加斜体标记的为高中阶段的教学范畴,从初中一直延续到大学普通化学,氧化还原反应一直在“进阶”过程中。初中例介绍以得氧为特征的氧化反应和以失氧为特征的还原反应;进入高中后,老师会再次举例(如Zn+Cu2+原反应”是有局限性的,于是提出氧化还原反应的宏观特征——化合价的变化和微观本质——电子转移,于是一个较为完备的氧化还原反应概念建构完成了;可是到了大学学习《普通化学》或《无机化学》时发现氧化还原反应是和电化学联系在一起的,而且化合价的概念往往被氧化数代替……。笔者在多轮教学后开始反思:是不是从得失氧角度认识氧化还原反应就是不科学、不完善甚至是“过时”的?从电子转移角度认识就是科学的、完美的?
一、从得失氧角度认识氧化还原反应——近代化学的萌芽
对于反应“CuO+H2======△Cu+H2O”,H2在反应中“得氧”生成了水,则氢气发生了氧化反应;而氧化铜则因“失氧”发生了还原反应。这样的定义简单、直观,并没有科学性的失误,我们回顾一下相关科学史。
史料1:燃素学说和氧化学说
1777年,拉瓦锡重做了普利斯特里和卡文迪许的实验,精确地称量了他的试剂和产物,在1780年出版的论文《燃烧通论》中提出他的新的燃烧学说,证明物质虽然在一系列的化学反应中改变状态,物质的量在每一反应之终与每一反应之始却是相同的;燃烧和呼吸终于被证明为同类的作用,两者同是氧化,区别只在迅速与缓慢,结果都增加重量,这个重量等于化合的氧气的重量。具负重量的燃素的概念从此就从科学中消失了。
从史料1可见,拉瓦锡(图2)的氧化理论虽然停留在得失氧的阶段,但在当时却让“燃素学说”宣告失败,由此萌发出近代化学的萌芽。对氧化还原反应从“得失氧角度”进行定义不仅不是片面、落后的,相反在化学发展史上具有里程碑意义,维基百科在定义氧化还原反应(Redox Reaction)仍将之完整地呈现“The word oxidation originally implied reaction with oxygen(O2)to form an oxide(氧化物).The word reduction origi⁃nally referred to the loss in weight upon heating a metallic ore(金属矿物)such as a metal oxide to extract the metal.”
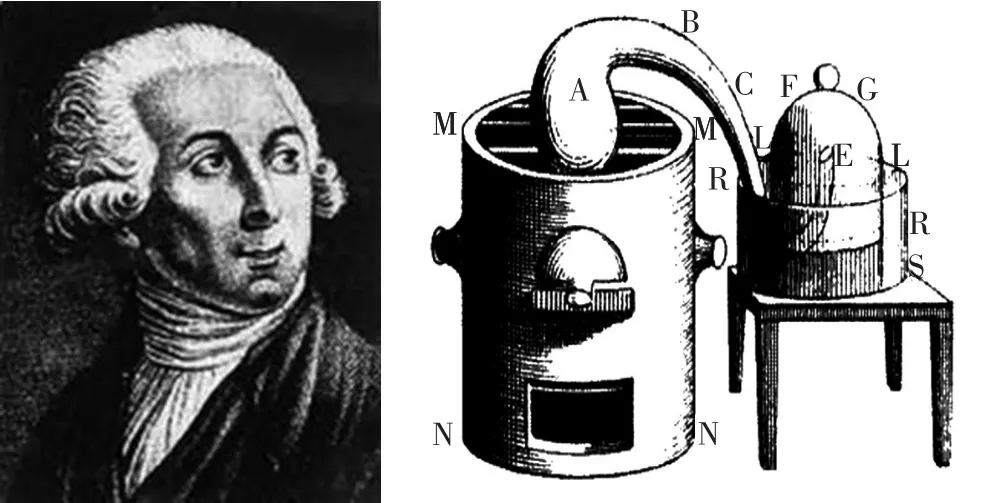
图2 拉瓦锡和拉瓦锡加热水银的实验装置图
二、从化合价升降到电子转移——现代化学理论的完善
1.氧化还原反应与化合价
中学课本中提到有化合价升降的反应是氧化还原反应,这对氧化还原反应的初学者来说非常方便、直观,也被称为氧化还原反应的“宏观特征”。而化合价的经典概念是对元素基本性质的描述,表明原子间的结合能力,如1个氢原子只能和1个其他原子结合,化合价为1(无正负之别)。徐光宪先生在《化学哲学基础》中《原子价概念的发展》一文中提到,原子价概念的提出应追溯到英国化学家E.P.Frankland(1825-1899),他在1852年提出:金属或其他元素的每一个原子在化合时具有一种特殊的性质,叫做“饱和能力”,即倾向于和一定数目的其他原子相结合。
史料2 化合价和氧化数的提出
1852年,富兰克林(E.P.Frankland(1825-1899))提出不管原子结合的原子的特性如何,吸引元素的化合能力(combining power)总是为相同数目的结合原子所满足。后来,把此处的化合能力称为化合价或原子价(quantivalence或valency,美国化学家仍用老名称valence)。
1919年,德国化学家阿尔弗雷德·斯托克(Alfred Stock)提出了“斯托克体系”命名方式,其中所有元素的氧化数(氧化态)均用相应罗马数字表示。
1948年,在价键理论和电负性的基础上提出了氧化数(oxidation number)的概念。在老的化合价理论里,电离化合物(即离子化合物,如NaCl)和非电离化合物(即共价化合物,如CO2)是不加区别的,柯塞尔和路易斯提出的理论认为它们根本不同。
20世纪70年代初,国际纯粹和应用化学联合会(IUPAC)在《无机化学命名法》中,进一步严格定义了氧化数概念。
从史料2中能看到今天“化合价”的概念模型,但这里的化合价解释氧化还原反应是欠妥的,华彤文教授主编的《普通化学原理》中也指出中学化学课本中用化合价升降表示氧化还原反应中电子转移的情况,那里的化合价其实就是氧化数(oxidation number)。随着“氧化数”的提出,氧化还原反应的概念也随之有了进一步的变化:在化学反应中,元素的原子或离子在反应前后氧化数发生变化的一类反应称作氧化还原反应。至此,氧化还原反应学说已经较为完善,不仅摆脱了是否得失“氧”的局限,也指出了氧化过程和还原过程同时发生的辩证观点,但后期的氧化还原过程还是和电化学紧密联系的(史料3),高中教师反复强调的“氧化还原反应的本质是电子转移的问题”又是如何应运而生的?
史料3 电化学的起源和发展
1786年左右,意大利人伽法尼发现如果使神经或肌肉同两种不相类似的金属连接起来,而使金属互相接触,蛙腿会发生收缩。
1800年,意大利的伏打证明这种基本现象并不依赖于一种动物物质的存在,并发明了以他的姓名命名的电池(图3)。1836年,英国科学家丹尼尔对“伏打电池”进行了改良,制造了一个能稳定工作的铜锌原电池,称为丹尼尔电池(图4)。
1806年,戴维证明电效应与电池内化学变化有密切关系,他在皇家学院实验室的助手和继承人法拉第更是制造了目前广泛使用的电化学名词(如电极、离子等),并通过实验得出了法拉第定律。

图3 伏打展示伏打电堆(voltaic pile)
2.氧化还原反应与电化学
国内常见的各版本《无机化学》、《普通化学》等大学教材中氧化还原反应均出现于电化学相关章节,可见电化学层面研究氧化还原反应是在氧化数层面定义的基础上更具可视性和可操作性,结合标准电极电势和能斯特方程,也更有利于研究氧化还原反应的趋势和限度。不能不说电化学的兴起和发展让氧化还原反应这一重要概念有了进一步发展。目前教材中原电池装置的雏形就起源于19世纪初的丹尼尔电池模型(图4、图5)。

图4 丹尼尔电池(原型存于National Museum of American Histo⁃ry,USA.)
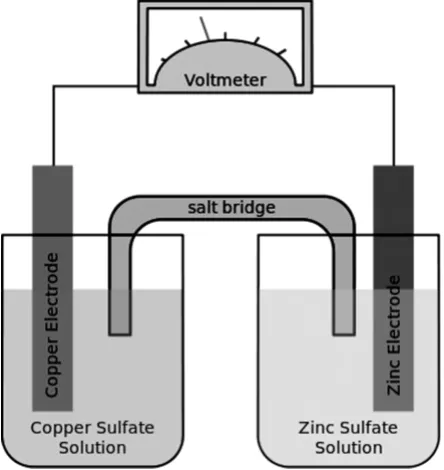
图5 丹尼尔电池的课堂展示模型
电池的出现让氧化还原反应的电子转移为特征的定义有了实物载体,但这并不意味着电子转移比化合价(氧化数)升降的定义更加本质,氧化数是化合物中某元素所带形式电荷的数值,是有实验依据的,人们把反映电子转移和偏移的电子数称为氧化数,从这个意义上说,氧化数变化和电子转移层面的氧化还原反应的定义是没有所谓“宏观现象”和“微观本质”之分的,二者是对同一问题的不同表述而已。
三、反思
从上述史料(史料1~史料3)中不难发现,氧化还原反应的概念进阶本身就是“科学知识是变化的”真实体现。从这个层面上说,维基百科对氧化还原反应(Redox Reaction)给出的定义是符合“科学知识是变化的”这一科学本质的,并且从“originally”、“Later”及“Ultimately”等副词中可以看出概念的演变过程。以氧化反应为例:
●The word oxidation originally implied reaction with oxygen to form an oxide,since dioxygen(O2(g))was historically the first recognized oxidizing agent.
●Later,the term was expanded to encompass oxy⁃gen-like substances that accomplished parallel chemical reactions.
●Ultimately,the meaning was generalized to in⁃clude all processes involving loss of electrons.”
18世纪末,氧化学说确立,人们把与氧化合的反应叫氧化反应,把从氧化物中夺取氧的反应叫还原反应;19世纪中,有了化合价的概念,人们把化合价升高的过程叫氧化,把化合价降低的过程叫还原;20世纪初,由于建立了化合价的电子理论,人们把失电子的过程叫氧化,得电子的过程叫还原。每一次氧化还原概念的进阶都伴随新的理论的提出(表1),这不正是“科学知识是变化的”这一科学本质的完美体现:新的现象和发现可以对现行的理论提出挑战,或者尽管一种理论对现象解释得很好但可能还有其他理论适用,甚至更好、适用范围更广。
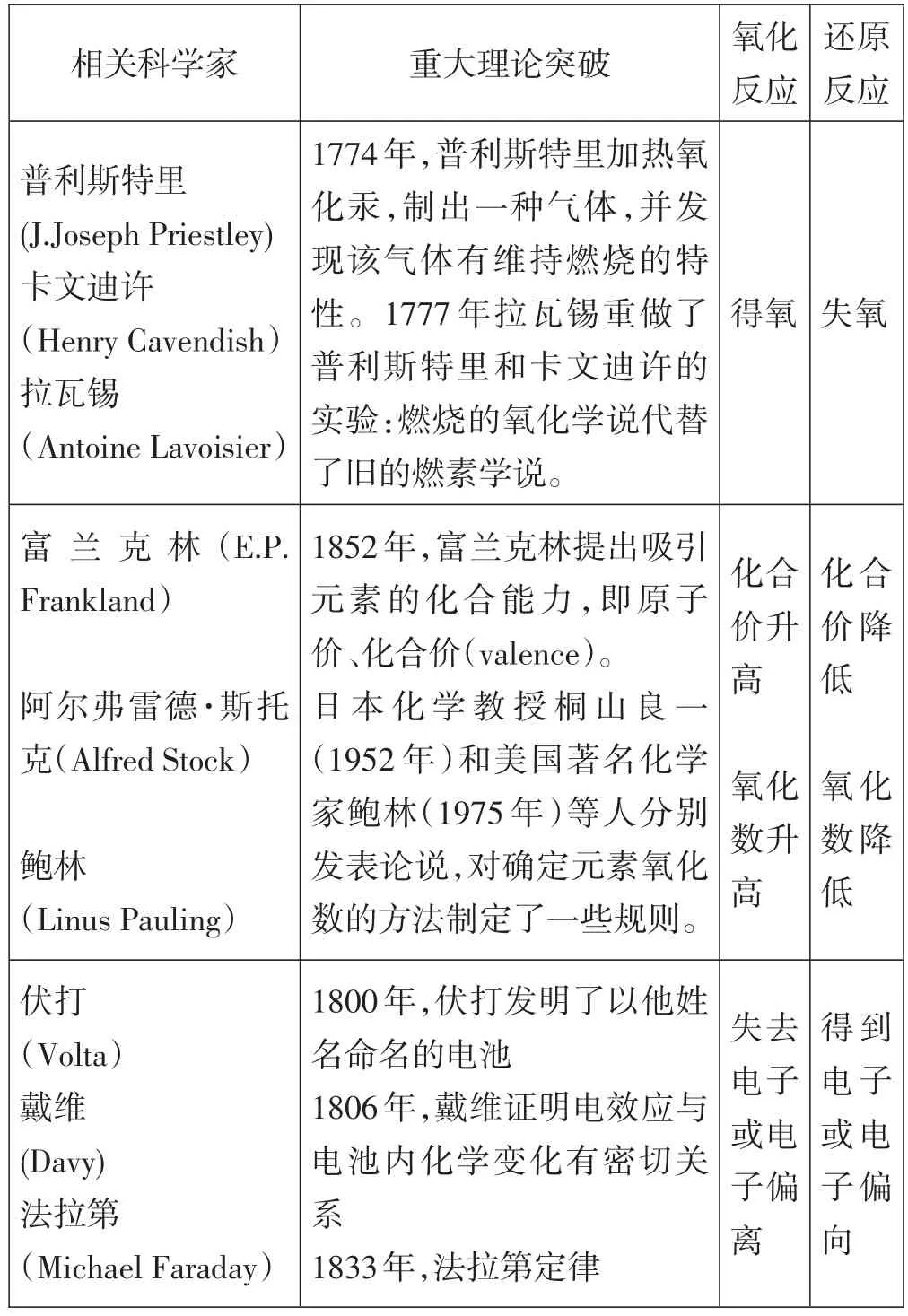
表1 科学史视角下的氧化还原反应的概念进阶
“科学知识是变化的”本身是无可争议的,但在教学过程中,教师常常倾向否定这样的动态变化,而希望将之“讲死”,甚至对“前概念”大加否定!这与“科学的本质”的理解是背道而驰的。从全球化考试来看,自2016年起IBO将会在所有笔试部分(包括卷一、卷二、卷三)中考查标准水平和高水平学生对科学的本质的理解。这种考查不是单独的考查,而是以特定的学科内容为背景。因而说明某一知识缺乏科学本质的片面认识是不符合将科学本质整合到课程中去的理念的。
[1] 王茹.科学的本质怎么教[J].上海教育,2014(32):48-50
[2] 中国自然辩证法研究会化学化工专业组编.化学哲学基础[M].北京:科学出版社,1986
[3] 顾晔.从“三序结合”视角研讨人教版《化学1》的使用[J].化学教学,2012(10):13-15
[4] W.C.丹皮尔.科学史[M].北京:中国人民大学出版社,2010
[5] J.R.柏廷顿.化学简史[M].北京:商务印书馆,1979
1008-0546(2017)10-0038-03
G632.41
B
10.3969/j.issn.1008-0546.2017.10.013
