5-甲基-2-苯基-2,3-二氢-1,3,4-噁二唑的合成研究
2017-09-28陆甲第徐益培甘婉儿陈佳倩邱方利
陆甲第,徐益培,袁 燕,甘婉儿,陈佳倩,邱方利
(台州学院 医药化工学院,浙江 台州 318000)
工程师园地
5-甲基-2-苯基-2,3-二氢-1,3,4-噁二唑的合成研究
陆甲第,徐益培,袁 燕,甘婉儿,陈佳倩,邱方利*
(台州学院 医药化工学院,浙江 台州 318000)
本文介绍了5-甲基-2-苯基-2,3-二氢-1,3,4-噁二唑的合成方法。以苯甲醛和丙二腈为起始原料,NaOH为催化剂,水为溶剂,经缩合反应得到中间体2-亚苄基-丙二腈,然后与乙酰肼反应,碳酸铯为催化剂,经环合得到目标产物,总收率为58.6%,产物结构经1H NMR确证。
苯甲醛;噁二唑;乙酰肼;环化反应
5-甲基-2-苯基-2,3-二氢-1,3,4-噁二唑,分子式:C9H10N2O,分子量:162,本品为黄色固体粉末。它是典型的噁二唑类化合物,该类化合物是一种具有较强生物活性的杂环化合物[1]。在医药方面主要可以应用于抗菌[2]、抗炎[3]、低血糖症、心血管活性[4]、惊厥症以及抗癌等,在设计新药过程中常把它作为药效团。其耐热性和抗氧化性比较好[5-7],故相比对应的全碳芳香体系,其电导率更高,是一类具有重要应用前景的纤维和成膜材料,如果在其2位上引入芳基,可以使材料更加容易接受电子,即降低了分子的HUMO能级,使电子容易与空穴复合发蓝或紫光,弥补目前缺乏蓝、紫光的现状[8,9]。由于噁二唑的性能及其特点,受到了广大科研工作者的关注,在噁二唑的合成和性质方面的研究做了大量的工作。
目前,通过大量科研工作者的不断努力研究,发现了各种1,3,4-噁二唑的合成方法,主要有以下几种:(1)二苯甲酰肼化合物脱水环化;(2)N-苯亚甲基苯甲酰肼氧化环化;(3)S- 二酰基肼脱水;(4)双-2- 氯苄腙经环化;(5)酰胺腙与 HNO2反应;(6)酰氯和酰肼反应生成对称酰胺,再用硫酸、三氯氧磷等脱水剂进行环合。
本文采用的方法是先用苯甲醛和丙二腈反应得到2-亚苄基-丙二腈,然后与乙酰肼反应得到1,3,4-噁二唑类化合物,并且探究了不同的原料配比、溶剂、催化剂、温度等因素对反应产物收率的影响,得到较佳的实验结果。
1 实验部分
1.1 试剂及仪器
苯甲醛、丙二腈、Cs2CO3、蒸馏水、NaOH、乙酸乙酯、二氯甲烷、乙醇等均为市售化学纯。
Bruker AVANCE III 400核磁共振波谱仪;ZNHW型电子控温仪;85-1型磁力搅拌器;SHZ-D(Ⅲ)型循环水式真空泵;RE-52AA旋转蒸发器;FA2004A电子天平等。
1.2 5-甲基-2-苯基-2,3-二氢-1,3,4-噁二唑的合成路线
以苯甲醛为原料,水为溶剂,在碱催化下与丙二腈发生反应,生成中间体,然后继续与碳酸铯进行环化反应,得到目标产物5-甲基-2-苯基-2,3-二氢
-1,3,4-噁二唑(1)。合成路线如下:

图1 合成2-亚苄基-丙二腈的过程Fig.1 Process for synthesis of 2-benzylidene-malononitrile

图2 5-甲基-2-苯基-2,3-二氢-1,3,4-噁二唑的合成路线Fig.2 Synthesis route of 5-methyl-2-phenyl-2,3-dihydro-1,3,4-oxadiazole
1.3 实验步骤
在50mL烧杯中加入丙二腈0.66g(10mmol)和水10mL,搅拌溶解后得丙二腈溶液,待用。在100mL的烧瓶中,先加入NaOH 0.04g(10mmol)和蒸馏水15mL,加磁石搅拌溶解,然后加入苯甲醛1.06g(10mmol),搅拌均匀后,缓慢滴加上述配置的丙二腈溶液,滴加完后,室温下继续反应1h。反应结束后,将反应液抽滤,滤饼用适量蒸馏水洗涤后,得到白色固体,放进烘箱在85℃条件下干燥12h,干燥完后,得到白色粉末状产物,称重得 1.1815g(7.67mmol),收率为76.7%。
在50mL烧杯中加入乙酰肼0.888g(12mmol)和乙醇15mL,搅拌溶解后得乙酰肼溶液,待用。在100mL烧瓶中,先加入2-亚苄基-丙二腈1.54g(10mmol)和乙醇15mL,加磁石搅拌得到白色浑浊液,然后加入碳酸铯4.238g(13mmol),缓慢滴加上述配置的乙酰肼溶液,滴加完后,于35℃下反应8h,通过点板判断原料是否反应完全。反应结束后,先将反应液旋蒸除去乙醇,蒸余液加入二氯甲烷20mL和30mL水搅拌,分层,水相再用二氯甲烷萃取(20mL×2),合并有机层,旋蒸除去二氯甲烷后得到黄绿色固体物,用洗脱剂[V石油醚:V乙酸乙酯=10∶3]过柱分离,得到黄色固体产物 0.95g(5.86mmol),收率为58.6%。产物用1H NMR进行确认。
2 结果与讨论
2.1 不同原料比对环化反应的影响
在环化反应过程中,实验在一定条件下,考察原料2-亚苄基-丙二腈和乙酰肼的不同比例,对反应产率的影响,结果见表1。
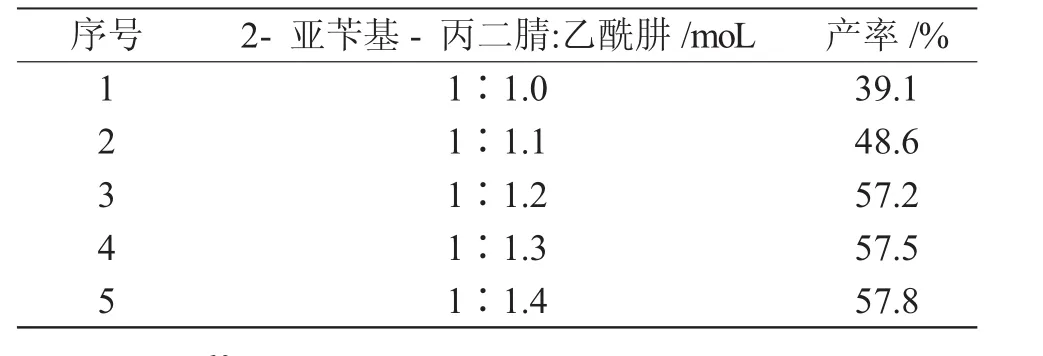
表1 原料比对反应收率的影响Tab.1 Effect of raw material ratio on reaction yield

图3 原料比对反应收率的影响Fig.3 Effects of different inventory on the cyclization reaction
从图3中可知,反应产物的收率随着乙酰肼投料量的增加而增加,但当原料比超过1∶1.2时,继续增加投料配比,产率增加不明显。为减少原料的浪费,选择反应最佳的原料比为2-亚苄基-丙二腈:乙酰肼为1∶1.2。
2.2 不同催化剂对环化反应的影响
在环化反应过程中,试验了不同催化剂对2-亚苄基-丙二腈和乙酰肼反应所得产物的收率的影响,结果见表2。
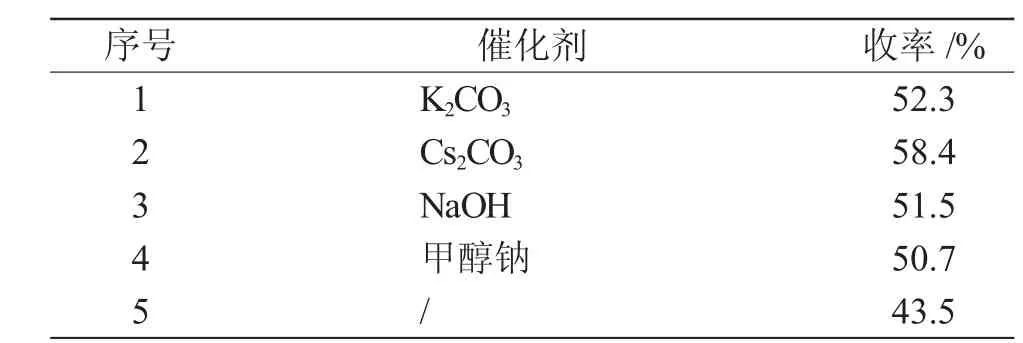
表2 不同催化剂对反应收率的影响Tab.2 Effect of various catalysts on reaction yield
从表2可知,加入催化剂后比不加催化剂时反应产物的收率增加明显,并且不同的催化剂对反应的影响效果也不同,其中使用CS2CO3做催化剂时收率最高。
2.3 溶剂对环化反应的影响
在环化反应过程当中,溶剂起着重要的作用,实验中考察了不同溶剂对2-亚苄基-丙二腈和乙酰肼反应产物收率的影响,具体结果见表3。
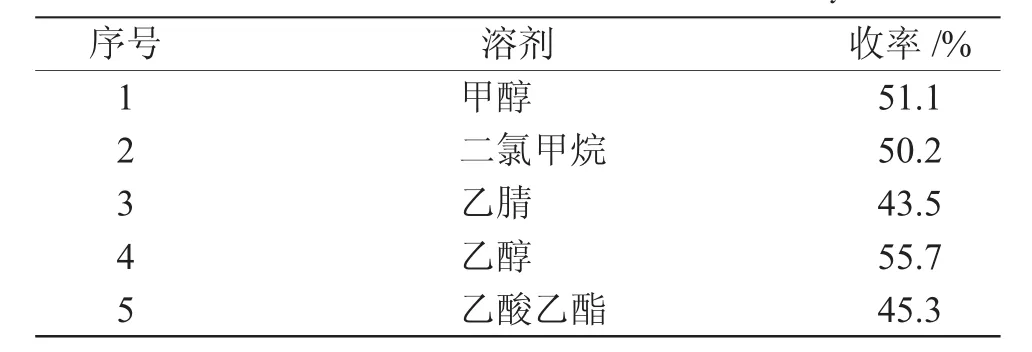
表3 不同溶剂对反应收率的影响Tab.3 Effect of different solvents on reaction yield
从表3可知,不同溶剂种类对反应产物收率的影响不同,其中使用无水乙醇做溶剂时产率最高。
2.4 温度对环化反应的影响
在环化反应过程中,温度对反应的速度影响较大,实验中考察了不同反应温度对2-亚苄基-丙二腈和乙酰肼反应所得产物的收率的影响,具体结果见表4。

表4 不同温度对反应收率的影响Tab.4 Effect of different temperature on reaction yield

图4 不同温度对反应收率的影响Fig.4 Effect of different temperature on reaction yield
从图4可知,随着温度的提高反应产物的收率增长,其中当温度为35℃时产率最高,然而当温度继续上升时,产率反而略有下降,可能是副反应增加生成了副产物,故选择在35℃条件下进行反应。
2.5 反应产物的核磁表征分析
2-亚苄基-丙二腈的核磁氢谱图(图5),测得1H NMR(400 MHz,CDCl3)δ7.91(d,J=7.5 Hz,2H),7.79(s,1H),7.64(t,J=7.4Hz,1H),7.55(t,J=7.6Hz,2H),与此化合物的结构一致。

图5 2-亚苄基-丙二腈的核磁氢谱图Fig.5 1H NMR spectrum of 2-Benzylidene-malononitrile
5-甲基-2-苯基-2,3-二氢-1,3,4-噁二唑的核磁氢磁图(图 6),测得1H NMR(400MHz,CDCl3)δ10.71(s,1H),7.89(s,1H),7.68(dd,J=6.5,3.0Hz,2H),7.39(dd,J=4.9,1.6 Hz,3H),2.40(s,3H),与此化合物的结构一致。

图6 5-甲基-2-苯基-2,3-二氢-1,3,4-噁二唑的核磁氢谱图Fig.6 1H NMR spectrum of 5-Methyl-2-phenyl-2,3-dihydro-1,3,4-oxadiazole
3 结论
(1)本文先由苯甲醛和丙二腈反应得到2-亚苄基-丙二腈,然后由2-亚苄基-丙二腈和乙酰肼反应得到5-甲基-2-苯基-2,3-二氢-1,3,4-噁二唑。
(2)并探究了不同的投料比、催化剂、溶剂、温度对反应收率的影响,最终得出最佳条件为:2-亚苄基-丙二腈和乙酰肼为1∶1.2,Cs2CO3做催化剂,乙醇做溶剂,温度为35℃;在该条件下反应得到产物的收率最高,为58.6%。
[1] 陈悟,陈琼,吴琼友,等.含噁二唑杂环取代的新型三唑并嘧啶衍生物的合成及其生物活性[J].有机化学,2005,25(11):1477-1481.
[2] TalarMB,Dejai SR,Sommanavar YS,et al.Synthesis and antimicrobial activityof1,2,4-triazoles,1,3,4-oxadiazoles and 1,3,4-thiadiazoles[J].Indian J HeterocyclChem,1996,5(4):215-218.
[3] Zhang Y,Qiao RZ,Zhang ZY,et al.Synthesis and antibacterial activities of 2-(1-aryl-5-methyl-1,3,4-triazol-4-yl)-1,3,4-oxadiazole derivatives[J].J.Chin.Chem.Soc.,2002,49(3):369-373.
[4] HuGQ,Zhang ZQ,Xu QT,et al.Phase transfer catalysed synthesis and bioactivity ofS-triazolo[3,4-b]thiadiazolnes[J].Acta.Chim.Sin.,2004,62(2):204-207.
[5] 刘卫军,陈阳如,熊国宣.含1,3,4-噁二唑环的有机电致发蓝光材料及器件研究进展[J].化工进展,2006,25(8):895-900.
[6] 柴春鹏,范星河,陈小芳,等.含1,3,4-噁二唑环聚合物电致发光材料的近期进展[[J].化学进展,2006,18(11):1499-1507.
[7] 朱为宏,田禾,世琴.有机分子电致发光材料进展[J].化学进展,2002,14(1):18-23.
[8] 赖文勇,梅群波,宋娟,等.蓝光高分子电致发光材料研究进展[J].南京邮电大学学报,2008,28(2):88-94.
[9] 刘莹,陈或,白金瑞.蓝光聚合物电致发光材料研究[J].高分子材料科学与工程,2007,23(3):11-15.
Study on synthesis of 5-methyl-2-phenyl-2,3-dihydro-1,3,4-oxadiazole
LU Jia-di,XU Yi-pei,YUAN Yan,GAN Wan-er,CHEN Jia-qian,QIU Fang-li*
(School of Pharmaceutical Chemicals,Taizhou University,Taizhou 318000,China)
The synthesis of 5-methyl-2-phenyl-2,3-dihydro-1,3,4-oxadiazole was introduced with benzaldehyde and malononitrile as raw materials,sodium hydroxide as catalyst and water as solvent,the intermediate 2-benzylidene-malononitrile was obtained by condensation reaction.Then reacted with acethydrazide,cesium carbonate as catalyst to obtain the target product.The yield was 58.6%and the product structure was confirmed by1H NMR.
benzaldehyde;oxadiazole;acethydrazide;reaction condition
O0629.32
A
10.16247/j.cnki.23-1171/tq.20170961
2017-04-28
陆甲第(1997-),女,汉族,甘肃陇西人,台州学院2016级制药工程专业学生。
邱方利(1966-),男,汉族,浙江临海人,副教授,主要从事化工产品与药品的工艺研究。
