微流控芯片非接触电导法测定药品中的精氨酸布洛芬含量
2017-09-26ALAAALHAKIMI陈缵光
ALAA ALHAKIMI,陈缵光
(中山大学 药学院,广东 广州 510006)
微流控芯片非接触电导法测定药品中的精氨酸布洛芬含量
ALAA ALHAKIMI,陈缵光*
(中山大学 药学院,广东 广州 510006)
建立了微流控芯片非接触电导检测快速测定精氨酸布洛芬含量的方法。考察了缓冲液种类和浓度、添加剂、分离电压以及进样时间等因素对分离检测的影响。优化条件为:20 mmol/L Tris-20 mmol/L H3BO3(pH 8.6)为缓冲溶液、不加添加剂、分离电压2.0 kV、进样时间10.0 s,在 45.0 s内可实现精氨酸布洛芬的快速分离测定。结果表明,布洛芬和精氨酸在80.0~1.00×103mg/L范围内线性关系良好,相关系数(r)分别为 0.998 和0.997,检出限(S/N=3)为60 mg/L,相对标准偏差分别为1.9%和 1.8%,加标回收率分别为 97.9%~103%和97.3%~102%。该方法快速、简便,为精氨酸布洛芬非甾体抗炎药物的分析和质量控制提供了一种新方法。
微流控芯片;非接触电导检测;精氨酸布洛芬片;精氨酸布洛芬小颗粒
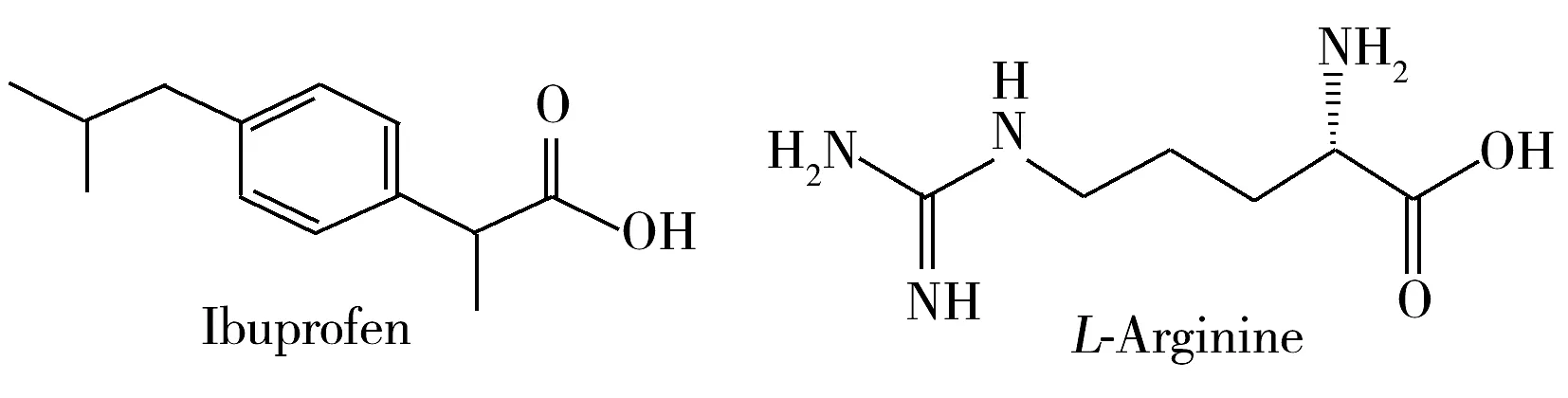
图1 布洛芬和精氨酸的分子式Fig.1 Molecular structure of ibuprofen and arginate
布洛芬(Ibuprofen)为白色结晶性粉末,是一种非甾体抑制前列腺素合成的抗炎药物,具有非麻醉性镇痛和解热性能,其分子量为206.27,水溶性低,在有机溶剂中溶解度高。精氨酸布洛芬为精氨酸与布洛芬生成的盐,分子结构如图1所示。它吸收快速,镇痛效果更好,可用于治疗牙痛、痛经、头痛,以及流感引起的发热等[1]。已报道的精氨酸布洛芬含量的测定方法有高效液相色谱法[2-4]、紫外可见分光光度法[5]、毛细管电泳法[6]和电位滴定法等[7]。高效液相色谱法分析成本高,样品处理繁琐,分析时间长。紫外-可见分光光度法的选择性相对较低。与传统方法相比,微流控芯片分析法具有分析速度快、准确、稳定性好、灵敏度高、操作简便等特点[8-11],但将其用于精氨酸布洛芬含量分析的研究目前国内外尚未见报道。本文考察了微流控芯片分析法测定精氨酸布洛芬的条件,为精氨酸布洛芬含量的快速测定提供了一种新的分析方法。
1 实验部分
1.1 仪器与试剂
微流控芯片分析仪(型号 μD-CCD/HV-2014,中山大学药学院研制),由微型压电陶瓷高压电源(自制)[12]、非接触电导检测器(自制)[13]和数据工作站组成。 PMMA 芯片(微通道上宽30 μm,下宽100 μm,深 30 μm,进样通道为十字结构,分离通道长44 mm,有效分离长度 43 mm)。循环水式真空泵(SHZ-D(Ⅲ)型,巩仪市英峪予华仪器厂)。超声波提取器(DA-3A 型,顺德乐从灵通电子厂)。数据记录与处理在普通微机上完成。硼酸(H3BO3,天津市永达化学试剂限公司)、三羟基氨基甲烷(Tris)、精氨酸对照品、布洛芬对照品、2-(N-吗啉代)乙磺酸(MES)(阿拉丁试剂公司);精氨酸布洛芬片(0.4 g,海南赞邦制药有限公司,批号:20161208),精氨酸布洛芬小颗粒(0.4 g,海南赞邦制药有限公司,批号:20161209)。实验用水为二次蒸馏水,其它试剂均为国产分析纯。
1.2 对照品与样品溶液的制备
称取布洛芬和精氨酸对照品各0.010 0 g,用 20 mmol/L Tirs+20 mmol/L H3BO3缓冲液(pH 8.6)溶解并定容至10 mL,制得1.00 g/L的储备液,4 ℃下保存。各种浓度的对照品溶液可在使用时用储备液稀释而得。
取精氨酸布洛芬片剂和小颗粒,研细,精密称定0.010 0 g,加入20 mmol/L Tirs+20 mmol/L H3BO3缓冲液(pH 8.6),超声波振荡10 min溶解,定容至10 mL,取滤液作供试品溶液,4 ℃保存。进样前,所有溶液均经0.22 μm微孔滤膜过滤。
1.3 分离测定
PMMA新芯片使用前先用0.1 mol/L HNO3冲洗并浸泡20 min。每次实验前,芯片通道依次用0.1 mol/L NaOH活化10 min,二次蒸馏水浸泡5 min,再用缓冲液平衡10 min。实验结束后,先依次用水、0.1 mol/L HNO3冲洗通道,再用水充满通道,避免通道堵塞。检测器激发电压为60 V(Vp-p),激发频率60 kHz。进样电压为500 V,分离电压为0.5~3.0 V。电迁移进样,进样时间为10.0 s,切换至分离状态并同时启动色谱工作站记录。
2 结果与讨论
2.1 运行缓冲液的选择
运行缓冲液的种类对分离分析效果影响很大。本实验考察了缓冲溶液的种类、浓度、pH值及添加剂对分离检测的影响。分别考察了柠檬酸-柠檬酸钠、氯化钾-盐酸、MES-Tris、Tris-硼酸等缓冲液体系在不同浓度、不同配比条件下对分离和检测效果的影响。实验结果显示,在柠檬酸-柠檬酸钠、氯化钾-盐酸等缓冲体系中,基线较为稳定,但精氨酸和布洛芬两个成分的峰形和分离效果较差。在MES-Tris缓冲体系中,基线平稳,布洛芬出峰快,但与水峰接近,分离度欠佳。在Tris-硼酸缓冲体系中,基线较稳定,电泳电流小,且精氨酸布洛芬的两个峰形较好,与杂质峰和水峰分离度大,灵敏度较高,因此选择Tris-硼酸作为优化的缓冲溶液。同时考察了Tris-硼酸的浓度比对分离检测的影响,发现当Tris-硼酸的浓度比为20 mmol/L∶20 mmol/L时,精氨酸布洛芬的峰强度较好,且峰形最佳。综合考虑,选择20 mmol/L Tris-20 mmol/L硼酸(pH 8.6)为分离介质。
2.2 添加剂的影响
考察了二甲基亚砜(DMSO)、乙醇、十二烷基硫酸钠(SDS)等添加剂对分离检测的影响。在缓冲溶液中分别加入0.5%~10%的添加剂,结果发现,上述添加剂对精氨酸和布洛芬的分离检测并无明显改善,反而会造成基线漂移、噪声增大、峰形变差。因此不加任何添加剂。
2.3 进样时间的优化
考察了进样时间(5.0~20.0 s)对分离检测的影响。结果表明,随着进样时间的延长,精氨酸和布洛芬的峰高及峰面积均增大,但进样时间超过10.0 s后,增高幅度减少,且峰形变差。综合考虑,选择优化的进样时间为10.0 s。
2.4 分离电压的优化
实验考察了分离电压在0.5~3.0 kV范围内对样品分离的影响。结果表明:随着电压升高,各成分的迁移时间缩短、峰强增大、分离度提高;但当分离电压高于2.0 kV时,噪音增加、分离度变差、基线不稳定,且高压电极与微芯片缓冲液池内的接触面有放电现象。综合考虑,选择优化的分离电压为2.0 kV。
2.5 线性关系、检出限及精密度
分别用布洛芬和精氨酸对照品储备液配制系列浓度的标准溶液,在上述优化条件下进样,考察峰高(Y,μV)与对应质量浓度(X,mg/L)的关系,确定线性范围为80.0~1.00×103mg/L,线性方程分别为Y=1 061X+11 890 和Y=201.0X+3 469,相关系数(r)分别为0.998和0.997。检出限(S/N=3)均为60.0 mg/L。以质量浓度为400.0 mg/L的精氨酸和布洛芬对照品溶液重复进样6次,测得两者峰高的相对标准偏差(RSD)分别为1.9%和1.7%。
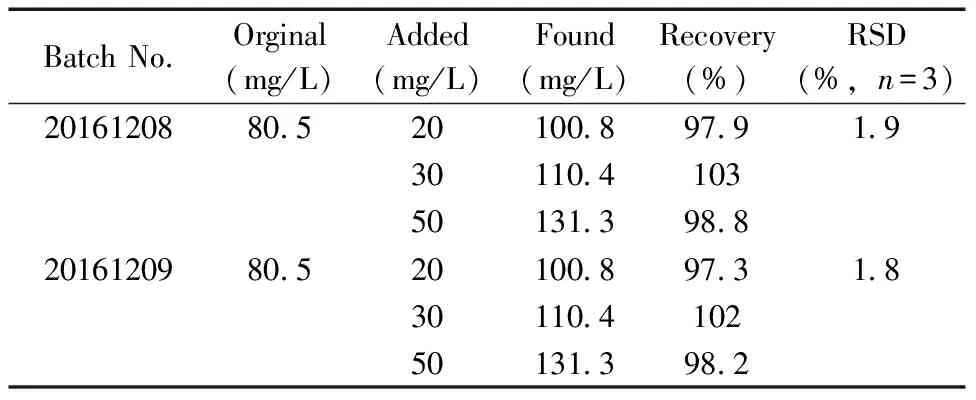
表1 加标回收率结果Table 1 Results of spiked recoveries
2.6 样品测定及回收率
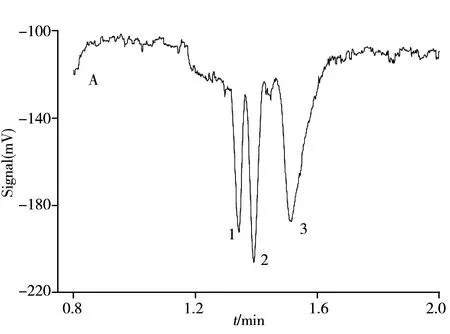
在优化条件下,取精氨酸布洛芬供试品(批号:20161208、20161209)溶液适量,分别进样,记录电泳图(图2)。取样品溶液3次测定所得峰高的平均值,根据线性回归方程计算出两样品溶液中布洛芬精氨酸的浓度,折算成标示量百分含量分别为95.1%和96.3%。
精密量取精氨酸布洛芬供试品(批号:20161208、20161209)溶液各3份,按高、中、低3个浓度分别加入精氨酸布洛芬对照品溶液,分别进样3次,测定结果如表1所示。回收率为97.3%~103%,RSD为1.8%~1.9%。
3 结 论
本文采用微流控芯片非接触电导法测定了药品中精氨酸布洛芬的含量,在45 s内实现了布洛芬精氨酸的分离检测,方法简便快速、重复性好、可靠性高、分析成本低,可用于精氨酸布洛芬药品的质量控制。
[1] Zhang J.Chin.Comm.Doc.(张娇.中国社区医师),2011,19(38):63-64.
[2] Wang J M,Wang H,Han Q,Jiang C L .J.HubeiUniv.Trad.Chin.Med.(王家满,王浩,韩琼,姜从良.湖北中医药大学学报),2014,16(4):55-56.
[3] Hao H F.Strait.Pharm.J.(郝红芬.海峡药学),2014,26(1):68-70.
[4] Liu R,Liu F L,Luo G P,Li P Y,Yang L Y.NorthwestPharm.J.(刘瑞,刘福利,罗国平,李品颖,杨丽英.西北药学杂志),2013,28(4):361-365.
[5] Liu Y P,Shi Y H.J.NorthPharm.(刘业萍,史永惠.北方药学),2009,6(4):17,41.
[6] Zhang H,Xue H B,Liu Y X,Liang L L.Appl.Chem.Ind.(张晖,薛洪宝,刘亚新,梁丽丽.应用化工),2016,45(1):179-182.
[7] Hong S S,Wang H X,Wang S L.J.Pharm.Res.(洪桑桑,王海翔,王岁楼.药学研究),2016,35(11):642-645.
[8] Yang X J,Li O L,Chen Z G,Liu C,Lan Y,Zhao S.Chin.J.Anal.Chem.(杨秀娟,李偶连,陈缵光,刘翠,蓝悠,赵慎.分析化学),2008,36(5): 673-677.
[9] Li Y C,Cai Z Y,Wang C,Chen Z G.J.Instrum.Anal.(李永冲,蔡自由,王充,陈缵光.分析测试学报),2010,29(8): 864-866.
[10] Zhou X,Zhang Y M,Zhu C L,Chen Z G.J.Instrum.Anal.(周勰,张吟眉,朱嫦琳,陈缵光.分析测试学报),2010,29(9): 966-969.
[11] Cai Z Y,Li Y C,Tong Y L,Chen Z G.J.Instrum.Anal.(蔡自由,李永冲,童艳丽,陈缵光.分析测试学报),2011,30(4): 453-456.
[12] Chen Z G,Wang L S,Mo J Y.Chem.J.Chin.Univ.(陈缵光,王立世,莫金垣.高等学校化学学报),2004,25(suppl): 26-27.
[13] Chen Z G,Li Q W,Li O L,Zhou X,Lan Y,Wei Y F,Mo J Y.Talanta,2007,71(5): 1944-1950.
Determination of Ibuprofen Arginine by Contactless Conductivity Detection with Microfluidic Chip
ALAA ALHAKIMI,CHEN Zuan-guang*
(School of Pharmaceutical Sciences,Sun Yat-sen University,Guangzhou 510006,China)
A rapid analytical method was developed for the determination of ibuprofen arginine by contactless conductivity detection with microfluidic chip.Influence parameters on separation and detection such as type and concentration of buffer,additive,separation voltage and injection time were investigated and optimized.Under the optimum conditions,i.e.20 mmol/L Tris-20 mmol/L H3BO3(pH 8.6)as buffer solution,no additive,a separation voltage of 2.0 kV and an injection time of 10.0 s,ibuprofen arginine could be separated and detected within 45.0 s.The results showed that good linearities for ibuprofen and arginine existed in 80.0-1.00×103mg/L,with their correlation coefficients(r)of 0.998 and 0.997,respectively.The limits of detection(S/N=3)for them were 60 mg/L with RSDs of 1.9%and 1.8%,respectively.And their recoveries were in the ranges of 97.9%-103%and 97.3%-102%,respectively.This method was rapid and simple,and could be used for the detection and quality control of non-steroidal arginine ibuprofen anti-inflammatory drugs.
microfluidic chip;contactless conductivity detection;arginine ibuprofen tablets;arginine ibuprofen granules
O657.1;TQ460.72
:A
:1004-4957(2017)09-1129-04
2017-04-09;
:2017-06-11
国家自然科学基金项目(21375152,21675177);广东省科技计划项目(2016B030303002)
*
:陈缵光,博士,教授,研究方向:药物分析、微流控芯片,Tel:020-39943044,E-mail:chenzg@mail.sysu.edu.cn
10.3969/j.issn.1004-4957.2017.09.013
