I EX-1蛋白在胃癌中的表达及其意义*
2017-09-19毛山山程小珍崔荣花元建华王美清
毛山山,程小珍,崔荣花,元建华,王美清
(中南大学湘雅医学院附属海口医院 肿瘤化疗科,海南 海口 570208)
I EX-1蛋白在胃癌中的表达及其意义*
毛山山,程小珍,崔荣花,元建华,王美清
(中南大学湘雅医学院附属海口医院 肿瘤化疗科,海南 海口 570208)
目的揭示即刻早期反应X-1(IEX-1)蛋白在胃癌组织及细胞系中的表达,探讨其对人胃癌细胞凋亡和增殖的影响。方法采用免疫组织化学法检测100例胃镜活检标本中IEX-1蛋白的表达,用实时荧光定量聚合酶链反应和Western blot检测人正常胃黏膜细胞GES-1和胃癌细胞MKN28中IEX-1基因和蛋白的表达,同时转染IEX-1的过表达质粒pcDNA3-FLAG-IEX-1和干扰质粒pLL3.7-si-IEX-1,分别采用流式细胞术及四甲基偶氮唑盐比色法检测IEX-1对细胞周期、凋亡及增殖的影响。结果胃癌组织中IEX-1蛋白表达水平高于正常胃组织和慢性胃炎组织(P<0.05),且随着病情进展,IEX-1表达水平有逐渐升高的趋势。相对于人正常胃黏膜细胞GES-1,胃癌细胞MKN28中IEX-1基因和蛋白表达更高(P<0.05)。与对照组相比,IEX-1蛋白表达增高后S期细胞比例升高,G2期细胞比例降低,细胞增殖率升高,凋亡减少(P<0.05),而干扰IEX-1蛋白表达后,G1期细胞升高,G2期细胞比例下降,细胞增殖率下降,细胞凋亡增加(P<0.05)。结论IEX-1蛋白在胃癌组织中呈高表达,在人胃癌细胞中上调IEX-1蛋白能促进细胞增殖,发挥抗凋亡能力,干扰IEX-1蛋白表达能阻滞细胞周期进程,并诱导凋亡。
胃癌;即刻早期反应X-1;增殖;凋亡
胃癌是来于自胃黏膜上皮的恶性肿瘤,在全部恶性肿瘤中排第3位,是消化道最常见的恶性肿瘤,可见胃癌是威胁人类健康的常见病。人类即刻早期反应基因X-1(immediate early responsegene X-1,IEX-1)位于人染色体6p21.3,全长1.2 kb,表达含156个氨基酸残基的蛋白,分子量约为18 kD[1-2]。IEX-1表达有组织差异性,被证实是一种凋亡相关调节蛋白,在不同细胞和组织中能够正性或负性调控凋亡相关过程,参与很多肿瘤分子生物学过程[3-5]。但目前关于其在胃癌研究中的报道较少,在胃癌中的功能尚不清楚。本研究拟通过检测IEX-1蛋白在胃癌组织中的表达水平,并分析其对人胃癌细胞凋亡和增殖的影响,探讨其在胃癌进程中的作用,现报道如下。
1 材料与方法
1.1 材料
1.1.1 主要试剂和仪器 达尔伯克必需基本培养基(dulbecco's minimum essential medium,DMEM)购自美国Gibco公司,胎牛血清购自法国Biowest公司,兔抗人IEX-1多克隆抗体购自美国Sigma公司,鼠抗人Tunbulin单克隆抗体购自加拿大Fermentas公司,LipoTM2000转染试剂、逆转录试剂盒、实时荧光定量聚合酶链反应(quantitative real-time polymerase chain reaction,qRT-PCR)试剂盒及限制性内切酶均购自日本TaKaRa公司,pcDNA3-flag质粒、pLL3.7质粒、T4连接酶、DNA抽提试剂盒、凝胶回收试剂盒、即用二氨基联苯胺(Diaminobenzidine,DAB)显色剂、四甲基偶氮唑盐比色法[3-(4,5-dimethyl-2-thiazolyl)-2,5-diphenyl-2-H-tetrazolium bromide,MTT]试剂及碘化丙啶试剂均购自北京鼎国昌盛生物技术有限责任公司,培养箱和超净工作台购自美国Thermo Forma公司,ABI PRISM 7700 qRT-PCR仪购自美国ABI公司,水平式琼脂糖凝胶电泳仪、垂直式电泳仪及湿式电转移均购自美国Bio-Rad公司,ACEA Novo CyteTM流式细胞仪购自杭州艾森生物有限公司,凝胶成像系统购自美国Gene公司,光学显微镜购自日本Nikon公司。所有引物委托北京鼎国昌盛生物技术有限责任公司合成。
1.1.2 组织标本和细胞 为研究正常胃组织→慢性胃炎→胃癌过程中IEX-1蛋白的表达变化,在中南大学湘雅医学院附属海口医院2014年1月-2015年12月胃镜活检患者中收集10例正常胃组织、40例慢性胃炎组织及50例胃癌组织标本。所有患者签署标本研究知情同意书。人正常胃黏膜细胞GES-1购自上海拜力生物科技有限公司,胃癌细胞MKN28购自国家实验细胞资源共享平台。
1.2 方法
1.2.1 免疫组织化学法 采用二步法检测正常胃组织、慢性胃炎组织及胃癌组织中IEX-1蛋白的表达。4μm切片56℃过夜。次日常规脱蜡和去内源性过氧化物酶,加入三羟基甲胺 -盐酸缓冲盐溶液(Tris-HCl buffer saline,TBS)进行抗原修复。擦去组织周围TBS,置切片于湿盒内,滴加正常绵羊血清(1∶20),70μl/片,37℃、20 min。吸去切片上部分血清,滴加工作浓度兔抗人IEX-1多克隆抗体(1∶200),70μl/片,37℃、1 h后,4℃放置过夜。阴性对照用TBS代替一抗。次日滴加相对应工作浓度二抗,70μl/片,37℃、1 h,滴加DAB显色。开始出现背景时,用蒸馏水终止显色。苏木素复染后立即流水冲洗。将切片于56℃烤箱内烤干,中性树胶封片,光镜下观察。染色程度由2位病理医生在不知临床资料的情况下独立评价。400倍光镜下观察8个任一视野,得到染色强度和阳性细胞百分率。IEX-1染色评分由染色强度(0~3级:0级为阴性,1级为弱阳性,2级为中等阳性,3级为强阳性)和阳性细胞百分率(0~4级:0级为0%,1级为1%~25%,2级为26%~50%,3级为51%~75%,4级为76%~100%)的乘积得到,分为不同等级(0、1、2、3、4、6、8、9和12)。0级为阴性表达,1、2和3级为弱阳性表达,4和6级为中度阳性表达,8、9和12级为强阳性表达。
1.2.2 细胞培养 液氮冻存细胞拿出后迅速放于37℃水浴中溶解,使用DMEM培养基(含10%胎牛血清,1%抗生素)37℃、5%二氧化碳CO2、95%空气饱和湿度培养箱中培养。复苏次日更换新鲜培养基。细胞密度>80%时需使用胰酶消化传代。传代比例1∶6~1∶4。
1.2.3 Western blot检测 在细胞样品中加入预冷的裂解液,超声破碎后4℃、13 000 r/min离心10 min;轻轻吸取上清,转移至新的离心管中置于冰上待用。使用BCA蛋白定量试剂盒通过标准曲线计算出样品的蛋白浓度。取等量蛋白样品(30μg),加入上样缓冲液,97℃加热6 min变性,室温冷却离心后上样。十二烷基磺酸钠-聚丙烯酰胺凝胶电泳结束后,采用电转仪将蛋白从分离胶转移至聚偏二氟乙烯膜(polyvinylidene fluoride,PVDF)膜上。转膜完成后,将PVDF膜封闭后加入一抗(1∶1 000,用封闭液稀释),4℃杂交过夜。加入适当比例稀释的二抗,室温孵育1 h,将电化学发光试剂盒的A液和B液等体积混合后均匀滴在PVDF膜上,放入暗盒中显影。使用Quantity One软件进行光密度分析。
1.2.4 qRT-PCR 在样品中加入1 ml Trizol,剧烈震荡混匀,室温放置5 min后加入200μl氯仿剧烈震荡,4℃静置5 min。4℃、12 000 r/min离心15 min,将约600μl上清液转移至新的无核糖核酸酶(Ribonuclease,RNase)1.5 ml离心管中。加入等体积氯仿,剧烈震荡,4℃静置2 min。4℃、12 000 r/min离心15 min,吸取上清液至新的无RNase 1.5 ml离心管中。按等体积加入异丙醇,上下颠倒充分混匀后于-20℃静置30 min。4℃、12 000 r/min离心10 min,弃上清,沉淀用75%预冷乙醇洗涤后,离心弃上清,充分干燥后加入适量焦碳酸二乙酯(diethy pyrocarbonate,DEPC)水溶解RNA并测定浓度。为防止DNA对逆转录的影响,要用脱氧核糖核酸酶消化提取的RNA中的DNA,其消化程序和反应液的量按说明书操作。按照逆转录试剂盒说明书操作将RNA逆转录为互补脱氧核糖核酸(complementary deoxyribonucleic acid,cDNA),即可作为qRT-PCR的反应模板。从美国国立生物技术信息中心获得IEX-1 mRNA的全长序列,利用Primer Blast设计引物序列。IEX-1正向引物:5'-CGGTCCTGAGATCTTCACCT-3',反向 引 物 :5'-TGGTGAGCAGCAGAAAGAGA-3';GAPDH正向引物:5'-ACATGTTCCAATATGCTTCC-3',反向引物:5'-TGGACTCCACCACGTACTCAG-3'。配置标准的PCR体系,以GAPDH作为内参进行相对定量,每组设3个复孔,于qRT-PCR仪上设置所需的反应条件,反应结束后读取数据。
1.2.5 构建pcDNA3-FLAG-IEX-1和pLL3.7-si-IEX-1真核表达载体 以MKN28 cDNA为模板,从NCBI获得IEX-1 mRNA的全长序列。NotⅠ:5'-ATAAGAATGCGGCCGCATGTGTCACTCTCGCAGCTgCCACC-3';EcoRⅠ:3'-CCGGAATTCGCGAAGGCGgCCGGgTGTTGCTGGAGG-5'。配置标准的PCR体系,在PCR仪上设置所需的反应条件,将PCR产物与pcDNA3-flag质粒使用NotⅠ和EcoRⅠ双酶切。将上述酶切产物跑1%琼脂糖凝胶,切胶回收,使用T4Ligase 16℃连接过夜。连接产物转化DH5α,涂布氨苄平板。37℃培养过夜。挑取平板上长出菌落,质粒小提后送上海美吉生物医药科技有限公司测序。pLL3.7-si-IEX-1真核表达载体的构建方法相同,使用载体为pLL3.7,双酶切位点为HpaⅠ和XhoⅠ。干扰序列为250~270 kb,正向引物:5'-AAAAGgCTTCTCTTTCTGCTG-3',反向引物:5'-CAGCAGA AAGAGAAGCCTTTT-3'。
1.2.6 细胞转染实验 转染前1 d传代MKN28细胞,转染时细胞密度需达80%~90%。严格按照LipoTM2000转染试剂的说明书进行操作。每个培养血(直径6 cm)细胞使用质粒量4μg。分别转染对照质粒 pcDNA3-flag、pLL3.7、过表达质粒 pcDNA3-flag-IEX-1及干扰质粒pLL3.7-si-IEX-1。在转染后48 h检测IEX-1的蛋白表达水平,验证转染效率。
1.2.7 流式细胞术 将转染上述质粒48 h后的MKN28细胞进行流式细胞术检测,每个样品收集细胞5×106个,用磷酸盐缓冲液(phosphate buffered saline,PBS)洗细胞2次,2 000 r/min离心2 min,弃上清液。70%预冷乙醇固定过夜,4℃保存备用,染色前用PBS洗去固定液,弃上清液。每管中加RNase A,37℃水浴30 min,PI染色混匀,4℃避光30 min,上流式细胞仪检测细胞周期。实验重复3次。
1.2.8 MTT法 MTT法检测转染上述质粒48 h后的MKN28细胞。转染后的细胞用培养液配成单细胞悬液,以3 000个细胞/孔接种到96孔板,体积200μl/孔。每组均设置3个复孔,培养48h后加MTT溶液(5 mg/ml)20μl/孔。492 nm处检测吸光度值。
1.3 统计学方法
数据分析采用SPSS 21.0统计软件,计量资料以均数±标准差(±s)表示,用t检验或方差分析,两两比较用LSD-t检验。等级资料以频数表示,用Kruskal-WallisH检验,P<0.05为差异有统计学意义。
2 结果
2.1 正常胃组织、慢性胃炎及胃癌组织中I EX-1的表达
IEX-1蛋白在各类组织中均有阳性表达(100/100)(见附表)。正常胃黏膜上皮细胞的胞质中IEX-1表达丰富(见图1A、B);慢性胃炎组织中,肠上皮化生细胞胞质有中等量的IEX-1表达(见图1C、D);而在胃癌组织中,IEX-1有强阳性表达(见图1E、F)。经Kruskal-WallisH检验,差异有统计学意义(H= 38.609,P=0.000),相对于正常胃组织和慢性胃炎组织,胃癌组织中IEX-1蛋白表达的阳性程度更高。
2.2 人胃正常黏膜细胞和胃癌细胞中I EX-1基因和蛋白表达水平
为进一步验证免疫组织化学结果,本实验选择人正常胃黏膜细胞GES-1和胃癌细胞MKN28进行qRT-PCR和Western blot检测。IEX-1基因和蛋白表达水平比较,经t检验,差异有统计学意义(t= 13.019和6.120,P=0.006和0.026),胃癌细胞MKN28中IEX-1基因和蛋白表达水平高于人正常胃黏膜细胞GES-1。见图2、3。

附表 不同组织中I EX-1蛋白表达程度的比较 例(%)
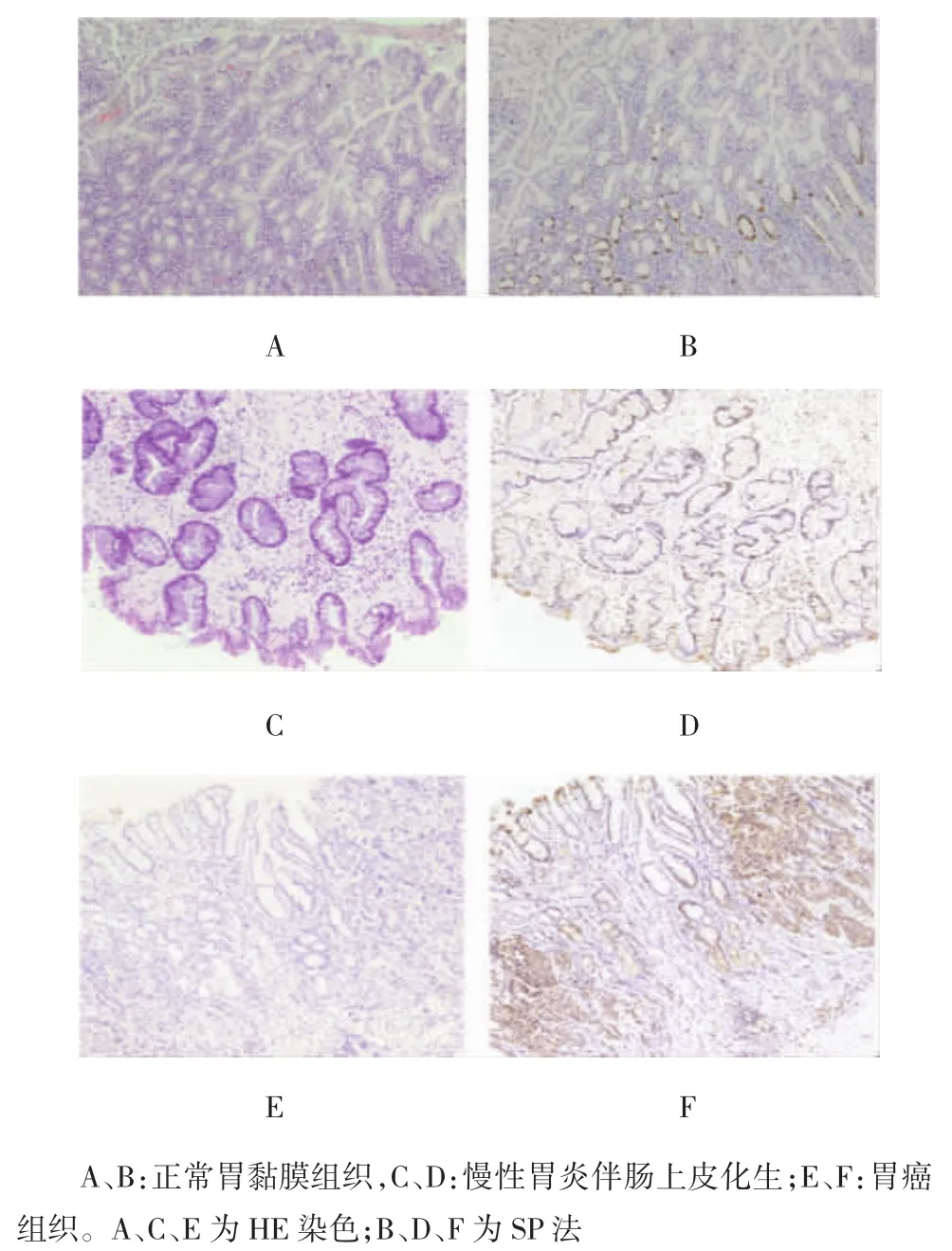
图1 I EX-1蛋白在正常胃组织、慢性胃炎及胃癌组织中的表达 (×10)
2.3 pcD N A3-FLAG-I EX-1和pLL3.7-si-I EX-1真核表达载体的构建和鉴定
为下一步了解IEX-1蛋白在胃癌进展中的意义,本实验构建IEX-1的过表达质粒pcDNA3-FLAGIEX-1和干扰质粒pLL3.7-si-IEX-1。将NotⅠ和EcoRⅠ双酶切连接好的pcDNA3-FLAG-IEX-1质粒,经1%琼脂糖电泳后,紫外线下可见在靠近500 bp处有1条带,与IEX-1 mRNA的长度相符(见图4)。将双酶切鉴定正确的过表达质粒pcDNA3-FLAGIEX-1和提取好的干扰质粒pLL3.7-si-IEX-1送上海美吉生物医药科技有限公司测序,应用Chromas软件读取测序结果,使用NCBI BLAST验证测序结果正确,说明pcDNA3-FLAG-IEX-11和pLL3.7-si-IEX-1真核表达载体构建成功。

图2 人胃正常黏膜细胞G ES-1和胃癌细胞M KN 28中I EX-1基因表达水平

图3 人胃正常黏膜细胞G ES-1和胃癌细胞M KN 28中I EX-1蛋白表达水平
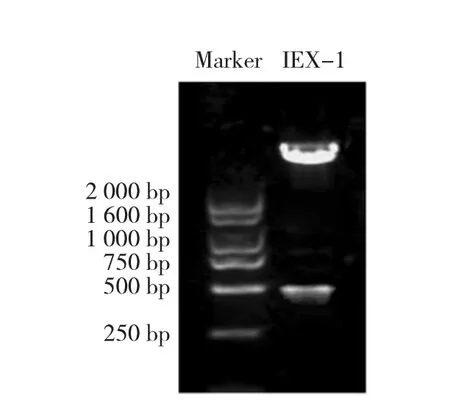
图4 pcD N A3-FLAG-I EX-1真核表达载体双酶切鉴定结果
2.4 过表达质粒pcD N A3-FLAG-I EX-1和干扰质粒pLL3.7-si-I EX-1转染胃癌细胞M KN 28后I EX-1基因和蛋白表达水平的变化
为验证过表达质粒pcDNA3-FLAG-IEX-1和干扰质粒pLL3.7-si-IEX-1在MKN28中的效果,将2种质粒转染胃癌细胞MKN28 48 h后,经qRT-PCR和Western blot检测IEX-1基因和蛋白的表达。3组IEX-1基因表达水平比较,经方差分析,差异有统计学意义(F=3 438.589,P=0.000),过表达组转染48 h后IEX-1基因表达水平升高,而干扰组IEX-1基因表达水平降低(见图5)。过表达组与对照组比较,差异有统计学意义(P<0.05);干扰组与对照组比较,差异有统计学意义(P<0.05)。3组IEX-1蛋白表达水平比较,经方差分析,差异有统计学意义(F= 311.85,P=0.000)。过表达组转染48 h后IEX-1蛋白表达水平升高,而干扰组IEX-1蛋白表达水平降低(见图6)。过表达组与对照组比较,差异有统计学意义(P<0.05);干扰组与对照组比较,差异有统计学意义(P<0.05)。过表达组IEX-1基因和蛋白表达水平均高于对照组,而干扰组IEX-1基因和蛋白表达水平均低于对照组,说明重组质粒过表达和干扰效果显著。
2.5 过表达质粒pcD N A3-FLAG-I EX-1和干扰质粒pLL3.7-si-I EX-1转染后对胃癌细胞M KN 28细胞周期的影响

图5 过表达质粒pcD N A3-FLAG-I EX-1和干扰质粒pLL3. 7-si-I EX-1转染胃癌细胞M KN 28后I EX-1基因表达水平
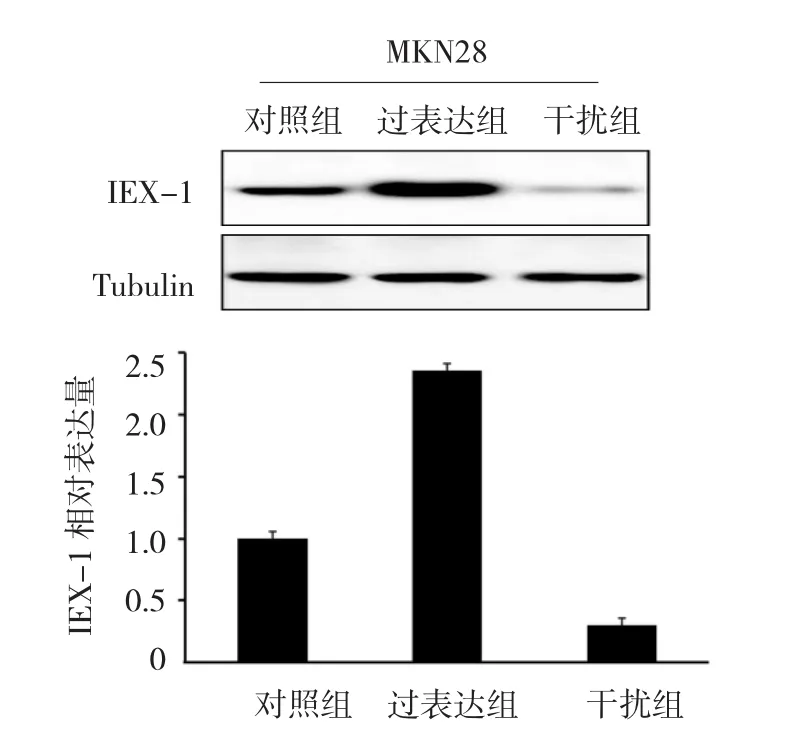
图6 过表达质粒pcD N A3-FLAG-I EX-1和干扰质粒pLL3.7-si-I EX-1转染胃癌细胞M KN 28后I EX-1蛋白表达水平
质粒转染48 h后,流式细胞术检测各组细胞周期的变化。过表达组各期细胞比例比较,经方差分析,差异有统计学意义(F=78.537,P=0.000),过表达组细胞合成期(synthesis phase,S)细胞比例升高,第二间隙期(gap phase 2,G2)细胞比例降低。过表达组S期与对照组S期比较,差异有统计学意义(P<0.05);过表达组G2期与过表达对照组G2期比较,差异有统计学意义(P<0.05)。第一间隙期(gap phase 1,g1)和G2/G1期细胞比例变化不大,经方差分析,差异无统计学意义(F=0.237,P=0.572)。过表达IEX-1后,MKN28细胞增殖更加旺盛。干扰组各期细胞比例比较,经方差分析,差异有统计学意义(F=88.324,P=0.000),干扰组G1期细胞比例升高,G2期细胞比例下降。干扰组G1期与干扰对照组G1期比较,差异有统计学意义(P<0.05),干扰组G2期与干扰对照组G2期比较,差异有统计学意义(P<0.05)。干扰组、干扰对照组各期细胞比例比较,经方差分析,差异有统计学意义(F=54.779,P=0.000),干扰组S期和G2/G1期细胞比例有所下降。干扰组S期与干扰对照组S期比较,差异无统计学意义(P>0.05),干扰组G2/G1期与干扰对照组G2/G1期比较,差异无统计学意义(P>0.05),说明干扰IEX-1蛋白表达后,MKN28细胞增殖活动受抑制,使细胞滞留于G1期。见图7。
2.6 过表达质粒pcD N A3-FLAG-I EX-1和干扰质粒pLL3.7-si-I EX-1转染后对胃癌细胞M KN 28凋亡的影响
质粒转染48 h后,流式细胞术检测各组细胞凋亡变化。各组凋亡率比较,经方差分析,差异有统计学意义(F=107.892,P=0.000)。过表达组与过表达对照组比较,差异有统计学意义(P<0.05),干扰组与干扰对照组比较,差异有统计学意义(P<0.05),说明过表达组凋亡水平低于过表达对照组,而干扰组凋亡水平高于干扰对照组。见图8。
2.7 过表达质粒pcD N A3-FLAG-I EX-1和干扰质粒pLL3.7-si-I EX-1转染后对胃癌细胞M KN 28增殖的影响
质粒转染48 h后,MTT法检测各组细胞增殖变化情况,各组增殖率比较,经方差分析,差异有统计学意义(F=88.643,P=0.000)。过表达组与过表达对照组比较,差异有统计学意义(P<0.05),干扰组与干扰对照组比较,差异有统计学意义(P<0.05),说明过表达组细胞增殖率高于过表达对照组,而干扰组细胞增殖率低于对照组。见图9。
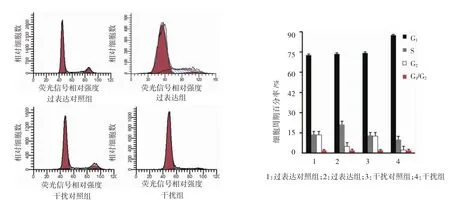
图7 过表达质粒pcD N A3-FLAG-I EX-1和干扰质粒pLL3.7-si-I EX-1转染后对胃癌细胞M KN 28细胞周期的影响
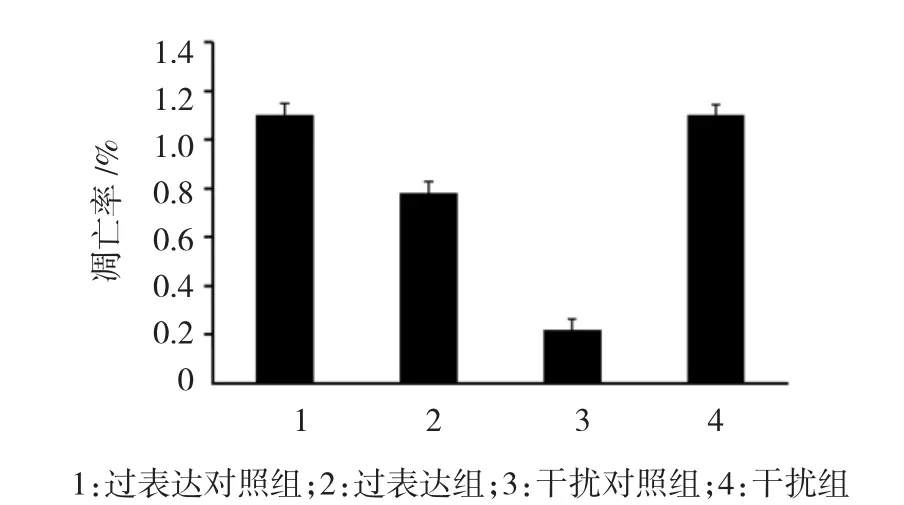
图8 过表达质粒pcD N A3-FLAG-I EX-1和干扰质粒pLL3.7-si-I EX-1转染后对胃癌细胞M KN 28凋亡的影响(±s)
3 讨论
胃癌是全球最常见的恶性肿瘤之一,更是引起恶性肿瘤患者死亡的第2大原因。我国是胃癌的高发区,其发病率和死亡率高居前列[6-7]。多年来胃癌治疗后的5年生存率一直<24%[8]。尽管目前有很多关于胃癌发生、发展过程中的知识被发现和了解,但是能够对患者更有效的胃癌基因治疗的靶向分子仍在寻找中。
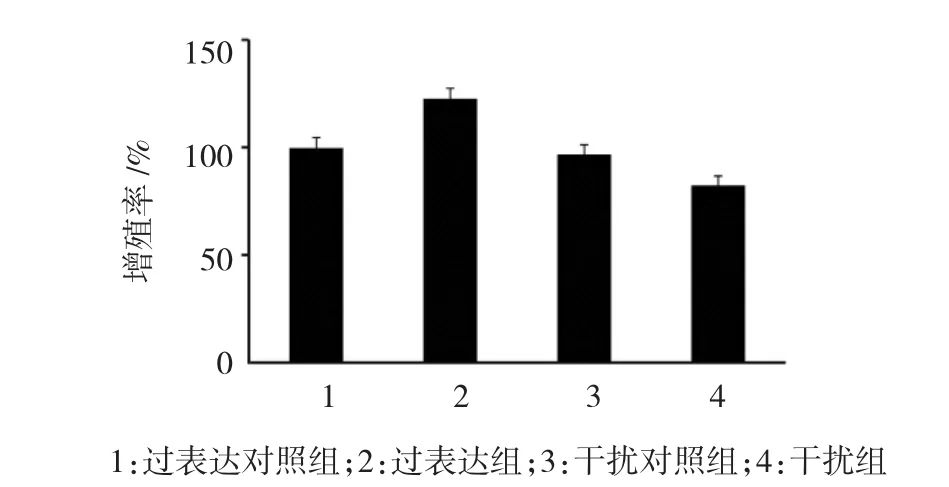
图9 过表达质粒pcD N A3-FLAG-I EX-1和干扰质粒pLL3.7-si-I EX-1转染后对胃癌细胞M KN 28增殖的影响(±s)
IEX-1首次发现于人类X射线照射引起的肿瘤细胞中[1-2],其表达有组织差异性,在皮肤、呼吸道、胃肠道、泌尿生殖系统的上皮细胞,以及多组织或器官的血管内皮细胞中广泛表达,在胰腺和乳腺中高表达;在肝、肺、淋巴结、胎盘中表达较弱;而在胸腺、睾丸、卵巢、心肌、骨骼肌、脾脏中未检测到[9-10]。同样在不同的癌组织中,其表达也有差异。仅有38.3%的卵巢癌表达IEX-1[11],胰腺癌中IEX-1则有53%的阳性表达率[12],并通过ERK磷酸化途径促进胰腺细胞的恶性转化[13];在乳腺癌组织和乳腺癌细胞株中IEX-1表达大幅度下调[14];同样直肠癌组织中IEX-1的表达比癌旁正常组织降低[15],而在骨肉瘤组织中IEX-1则呈高阳性表达[16]。目前,鲜有关于成人正常胃组织和胃癌组织中IEX-1蛋白表达的报道,且存在相互矛盾的情况。
多项研究表明,IEX-1是一种凋亡相关调节蛋白[17-19]。其可正性或负性调节细胞凋亡功能[20]。IEX-1在293细胞中通过抑制核转录因子-κB(nuclear transcription factor-κB,NF-κB)抑制剂IkBα的降解,下调基础水平和诱导水平NF-κB的活性,从而对抗NF-κB的抗凋亡作用[21]。胃泌素17对表达野生型CCK2受体结肠癌细胞的促凋亡作用也是通过IEX-1介导,依赖NF-κB抗凋亡途径而产生[22]。转染IEX-1基因的人皮肤角质形成细胞,相对于未转染细胞,细胞培养液中Caspase-3的活性增加[23]。而更早期的报道则显示,IEX-1能够抵抗TNF-α诱导的细胞凋亡作用[24]。目前关于IEX-1调节胃癌细胞生物学行为的研究,尚无定论。
本研究发现,正常胃组织中有IEX-1蛋白的表达,与FELDMANN等[9]报道一致,但胃癌组织的IEX-1蛋白表达水平要高于正常胃组织和慢性胃炎组织,为进一步验证免疫组织化学结果,本实验用qRT-PCR和Western blot检测人正常胃黏膜细胞GES-1和胃癌细胞MKN28中IEX-1基因和蛋白表达水平,结果同样显示其在胃癌细胞中呈现更高表达状态。另外,本研究结果还发现,正常胃组织发展到慢性胃炎,再至胃癌的疾病进展过程中,IEX-1的表达水平有逐渐升高的趋势,揭示IEX-1蛋白的升高可能是胃癌发生、发展过程中潜在机制之一。为探究IEX-1在胃癌进程中所起的作用,考虑其为凋亡相关调节蛋白,本实验通过外源性导入过表达质粒pcDNA3-FLAG-IEX-1和干扰质粒pLL3.7-si-IEX-1,使用流式细胞术检测IEX-1蛋白对胃癌细胞MKN28细胞周期和凋亡的影响,结果证实上调IEX-1蛋白表达能使S期细胞比例升高,G2期细胞比例降低,细胞凋亡减少,说明过表达IEX-1蛋白后,MKN28细胞增殖更加旺盛。而将IEX-1蛋白表达干扰后,胃癌细胞发生G1期阻滞,增殖受抑制并且诱导细胞凋亡。MTT法则进一步验证IEX-1蛋白促进胃癌细胞增殖的作用,说明IEX-1在调控胃癌细胞的凋亡和增殖发生转换过程中发挥重要作用。
综上所述,IEX-1蛋白在胃癌组织中呈高表达水平状态,在人胃癌细胞中上调IEX-1蛋白表达能够促进细胞增殖,发挥抗凋亡能力,干扰IEX-1蛋白表达能够阻滞细胞周期进程并诱导凋亡。因此,IEX-1蛋白在胃癌进程中发挥癌蛋白的作用。下一步笔者将就IEX-1在胃癌中相关的分子机制及下游信号通路进行研究,为IEX-1作为胃癌基因治疗的靶向分子提供科学理论依据。
[1]CHARLES C H,YOON J K,SIMSKE J S,et al.Genomic structure,cDNA sequence and expression ofgly96,agrowth factor-inducibleimmediate-earlygene encoding a short-livedglycosylated protein[J].Oncogene,1993,8(3):797-801.
[2]KONDRATYEV A D,CHUNG K N,JUNG M O.Identification and characterization of a radia tion-inducibleglycosylated human early-responsegene[J].Cancer Res,1996,56(7):1498-1502.
[3]WU M X,USTYUGOVA I V,HAN L,et al.Immediate early responsegene X-1,a potential prognostic biomarker in cancers[J]. Expert Opin Ther Targets,2013,17(5):593-606.
[4]USTYUGOVA I V,ZHI L,ABRAMOWITZ J,et al.IEX-1 deficiency protects against colonic cancer[J].Mol Cancer Res,2012, 10(6):760-767.
[5]ARLT A,SCHAFER H.Role of the immediate early response 3 (IER3)gene in cellular stress response,inflammation and tumorigenesis[J].Eur J Cell Biol,2011,90(6/7):545-552.
[6]BRENNER H,ROTHENBACHER D,ARNDT V.Epidemiology of stomach cancer[J].MethodsMol Biol,2009,472:467-477.
[7]CATALANO V,LABIANCA R,BERETTAg D,et al.Gastric cancer[J].Crit Rev Oncol Hematol,2009,719(2):127-164.
[8]FERLAY J,SHIN H R,BRAY F,et al.Estimates of worldwide burden of cancer in 2008:GLOBOCAN 2008[J].Int J Cancer, 2010,127(12):2893-2917.
[9]FELDMANN K A,PITTELKOW M R,ROCHE P C,et al.Expression of an immediate earlygene,IEX-1,in human tissues[J]. Histochem Cell Biol,2001,115(6):489-497.
[10]张明,朱武,肖涛.1种独特的凋亡调节蛋白IEX-1[J].中南大学学报(医学版),2011(3):274-277.
[11]HAN L,GENG L,LIU X,et al.Clinical significance of IEX-1 expression in ovarian carcinoma[J].Ultrastruct Pathol,2011,35(6):260-266.
[12]SASADA T,AZUMA K,HIRAI T,et al.Prognostic significance of the immediate early responsegene X-l(IEX-l)expression in pancreatic cancer[J].Ann Surg Oncol,2008,15(2):609-617.
[13]GARCIA M N,GRASSO D,LOPEZ-MILLAN M B,et al.IER3 supports KRASG12D-dependent pancreatic cancer development by sustaining ERK1/2 phosphorylation[J].J Clin Invest,2014:124(11):4709-4722.
[14]HU Y,SUN H,DRAKE J,et al.From mice to humans:identification of commonly deregulatedgenes in mammay cancer viacomparative SAGE studies[J].Cancer Res,2004,64(21):7748-7755.
[15]NAMBIAR P R,NAKANISHI M,GUPTA R,et al.Genetic signatures of high-and low-risk aberrant crypt foci in a mouse model of sporadic colon cancer[J].Cancer Res,2004,64(18):6394-6401.
[16]XIAO T,LI K H,LIg Y,et al.Mechanism of apoptosis of human osteosarcoma MG-63 induced by arsenic trioxide[J].Journal of Central South University of Technology,2005,12(suppl 1):317-321.
[17]de KEULENAERg W,WANG Y,FENG Y,et al.Identification of IEX-1 as a biomechanically controlled nuclear factorkappa β targetgene that inhibits cardiomyocyte hypertrophy[J]. Circ Res,2002,90(6):690-696.
[18]KOBAYASHI T,PITTELKOW M R,WARNERg M,et al. Regulation of a novel immediate early responsegene,IEX-1,in keratinocytes by 1alpha,25-dihydroxyvitamin D3[J].Biochem Biophys Res Commun,1998,251(3):868-873.
[19]ZHANG Y,SCHLOSSMAN S F,EDWARDS R A.et al.Impaired apoptosis,extended duration of immune responses,and a lupus-like autoimmune disease in IEX-1-transgenic mice[J]. Proc Natl Acad Sci USA,2002,99(2):878-883.
[20]耿莉娜,张晓雪,韩丽萍.即刻早期基因IEX-1与肿瘤[J].中国肿瘤临床,2012(4):234-236.
[21]ARLT A,MINKENBERG J,KOCS B,et al.The expression of immediate earlygene X-1 (IEX-1)is differentially induced by retinoic acids in NB4 and KG1 cells:possible implication in the distinct phenotype of retinoic acid-responsive and-resistant leukemic cells[J].Leukemia,2004,18(10):1646-1655.
[22]SEBENS MÜERKÖSTER S,RAUSCH A V,ISBERNER A.The apoptosis-inducing effect ofgastrin on colorectal cancer cells relates to an increased IEX-1 expression mediating NF-kappa B inhibition[J].Oncogene,2008,27(8):1122-1134.
[23]SCHILLING D,PITTELKOW M R,KUMAR R,et al.IEX-1, an immediate earlygene,increases the rate of apoptosis in keratinocytes[J].Oncogene,2001,20(55):7992-7997.
[24]WU M X,AO Z,PRASAD K V,et al.IEX-1L,an apoptosis inhibitor involved in NF-kappa β-mediated cell survival[J]. Science,1998,281(5379):998-1001.
(童颖丹 编辑)
Expression of IEX-1 protein ingastric carcinoma and its effect on apoptosis and proliferation of humangastric cancer cells*
Shan-shan Mao,Xiao-zhen Cheng,Rong-hua Cui,Jiang-hua Yuan,Mei-qing Wang
(Department of Oncology,Haikou Hospital Affiliated to Xiangya Medical College of Central South University,Haikou,Hainan 570208,China)
ObjectiveTo reveal the expression of IEX-1 protein ingastric cancer tissues and cell lines, and investigate the effect of IEX-1 on the proliferation and apoptosis of humangastric cancer cells.MethodsImmunohistochemistry was used to detect IEX-1 protein expression in 100 samples ofgastric mucosal biopsy. IEX-1gene and protein expressions were detected by fluorescence qRT-PCR and Western Blot respectively in normalgastric mucosagES-1 cells andgastric cancer MKN28 cells.pcDNA3-FLAG-IEX-1 plasmid and pLL3.7-si-IEX-1 plasmid were transfected into MKN28 cells respectively,and then cell cycle,apoptosis and proliferation were detected by flow cytometry and MTT assay.MethodsThe expression of IEX-1 protein in thegastric cancer tissues was higher than that in the normalgastric tissues and the chronicgastritis tissues (P<0.05),and the expression level of IEX-1 wasgradually increased with the progress of the disease.The expressions ofIEX-1gene and protein in thegastric cancer MKN28 cells were higher than those in the normalgastric mucosalgES-1 cells (P<0.05).Compared with the controlgroup,the increased expression of IEX-1 protein could increase the proportion of the cells in S phase,decrease the proportion of the cells ing2 phase,increase the rate of cell proliferation,and decrease apoptosis (P<0.05).After the expression of IEX-1 protein was interfered,the percentage ofg1 phase cells increased,that ofg2 phase cells decreased, the rate of cell proliferation decreased,apoptosis increased (P<0.05).ConclusionsIEX-1 protein is highly expressed ingastric cancer tissues.Up-regulation of IEX-1 protein expression can promote the proliferation ofhumangastric cancer cells and play an anti-apoptotic role.Interfering with the expression of IEX-1 protein could block cell cycle progression and induce apoptosis.
gastric cancer;IEX-1;proliferation;apoptosis
R735.2
A
2017-03-20
2013年海南省海口市重点科技计划项目(No:2013-70)
10.3969/j.issn.1005-8982.2017.20.006
1005-8982(2017)20-0026-08
