双氢青蒿素合成工艺探讨
2017-09-16王令兆吴洪达王读福管廷江
王令兆,吴洪达,王读福,管廷江
(1.山东潍焦集团工程技术有限公司,山东 潍坊 262404;2.广西科技大学 生物与化学工程学院,广西 柳州 545006)
双氢青蒿素合成工艺探讨
王令兆1,吴洪达2*,王读福1,管廷江1
(1.山东潍焦集团工程技术有限公司,山东 潍坊 262404;2.广西科技大学 生物与化学工程学院,广西 柳州 545006)
用硼氢化钠还原青蒿素合成双氢青蒿素,用高效液相色谱法分析组分含量;考察了反应溶剂、还原剂用量、添加剂种类和用量、反应温度等因素对合成反应的影响。结果表明,溶剂性质影响青蒿素的溶解度和硼氢化钠的稳定性,但不是影响反应速率及双氢青蒿素产率的决定性因素;甲醇是最适宜的反应溶剂,反应过程中,硼氢化钠与甲醇反应生成甲氧基硼氢负离子(BH3(OCH3)-),然后将青蒿素还原为双氢青蒿素;添加氯化钙有助于提高反应速率;反应温度过高以及反应时间过长会导致副反应增多。在甲醇溶液中,当n(CaCl2)/n (DHA)=0.3,n(NaBH4)/n(ART)=2.5,0℃反应1.5 h。青蒿素转化率高于98%,双氢青蒿素产率高于96%。
青蒿素;双氢青蒿素;硼氢化钠;无水氯化钙
青蒿素是我国首次发现的抗疟特药物,由于其油溶性、水溶性均不佳,稳定性差,限制了它的医用价值,因此,人们制备了一系列青蒿素衍生物,其中双氢青蒿素与青蒿素相比具有更好的水溶性,更易吸收且具有排泄和代谢迅速、高效、低毒等优点[1],其抗疟作用是青蒿素的4~ 8倍[2];同时,双氢青蒿素也是合成青蒿素衍生物抗疟药的中间原料,深入研究其合成工艺具有重要意义。过去的研究[3-8]表明,由青蒿素合成双氢青蒿素过程中,还原剂用量、溶液酸碱度、溶剂性质、反应温度和反应时间会显著影响青蒿素转化率和双氢青蒿素产率,但有关反应机理未有详尽的表述。本文进一步研究了青蒿素合成双氢青蒿素的工艺,对硼氢化钠还原青蒿素的反应机理进行了分析,探讨了一些添加剂在合成反应中的作用。
1 实验部分
1.1 仪器与试剂
1.1.1 仪器
高效液相色谱仪(岛津LC一20AT);紫外检测器(岛津SPD-20A);自动双重纯水蒸馏器(上海亚荣生化仪器厂)。
1.1.2 试剂
青蒿素(广西仙草堂制药有限责任公司,纯度≥99.99%),乙腈(色谱纯);硼氢化钠,氯化钙等试剂均为分析纯。
1.2 合成与检测
在圆底烧瓶中加入青蒿素和溶剂,室温搅拌溶解,加入助剂继续搅拌溶解,转移到冰水浴中,分批加入一定量硼氢化钠,搅拌反应一定时间后,用盐酸终止反应,调节溶液pH值在5~6。样品经过滤后用HPLC法分析组分含量。色谱条件:色谱柱: 岛津ODS-C18(4.6 mm × 250 mm,5μm); 流动相: 20 mmol/L 磷酸盐溶液(pH值5.0)-乙腈(40∶60);柱温25℃;检测波长210nm;流速1.0 mL/min。
2 结果与讨论
2.1 反应溶剂的影响
为了选择合适的溶剂,首先研究了硼氢化钠在几种常见溶剂中的稳定性,用碘量法[9]测定溶剂中硼氢化钠的剩余量,结果如图1所示。由图1可见,硼氢化钠溶于溶剂后的最初几分钟内,其分解反应速率很高,10min后,硼氢化钠的分解率变化相对较小;原因是,而硼氢化钠与溶剂接触反应后,溶液的碱性增强,提高了硼氢化钠的稳定性[10]。由图1还可看出,硼氢化钠在溶剂里的稳定性排序为:无水乙醇>蒸馏水>N,N-二甲基甲酰胺>二氯甲烷和N,N-二甲基甲酰胺混合液(体积比1∶1)>甲醇和N,N-二甲基甲酰胺混合液(体积比1∶1)>甲醇和二氯甲烷混合液(体积比1∶4)>甲醇。显然,硼氢化钠在甲醇中很不稳定,这与甲醇的羟基氢较活泼有关。因此,在甲醇溶剂中使用硼氢化钠作还原剂时,应将硼氢化钠固体分多次少量加入为宜。
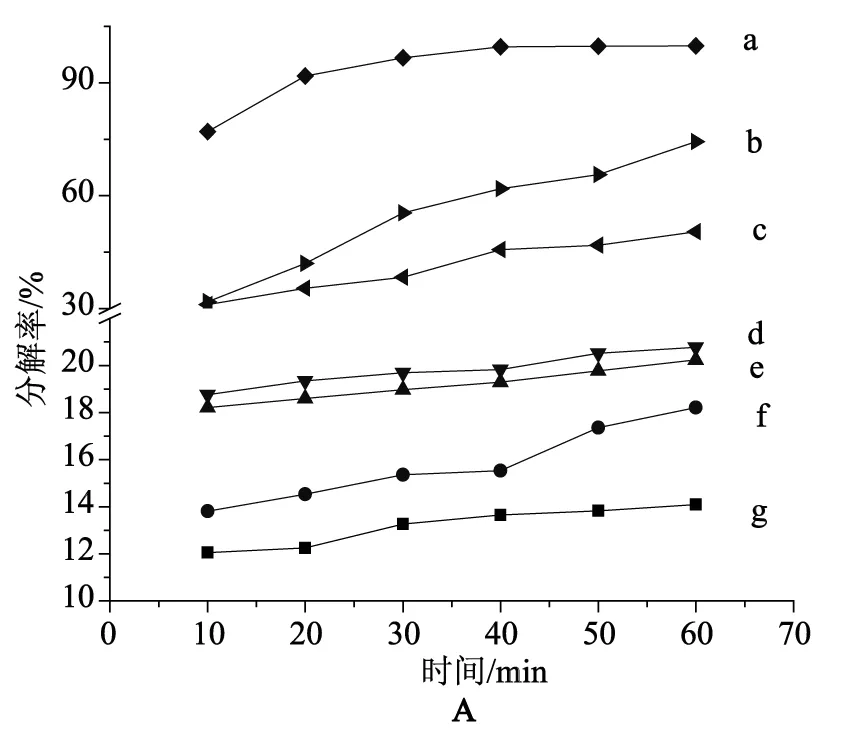
a.甲醇;b.甲醇和二氯甲烷(1∶4);c.甲醇和N,N-二甲基甲酰胺(1∶1);d.二氯甲烷和N,N-二甲基甲酰胺(1∶1);e.N,N-二甲基甲酰胺;f.水;g.乙醇
图1 硼氢化钠在0℃(A)和20℃(B)不同溶剂中的稳定性
Fig.1 Stability of sodium borohydride in different solvent
在二氯甲烷溶剂中合成双氢青蒿素的研究已有文献报道[4],我们考察了其它几种溶剂对双氢青蒿素产率的影响,实验选择0℃下反应1.5 h,结果如表1所示。

表1 不同溶剂中,双氢青蒿素在不同时间的产率
表1说明,溶剂性质对反应速率及双氢青蒿素产率的影响十分显著。虽然图1表明,硼氢化钠在乙醇和N,N-二甲基甲酰胺溶剂稳定性好,而在甲醇溶剂中稳定性很差;但表1显示,在乙醇、N,N-二甲基甲酰胺和乙酸甲酯溶剂中,青蒿素与硼氢化钠的反应速率很小,双氢青蒿素产率较低,不是合成双氢青蒿素的好溶剂;而甲醇表现为良好的反应溶剂,0℃下反应1.5 h,青蒿素转化率为97.67 %,双氢青蒿素产率达到96.57 %。因此,从硼氢化钠在溶剂中的稳定性不能对实验结果作出好的解释。我们再来考虑溶剂极性的影响,文献[5]曾指出,在水溶液中,硼氢化钠对青蒿素的还原反应经历了SN1反应历程;按照SN1反应的特征,溶剂极性增大时,应有利于青蒿素转化为极性更大的双氢青蒿素。但表1所用的溶剂中,甲醇极性为6.6,N,N-二甲基甲酰胺极性为6.4,两者极性相差不大,而在甲醇中硼氢化钠与青蒿素的反应速率要比在甲醇和N,N-二甲基甲酰胺组成的混合溶剂中的反应速率大很多。因此,溶剂极性的改变也不是影响硼氢化钠与青蒿素反应速率的主要因素。表1给出的结果差异可能提示硼氢化钠或四氢化硼负离子与青蒿素直接反应的速率比较小,而烷氧基硼氢负离子BH3(OR)-可能是更好的还原剂。我们认为,在甲醇溶剂中,硼氢化钠先与甲醇反应生成的烷氧基负离子可能与新生态硼烷(BH3)结合成中间产物—烷氧基硼氢负离子BH3(OR)-,由于烷氧基的供电子性,提高了烷氧基硼氢负离子中氢原子的电子云密度,从而增强了烷氧基硼氢负离子上的氢向青蒿素带正电性的羰基碳原子进攻的能力。乙醇分子上的氢原子活泼性小,不易生成乙氧基负离子,所以,在乙醇溶剂中,青蒿素与硼氢化钠的反应速率较小;在乙酸甲酯和N,N-二甲基甲酰胺溶剂中,硼氢化钠不能生成烷氧基,只能以四氢化硼负离子与青蒿素反应,故速率小。综上所述,在甲醇溶液中,烷氧基负离子的存在及其浓度才是影响硼氢化钠与青蒿素反应速率的主要因素。
2.2 还原剂用量的影响
硼氢化钠,硼氢化钾,氢化铝锂,硼烷等均是有机反应中常用的还原剂,硼氢化钠,硼氢化钾的还原性较弱,适用于醛或酮羰基的还原反应,而氢化铝锂,硼烷等试剂的还原性较强,会导致青蒿素过氧基团的还原,所以,由青蒿素制备双氢青蒿素常用比较温和的硼氢化钠作还原剂。图2给出甲醇为溶剂,在0℃反应1.5 h,硼氢化钠的用量与青蒿素转化率以及双氢青蒿素产率的关系。

图2 还原剂用量对原料转化率和产物产率的影响
从图2可知,随着硼氢化钠用量递增,青蒿素转化率逐渐升高,在硼氢化钠用量为0.20 g时,青蒿素转化率可达99%。双氢青蒿素的产率也随着还原剂用量递增而增大,在硼氢化钠用量为0.16 g时,产率最高,达92.77%,但继续增加硼氢化钠用量时,双氢青蒿素产率有降低的趋势。这是因为,过量的硼氢化钠将与双氢青蒿素分子中的过氧基反应[6],甚至与分子中的内酯键反应[11],导致副产物增加,双氢青蒿素产率下降。因此,控制硼氢化钠的用量是必要的。
2.3 添加剂的作用
文献[12]研究表明,在硼氢化钠与有机物的还原反应中,加入某些无机路易斯酸可显著提高还原剂的活性和选择性。为此,我们研究了几个添加剂对合成反应的影响。结果如表2和表3所示。

表2 添加剂对青蒿素转化率的影响

表3 添加剂对双氢青蒿素产率的影响
从表2可见,随反应时间延长,青蒿素转化率逐渐升高;但只有CaCl2,MgCl2,MgSO4能够促进反应;ZnSO4、ZnCl2对反应起抑制作用。从表3看,无添加剂或以CaCl2、MgCl2、MgSO4为添加剂时,在1.5 h内,双氢青蒿素的产率随反应时间增加而升高;反应时间增至2 h后,无添加剂的反应体系中,双氢青蒿素的产率仍然升高,但有添加剂的反应体系中,双氢青蒿素的产率均出现降低的趋势。
Ca2+,Mg2+离子能够促进反应,可能由于碱土金属离子是一种较为适宜的路易斯酸。在甲醇溶液中,这种离子可能与硼氢化钠及甲醇反应形成还原能力较强的烷氧基硼氢化钙(镁),然后,利用钙(镁)离子跟青蒿素分子中的羰基氧配位,导致羰基碳原子正电性增大,有利于烷氧基硼氢负离子进攻羰基碳,随着氢负离子加成到羰基碳上,金属离子与羰基氧的配位键断裂,氧基负离子再与溶液中的氢离子结合形成羟基。其反应机理如图3所示。
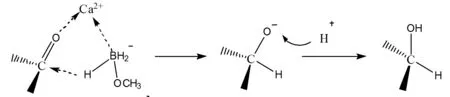
图3 Ca2+存在下,烷氧基硼氢负离子还原羰基
Fig.3 Alkox boron hydrogen anion reductive carbonyl group under Ca2+
比较表2和表3中,以MgCl2、MgSO4为添加剂时,共存阴离子对反应也有影响,Cl-离子对反应速率的增效比SO42-离子更好,可能与Cl-离子更易参与配位反应有关。在反应体系中加入ZnSO4和ZnCl2时,青蒿素转化率和双氢青蒿素产率均非常小,显示其强烈地抑制反应。
2.4 添加剂用量
为了探究添加剂用量对合成反应的影响,以甲醇为溶剂,催化剂用量为n(NaBH4)/n(ART) = 2.5,选择不同的添加剂用量,0℃下反应1.5 h,结果如图4所示。
从图4可以看出,在反应体系加入氯化钙时,青蒿素转化率随着氯化钙量增加而增大。当氯化钙与青蒿素的物质的量之比为0.5时,青蒿素转化率达100%,继续增加氯化钙用量,青蒿素的转化率趋于稳定。但氯化钙加入量过多时,双氢青蒿素产率降低,推测是因为钙离子浓度大时,生成的烷氧基硼氢负离子浓度太大,导至双氢青蒿素中的过氧基或内酯键被还原,故双氢青蒿素产率降低。为了验证上述推测,我们考察了氯化钙对双氢青蒿素稳定性的影响,结果如图5所示。

图4 添加剂用量对青蒿素转化率和双氢青蒿素产率的影响

图5 时间对双氢青蒿素的稳定性的影响
实验表明,双氢青蒿素在单一的甲醇溶液中3h内是稳定存在的,而加入氯化钙后,双氢青蒿素半小时即发现分解。当氯化钙加入量为n(CaCl2)/n(DHA)=0.3时,共存1.5 h,双氢青蒿素分解率达80%,继续增加氯化钙用量,双氢青蒿素分解率升高,但幅度比较小。而且双氢青蒿素的分解率在80%左右与合成实验产率是吻合的。
2.5 反应时间
为了探究反应时间对合成反应的影响,以甲醇为溶剂,n(NaBH4)/n(ART)=2.5,n(CaCl2)/n(DHA)=0.3,在0℃下反应,结果如图6所示。

图6 反应时间对青蒿素转化率和双氢青蒿素产率的影响
从图6中可以看出,随着反应时间的延长,青蒿素的转化率逐渐增大,在反应1.5 h后,转化率变化已经很小;双氢青蒿素产率随着反应时间的延长,先增大后减小,反应1.5 h双氢青蒿素产率最大。这是因为,双氢青蒿素在碱性溶液不稳定[7],会逐步开环脱去环中醚键上的氧,并脱去环内过氧键,在甲醇溶液中形成甲基化的环状半羧醛[13]。
2.6 反应温度
以甲醇为溶剂,催化剂用量为:n(NaBH4)/n(ART)=2.5,n(CaCl2)/n (DHA)=0.3,在不同温度下反应1.5h,发现反应温度对合成反应的影响结果如图7所示。

图7 反应温度对青蒿素转化率和双氢青蒿素产率的影响
从图7可以看出,在试验所涉温区,青蒿素的转化率随温度变化不大,转化率都在98%以上;但温度对双氢青蒿素的产率有明显的影响,随着温度的升高,双氢青蒿素的产率逐渐降低。这是因为,温度升高时,双氢青蒿素分子中的过氧键发生分解[8,14]。高效液相色谱分析结果也表明,随着温度的升高,生成的杂质峰逐渐增多,杂质峰面积也增大,如图8所示。

a.杂质;b. α-双氢青蒿素;c. β-双氢青蒿素;d. 青蒿素
2.7 优化条件的验证
在圆底烧瓶中加入青蒿素和无水甲醇,室温搅拌溶解后,加入无水氯化钙(n(CaCl2)/n (DHA)=0.3)搅拌溶解,然后分批加入硼氢化钠(n(NaBH4)/n(ART)=2.5),0℃反应1.5h。青蒿素转化率高于98%,双氢青蒿素产率高于96%。
3 结论
(1)在甲醇溶剂中硼氢化钠还原青蒿素时,起到还原作用的是甲氧基硼氢负离子,添加氯化钙能提高青蒿素还原反应速率。
(2)以甲醇为溶剂,硼氢化钠为还原剂,氯化钙为添加剂,0℃反应1.5 h,青蒿素的转化率高于98%,双氢青蒿素的产率高于96%。
[1] 韩丽平,黄 强,曾丽艳,等. 青蒿素及其衍生物的抗疟机制研究进展[J]. 自然科学通报,2009,19(1):25-32.
[2] 赵凯存,宋振玉. 双氢青蒿素在人的药代动力学及与青蒿素的比较[J].药学学报,1993,28(5):342-346.
[3] 江剑芳,张友全,李晓华,等. 正交实验法研究双氢青蒿素的制备工艺[J]. 应用化工,2008,37(10):1175-1178.
[4] 赵金召,徐 杰,张 梅,等. 蒿甲醚的合成工艺改进[J]. 广东化工,2013,40(16):58-59.
[5] 李雪芳. 蒿甲醚的合成工艺和分析研究[D]. 成都: 电子科技大学,2008.
[6] Galasso V,Kovac B,Modelli A. A theoretical and experimental study on the molecular and electronic structures of artemisinin and related drug molecules[J]. Chemical Physics,2007,335(2-3):141-154.
[7] Boehm M,Fuenfschilling P C,Krieger M,et al. An improved manufacturing process for the antimalaria drug coartem.Part I[J]. Organic Process Research & Development ,2007,11: 336-340.
[8] Stringham R W,Teager D S. Streamlined process for the conversion of artemisinin to artemether[J].Organic Process Research&Development,2012,16: 764-768.
[9] 赵家雄. 电解偏硼酸钠合成硼氢化钠的研究[D]. 重庆: 重庆大学,2008.
[10] Huang Shiping,Liu Chuan,Li Jia,et al. Frist-principles study on the synergistic effects of Ti and F co-doping on the structure and dehydrogenation properties of NaBH4[J]. International Journal of Hydrogen Energy,2014,39(25): 13512-13518.
[11] 王 赟,杨郭明,李秀珍,等. (S)-(+)-5-羟甲基-2-吡硌烷酮的合成方法改进[J].化学试剂,2005,27(1):41-42.
[12] 张江华. HfCl4/硼氢化物体系的还原性研究[D].大连:大连理工大学,2010.
[13] Sy L K,Hui S M,Cheung K K,et al.A rearranged hydroperoxide from the reduction of artemisinin[J].Tetrahedron,1997,53(22): 7493-7500.
[14] Lin A J,Theoharides A D,Klayman D L.Therma decomposition products of dihydroartemisinin[J].Tetrahedron,1986,42: 2181-2184.
(本文文献格式:王令兆,吴洪达,王读福,等.双氢青蒿素合成工艺探讨[J].山东化工,2017,46(7):52-55,60.)
Study on Synthesis of Dihydroartemisinin
WangLingzhao1,WuHongda2*,WangDufu1,GuanTingjiang1
(1.Shandong Weijiao Holdings Group Co.,Ltd.,Weifang 262404,China; 2.College of Biological and Chemical Engineering, Guangxi University of Science and Technology,Liuzhou 545006,China)
The dihydroartemisinin were formed from artemisinin using sodium borohydride as reductant, and the content of each component were analysised by high performance liquid chromatography (HPLC);The factors on the influence of synthetic reaction were investigated,such as reaction solvent,dosage of reducing agent,additives,reaction temperature and so on. The results showed that the solvent affects the solubility of artemisinin and the stability of sodium borohydride,and it is also not the decisive factor of the reaction rate and the yield of dihydroartemisinin; Methanol is the most suitable solvents in the process,and the reduction of artemisinin to dihydroartemisinin promoted by BH3(OCH3)-,which producted from the reaction sodium borohydride with methanol; The calcium chloride helps to improve the reaction rate; The side effect were significantly when temperature rising and time prolonged. As a result,in methanol solution,when n (CaCl2)/n (DHA) = 0.3,n (NaBH4)/n (ART) = 2.5,the reacton temperature is 0 ℃ and reactin time is 1.5 h,the conversion of artemisinin above 98%,the yield of dihydroartemisinin is higher than 96%.
artemisinin;dihydroartemisinin;sodium borohydride;anhydrous chloride calcium
2017-03-03
王令兆(1989—),男,山东昌乐人,硕士;通讯作者:吴洪达(1958—),男,广西罗城人,教授,主要从事催化化学的研究。
O626
A
1008-021X(2017)07-0052-04
