大瓶装医用超声耦合剂卫生状况调查
2017-09-15司徒敏雄郭巧芝赵丹洋王洁琳
司徒敏雄, 郭巧芝, 周 轶, 赵丹洋, 罗 睿, 王洁琳
(广州市妇女儿童医疗中心, 广东 广州 510623)
大瓶装医用超声耦合剂卫生状况调查
司徒敏雄, 郭巧芝, 周 轶, 赵丹洋, 罗 睿, 王洁琳
(广州市妇女儿童医疗中心, 广东 广州 510623)
目的了解医疗机构大瓶装医用超声耦合剂卫生状况。方法2012年2月—2016年4月,通过现场随机抽样检测方法,对某妇女儿童专科医院使用的大瓶装医用超声耦合剂微生物污染情况进行调查与分析。结果共抽取样本170份,合格25份,合格率为14.71%。来源部门主要为住院病房(58.24%)及手术部门(21.76%);各部门标本合格率比较,差异无统计学意义(P>0.05)。 开启前后的耦合剂污染率均达80%以上,差异无统计学意义(P>0.05)。共检出145株病原菌,其中未开启的大瓶装耦合剂中检出18株,已开启的检出127株。开启前后主要污染菌均为洋葱伯克霍尔德菌,分别占83.33%、54.33%,启用后的污染菌还有铜绿假单胞菌及黏质沙雷菌(各占15.75%),复合污染菌中均含黏质沙雷菌。结论大瓶装医用超声耦合剂细菌含量超标严重,生产商应严格质量控制标准,医疗机构在使用中应采取有效清洁消毒措施。
医用耦合剂; 卫生状况; 微生物
[Chin J Infect Control,2017,16(9):849-851]
大瓶装(0.25 L/瓶,以下略)医用耦合剂在临床工作中被广泛应用,且直接与患者皮肤甚至黏膜接触。但现行的医用耦合剂国家标准是修订于2008年的YY0299-2008《医用超声耦合剂》[1](2010 年6 月1 日实施),未对医用耦合剂做卫生学要求,给医院感染管理带来困惑。近年来,国内外研究[2-5]对医用耦合剂卫生状况及由此引发的医院感染情况进行了报道。为进一步了解专科医院医用耦合剂使用过程中的卫生状况,便于国家行政管理部门及医院感染管理部门制定医疗机构内医用耦合剂使用管理细则,本研究对某三甲专科医院内广泛使用的大瓶装医用耦合剂进行卫生学检测。
1 对象与方法
1.1 调查对象 2012年2月—2016年4月,在该院广泛使用的接触未破损皮肤的大瓶装医用耦合剂(广东广工技术开发公司轻化部生产,粤穗食药监械(准)字2013第1230064号不同批次医用耦合剂),包括用于B超机、心脏彩超机、胎心/多普勒监测仪、康复治疗仪等各种仪器(加入了消毒/灭菌成分的耦合剂除外)。医用耦合剂存储于医院各部门治疗室或储物间,医院环境采用中央空调,室内温度24~26℃,湿度30%~60%。
1.2 调查方法 2012年2月—2016年4月,对上述仪器的已启用一周内的大瓶装医用耦合剂随机采样。采集的标本送微生物实验室进行卫生学检测。在一些使用量大、存放未开启耦合剂的科室,同时从未开启的耦合剂瓶内采样并送检。
1.3 采样方法 根据WS/T367-2012《医疗机构消毒技术规范》[6]规范性附录A,采用无菌操作技术进行耦合剂采样及检测,包括细菌菌落数定量及菌种鉴定。采样时先挤出2 mL弃掉,再用无菌干燥试管收集2 mL送检。
1.4 评价标准 普通医用耦合剂参照GB15979-2002《一次性使用卫生用品的卫生标准》[7]规定,细菌总数≤200 CFU/g,真菌总数≤100 CFU/g,均未检出大肠菌群和致病菌为合格。
2 结果
2.1 大瓶装医用耦合剂来源部门及合格率 大瓶装医用耦合剂标本来源于医院内各临床科室,共采样170份,合格25份,合格率为14.71%。来源部门包括住院病房(99份,58.24%)、手术部门(37份,21.76%)、门急诊(23份,13.53%)、辅助科室(11份,6.47%);微生物检测合格率门急诊较高(5份,21.74%),其次为住院病房(14份,14.14%)、手术科室(5份,13.51%),辅助科室最低(1份,9.09%),各部门合格率比较,差异无统计学意义(χ2=1.251,P=0.74)。
2.2 大瓶装医用耦合剂开启前后污染情况 检测的耦合剂污染率达85.29%,其中开启的耦合剂污染率为85.81%(127/148),未开启的污染率为81.82%(18/22),开启前后比较,差异无统计学意义(χ2=0.702,P=0.40)。
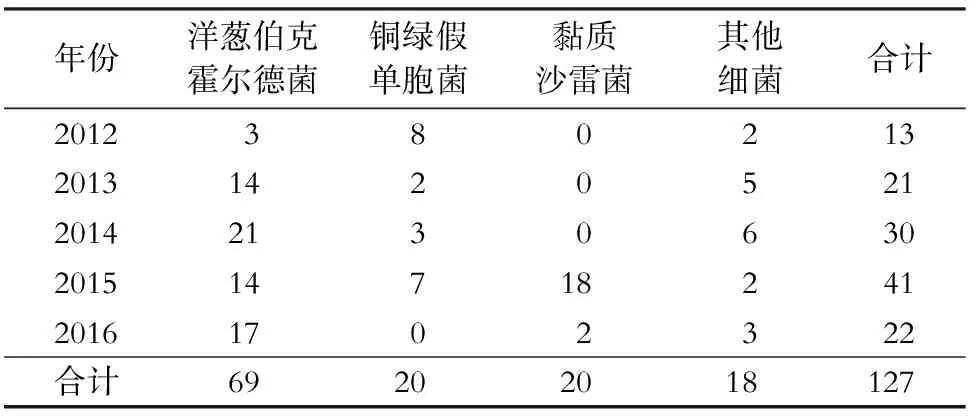
2.3 大瓶装耦合剂污染病原菌分布 共检出145株病原菌,其中未开启的大瓶装耦合剂污染菌主要为洋葱伯克霍尔德菌(15株,占83.33%),大肠埃希菌、鲁氏不动杆菌及铜绿假单胞菌各1株(各占5.56%)。已开启的大瓶装耦合剂污染病原菌主要为洋葱伯克霍尔德菌(69株,54.33%)、铜绿假单胞菌及黏质沙雷菌(各20株,各占15.75%),其他污染菌(18株,14.17%);其中有3份标本中检出复合污染菌,2份标本中检出黏质沙雷菌和洋葱伯克霍尔德菌,1份标本中检出黏质沙雷菌和铜绿假单胞菌;其他污染菌包括肺炎克雷伯菌、鲁氏不动杆菌、大肠埃希菌、阴沟肠杆菌、鲍曼不动杆菌、门多萨假单胞菌及嗜麦芽窄食单胞菌等;2015年黏质沙雷菌异常增多,占全年检出病原菌的43.90%。见表1。
表1已开启大瓶装医用耦合剂污染病原菌分布
Table1Distribution of contaminated pathogens in medical coupling gel in large bottles
年份洋葱伯克霍尔德菌铜绿假单胞菌黏质沙雷菌其他细菌合计2012380213201314205212014213063020151471824120161702322合计69202018127
3 讨论
随着诊疗技术的进步,医用超声探头和耦合剂在临床和医技部门的使用越来越普遍,微生物污染状况及可能带来的医院感染风险也日益凸显。国内研究[2-3]显示,医用超声耦合剂的卫生状况不容乐观。沈芃等[8]检测发现使用的超声耦合剂细菌总数超标率50%,市售耦合剂细菌总数超标率也达40%。本调查显示,大瓶装医用耦合剂污染率达85.29%,其中开启的耦合剂为85.81%,未开启的为81.82%。可见,医用超声耦合剂污染状况严重,应引起重视。
本次调查发现,医用超声耦合剂标本来源部门之间的合格率比较差异无统计学意义。同时开启前后医用耦合剂污染率比较差异也无统计学意义。可见,未开启的医用耦合剂已存在污染情况,提示污染的源头包括生产厂家未严格执行质控标准,在生产场所、产品运输过程中已产生污染。国家未对该类产品设定卫生学标准,因此,给医疗机构带来潜在风险。国外也有研究[9]发现医用耦合剂污染来源于制造商的报道。启用后的耦合剂后续污染情况较严重,可能与操作使用后无法清洁消毒有关,尤其各种探头接触耦合剂后未能及时清洁消毒,反复交叉污染极为常见。
污染病原菌分布结果显示,开启前后主要污染菌均为洋葱伯克霍尔德菌,分别占83.33%、54.33%,启用后的污染菌还有铜绿假单胞菌及黏质沙雷菌(各占15.75%),复合污染菌中均含黏质沙雷菌。在国外,因超声耦合剂污染而导致的肠道、呼吸道等各种感染也时有报道[10-12],可见被污染的耦合剂极易成为医院感染的高度危险性物品,是医院感染的高危因素之一。近年黏质沙雷菌引起医院内流行性感染报道日见增多[ 13-15],结合本调查2015年耦合剂污染菌中黏质沙雷菌异常增多现象,为防止医院内污染耦合剂的媒介传播作用,选用零污染的医用耦合剂是医疗机构医院感染防控措施之一。
建议国家相关部门尽快制定医用耦合剂卫生学标准,便于使用的医疗机构有章可循,降低感染风险。使用部门对耦合剂的选用及以下操作均应使用无菌型耦合剂:以器件穿过组织(如用针抽吸、用针定位和组织活检)的有创性操作,涉及无菌环境的操作(如术中超声操作),与非完整皮肤直接接触(如组织切口),与黏膜直接接触(如阴道超声),对新生儿、重症监护病房、血液移植患者等保护性隔离患者及传染病患者进行的操作。如果条件允许,其他接触完整皮肤的操作,也应尽量使用无菌型耦合剂。对于接触耦合剂的各种探头使用后应及时清洁消毒并确保措施的实施,把重复污染风险降至最低。
本调查未对耦合剂污染菌做同源性分析,无法与临床感染病例进行分析,有待进一步完善。
[1] 国家食品药品监督管理局.医用超声耦合剂:YY0299—2008[S].北京:中国标准出版社, 2008.
[2 ] 林必杰, 林辉.我国医用超声耦合剂现状和质量标准的探讨[J].中国药学杂志, 1996, 31(11):690.
[3] 谈智, 孙巍, 陈越英, 等.医用超声耦合剂卫生质量状况调查[J].中国消毒学杂志, 2014, 31(6):574-576, 579.
[4] Cheng A, Sheng WH, Huang YC, et al. Prolonged postprocedural outbreak ofMycobacteriummassilienseinfections associated with ultrasound transmission gel[J]. Clin Microbiol Infect, 2016, 22(4): 382.e1-382.e11.
[5] Muradali D, Gold WL, Phillips A,et al.Can ultrasound probes and coupling gel be a source of nosocomial infection in patients undergoing sonography? An in vivo and in vitro study[J]. AJR Am J Roentgenol, 1995, 164(6): 1521-1524.
[6] 中华人民共和国卫生部.医疗机构消毒技术规范:WS/T367—2012 [S].北京, 2012.
[7] 中华人民共和国国家质量监督检疫总局.一次性使用卫生用品卫生标准:GB15979-2002[S].北京, 2002.
[8] 沈芃, 费春楠, 刘军, 等.医院超声探头及耦合剂带菌状况调查[J].中国消毒学杂志, 2012, 29(4):290-291.
[9] Provenzano DA, Liebert MA. Steen B, et al. Investigation of current infection-control practices for ultrasound coupling gel: a survey, microbiological analysis, and examination of practice patterns[J]. Reg Anesth Pain Med, 2013, 38(5): 415-424.
[10] Chittick P, Russo V, Sims M, et al. An outbreak ofPseudomonasaeruginosarespiratory tract infections associated with intrinsically contaminated ultrasound transmission gel [J]. Infect Control Hosp Epidemiol, 2013, 34(8): 850-853.
[11] Jacobson M, Wray R, Kovach D, et al.Sustained endemicity ofBurkholderiacepaciacomplex in a pediatric institution, associated with contaminated ultrasound gel[J].Infect Control Hosp Epidemiol, 2006, 27(4): 362-366.
[12] Hutchinson J, Runge W, Mulvey M, et al.Burkholderiacepaciainfections associated with intrinsically contaminated ultrasound gel: the role of microbial degradation of parabens[J].Infect Control Hosp Epidemiol, 2004, 25(4): 291-296.
[13] 吴建荣, 鲍千红, 徐公民.某医院粘质沙雷菌感染的临床分布及耐药性分析[J].中国消毒学杂志, 2016, 33(4):341-342, 345.
[14] 乐菊芳, 严珊玲.一起粘质沙雷菌院内感染11例报告[J].临床儿科杂志, 1995, 13(4):224-225.
[15] 陈炜, 甄国东, 赵琼, 等.引发重症监护室内血流感染的粘质沙雷菌同源性分析[J].中华微生物学和免疫学杂志, 2015, 35(3):183-187.
(本文编辑:陈玉华)
Surveyonhygienicstatusoflargebottlesofmedicalultrasoniccouplinggel
SITUMin-xiong,GUOQiao-zhi,ZHOUYi,ZHAODan-yang,LUORui,WANGJie-lin
(GuangzhouWomenandChildren’sMedicalCenter,Guangzhou510623,China)
ObjectiveTo investigate the hygienic status of large bottles of medical ultrasonic coupling gel in medical institution.MethodsFrom February 2012 to April 2016, microbial contamination of large bottles of medical ultrasonic coupling gel in a women and children’s hospital was investigated and analyzed through on-the-spot random sampling and detection method.ResultsA total of 170 large bottles of medical ultrasonic coupling gel specimens were collected, 25 specimens were qualified, the qualified rate was 14.71%. Specimens were mainly from inpatient wards(58.24%) and operating departments(21.76%); there was no statistical difference in the qualified rate of specimens in each department(P>0.05). Contamination rates of coupling gel before and after the opening were both>80%, difference was not significant(P>0.05). A total of 145 strains of pathogenic bacteria were isolated, 18 of which were from unopened bottles, and 127 from opened bottles.Burkholderiacepaciawas the main strain in both unopened and opened bottles, which accounting for 83.33% and 54.33% respectively,in addition,PseudomonasaeruginosaandSerratiamarcescenswere also isolated from opened bottles, both were 15.75%, mixed contamination bacteria all includedSerratiamarcescens.ConclusionThe total bacteria counts in medical ultrasonic coupling gel in large bottles exceed the standard seriously, the manufacturer should strictly observe the quality control standards, medical institutions should adopt effective cleaning and disinfection measures.
medical ultrasonic coupling gel; hygienic status; microbe
2016-07-10
2014年度广东现代医院管理研究所科研立项课题(WSTJJ20131021);广州市科技计划项目(2014Y2-00031)
司徒敏雄(1965-),女(汉族),广东省广州市人,副主任护师,主要从事医院感染管理研究。
司徒敏雄 E-mail:mx_6588@163.com
10.3969/j.issn.1671-9638.2017.09.014
R187
A
1671-9638(2017)09-0849-03
