中药渣基活性炭的制备及其对头孢拉定的吸附研究
2017-09-03孙显涛陈建秋明广奇商景阁
于 颖, 孙显涛, 陈建秋, 明广奇, 商景阁
(中国药科大学 工学院, 江苏 南京 211198)
·研究报告——生物质材料·
中药渣基活性炭的制备及其对头孢拉定的吸附研究
于 颖, 孙显涛, 陈建秋, 明广奇, 商景阁*
(中国药科大学 工学院, 江苏 南京 211198)

中药渣;碳酸钠;活性炭;头孢拉定;吸附

我国作为抗生素生产和使用大国,据统计,2013年全国抗生素使用量约16.2万吨[1],环境中抗生素的来源主要有生产抗生素的药企、医疗、畜禽及水产养殖业[2]。抗生素在人体和动物体内分解很少,30 %~90 %以原形式排放到环境中[3],这些抗生素的存在会影响环境中正常的菌群分布,增强细菌的耐药性并最终影响人类的健康[4]。抗生素广泛存在于水环境中,大环内酯类药物在珠江流域的检出度较高,清河流域检出度较高的为四环素类和大环内酯类抗生素,而水体中的抗生素被人体摄入后,会对人的免疫系统造成干扰[5],所以采取有效措施降低水体中抗生素的水平至关重要。常用的抗生素废水的处理方法主要有物理法、电化学氧化法、光催化氧化法和生物化学处理法[6]。其中物理法中的活性炭吸附法因具有处理效率高且活性炭可再生的优点而被大量使用。活性炭是一种含有大量孔隙结构的碳材料,其比表面积巨大,具有很强的吸附能力。活性炭的制备方法主要分为物理活化法和化学活化法[7]。物理活化法是将生物质炭化后,再通入水蒸气[8]或二氧化碳[9]进行活化得到活性炭,该方法操作简单但活化程度不易控制。而化学活化法是将生物质与活化剂按一定比例浸渍后,烘干置于氮气保护的马弗炉中,在设定的温度下进行活化,再对活化产物进行清洗得到活性炭。常用的活化剂主要有磷酸[10]、氯化锌[11]、氢氧化钠[12]和氢氧化钾[13]等。Uçar等[14]采用Na2CO3为活化剂,制备的油菜籽基活性炭的比表面积达到850 m2/g。随着中药产业的快速发展,每年中药渣的产生量在不断增长,仅江苏省中药渣年排放量就已经达到100万吨[15]。而中药渣本质上属于生物质范畴,可以作为活性炭的制备原料。将中药渣制备成活性炭有助于缓解中药渣对环境的污染,还可以将制备的活性炭用于处理抗生素废水,对环境保护有重要意义。本研究选取香橼(CitrusmedicaL.,CM)、桂枝(RamulusCinnamomi,RC)和板蓝根(Isatictinctoria,IT) 3种中药渣,以Na2CO3为活化剂制备活性炭,并用制得的活性炭吸附溶液中的抗生素头孢拉定,考察其吸附动力学、吸附等温线及溶液初始pH值、共存离子浓度等因素对活性炭吸附的影响,比较3种活性炭与商用粉末活性炭(AC-CP)和商用颗粒活性炭(AC-CG)的吸附能力;同时结合扫描电子显微镜(SEM)、红外光谱(FT-IR)和BET比表面积分析等表征方法,研究活性炭特性及其对头孢拉定的吸附能力和吸附机理,以期为活性炭处理抗生素废水提供理论依据。
1 实 验
1.1 原料与仪器
选取中药香橼、桂枝和板蓝根的提取废渣,烘干后,用粉碎机粉碎至0.180 mm;Na2CO3、NaCl、HCl、NaOH均为分析纯;头孢拉定为原料药(99 %);商用活性炭,购自上海沪试实验室器材股份有限公司。
实验仪器有S8400扫描电子显微镜(日立公司),8400S傅里叶变换红外光谱仪(岛津公司),Autosorb比表面积分析仪(康塔有限公司),PB-10型玻璃膜电极pH计(赛多利斯科学仪器(北京)有限公司),HPLC-1260高效液相色谱仪(美国安捷伦公司)。
1.2 活性炭的制备
取质量分数为10 %的Na2CO3溶液800 g与200 g的上述中药渣粉末混合浸渍24 h并充分搅拌后烘干。取适量置于马弗炉中,在800 ℃条件下活化1.5 h(N2气氛)。活化产物经水洗至pH值稳定,再用0.1 mol/L盐酸浸泡24 h,之后用水洗至pH值稳定。清洗后烘干粉碎得香橼活性炭(AC-CM)、桂枝活性炭(AC-RC)和板蓝根活性炭(AC-IT)。
1.3 样品表征
用扫描电子显微镜(SEM)观察活性炭的表面形貌;用傅里叶变换红外光谱仪(FT-IR)测定3种中药渣及活性炭的红外谱图,测定范围400~4000 cm-1;比表面积采用比表面积分析仪结合BET法测定;活性炭的pH值的测定采用文献[16]的方法:以固液比1∶20(g∶mL,下同)将1 g活性炭与20 mL纯净水混合,充分搅拌1.5 h后静置1 h,用玻璃膜电极pH计测定pH值。活性炭零电荷点(pHpzc)的测定采用pH位移法[17]。
1.4 头孢拉定液相色谱检测
使用高效液相色谱仪检测头孢拉定质量浓度,色谱柱为Symmetry C18柱(4.6 mm×150 mm,5 μm),流动相为乙腈-醋酸盐缓冲液(醋酸盐缓冲液配制方法为称取醋酸钠0.7 g和冰醋酸0.15 g加水稀释到1 000 mL)体积比12∶88,流速为1.0 mL/mim,采用可变波长(19~600 nm)紫外检测器,检测波长为254 nm,室温。
1.5 吸附实验
1.5.1 吸附动力学 取质量浓度为100 mg/L的头孢拉定溶液(配制方法为:精密称取0.1 g头孢拉定,溶于1 000 mL水中)200 mL于250 mL锥形瓶中,向锥形瓶中加入0.2 g的活性炭。然后将锥形瓶置于摇床中,30 ℃下振摇,振摇频率为200 r/min,每隔一定的时间取样,48 h后停止取样,样品经0.45 μm滤膜过滤后用高效液相色谱测定其质量浓度。
1.5.2 吸附等温线 各取质量浓度为20、50、80、100和200 mg/L的头孢拉定溶液100 mL于250 mL锥形瓶中,分别加入0.1 g的活性炭,30 ℃条件下振摇,振摇频率为200 r/min,48 h后取样,经0.45 μm滤膜过滤后用高效液相色谱测定其质量浓度。
1.5.3 溶液pH值的影响 不同溶液pH值下,头孢拉定的存在形式及活性炭的表面电荷分布不同,会导致活性炭的吸附能力不同。取质量浓度为100 mg/L的头孢拉定溶液100 mL于250 mL锥形瓶中,分别用盐酸或NaOH溶液调节各锥形瓶中溶液pH值为3、5、7、9、10和11。分别向锥形瓶中加0.1 g活性炭,30 ℃下振摇,振摇频率为200 r/min,48 h后取样,样品经0.45 μm滤膜过滤后采用高效液相色谱测定其质量浓度。
1.5.4 NaCl浓度的影响 活性炭在实际应用中,吸附的抗生素废水中会存在共存离子,可能会对活性炭的吸附能力产生影响。取质量浓度为100 mg/L的头孢拉定溶液100 mL,置于250 mL锥形瓶中,向头孢拉定溶液中加入NaCl使其质量浓度分别为0、10、50、80、100 mg/L,向各锥形瓶中分别加入0.1 g活性炭,30 ℃、200 r/min振摇48 h,取样,经0.45 μm滤膜过滤后利用高效液相色谱测定样品中头孢拉定质量浓度。
2 结果与讨论
2.1 样品表征
2.1.1 原料工业分析 表1为原料香橼中药渣(CM)、桂枝中药渣(RC)和板蓝根中药渣(IT)的工业分析结果。

表1 3种原料的工业分析
从表1中可以看出,CM、RC和IT的灰分含量均较低,物质组成中含量最高的是挥发分,均大于71 %,而水分只占了约10 %, 3者的固定碳含量也较为接近。
2.1.2 活性炭结构、特征及产率 3种活性炭的孔隙结构、产率、pH值及pHpzc值结果见表2。 从表2可以看出,AC-RC与AC-CM的比表面积大小接近,且相对AC-IT要大很多,这将直接影响3种活性炭对头孢拉定的吸附能力,使得AC-RC与AC-CM对头孢拉定的吸附量高于AC-IT。活性炭的平均孔径在3~4 nm之间,属于中孔孔径。由表2还可以看出,活性炭产率在10%左右,这是由于制备过程中,马弗炉的气密性不好,使得氧气混入炉中与活性炭发生反应,导致活性炭产率偏低。3种活性炭的pH值均大于8,显碱性,说明活性炭表面含有较多的碱性基团。AC-CM、AC-RC和AC-IT的pHpzc值分别为9.28、9.21和9.38,所以当溶液pH值分别低于这3个值时,活性炭表面将带有正电荷,相反当溶液pH值分别大于这3个值时,活性炭表面将带有负电荷[18]。

表2 活性炭的结构、特征及产率
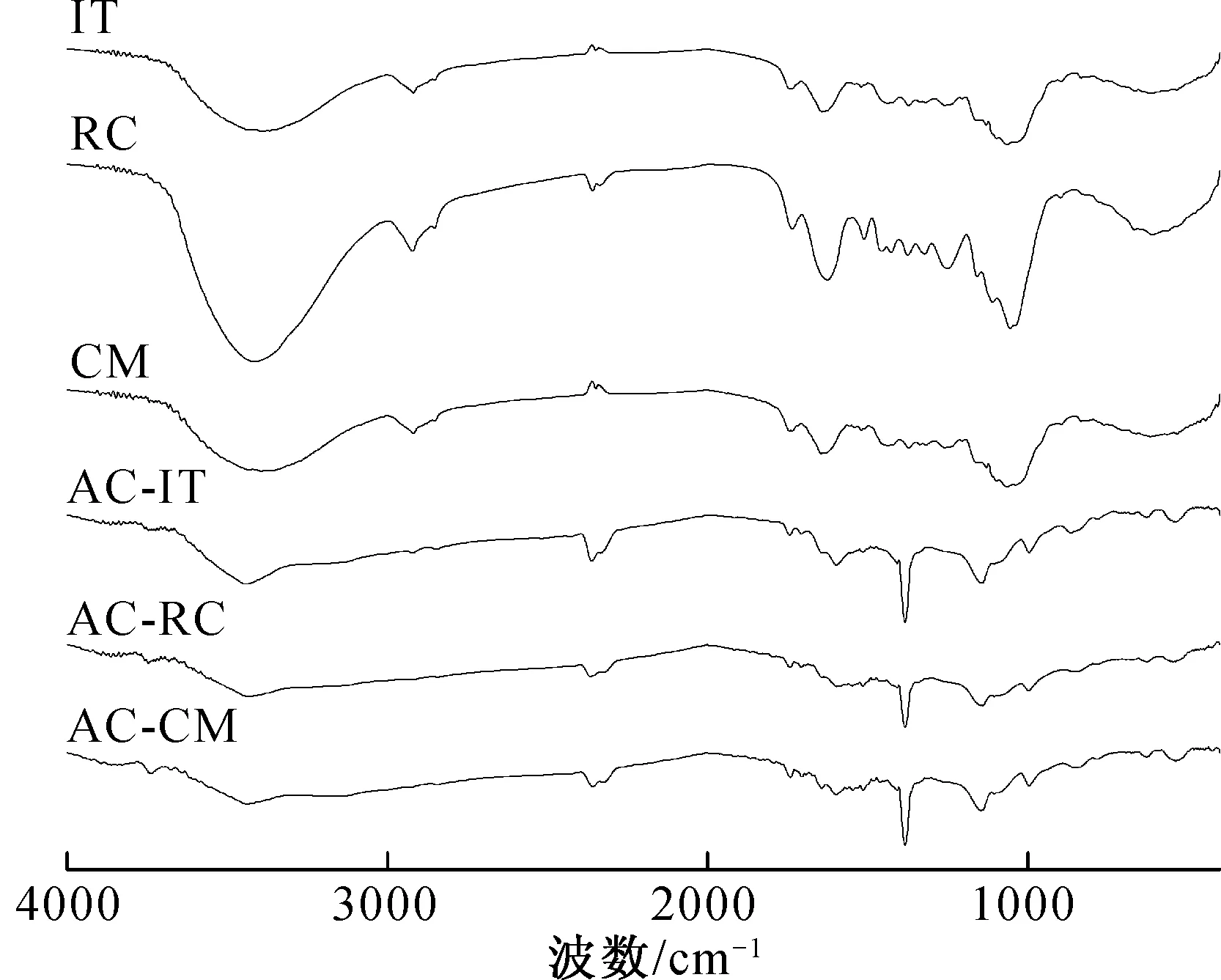
图1 样品红外谱图Fig. 1 FT-IR spectra of samples

2.1.4 活性炭的SEM表征 图2为AC-CM、AC-RC和AC-IT的扫描电镜图,从图中可以看出,AC-CM和AC-IT的孔呈蜂窝状结构,AC-RC的孔呈不规则孔状结构且3种活性炭较大的孔的内壁均存在较小的孔,大量的孔结构极大增加了活性炭的比表面积及对头孢拉定的吸附能力。

图2 活性炭的扫描电镜图Fig. 2 SEM images of activated carbons
2.2 吸附动力学
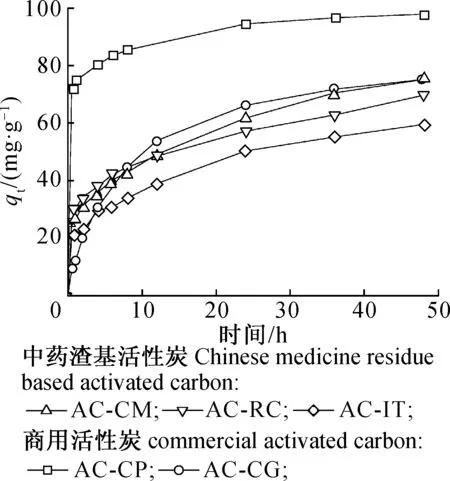
图3 时间对活性炭吸附容量的影响Fig. 3 Effect of contact time on cefradine adsorption on activated carbons
图3为3种活性炭与商用活性炭对头孢拉定的吸附动力学曲线。从图3可以看出,在0~5 h内3种活性炭对头孢拉定的吸附速率均处于较快阶段,之后吸附速率逐渐趋于缓慢,48 h左右达到吸附平衡。通过对比制备的3种活性炭与商用活性炭的吸附量变化曲线可以发现,商用粉末活性炭(AC-CP)的吸附能力最好,AC-RC与AC-IT的吸附能力较弱。AC-CM活性炭对头孢拉定的吸附量与商用颗粒活性炭(AC-CG)的吸附量相近,而与商用粉末活性炭(AC-CP)的吸附容量有一定差距。在吸附的开始阶段,AC-CM与AC-RC的吸附速率要快于商用颗粒活性炭的吸附速率。
为了研究该活性炭的吸附机理,采用伪一级(式(1))、伪二级(式(2))和粒内扩散(式(3))3种动力学模型分别对实验数据进行拟合[19]。
ln(qe-qt)=lnqe-K1t
(1)
(2)
qt=Kintt1/2+C
(3)
式中:qe—吸附平衡时的吸附量,mg/g;qt—t时刻的吸附量,mg/g;K1—伪一级吸附速率常数,h-1;K2—伪二级吸附速率常数,g/(mg·h);Kint—粒内扩散吸附速率常数,mg/(g·h0.5)。
表3为3种动力学模型分别对Na2CO3活化的3种活性炭和商用活性炭吸附头孢拉定数据的拟合结果。由表3可以看出,AC-CP和AC-CG的伪二级动力学的R2值均大于伪一级动力学和粒内扩散模型的R2值,即AC-CP和AC-CG的动力学数据符合伪二级动力学模型,说明这2种商用活性炭对头孢拉定的吸附速率受化学吸附控制[20]。AC-CM、AC-RC和AC-IT吸附数据的粒内扩散模型R2值分别为0.996 6、0.989 9和0.995 5,均大于伪一级动力学、伪二级动力学的R2值,即3种活性炭对头孢拉定的吸附速率受到颗粒内扩散机制控制。同时,3种活性炭的粒内扩散模型中参数C均不为0,即拟合曲线均不过原点,说明粒内扩散不是这3种活性炭对头孢拉定的吸附速率的唯一控制步骤[21]。为进一步研究性炭的吸附机理,分别比较了3种活性炭的伪一级动力学和伪二级动力学。从表3中可以看出,3种活性炭的伪二级动力学的R2值均大于伪一级动力学R2值,说明这3种活性炭对头孢拉定的吸附速率除受粒内扩散机制控制外还受到化学吸附的控制,包括活性炭和头孢拉定分子之间形成共价键且存在电子交换[20]。

表3 活性炭的动力学模型拟合参数
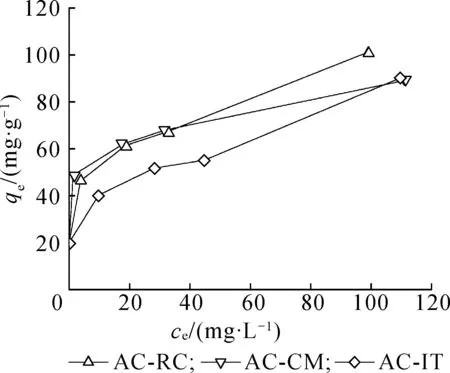
图4 活性炭对头孢拉定的吸附等温线Fig. 4 Effect of temperature on cefradine adsorption isotherm on activated carbons
2.3 吸附等温线
3种活性炭对头孢拉定的吸附等温线如图4所示。由图4可以看出,随着平衡质量浓度的增加,活性炭平衡吸附量也随之增大,但增速逐渐趋缓。
为了研究活性炭对头孢拉定的吸附特性及头孢拉定在活性炭表面的分布规律,采用Langmuir[22]和Freundlich[23]等温线模型对3种活性炭的等温吸附数据进行拟合,公式分别为式(4)和(5):
(4)
(5)
式中:ce—吸附平衡后的质量浓度,mg/L;qe—平衡吸附量,mg/g;qm—Langmuir单分子层饱和吸附量,mg/g;KL—Langmuir吸附常数,L/mg;KF—Freundlish吸附常数,(mg/g)·(L/mg)1/n;n—与吸附强度相关的常数。
拟合结果如表4所示,结果显示,相比Langmuir模型,AC-RC、AC-CM和AC-IT对头孢拉定的等温吸附过程更符合Freundlich模型(R2=0.979 5、0.993 3和0.991 3)。Freundlich模型假设吸附过程发生在非均匀的吸附剂表面,且不同吸附位点的吸附能不同[17]。3种活性炭的n值均大于1,说明吸附过程容易进行。

表4 活性炭的等温线模型拟合参数
2.4 吸附条件对吸附的影响
2.4.1 溶液的初始pH值 溶液初始pH值对3种活性炭吸附头孢拉定的影响如图5所示。从图5中可以看出,pH值为3时,AC-CM、AC-RC和AC-IT对头孢拉定都有很强的吸附能力,吸附量分别达到74.76、79.44和62.55 mg/g。随着pH值的增大,吸附量大幅下降,但是在pH值9时,吸附量又有小幅提升,pH值继续增大时,吸附量再次减小。从整体来看,溶液初始pH值对3种活性炭吸附头孢拉定均有较大的影响。红外分析结果和pH值测定结果表明,3种活性炭表面均含有大量偏碱性的含氮基团,且pHpzc值大于9,所以在强酸性条件下,活性炭表面吸附大量H+而带有正电荷,头孢拉定在酸性和近中性(pH值3~6)条件下稳定存在[24],头孢拉定分子内部含有较多的N、O等电负性较强的杂原子,导致强酸性条件下头孢拉定与活性炭之间存在较强的引力作用,活性炭的吸附能力得到增强。而在弱酸性以及中性条件下,活性炭表面正电荷减少,引力作用减弱,活性炭的吸附量降低。当pH值等于9时,活性炭表面正电荷继续减少,但头孢拉定的β-内酰胺环在碱性条件下开环[24],变成阴离子形式,活性炭与头孢拉定之间的引力作用增强,活性炭的吸附量反而有一定的增大。当pH值增大到10以上时,活性炭表面带负电,活性炭与头孢拉定之间存在排斥的作用力,导致活性炭的吸附量再次减小。
2.4.2 NaCl质量浓度 离子强度也是影响吸附剂和吸附质之间静电和非静电作用力的因素之一[25]。NaCl质量浓度对3种活性炭吸附头孢拉定的影响如图6所示。从图6可以看出,NaCl的存在使3种活性炭对头孢拉定的吸附量增加,随NaCl质量浓度的增大,吸附量呈现先增大后减小的趋势。溶液与活性炭颗粒之间由于静电作用会形成双电层,NaCl的存在压缩了活性炭表面双电层的厚度[26],使头孢拉定分子更容易接近活性炭的表面,从而增大了活性炭对头孢拉定的吸附量。而随着NaCl质量浓度的增大,Na+占据活性炭表面部分吸附位点,与头孢拉定产生竞争吸附作用,使得活性炭对头孢拉定的吸附量下降[27]。

图5 溶液初始pH值对活性炭吸附容量的影响Fig. 5 Effect of initial pH value on cefradine adsorption on activated carbons

图6 氯化钠质量浓度对活性炭吸附容量的影响Fig. 6 Effect of NaCl mass concentration on cefradine adsorption on activated carbons
3 结 论
3.2 对3种活性炭吸附头孢拉定的吸附动力学和吸附等温线进行分析,发现3种活性炭对头孢拉定的吸附均符合伪二级动力学和粒内扩散模型,吸附速率受化学吸附和粒内扩散机制控制。Freundlich模型能够很好地描述3种活性炭对头孢拉定的等温吸附过程,n均大于1,说明吸附过程容易进行。
3.3 分析溶液初始pH值和NaCl质量浓度对吸附量的影响,发现溶液初始pH值对3种活性炭的吸附量的影响较大,在pH值为3(在100 mg/L头孢拉定溶液中,添加0.1 g活性炭,吸附48 h)时,AC-CM、AC-RC和AC-IT的吸附量最大,分别为74.76、79.44和62.55 mg/g。NaCl的存在也增加了活性炭的吸附量。
[1]ZHANG Q Q,YING G G,PAN C G,et al. Comprehensive evaluation of antibiotics emission and fate in the river basins of China: Source analysis,multimedia modeling,and linkage to bacterial resistance[J]. Environmental Science & Technology,2015,49(11):6772-6782.
[2]高立红,史亚利,厉文辉,等. 抗生素环境行为及其环境效应研究进展[J]. 环境化学,2013,32(9):1619-1633.
[3]DU L F,LIU W K. Occurrence, fate, and ecotoxicity of antibiotics in agro-ecosystems. A review[J]. Agronomy for Sustainable Development,2012,32(2):309-327.
[4]MARTI R,SCOTT A,TIEN Y C,et al. Impact of manure fertilization on the abundance of antibiotic-resistant bacteria and frequency of detection of antibiotic resistance genes in soil and on vegetables at harvest[J]. Applied and Environmental Microbiology,2013,79(18):5701-5709.
[5]李经纬,刘小燕,王美欢,等. 抗生素在水环境中的分布及其毒性效应研究进展[J]. 广州化工,2016(17):10-13.
[6]晁显玉,曹红翠,古小超. 抗生素类废水处理方法的研究概述[J]. 山西化工,2015,35(3):78-82.
[7]JIANG B C,ZHANG Y C,ZHOU J X,et al. Effects of chemical modification of petroleum cokes on the properties of the resulting activated carbon[J]. Fuel,2008,87(10/11):1844-1848.
[8]龚建平,陈超,戴伟娣,等. 山楂核制备活性炭工艺的优化[J]. 生物质化学工程,2013,47(2):19-22.
[9]彭宏,肖鸿,尹华强. 二氧化碳活化对蜂窝活性炭制备及其性能的影响[J]. 资源开发与市场,2008,24(8):673-676,703.
[10]孙康,蒋剑春,卢辛成,等. 磷酸法水稻秆活性炭的制备[J]. 生物质化学工程,2011,45(6):19-23.
[11]BOUGUETTOUCHA A,REFFAS A,CHEBLI D,et al. Novel activated carbon prepared from an agricultural waste,Stipatenacissima, based on ZnCl2activationcharacterization and application to theremoval of methylene blue[J]. Desalination and Water Treatment,2016,57(50):24056-24069.
[12]BYAMBA-OCHIR N,SHIM W G,BALATHANIGAIMANI M S,et al. Highly porous activated carbons prepared from carbon rich Mongolian anthracite by direct NaOH activation[J]. Applied Surface Science,2016,379:331-337.
[13]CHENG S,ZHANG L B,XIA H Y,et al. Crofton weed derived activated carbon by microwave-induced KOH activation and application to wastewater treatment[J]. Journal of Porous Materials,2016,23(6):1597-1607.
[14]UÇAR S,ERDEM M,TAY T,et al. Removal of lead (II) and nickel (II) ions from aqueous solution using activated carbon prepared from rapeseed oil cake by Na2CO3activation[J]. Clean Technologies and Environmental Policy,2015,17(3):747-756.
[15]杨绪勤,袁博,蒋继宏. 中药渣资源综合再利用研究进展[J]. 江苏师范大学学报:自然科学版,2015,33(3):40-44.
[16]吴诗雪,王欣,陈灿,等. 凤眼莲、稻草和污泥制备生物炭的特性表征与环境影响解析[J]. 环境科学学报,2015,35(12):4021-4032.
[17]YANG Y N,CHUN Y,SHENG G Y,et al. pH-dependence of pesticide adsorption by wheat-residue-derived black carbon[J]. Langmuir,2004,20(16):6736-6741.
[18]BARKA N,OUZAOUIT K,ABDENNOURI M,et al. Dried prickly pear cactus (Opuntiaficusindica) cladodes as a low-cost and eco-friendly biosorbent for dyes removal from aqueous solutions[J]. Journal of the Taiwan Institute of Chemical Engineers,2013,44(1):52-60.
[19]FENG J,SHI S L,PEI L Y,et al. Preparation of activated carbon fromPolygonumorientaleLinn. to remove the phenol in aqueous solutions[J]. Plos One,2016,11(10):1-17.
[20]UNER O,GECGEL U,BAYRAK Y. Adsorption of methylene blue by an efficient activated carbon prepared fromCitrulluslanatusrind: Kinetic, isotherm, thermodynamic, and mechanism analysis[J]. Water Air and Soil Pollution,2016,227(7):1-15.
[21]岳钦艳,解建坤,高宝玉,等. 污泥活性炭对染料的吸附动力学研究[J]. 环境科学学报,2007,27(09):1431-1438.
[22]GHAEDI M,NASAB A G,KHODADOUST S,et al. Application of activated carbon as adsorbents for efficient removal of methylene blue: Kinetics and equilibrium study[J]. Journal of Industrial and Engineering Chemistry,2014,20(4):2317-2324.
[23]SAYGILI H,GUZEL F. Effective removal of tetracycline from aqueous solution using activated carbon prepared from tomato (LycopersiconesculentumMill.) industrial processing waste[J]. Ecotoxicology and Environmental Safety,2016,131: 22-29.
[24]霍佳丽. 电喷雾质谱在抗生素类药物中的分析研究[D]. 重庆:重庆大学硕士学位论文,2012.
[25]XUE Y J,HOU H B,ZHU S J. Adsorption removal of reactive dyes from aqueous solution by modified basic oxygen furnace slag: Isotherm and kinetic study[J]. Chemical Engineering Journal,2009,147(2/3):272-279.
[26]于富玲. 颗粒活性炭吸附染料的影响因素和分形特征的研究[D]. 北京:北京林业大学硕士学位论文,2005.
[27]张端怡. 石油焦基活性炭的制备及其对水体中四环素的吸附研究[D]. 天津:河北工业大学硕士学位论文,2015.
Adsorption of Cefradine on Activated Carbon Prepared from Chinese Medicine Residue
YU Ying, SUN Xiantao, CHEN Jianqiu, MING Guangqi, SHANG Jingge
(College of Engineering,China Pharmaceutical University, Nanjing 211198, China)
Chinese medicine residue;sodium carbonate;activated carbon;cefradine;adsorption
10.3969/j.issn.1673-5854.2017.04.004
2017- 01- 03
江苏省自然科学基金资助项目(BK20150693)
于 颖(1968— ),女,江苏南京人,副教授,博士,主要从事制药过程工艺及装备技术方面的研究;E-mail:yyinga@vip.sina.com
*通讯作者:商景阁,男,讲师,博士,研究领域为制药三废处理;E-mail:shangjingge@163.com。
TQ35;TQ424
A
1673-5854(2017)04-0025-08
