不同剂量赛妥珠单抗治疗类风湿性关节炎有效性和安全性的系统评价
2017-09-03王洪梅赖翔宇
王洪梅 赖翔宇 白 浩
(重庆市肿瘤研究所/医院/癌症中心,沙坪坝400030)
不同剂量赛妥珠单抗治疗类风湿性关节炎有效性和安全性的系统评价
王洪梅 赖翔宇 白 浩
(重庆市肿瘤研究所/医院/癌症中心,沙坪坝400030)
目的:探究不同剂量赛妥珠单抗治疗类风湿性关节炎的有效性及安全性。方法:计算机检索Pubmed、Medline、Embase、The Cochrane Library、万方数据库(WANFANG)、中国期刊全文数据库(CNKI)、中国生物医学文献数据库中关于不同剂量赛妥珠单抗治疗类风湿性关节炎的随机对照研究(Randomized controlled trials,RCTs),检索时限均为建库至2015年3月。采用RevMan5.3软件进行统计分析。结果:共纳入6篇文献、4项研究,纳入文献质量均较高,本meta分析结果显示不同剂量CZP在改善类风湿患者病情的疗效(ACR20、ACR50、ACR70),关节疾病活动性评分,患者对疾病活动性评价指标(HAQ- DI、关节疼痛、疲劳),轻度、中度、重度不良反应方面差异无统计学意义。结论:不同剂量CZP治疗RA具有相同的治疗效果,短期安全性相似,不同剂量CZP长期疗效及安全性有待于进一步研究证实。
类风湿,关节炎;赛妥珠;剂量;meta分析
类风湿性关节炎(Rheumatoid arthritis,RA)作为最常见的以慢性滑膜炎为临床表现的自身免疫疾病,其致残率较高,可严重影响患者的生活质量[1]。传统改善病情的抗风湿药虽然对RA患者有一定的疗效,但都伴随着严重的不良反应[2]。TNF- α为RA病情进展过程中重要的免疫调节因子,在软骨基质降解、炎症反应及滑膜细胞增殖中起重要的作用[3]。TNF- α抑制剂如英夫利昔单抗(Infliximab)、依那西普(Etanercept)、阿达木单抗(Adalimumab)等治疗RA的有效性和安全性已有大量研究证实[4]。赛妥珠单抗(Certolizumab pegol,CZP)作为一种新型的TNF- α抑制剂已被广泛应用于消化系统疾病中如克罗恩病。不同于其他TNF- α抑制剂,CZP由人源单价体Fab抗体与聚乙二醇共价结合而形成,与聚乙二醇的结合使其拥有较长半衰期。其不含Fc片段,不能锚定补体及诱导淋巴细胞及单核细胞的程序性死亡,也不能引起抗体依赖细胞介导的细胞毒作用[5]。目前已有许多研究对不同剂量的CZP联合甲氨蝶呤(MTX)治疗RA的有效性和安全性做了评估,本研究拟用循证医学的方法和思路综合目前已发表的研究成果,对不同剂量的CZP的有效性和安全性作合理的评估,旨在为活动性RA的临床治疗提供依据。
1 资料与方法
1.1 检索策略 计算机检索Pubmed、The Cochrane Library、Embase、Medline、万方数据库(WANFANG)、中国生物医学文献数据库、中国期刊全文数据库(CNKI)中关于CZP治疗RA的随机对照研究(RCT),检索时限均为建库至2015年3月,检索中文检索词为“类风湿”、“赛妥珠”,英文检索词为“rheumatoid arthritis OR RA”,“Certolizumab pegol OR CZP”,检索语言限定为中文和英文。
1.2 纳入标准和排除标准 (1)研究类型:随机对照研究(RCT);(2)纳入对象:确诊为RA的患者、18岁以上;(3)干预措施:不同剂量CZP联合或不联合MTX治疗RA;(4)评价治疗:美国风湿病学会(ACR)制定的RA缓解标准,ACR20(疗效缓解20%),ACR50,ACR70,以红细胞沉降率(ESR)为基础的28 个关节疾病活动性指数(DAS- 28),关节疼痛,健康评估问卷功能障碍指数(HAQ- DI),疲劳评定,不良反应等。不满足以上标准的研究予以排除。
1.3 文献筛选及质量评价 由两名评价员独立按照检索策略、纳入和排除标准进行文献的筛选,对于存在争议的文献则由两名评价员讨论解决。文献中缺失的信息资料通过联系第一作者加以完善。采用Jadad评分量表对纳入所有RCT进行质量评估。标准包括:随机序列的产生、盲法的实施、随机化隐藏、撤出及退出的理由等4个方面。满分7分,大于3分则为高质量文献。
1.4 数据提取及统计分析 两名评价员对符合纳入标准的文献独立进行资料提取,意见不同通过讨论解决,提取资料包括纳入对象的基线资料、文献一般信息资料、结局指标等。采用Cochrane协作网提供的RevMan5.3软件进行统计分析,计数资料采用相对危险度(RR)及其95%置信区间(CI)进行评估,计量资料则采用加权均数差(MD)及其95%置信区间(CI)进行评估。研究间的异质性采用χ2检验(以P=0.1为异质性阈值)和I2检验(以I2=50%为异质性阈值),若各研究不存在异质性,则采用固定效应模型,反之则采用随机效应模型,并对其异质性来源进行分析。
2 结果
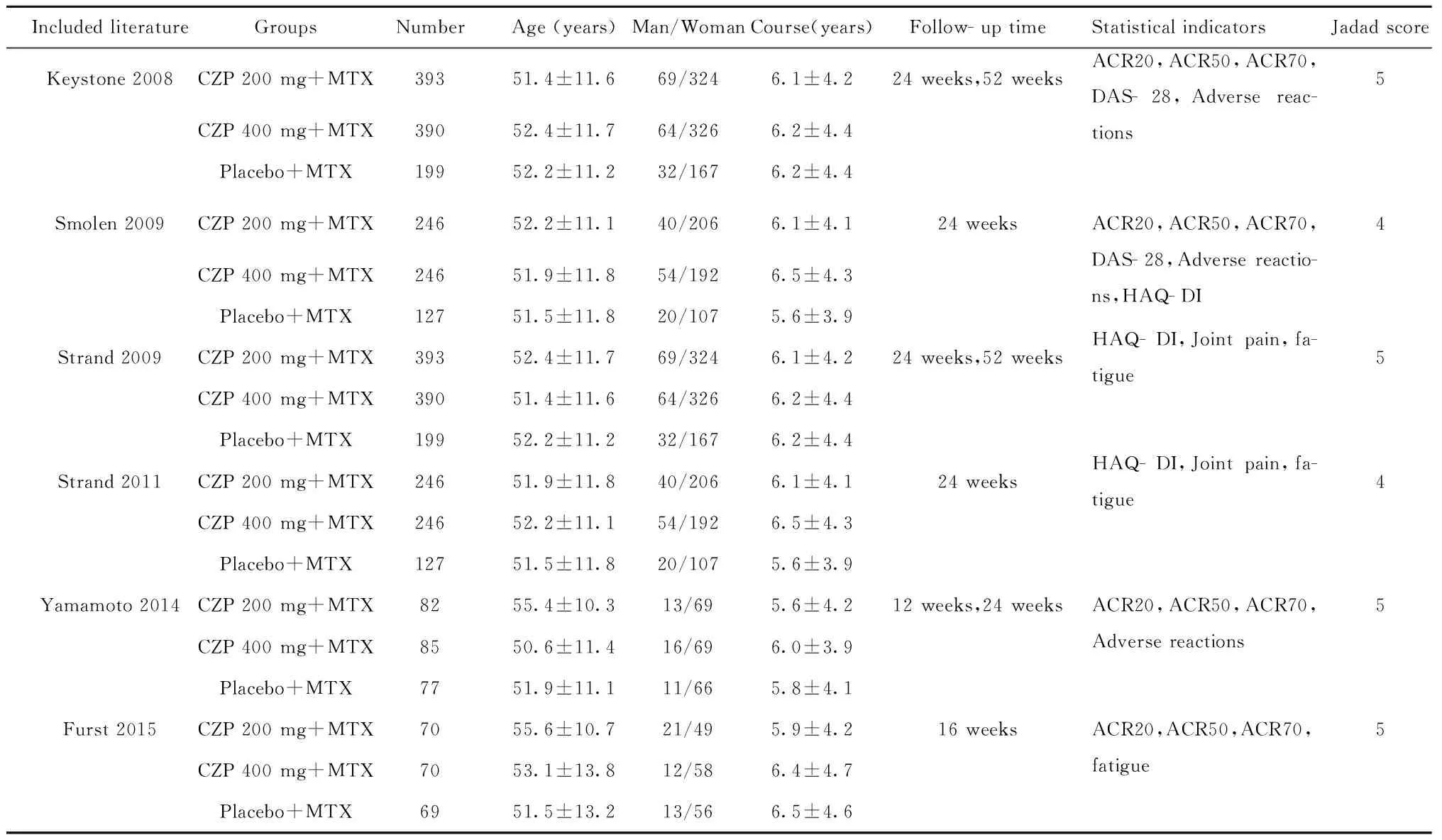
2.1 检索结果 初步检索出260篇相关英文文献,未检索出相关中文文献,全面筛查后最终纳入6篇文献[6- 11],4项研究,其中Strand等[9]和Smolen等[8]为同一研究,Strand等[7]和Keystone等[6]为同一研究,因以上文献的结局指标不同,故4篇文献均可纳入。共纳入1 851例RA患者,主要结局指标包括ACR20、ACR50、ACR70、不良反应等,随访时间包括12、16、24、52周。纳入所有研究均采用不同剂量CZP联合MTX治疗RA患者,纳入文献均属高质量文献,纳入文献基本特征详见表1。
表1 纳入文献基本特征
Tab.1 Basic characteristics of included literature
IncludedliteratureGroupsNumberAge(years)Man/WomanCourse(years)Follow-uptimeStatisticalindicatorsJadadscoreKeystone2008CZP200mg+MTX39351.4±11.669/3246.1±4.224weeks,52weeksACR20,ACR50,ACR70,DAS-28,Adversereac-tions5CZP400mg+MTX39052.4±11.764/3266.2±4.4Placebo+MTX19952.2±11.232/1676.2±4.4Smolen2009CZP200mg+MTX24652.2±11.140/2066.1±4.124weeksACR20,ACR50,ACR70,DAS-28,Adversereactio-ns,HAQ-DI4CZP400mg+MTX24651.9±11.854/1926.5±4.3Placebo+MTX12751.5±11.820/1075.6±3.9Strand2009CZP200mg+MTX39352.4±11.769/3246.1±4.224weeks,52weeksHAQ-DI,Jointpain,fa-tigue5CZP400mg+MTX39051.4±11.664/3266.2±4.4Placebo+MTX19952.2±11.232/1676.2±4.4Strand2011CZP200mg+MTX24651.9±11.840/2066.1±4.124weeksHAQ-DI,Jointpain,fa-tigue4CZP400mg+MTX24652.2±11.154/1926.5±4.3Placebo+MTX12751.5±11.820/1075.6±3.9Yamamoto2014CZP200mg+MTX8255.4±10.313/695.6±4.212weeks,24weeksACR20,ACR50,ACR70,Adversereactions5CZP400mg+MTX8550.6±11.416/696.0±3.9Placebo+MTX7751.9±11.111/665.8±4.1Furst2015CZP200mg+MTX7055.6±10.721/495.9±4.216weeksACR20,ACR50,ACR70,fatigue5CZP400mg+MTX7053.1±13.812/586.4±4.7Placebo+MTX6951.5±13.213/566.5±4.6
2.2 系统评价结果
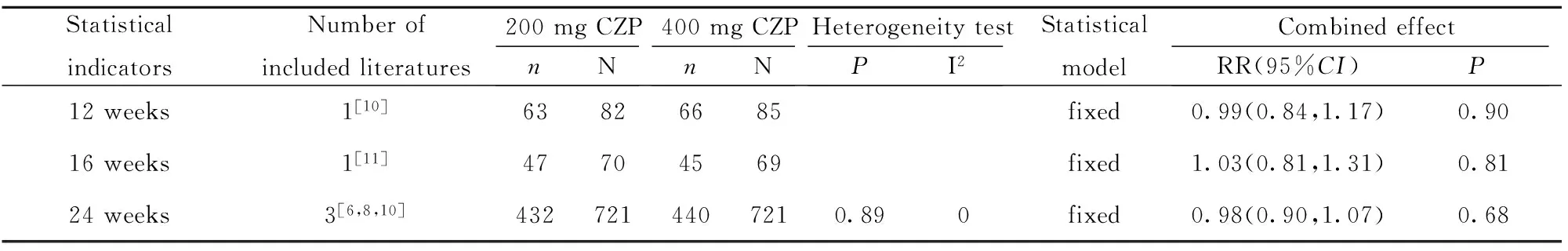
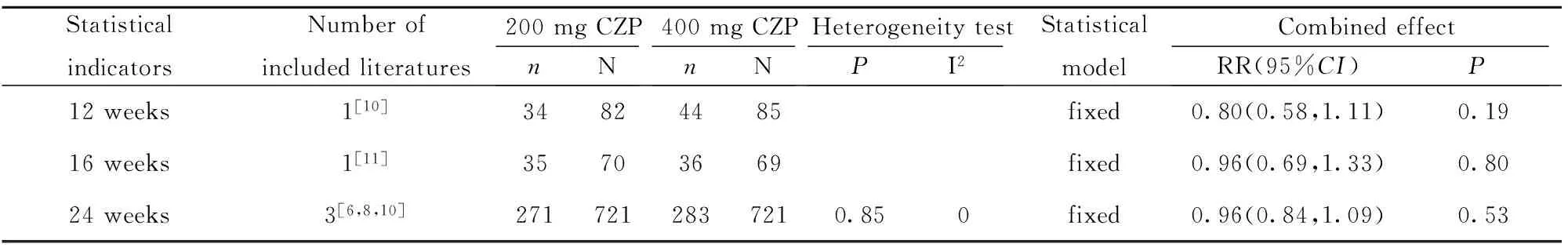
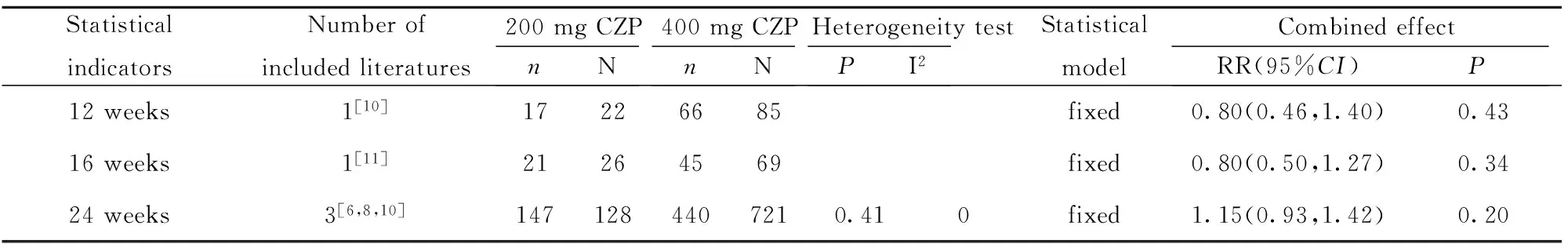
2.2.1 不同剂量CZP治疗效果评估 200 mg CZP与400 mg CZP相比,12、16、24周在ACR20方面差异无统计学意义(P>0.05),12、16、24周在ACR50方面差异无统计学意义(P>0.05),12、16、24周在ACR50方面差异无统计学意义(P>0.05),详见表2~4。2.2.2 DAS- 28(ESR)与基线资料变化评估 200 mg CZP与400 mg CZP相比,16、24、52周在DAS- 28(ESR)与基线资料变化值方面差异无统计学意义(P>0.05),详见表5。
2.2.3 RA患者对疾病活动性评价指标 200 mg CZP与400 mg CZP相比,24周在RA患者HAQ- DI改善达到最小临床意义变化值(MCIDs)的患者数量方面差异无统计学意义(P>0.05),16、24、52周在RA患者关节疼痛改善达到MCIDs的患者数量方面差异均无统计学意义(P>0.05),16、24、52周在RA患者疲劳改善达到MCIDs的患者数量方面差异均无统计学意义(P>0.05),详见图1、表6、7。
2.2.4 安全性评价 200 mg CZP与400 mg CZP相比,在轻度不良反应、中度及重度不良反应发生率方面差异均无统计学意义(P>0.05),详见表8。
表2 类风湿性关节炎患者ACR20系统评价结果
Tab.2 Systematic review of ACR20 in patients with rheumatoid arthritis
StatisticalindicatorsNumberofincludedliteratures200mgCZPnN400mgCZPnNHeterogeneitytestPI2StatisticalmodelCombinedeffectRR(95%CI)P12weeks1[10]63826685fixed0.99(0.84,1.17)0.9016weeks1[11]47704569fixed1.03(0.81,1.31)0.8124weeks3[6,8,10]4327214407210.890fixed0.98(0.90,1.07)0.68
表3 类风湿性关节炎患者ACR50系统评价结果
Tab.3 Systematic review of ACR50 in patients with rheumatoid arthritis
StatisticalindicatorsNumberofincludedliteratures200mgCZPnN400mgCZPnNHeterogeneitytestPI2StatisticalmodelCombinedeffectRR(95%CI)P12weeks1[10]34824485fixed0.80(0.58,1.11)0.1916weeks1[11]35703669fixed0.96(0.69,1.33)0.8024weeks3[6,8,10]2717212837210.850fixed0.96(0.84,1.09)0.53
表4 类风湿性关节炎患者ACR70系统评价结果
Tab.4 Systematic review of ACR70 in patients with rheumatoid arthritis
StatisticalindicatorsNumberofincludedliteratures200mgCZPnN400mgCZPnNHeterogeneitytestPI2StatisticalmodelCombinedeffectRR(95%CI)P12weeks1[10]17226685fixed0.80(0.46,1.40)0.4316weeks1[11]21264569fixed0.80(0.50,1.27)0.3424weeks3[6,8,10]1471284407210.410fixed1.15(0.93,1.42)0.20
表5 类风湿关节炎患者DAS- 28(ESR)变化值系统评价结果
Tab.5 Systematic review of DAS- 28(ESR) change in patients with rheumatoid arthritis
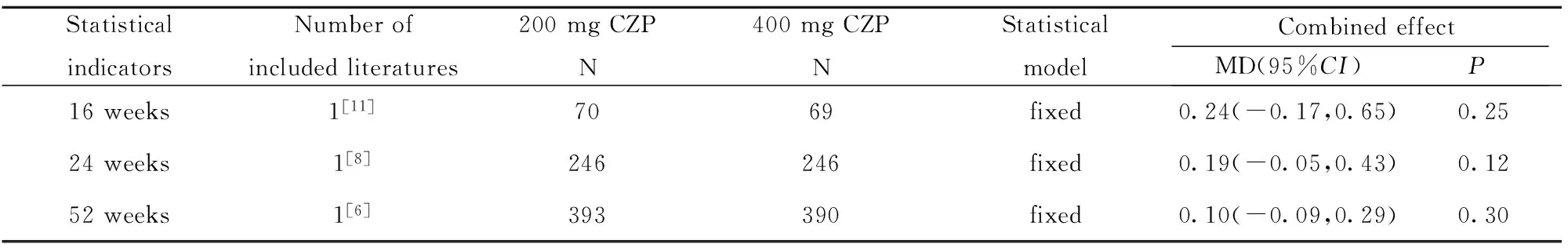
StatisticalindicatorsNumberofincludedliteratures200mgCZPN400mgCZPNStatisticalmodelCombinedeffectMD(95%CI)P16weeks1[11]7069fixed0.24(-0.17,0.65)0.2524weeks1[8]246246fixed0.19(-0.05,0.43)0.1252weeks1[6]393390fixed0.10(-0.09,0.29)0.30
表6 类风湿关节炎患者关节疼痛评价
Tab.6 Systematic review of joint pain in patients with rheumatoid arthritis
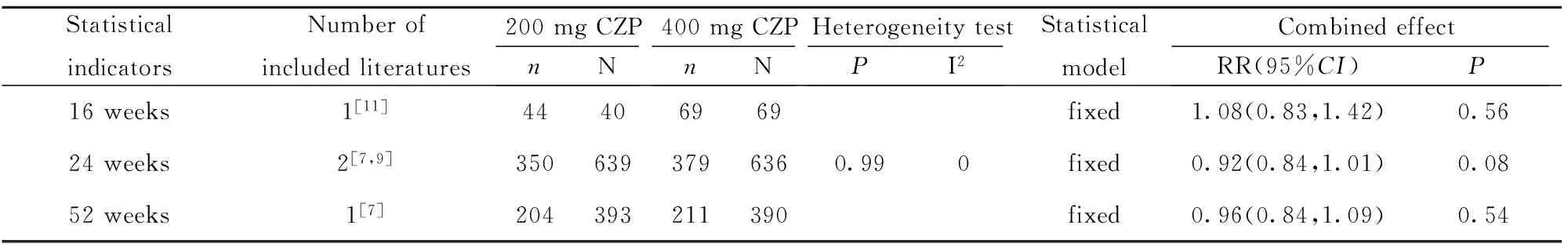
StatisticalindicatorsNumberofincludedliteratures200mgCZPnN400mgCZPnNHeterogeneitytestPI2StatisticalmodelCombinedeffectRR(95%CI)P16weeks1[11]44406969fixed1.08(0.83,1.42)0.5624weeks2[7,9]3506393796360.990fixed0.92(0.84,1.01)0.0852weeks1[7]204393211390fixed0.96(0.84,1.09)0.54
表7 类风湿关节炎患者疲劳评定系统评价
Tab.7 Systematic review of fatigue in patients with rheumatoid arthritis
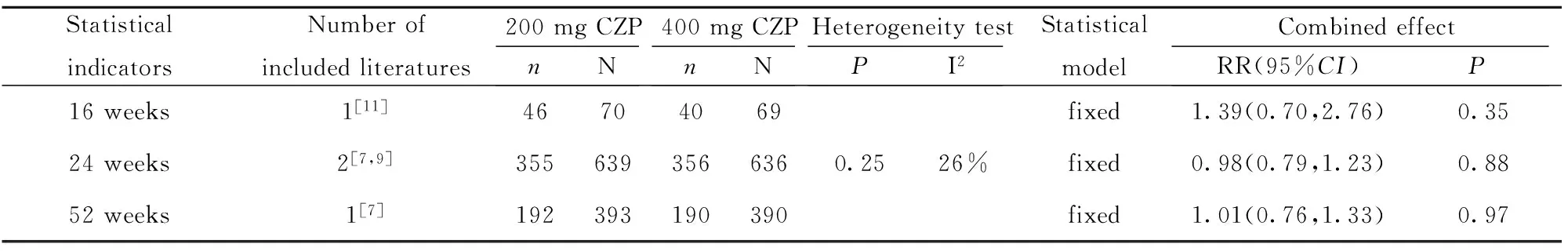
StatisticalindicatorsNumberofincludedliteratures200mgCZPnN400mgCZPnNHeterogeneitytestPI2StatisticalmodelCombinedeffectRR(95%CI)P16weeks1[11]46704069fixed1.39(0.70,2.76)0.3524weeks2[7,9]3556393566360.2526%fixed0.98(0.79,1.23)0.8852weeks1[7]192393190390fixed1.01(0.76,1.33)0.97
表8 类风湿关节炎患者不良反应系统评价
Tab.8 Systematic review of adverse reactions in patients with rheumatoid arthritis
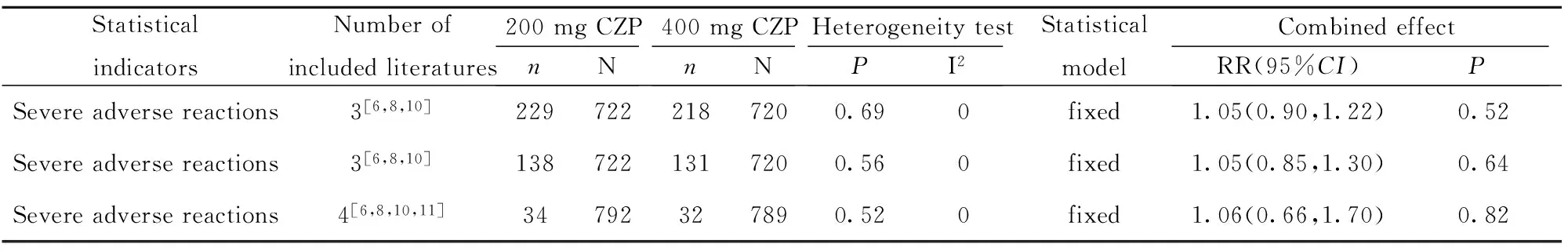
StatisticalindicatorsNumberofincludedliteratures200mgCZPnN400mgCZPnNHeterogeneitytestPI2StatisticalmodelCombinedeffectRR(95%CI)PSevereadversereactions3[6,8,10]2297222187200.690fixed1.05(0.90,1.22)0.52Severeadversereactions3[6,8,10]1387221317200.560fixed1.05(0.85,1.30)0.64Severeadversereactions4[6,8,10,11]34792327890.520fixed1.06(0.66,1.70)0.82
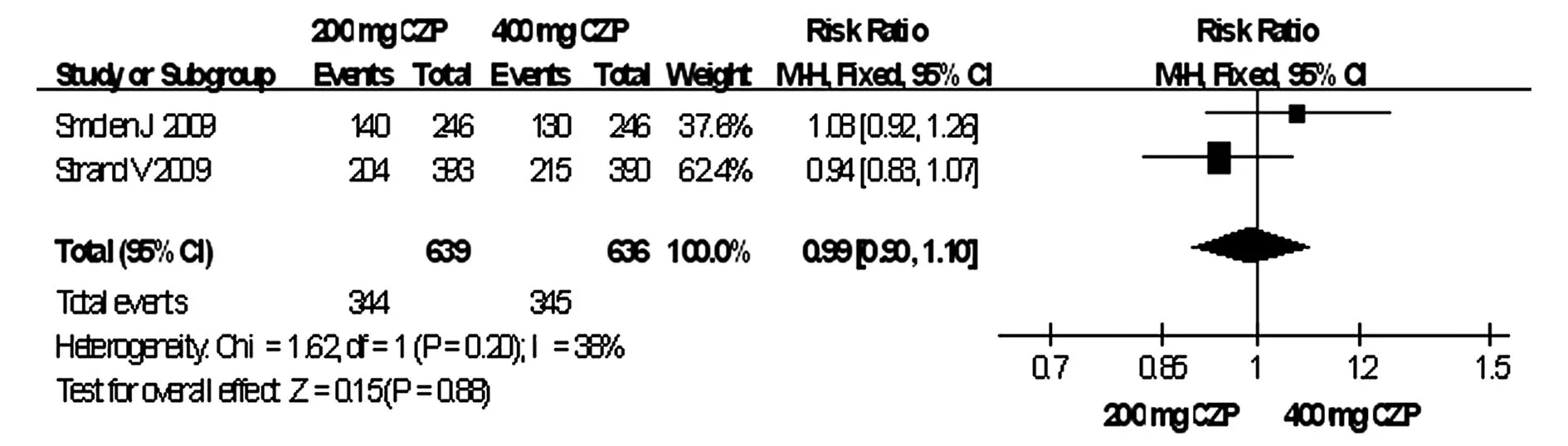
图1 类风湿关节炎患者HAQ- DI系统评价结果Fig.1 Systematic review of HAQ- DI in patients with rheumatoid arthritis
3 讨论
TNF- α为炎症和免疫应答的常见的细胞因子,RA患者关节腔滑膜液中TNF- α水平较高,在关节滑膜的炎症进展及软骨破坏中有着重要的作用[12]。通过抑制TNF- α的表达能有效缓解RA患者的疾病的活动性,TNF- α抑制剂是目前治疗RA的一个重要的方向[13]。国内外有大量研究表明RA患者早期应用TNF- α抑制剂可有效缓解病情进展,改善关节功能,MTX与TNF- α抑制剂合用的治疗效果要优于MTX单药治疗[14]。CZP作为一种新型的TNF- α抑制剂已被逐渐应用于临床如克罗恩病的治疗,近年来有许多研究发现CZP对RA有良好的治疗效果,短期安全性较高。为探究CZP治疗RA的最佳剂量,本系统评价纳入4项随机对照研究共6篇文献,均为高质量研究,各研究间具有基线可比性。
Meta分析结果显示200 mg CZP和400 mg CZP在改善类风湿患者病情的疗效(ACR20、ACR50、ACR70),关节疾病活动性评分DAS- 28(ESR),患者对疾病活动性评价指标(HAQ- DI、关节疼痛、疲劳)及不良反应方面差异无统计学意义,这说明了不同剂量的CZP治疗RA的有效性和安全性差异无统计学意义,单纯增加CZP给药剂量并不能增加CZP的治疗效果,高剂量CZP治疗RA时不良反应的发生率与低剂量CZP相近。本研究纳入的研究间同质性较好,但仍存在以下不足:(1)仅纳入4项研究,且样本容量较小;(2)纳入研究随访时间较短,最长随访时间为52周,不同剂量的CZP长期疗效和安全性有待于进一步研究;(3)部分结局指标由于数据不足无法进行meta分析,如简化疾病活动指数(SADI)、临床疾病活动指数(CAID)等;(4)部分研究结局指标数据不完整,需要统计计算后得出统计值后系统评价;(5)所有研究均存在的发表偏倚等。
尽管不同剂量的CZP治疗RA时其不良反应发生率差异无统计学意义,但TNF- α抑制剂可引起严重的心血管疾病、败血症或感染,甚至会导致患者死亡。使用TNF- α抑制剂治疗的RA患者易产生严重感染,因此对于CZP治疗过程中新发感染的患者应予以密切监测。在使用CZP治疗前,医生和患者均需要权衡利弊,同时RA患者必须严格在医生指导和监督下使用。
综上所述,本meta分析结果显示不同剂量的CZP治疗RA具有相同的治疗效果,短期安全性相似。鉴于本meta分析的局限性,建议进一步开展高质量、长时间随访的随机对照研究,对不同剂量的CZP治疗RA的长期有效性和安全性作更深入的评估,为RA患者提供最佳的治疗方案。
[1] 陈 盛,陈顺乐,黄 烽,等.依那西普治疗中国接受甲氨蝶呤治疗的活动性类风湿关节炎患者随机双盲多中心对照研究[J].中华风湿病学杂志,2010,14(7):450- 455.
[2] 丁 菱,何善智,钟伟秋.肿瘤坏死因子拮抗剂治疗风湿病的临床疗效分析[J].海南医学,2012,23(8):27- 29.
[3] 韩 望,李运曼.肿瘤坏死因子- α抑制剂治疗类风湿性关节炎的研究进展[J].药学与临床研究,2012,20(3):218- 222.
[4] Liu Y,Fan W,Chen H,etal.Risk of breast cancer and total malignancies in rheumatoid arthritis patients undergoing TNF- alpha antagonist therapy:a meta- analysis of randomized control trials[J].Asian Pac J Cancer Prev,2014,15(8):3403- 3410.
[5] Nesbitt A,Fossati G,Bergin M,etal.Mechanism of action of certolizumab pegol (CDP870):in vitro comparison with other anti- tumor necrosis factor alpha agents[J].Inflamm Bowel Dis,2007,13(11):1323- 1332.
[6] Keystone E,Heijde D,Mason DJ,etal.Certolizumab pegol plus methotrexate is significantly more effective than placebo plus methotrexate in active rheumatoid arthritis:findings of a fifty- two- week,phase III,multicenter,randomized,double- blind,placebo- controlled,parallel- group study[J].Arthritis Rheum,2008,58(11):3319- 3329.
[7] Strand V,Mease P,Burmester GR,etal.Rapid and sustained improvements in health- related quality of life,fatigue,and other patient- reported outcomes in rheumatoid arthritis patients treated with certolizumab pegol plus methotrexate over 1 year:results from the RAPID 1 randomized controlled trial[J].Arthritis Res Ther,2009,11(6):R170.
[8] Smolen J,Landewe RB,Mease P,etal.Efficacy and safety of certolizumab pegol plus methotrexate in active rheumatoid arthritis:the RAPID 2 study.A randomised controlled trial[J].Ann Rheum Dis,2009,68(6):797- 804.
[9] Strand V,Smolen JS,van Vollenhoven RF,etal.Certolizumab pegol plus methotrexate provides broad relief from the burden of rheumatoid arthritis:analysis of patient- reported outcomes from the RAPID 2 trial[J].Ann Rheum Dis,2011,70(6):996- 1002.
[10] Yamamoto K,Takeuchi T,Yamanaka H,etal.Efficacy and safety of certolizumab pegol plus methotrexate in Japanese rheumatoid arthritis patients with an inadequate response to methotrexate:the J- RAPID randomized,placebo- controlled trial[J].Mod Rheumatol,2014,24(5):715- 724.
[11] Furst DE,Shaikh SA,Greenwald M,etal.Two dosing regimens of certolizumab pegol in patients with active rheumatoid arthritis[J].Arthritis Care Res (Hoboken),2015,67(2):151- 160.
[12] Ohta S,Harigai M,Tanaka M,etal.Tumor necrosis factor- alpha (TNF- alpha) converting enzyme contributes to production of TNF- alpha in synovial tissues from patients with rheumatoid arthritis[J].J Rheumatol,2001,28(8):1756- 1763.
[13] 周 军,张红杰.赛妥珠单抗治疗克罗恩病的临床研究进展[J].中华临床医师杂志(电子版),2013,7(24):11717- 11720.
[14] 苏 妍,徐高四,涂卫平,等.英夫利西单抗联合甲氨蝶呤治疗类风湿性关节炎的Meta分析[J].实用医学杂志,2014(13):2142- 2147.
[收稿2016- 11- 19 修回2017- 12- 29]
(编辑 张晓舟)
Efficacy and safety about two dosing regimens of Certolizumab pegol in treatment of rheumatoid arthritis:a meta- analysis
WANG Hong- Mei,LAI Xiang- Yu,BAI Hao.
Chongqing Cancer Institute & Hospital & Cancer Center,Shapingba 400030,China
Objective:To explore the efficacy and safety about two dosing regimens of Certolizumab pegol in patients with rheumatoid arthritis.Methods: Such databases as Pubmed,Medline,Embase,The Cochrane Library,WANFANG,CNKI,Science,CBM and VIP were searched from their establishment to March 2015 for collecting the randomized controlled trials comparing different dosing regimens of Certolizumab pegol in the treatment of RA.The meta- analysis was undertaken using RevMan5.3 for Windows.Results: Six publications and four researches met the inclusion criteria with high quality.The ACR20,ACR50,ACR70 response rates,and physical function were no significant difference among two dosing regimens of Certolizumab pegol.The difference were not statistically significant associated with reduction in Disease Activity Score in 28 joints- Erythrocyte sedimentation rate,arthritis pain,and fatigue.There were no significant differences of incidence of treatment- related adverse events between two groups.Conclusion: 200 mg CZP and 400 mg CZP were comparable for maintaining clinical response in the treatment of RA.More large- scale RCTs are needed to evaluate the long- term efficacy and safety about different dosing regimens of CZP in the treatment of RA.
Rheumatoid arthritis;Certolizumab pegol;Dose;Meta- analysis
10.3969/j.issn.1000- 484X.2017.08.019
王洪梅(1982年-),女,主管药师,主要从事肿瘤、自生免疫性疾病等药物治疗方面的研究,E- mail:31767834@qq.com。
及指导教师:赖翔宇(1986年-),男,硕士,药师,主要从事肿瘤、自生免疫性疾病等药物治疗方面研究,E- mail:510327039@qq.com。 白 浩(1986年-),男,硕士,药师,主要从事肿瘤相关临床药物治疗方面的研究,E- mail:474027594@qq.com。
R979.5
A
1000- 484X(2017)08- 1213- 05
