Application of multiple b-value DWI in assessment of early treatment response in postoperative patients with glioma
2017-09-03,*,,,,
, *, , , ,
(1.Department of Medical Imaging, the Second Hospital of Hebei Medical University,Shijiazhuang 050000, China; 2.Department of Medical Imaging, HuanghuaMunicipal People's Hospital, Huanghua 061300, China)
Application of multiple b-value DWI in assessment of early treatment response in postoperative patients with glioma
SHUCaikun1,QUANGuanmin1*,YUANTao1,WEIJianhai2,ZHENGYongli1,LEIJianming1
(1.DepartmentofMedicalImaging,theSecondHospitalofHebeiMedicalUniversity,Shijiazhuang050000,China; 2.DepartmentofMedicalImaging,HuanghuaMunicipalPeople'sHospital,Huanghua061300,China)
Objective To evaluate the application value of ADC of different b-value ADC maps in multiple b-value DWI for assessment of early treatment response and detection of tumor progression. Methods Totally 47 postoperative patients with glioma were enrolled. All of them accepted chemoradiotherapy after operation. Conventional MRI and multiple b-value DWI (b=0, 1 000, 2 000, 3 000 s/mm2) scans were performed. The mean and minimal ADC values (ADCmeanand ADCmin) were measured in 5 differrent corresponding ADC maps, such as ADC(1 000/0), ADC(/2 000/0), ADC(3 000/0), ADC(3 000/1 000)and ADC(3 000/2 000). And the relative values (rADCmeanand rADCmin) were calculated. The differences of ADC values among different reaction types (complete response, partial response, stable disease and progressive disease)and between progressive and non-progressive groups were compared. ROC analysis was used to determine the best cutoff values and diagnostic efficiency of ADCvalue for diagnosis of tumor progression. Results The rADCmeanin ADC(3 000/0), ADC(3 000/1 000)and ADC(3 000/2 000)maps were significantly different among different response types and between progressive group and non-progressive group (allP<0.05). The ADCmeanin ADC(3 000/1 000)and ADC(3 000/2 000)maps were significantly different among different response types and between progressive group and non-progressive group (allP<0.05). The ADCmeanand rADCmeanin ADC(3 000/2 000)map had the maximum area under curve (0.86, 0.84). When ADCmeanand rADCmeanin ADC3 000/2 000map were 408.65×10-6mm2/s and 1.12, the sensitivities and specificities were 89.3%, 71.0% and 92.9%, 77.4%, respectively. Conclusion The ADCmeanand rADCmeanin high b-value ADC maps are helpful to discriminate the early treatment response from tumor progression, which can provide valuable information for identification of tumor progression of glioma after treatment.
Glioma; Therapy; Diffusion magnetic resonance imaging; Apparent diffusion coefficient; Tumor progression
胶质瘤是中枢神经系统最常见的原发肿瘤,手术切除联合术后放疗或放化疗是目前最有效的治疗方式[1],但多数胶质瘤生长具有侵袭性,术后复发率较高。对胶质瘤术后放化疗的患者定期复查评估治疗效果及早期发现肿瘤进展,对临床及时调整治疗方案和预测患者预后十分重要。常规MRI对胶质瘤治疗反应的监测主要通过FLAIR序列高信号和异常强化信号病灶的变化评估,但部分治疗反应的常规MRI表现与肿瘤进展存在较多重叠。功能MRI有助于鉴别肿瘤进展与治疗反应[2-3],DWI是其中最易获取且广泛应用的方法,通过探测组织内水分子的扩散受限程度间接反映组织结构和细胞特性,且高b值DWI对扩散受限更敏感,但目前关于b=1 000 s/mm2的DWI能否鉴别肿瘤进展与治疗反应仍存在争议[1]。有关高b值DWI鉴别胶质瘤进展的研究报道少见[4-5]。本研究比较不同b值ADC图的ADC值评估肿瘤治疗效果和鉴别肿瘤进展的价值,探讨评估胶质瘤治疗反应DWI的最适b值和最适ADC图。
1 资料与方法
1.1 一般资料 收集2014年9月—2015年10月间具有完整资料的脑胶质瘤术后放化疗患者47例,男29例,女18例,年龄7~84岁,平均(44.0±16.6)岁。纳入标准:①经手术病理确诊为胶质瘤;②术后接受联合放化疗,放疗剂量总剂量60 Gy;③在放化疗前1天及结束后2天接受MR扫描,之后每间隔3个月随访复查MRI;④随访时间>6个月。排除标准:①MR检查禁忌证;②治疗结束后2天MRI无明显异常强化病灶;③治疗后随访未行MR扫描;④DWI图像伪影(运动伪影和异物伪影)明显,影响诊断。47例患者中,WHO Ⅱ级6例,包括5例弥漫性星形细胞瘤、1例少突-星形细胞瘤;Ⅲ级14例,包括11例间变型星形细胞瘤瘤、3例间变型少突-星形细胞瘤;Ⅳ级27例,均为多形性胶质母细胞瘤。本研究经我院医学伦理委员会批准,MR扫描前所有患者均签署知情同意书。
1.2 仪器与方法 采用Philips Systems Achieva 3.0T MR扫描仪。扫描序列主要为T1WI、T2WI、FLAIR序列平扫、多b值DWI及T1WI增强扫描。T1WI,TR 900 ms,TE 20 ms;T2WI,TR 4 257 ms,TE 103.8 ms;FLAIR序列,TR 9 000 ms, TE 140 ms,TI 2 400 ms。增强扫描对比剂为Gd-DTPA,经肘前静脉注入,剂量0.1 ml/kg体质量,流率2.5 ml/s。T1WI增强扫描参数:TR 2 000 ms,TE 20 ms,TI 800 ms。多b值DWI扫描参数:b值分别为0、1 000、2 000、3 000 s/mm2,采用单次激发SE-EPI序列,TR 2 400 ms,TE 104 ms,FOV 220 mm×220 mm,矩阵128×128。以上序列层厚均为6.5 mm,层间隔1.3 mm。
1.3图像分析 采用Philips Extended MR WorkSpace 2.6.3.4工作站进行图像分析。在增强T1WI图像中病灶强化实性成分面积最大的层面,选择感兴趣区(region of interest, ROI),尽量避开术后囊腔、出血和血管。通过不同b值组合的DWI图像(b值组合分别为:0、1 000 s/mm2,0、2 000 s/mm2,0、3 000 s/mm2,1 000、3 000 s/mm2,2 000、3 000 s/mm2),每例患者获取5组ADC[ADC(1 000/0)、ADC(2 000/0)、ADC(3 000/0)、ADC(3 000/1 000)、ADC(3 000/2 000)]图。分别测量5组ADC图中病灶ROI内的平均和最小ADC值(ADCmean和ADCmin)。在同一层面测量病变对侧正常脑白质区域的平均和最小ADC值(nADCmean和nADCmin),计算病灶的相对ADC值(relative ADC, rADC),rADCmean=ADCmean/nADCmean, rADCmin=ADCmin/nADCmin。
1.4 随访与疗效评估 根据2010中枢神经系统肿瘤治疗反应RANO标准[4-6],于治疗结束后3个月行MRI随访进行疗效评估。完全有效:①无异常增强和新增病灶,②较随访前病变范围缩小或稳定;部分有效:
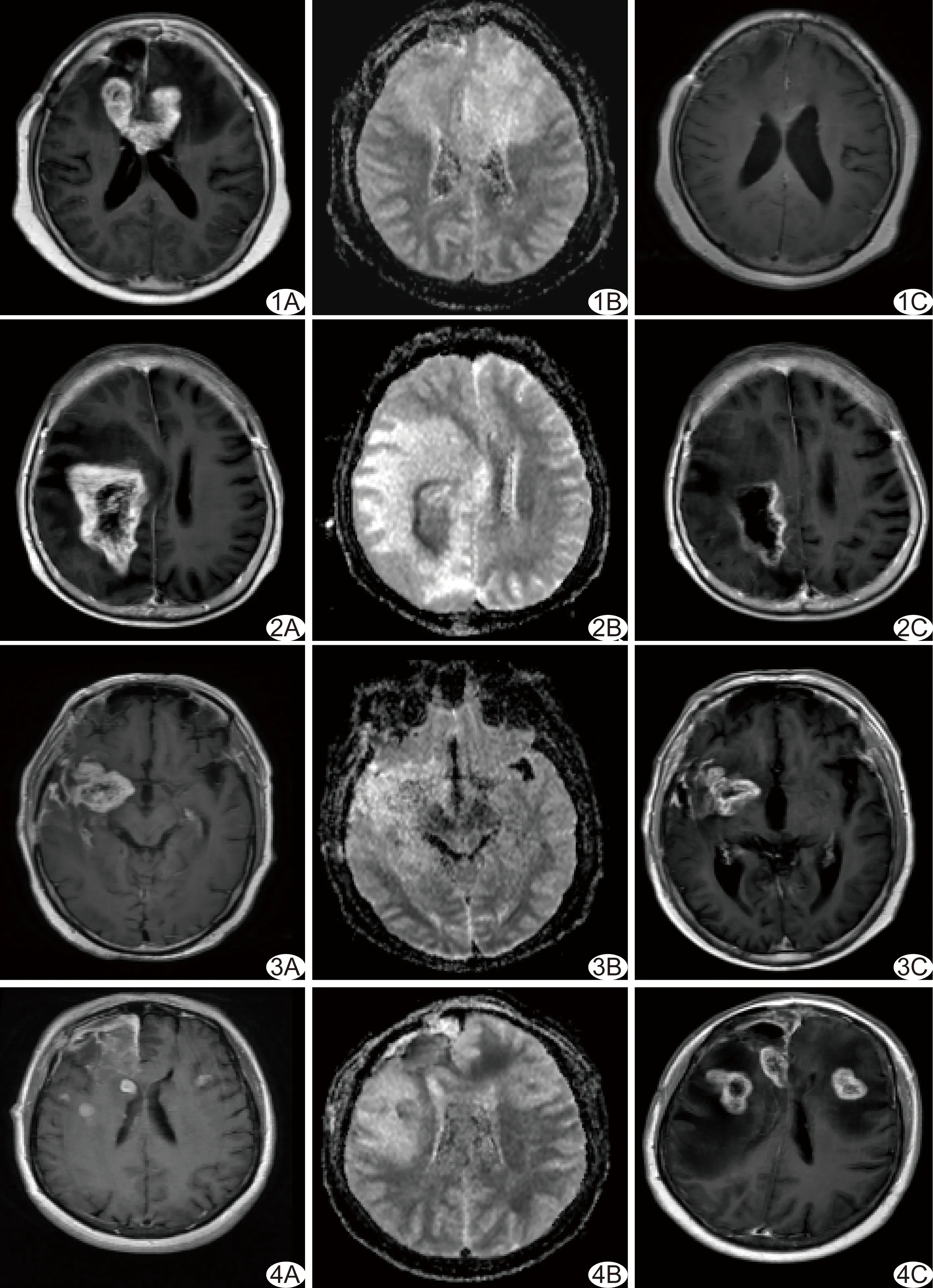
图1 患者女,70岁,胶质母细胞瘤放化疗后完全有效 A.治疗后2天增强T1WI; B.ADC(3 000/1 000)图; C.治疗后3个月随访复查增强T1WI 图2 患者女,84岁,胶质母细胞瘤放化疗后部分有效 A.治疗后2天增强T1WI; B.ADC(3 000/1 000)图; C.治疗后3个月随访复查增强T1WI 图3 患者男,62岁,胶质母细胞瘤放化疗后稳定 A.治疗后2天增强T1WI; B.ADC(3 000/1 000)图; C.治疗后3个月随访复查增强T1WI 图4 患者女,52岁,间变型星形细胞瘤放化疗后进展 A.治疗后2天强T1WI; B.ADC(3 000/1 000)图; C.治疗后3个月随访复查增强T1WI
①无新增病灶,②较随访前异常增强病灶体积缩小≥50%,③较随访前病变范围缩小或稳定;稳定:①无新增病灶,②较随访前异常增强病灶体积缩小<50%但增大<25%,③较随访前病变范围缩小或稳定;进展:①出现新增病变,②较随访前异常增强病灶体积增大≥25%,③较随访前病变范围增大,④临床症状恶化。多发肿瘤患者以疗效差的肿瘤病灶为准。依据肿瘤是否进展分为进展组和非进展组。
1.5统计学分析 采用SPSS 17.0统计分析软件,符合正态分布的计量资料以±s表示,采用单因素方差分析比较ADC值在不同治疗反应类型(完全有效、部分有效、稳定、进展)间的差异,应用两独立样本t检验比较ADC值在进展组与非进展组间的差异。不符合正态分布的资料以中位数(四分位数间距)表示,多组间比较采用Kruskal-WallisH检验。P<0.05为差异有统计学意义。分别对不同ADC图中各ADC值行ROC分析,确定鉴别肿瘤进展的最佳临界值,评价其敏感度和特异度。
2 结果
2.1 治疗效果 随访47例患者治疗后3个月随访,治疗反应类型为完全有效10例(图1)、部分有效4例(图2)、稳定13例(图3)、进展20例(图4)。47例患者治疗后共出现59个异常强化病灶,其中治疗反应类型为完全有效10个、部分有效4个、稳定16个、进展29个。进展组共20例29个病灶,非进展组共27例30个病灶。
2.2 不同治疗反应类型间比较 ADC(3 000/0)、ADC(3 000/1 000)和ADC(3 000/2 000)图中,rADCmean在不同治疗反应类型间差异有统计学意义(P均<0.05);ADC(3 000/1 000)和ADC(3 000/2 000)图中,ADCmean在不同治疗反应类型间差异有统计学意义(P均<0.05),见表1。所有ADC图中的ADCmin、rADCmin在不同治疗反应类型间差异均无统计学意义(P均>0.05),见表2。
2.3 进展组与非进展组间比较 ADC(3 000/0)、ADC(3 000/1 000)和ADC(3 000/2 000)图中,进展组与非进展组rADCmean差异均有统计学意义(P均<0.05);ADC(3 000/1 000)和ADC(3 000/2 000)图中,进展组与非进展组ADCmean差异均有统计学意义(P均<0.05),见表3。其余ADC图中ADCmean、rADCmean在进展与非进展组间差异均无统计学意义(P均>0.05),见表3。所有ADC图中ADCmin、rADCmin在进展与非进展组间差异均无统计学意义(P均>0.05),见表4。
2.4 诊断效能 ADC图中的ADCmean、rADCmean鉴别肿瘤进展的ROC曲线下面积(area under the curve, AUC)随b值增高有增高趋势,见表5。ADC(3 000/2 000)图中ADCmean和rADCmean诊断肿瘤进展的AUC最大,分别为0.86和0.84(P均<0.05,图5),分别取ADCmean=408.65×10-6mm2/s和rADCmean=1.12诊断胶质瘤进展的敏感度、特异度分别为89.3%、71.0%和92.9%、77.4%。
3 讨论
既往研究[7]证实ADC值与肿瘤的细胞密度呈负相关。胶质瘤治疗后肿瘤坏死,细胞密度减低;而肿瘤进展则由于肿瘤细胞增殖,细胞密度增加。因此,ADC值改变程度和范围有助于判断胶质瘤治疗效果[2];多项研究[8-11]认为肿瘤进展的平均ADC值低于放疗坏死。但由于肿瘤治疗后组织不均质,其内常混杂有小坏死、出血灶和血管源性水肿,因此少数研究的结果与上述结论有所不同。白雪菲等[9,11]对82例胶质瘤治疗后患者进行研究,发现肿瘤复发与放疗损伤者的ADC值差异无统计学意义(P>0.05)。本研究同样发现ADC(1 000/0)、ADC(2 000/0)图中平均ADC值及其相对值在不同治疗反应类型间差异无统计学意义(P均>0.05),提示通过低b值(b=1 000、2 000 s/mm2)DWI图像获取的ADC图强化区域的平均ADC值不能有效评估肿瘤治疗效果,其原因可能是由于肿瘤治疗后病变内不均质,肿瘤复发内可伴发坏死灶和较明显的血管源性水肿,传统的低b值DWI不能有效避免以上因素的干扰,导致肿瘤复发的ADC值不一定低于治疗后坏死。
表1 不同治疗反应类型间各ADC图中ADCmean、rADCmean比较(±s)
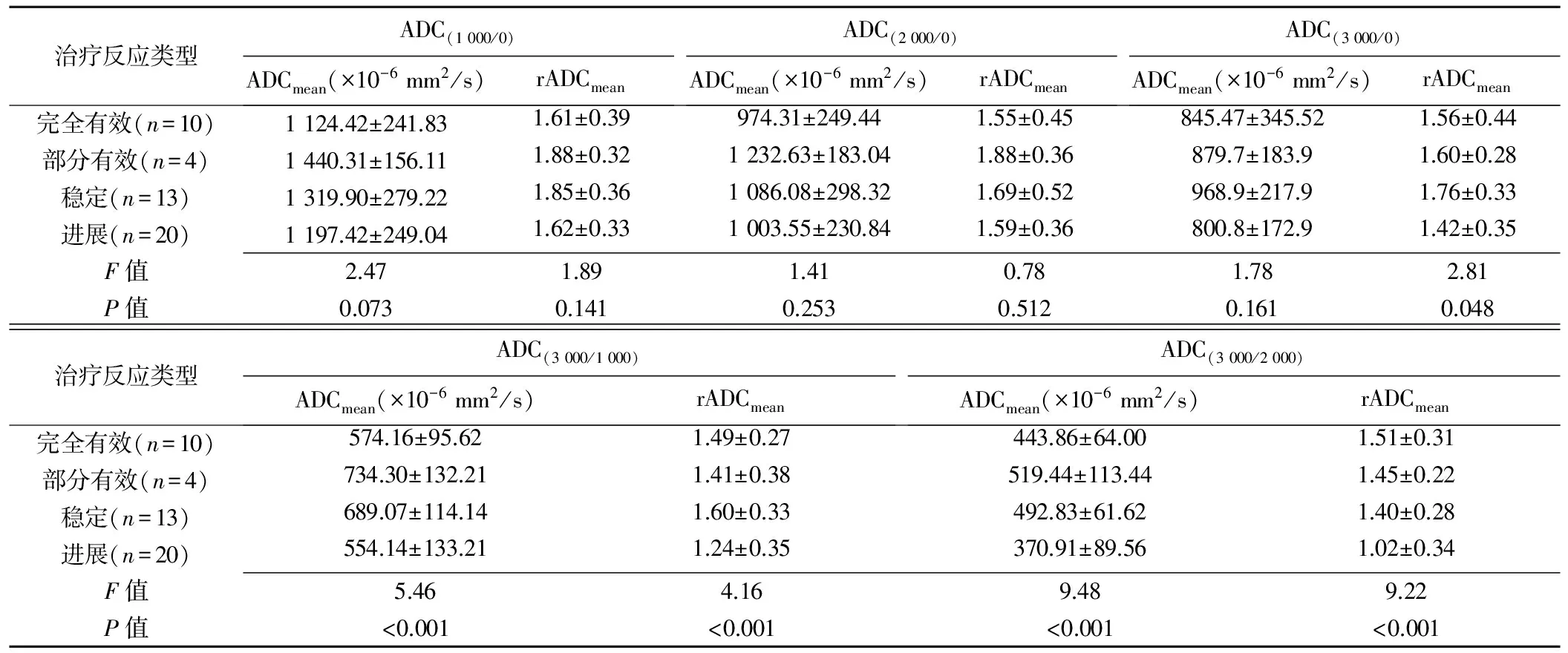
表1 不同治疗反应类型间各ADC图中ADCmean、rADCmean比较(±s)
治疗反应类型ADC(1000/0)ADCmean(×10-6mm2/s)rADCmeanADC(2000/0)ADCmean(×10-6mm2/s)rADCmeanADC(3000/0)ADCmean(×10-6mm2/s)rADCmean完全有效(n=10)1124.42±241.831.61±0.39974.31±249.441.55±0.45845.47±345.521.56±0.44部分有效(n=4)1440.31±156.111.88±0.321232.63±183.041.88±0.36879.7±183.91.60±0.28稳定(n=13)1319.90±279.221.85±0.361086.08±298.321.69±0.52968.9±217.91.76±0.33进展(n=20)1197.42±249.041.62±0.331003.55±230.841.59±0.36800.8±172.91.42±0.35F值2.471.891.410.781.782.81P值0.0730.1410.2530.5120.1610.048治疗反应类型ADC(3000/1000)ADCmean(×10-6mm2/s)rADCmeanADC(3000/2000)ADCmean(×10-6mm2/s)rADCmean完全有效(n=10)574.16±95.621.49±0.27443.86±64.001.51±0.31部分有效(n=4)734.30±132.211.41±0.38519.44±113.441.45±0.22稳定(n=13)689.07±114.141.60±0.33492.83±61.621.40±0.28进展(n=20)554.14±133.211.24±0.35370.91±89.561.02±0.34F值5.464.169.489.22P值<0.001<0.001<0.001<0.001
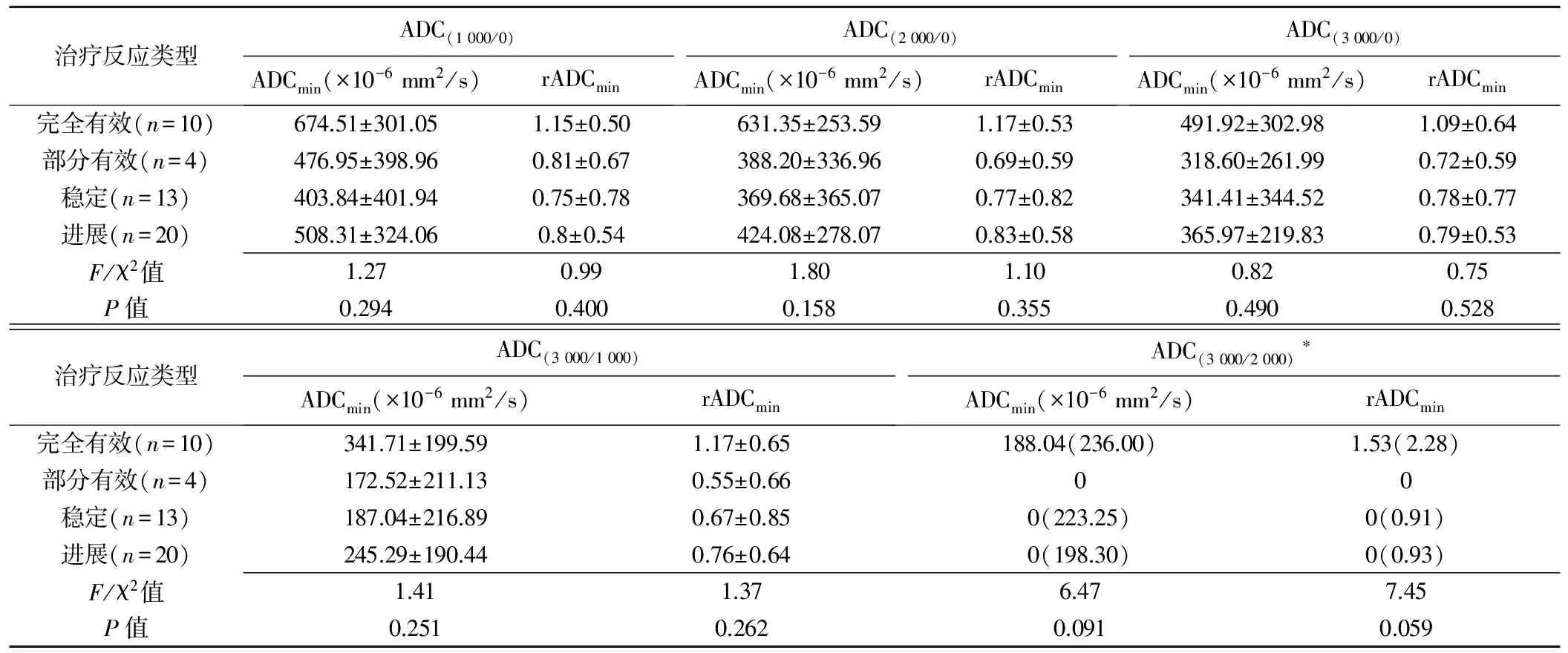
表2 不同治疗反应类型间各ADC图中ADCmin、rADCmin比较
注:*:资料不符合正态分布,以中位数(四分位数间距)表示,采用Kruskal-WallisH检验
表3 进展组与非进展组间各ADC图中ADCmean、rADCmean比较(±s)

表3 进展组与非进展组间各ADC图中ADCmean、rADCmean比较(±s)
治疗反应类型ADC(1000/0)ADCmean(×10-6mm2/s)rADCmeanADC(2000/0)ADCmean(×10-6mm2/s)rADCmeanADC(3000/0)ADCmean(×10-6mm2/s)rADCmean进展组(n=20)1197.39±249.061.62±0.321003.49±230.831.59±0.36800.76±173.001.41±0.35非进展组(n=27)1255.62±272.001.76±0.381063.10±272.121.67±0.48910.29±269.181.65±0.37t值0.861.530.910.661.892.54P值0.3910.1330.3690.5140.0730.010治疗反应类型ADC(3000/1000)ADCmean(×10-6mm2/s)rADCmeanADC(3000/2000)ADCmean(×10-6mm2/s)rADCmean进展组(n=20)554.15±133.221.24±0.35371.02±89.621.45±0.28非进展组(n=27)650.41±123.541.53±0.31477.40±73.901.02±0.34t值2.873.354.945.24P值<0.001<0.001<0.001<0.001
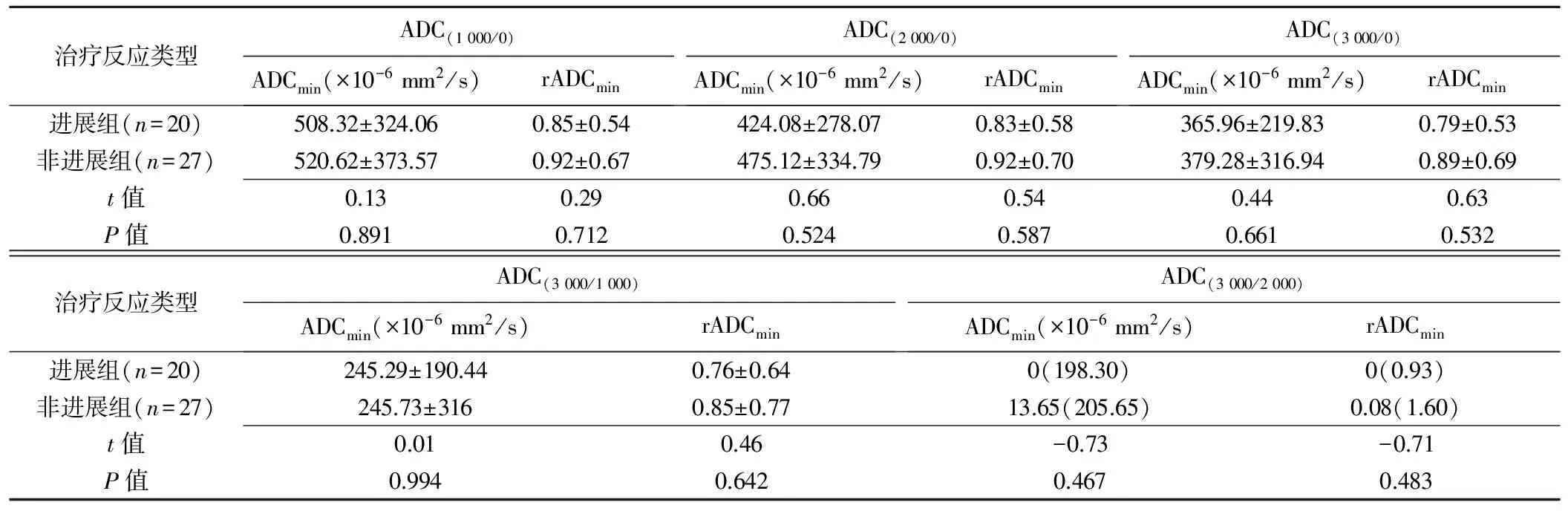
表4 进展组与非进展组间各ADC图中ADCmin、rADCmin比较

表5 不同ADC图的ADC值及其相对值鉴别肿瘤进展的ROC曲线AUC值
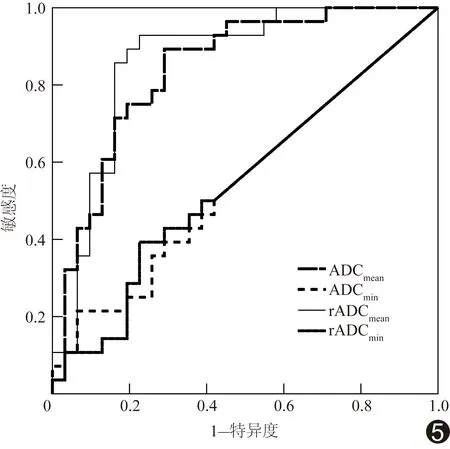
图5 ADC(3 000/2 000)图中各ADC值诊断肿瘤进展的ROC曲线 rADCmean、ADCmean的曲线下面积分别为0.86、0.84
本研究发现,5组ADC图中进展组的ADCmin、rADCmin均与非进展组差异无统计学意义(P均>0.05),与沙琳等[11]的研究结果不一致,分析原因为治疗有效的强化病灶内仍可能存在其他扩散受限病变的影响,如微小出血灶、瘢痕、纤维或胶质增生等,而这些扩散受限病变的ADCmin值可能小于肿瘤进展的ADCmin值,最终导致强化病灶的ADCmin值减低。
传统DWI显示的高信号包括扩散障碍和扩散受阻两部分,扩散障碍与细胞外间隙内水的含量和细胞的排列扭曲程度相关[12],由于肿瘤内坏死和微血管周围间隙的增加,加之血管源性水肿和肿瘤坏死导致细胞外水分子增多,致肿瘤实际ADC值高于预期ADC值[13]。DWI信号随b值呈非单指数衰减,高b值成像中扩散受阻的信号衰减明显大于扩散受限,因此高b值成像对真实扩散受限信号更敏感,能有效降低有血管源性水肿和坏死的影响,提高对肿瘤扩散受限程度的敏感性[14]。Pramanik等[14]认为高b值(b=3 000 s/mm2)DWI可提高胶质母细胞瘤术后高细胞密度区域显目性和轮廓清晰程度。谢璞等[4]对22例脑胶质瘤术后患者综合治疗近期(3~4周)疗效进行监测,同样发现高b值(b=3 000 s/mm2)DWI对肿瘤进展的敏感度、特异度和准确率均高于传统低b值(b=1 000 s/mm2)DWI(P均<0.05)。本研究表明,高b值ADC图[ADC(3 000/0)、ADC(3 000/1 000)和ADC(3 000/2 000)]中强化区域的平均ADC值及其相对值能有效评价治疗反应和鉴别肿瘤进展,而较低b值ADC图[ADC(1 000/0)、ADC(2 000/0)]中的平均ADC值及其相对值不能有效评价治疗反应和鉴别肿瘤治疗后进展;但本研究ADC(3 000/0)图中rADCmean鉴别肿瘤进展ROC曲线AUC为0.68,而谢璞等[4]的研究中AUC为0.86,可能与ROI的选择有关,本研究参照T1WI强化的典型层面中异常强化区域,ROI选择的范围固定,其内可能包含部分治疗后坏死的异常强化区,而谢璞等[4]选择手术区边缘2 cm内手动选择ROI。
Lemke等[15]发现应用较高b值(b=3 000 s/mm2)DWI与1个b值不等于0的DWI图像获取的ADC图可有效避免微血管灌注的影响,且对体素内非相干性运动更敏感。本研究发现以ADC(3 000/2 000)图中各ADC值鉴别治疗后肿瘤进展的ROC曲线AUC最大,分析原因为高b值DWI可有效避免血管源性水肿的影响,提高其对肿瘤进展扩散受限的敏感度。 虽然高b值能够提高DWI对扩散受限的敏感性,但同时图像质量也会造成一定程度的下降。
本研究的局限性:①由于扫描时间的限制,b值分段较少;②样本量相对较少,可能增大不同治疗反应类型间比较时的误差;③随访时间较短,未将生存期等判定预后的指标纳入;④缺乏对全肿瘤的所有体素分析。今后将扩大样本、采用更多b值进行中长期预后研究。
总之,通过高b值DWI获取的ADC图[ADC(3 000/0)、ADC(3 000/1 000)和ADC(3 000/2 000)]中的ADCmean、rADCmean可用于评估胶质瘤的治疗效果和鉴别肿瘤进展。
[1] Levy S, Chapet S, Mazeron JJ. Management of gliomas. Cancer Radiother, 2014,18(5-6):461-467.
[2] Galban S, Lemasson B, Williams TM, et al. DW-MRI as a biomarker to compare therapeutic outcomes in radiotherapy regimens incorporating temozolomide or gemcitabine in glioblastoma. PLoS One, 2012,7(4):e35857.
[3] Verma N, Cowperthwaite MC, Burnett MG, et al. Differentiating tumor recurrence from treatment necrosis: A review of neurooncologic imaging strategies. Neuro-Oncology, 2013,15(5):515-524.
[4] 谢璞,杨艳芳,胡德志,等.高b值DWI对脑胶质瘤术后治疗后早期疗效的价值研究.医学影像学杂志,2014,24(7):1116-1119.
[5] Chu SH, Choi I, Ryoo S, et al. Differentiation of true progression from pseudoprogression in glioblastoma treated with radiation therapy and concomi-tant temozolomide: Comparison study of standard and high-b-value diffusion-weighted imaging. Radiology, 2013,269(3):831-840.
[6] Wen PY, Macdonald DR, Reardon DA, et al. Updated response assessment criteria for high-grade gliomas:Response assessment in neuro-oncology working group. J Clin Oncol, 2010,28(11):1963-1972.
[7] Ellingson BM, Malkin MG, Rand SD, et al. Validation of functional diffusion maps (fDMs) as a biomarker for human glioma cellularity. J Magn Reson Imaging, 2010,31(3):538-548.
[8] 孟名柱,周胜利,苗重昌,等.DWI联合1H-MRS多参数分析鉴别胶质瘤术后复发与放射性脑损伤.中国医学影像技术,2011,27(5):905-909.
[9] 白雪菲,牛广明,韩晓东,等.PWI和DWI技术在鉴别脑胶质瘤复发与放射性脑损伤中的价值.磁共振成像,2014,5(1):7-10.
[10] Al Sayyari A, Buckley R, McHenery C, et al. Distinguishing recurrent primary brain tumor from radiation injury: A preliminary study using a susceptibility-weighted MR imaging-guided apparent diffusion coefficient analysis strategy. AJNR Am J Neuroradiol, 2010,31(6):1049-1054.
[11] 沙琳,范国光,曹倩,等.联合应用PWI与DWI鉴别胶质瘤复发与放射性损伤.中国临床医学影像杂志,2013,24(12):841-845.
[12] Sykova E, Nicholson C. Diffusion in brain extracellular space. Physiol Rev, 2008,88(4):1277-1340.
[13] White NS, McDonald C, Farid N, et al. Diffusion-weighted imaging in cancer: Physical foundations and applications of Restriction Spectrum Imaging. Cancer Res, 2014,74(17):4638-4652.
[14] Pramanik PP, Parmar HA, Mammoser AG, et al. Hypercellularity components of glioblastoma identified by high b-Value diffusion-weighted imaging. Int J Radiat Oncol Biol Phys, 2015,92(4):811-819.
[15] Lemke A, Stieltjes B, Schad LR, et al. Toward an optimal distribution of b values for intravoxel incoherent motion imaging. Magn Reson Imaging, 2011,29(6):766-776.
舒彩锟(1989—),男,贵州天柱人,硕士,医师。研究方向:神经影像学。现工作于武警重庆总队医院影像科。
全冠民,河北医科大学第二医院影像科,050000。E-mail: quanguanmin@163.com
2016-10-10
2017-05-30
多b值DWI在脑胶质瘤治疗后近期评价中的应用
舒彩锟1,全冠民1*,袁 涛1,魏建海2,郑永利1,雷建明1
(1.河北医科大学第二医院影像科,河北 石家庄 050000;2.黄骅市人民医院影像科,河北 黄骅 061300)
目的 探讨应用多b值DWI中不同b值ADC值评估胶质瘤近期治疗效果及鉴别肿瘤进展的价值。方法 对47例经手术病理证实为脑胶质瘤且接受联合放化疗的患者行常规MRI及多b值DWI(b=0、1 000、2 000、 3 000 s/mm2)扫描。分别在5种不同b值组合(b值组合分别为:0、1 000 s/mm2,0、2 000 s/mm2,0、3 000 s/mm2,1 000、 3 000 s/mm2,2 000、3 000 s/mm2)的ADC图[ADC(1 000/0)、ADC(/2 000/0)、ADC(3 000/0)、ADC(3 000/1 000)、ADC(3 000/2 000)]中测量病灶的平均和最小ADC值(ADCmean和ADCmin),计算其相对值(rADCmean、rADCmin)。比较治疗后不同反应类型(完全有效、部分有效、稳定、进展)间及进展组与非进展组间ADC值的差异,通过ROC曲线分析不同ADC值诊断肿瘤进展的最佳临界值和诊断效能。结果 ADC(3 000/0)、ADC(3 000/1 000)和ADC(3 000/2 000)图中的rADCmean在不同反应类型间和进展组与非进展组间差异均有统计学意义(P均<0.05);ADC(3 000/1 000)和ADC(3 000/2 000)图中的ADCmean在不同反应类型间和进展组与非进展组间差异均有统计学意义(P均<0.05)。ADC(3 000/2 000)图中ADCmean和rADCmean诊断肿瘤进展的曲线下面积最大,分别为0.86和0.84,以ADCmean=408.65×10-6mm2/s和rADCmean=1.12诊断胶质瘤进展的敏感度、特异度分别为89.3%、71.0%和92.9%、77.4%。结论 通过高b值ADC图中病灶的ADCmean和rADCmean可较准确地评估胶质瘤的近期治疗效果,并为鉴别胶质瘤术后肿瘤进展提供有价值的信息。
胶质瘤;治疗;扩散磁共振成像;表观扩散系数;肿瘤进展
R739.41; R445.2
A
1003-3289(2017)08-1190-07
E-mail: 1525475650@qq.com
10.13929/j.1003-3289.201610031
猜你喜欢
杂志排行
中国医学影像技术的其它文章
- Progresses of CAIPIRINHA-Dixon-TWIST-VIBE in diagnosis of small hepatocellular carcinoma
- Automatic infant brain segmentation based on diffusion tensor imaging
- Quantitative analysis of left ventricle myocardial fibrosis in patients with atrial fibrillation by cardiac MRI
- Comparative analysis of paravertebral lymphatic trunk by MR lymphangiography between intradermal and subcutaneous injection of Gadodiamide in rabbits
- Application value of Doppler ultrasound in early active axial spondyloarthropathy
- Percentage of attenuation drop of intra-mural coronary segment at diastolic phase coronary CTA in prediction of significant systolic compression of myocardial bridge
