高效液相色谱法测定多维元素片中泛酸钙的含量
2017-08-09李静静杨会鸽
李静静,范 菲,杨会鸽
(西安市食品药品检验所,陕西 西安 710054)
高效液相色谱法测定多维元素片中泛酸钙的含量
李静静,范 菲,杨会鸽
(西安市食品药品检验所,陕西 西安 710054)
建立测定多维元素片中泛酸钙含量的高效液相色谱法。采用C18柱(250mm×4.6mm,5μm),流动相为乙腈-0.1%的磷酸溶液(v/v)(3∶97),流速为1.0mL/min,检测波长205nm,柱温25℃。泛酸钙进样量线性范围为0.68~3.38μg(R=0.9999),平均回收率为99.4%,其RSD为1.68%(n=9)。该方法简单、准确,可用于泛酸钙的质量控制。
泛酸钙;高效液相色谱法;含量测定
前言
泛酸钙和泛酸没有本质的区别,泛酸钙的别名是维生素B5[1]。泛酸的一个重要功能是参加代谢过程,它既是二碳单位的载体,也是体内乙酰化酶的辅酶,是酰基的传递者[2]。泛酸钙作为辅酶A的组成物质参与调节蛋白质、糖和脂肪的代谢,是人体和动物体内维持正常生理机能不可或缺的物质[3]。特别是生长发育过程中脂肪的合成和分解,泛酸钙都是不可缺少的[4]。缺乏泛酸钙会导致生长迟缓、神经系统障碍、生殖机能发生障碍、皮肤毛发异常、消化器官失常、适应性降低等疾病[5]。临床上泛酸钙主要用于治疗维生素B缺乏症,周围神经炎,手术后肠绞痛等,在医药和食品饲料行业也经常作为添加剂使用[6]。
泛酸钙虽然广泛存在于食物中,但在加工烹饪等过程中经常会损失20%~40%,甚至高达50%,从而导致我们在食物中的摄入量有限[7]。为了弥补类似的损失,市面上出现的一些保健品或药品(如多维元素片)中,通常会添加泛酸钙作为其主要成分之一[8]。在本实验中,我们建立了用高效液相色谱法测定多维元素片中泛酸钙含量的方法,用于有效控制产品质量。
1 实验部分
1.1 仪器与试药
Ultimate 3000高效液相色谱仪(戴安);BSA124S-CW电子天平(赛多利斯);MS105电子天平(梅特勒);多维元素片(贵州神奇药业有限公司);泛酸钙对照品(中国药品生物制品检定所,批号100370-200301);乙腈为色谱纯,其他试剂均为分析纯,水为高纯水。
1.2 色谱条件与系统适用性试验
色谱柱:Agilent Eclipse Plus C18;流动相:乙腈-0.1%的磷酸溶液(v/v)(3∶97);流速1.0mL/min,检测波长为205nm,柱温为25℃;进样量:10μL。以峰面积外标法定量。
1.3 溶液制备
取本品20片,精密称定质量,研细,精密称取适量(约相当于泛酸钙10mg的量)置50mL容量瓶中,加入0.1%的磷酸溶液约40mL,超声处理20min,放冷,稀释至刻度,摇匀,过滤,续滤液作为供试品溶液。另取泛酸钙对照品适量,精密称定,用0.1%的磷酸溶液溶解,并定量稀释制成每1mL中约含0.2mg的溶液,作为对照品溶液。
1.4 方法学考察
线性关系考察:精密称取泛酸钙对照品33.78mg,置50mL容量瓶中,加0.1%的磷酸溶液溶解并稀释至刻度,摇匀,作为对照品贮备液。精密量取贮备液1mL、2mL、3mL、4mL、5mL,分别置10mL容量瓶中,加0.1%的磷酸溶液稀释至刻度,摇匀,制成5份系列浓度的样品,按上述拟定色谱条件测定,记录色谱图。
精密度试验:精密量取线性关系考察项下的第2份溶液,按上述拟定色谱条件连续进样6次,每次10μL,记录色谱图。
重复性试验:精密称取本品(批号为140203)适量,共8份,按1.3项下的方法制备供试品溶液,分别精密量取10μL,注入液相色谱仪,记录色谱图。
稳定性试验:配制供试品溶液,分别于0、1、2、4、8、12、18、24h进样10μL,记录色谱图。
回收率试验:精密称取9份已知含量的样品(批号为140203)适量,分别精密加入泛酸钙对照品贮备液0.5mL,1.5mL,2.5mL,按1.3项下的方法处理制成回收率试验溶液,分别精密量取10μL,注入液相色谱仪,记录色谱图。
1.5 样品含量测定
精密称取3份不同批次的样品,以及泛酸钙对照品,按溶液制备方法制备供试品溶液与对照品溶液。分别取10μL注入液相色谱仪,记录色谱图,按外标法以峰面积计算。
2 结果与讨论
2.1 色谱条件与系统适用性试验
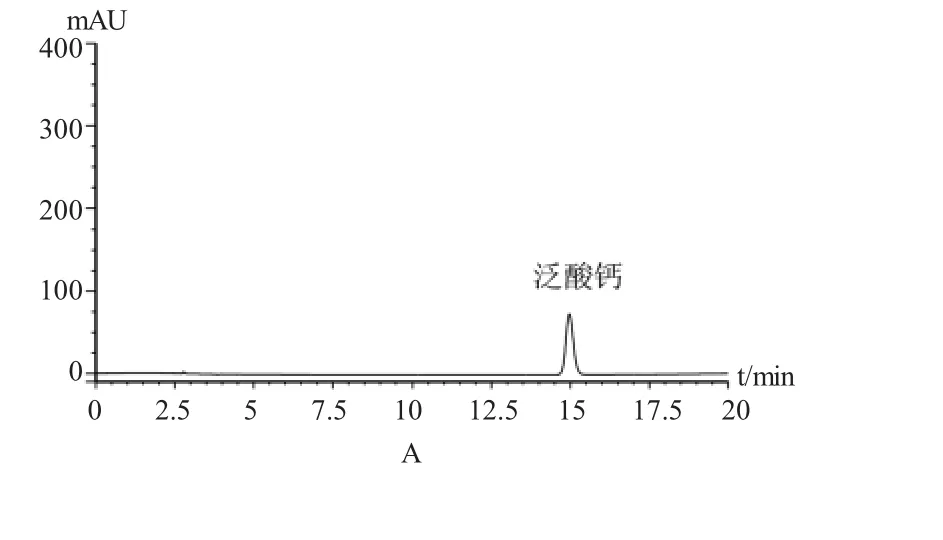
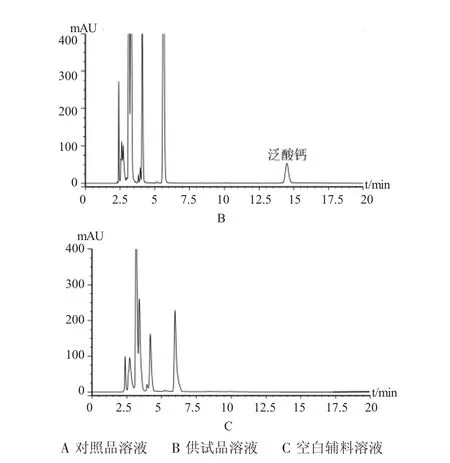
图1高效液相色谱图Fig.1 The HPLC
泛酸钙主峰保留时间为15.59min,与相邻杂质峰分离度r=5.27,峰形良好。理论板数按泛酸钙峰计算为18232。高效液相色谱图见图1。
2.2 方法学考察
线性关系考察:以进样量(X)与峰面积(Y)绘制标准曲线,得线性方程Y=6000000X+4491.2,R=0.9999。结果表明,泛酸钙进样量在0.68~3.38μg范围内与峰面积呈良好的线性关系。
精密度试验:6次峰面积的RSD为0.23%,表明仪器精密度良好。
重复性试验:8份测定结果的RSD为0.62%,表明方法的重复性良好。
稳定性试验:8次峰面积的RSD为0.24%,表明供试品溶液在24h内稳定。
回收率试验:平均回收率为99.4%,RSD为1.68%(n=9),结果详见表1。
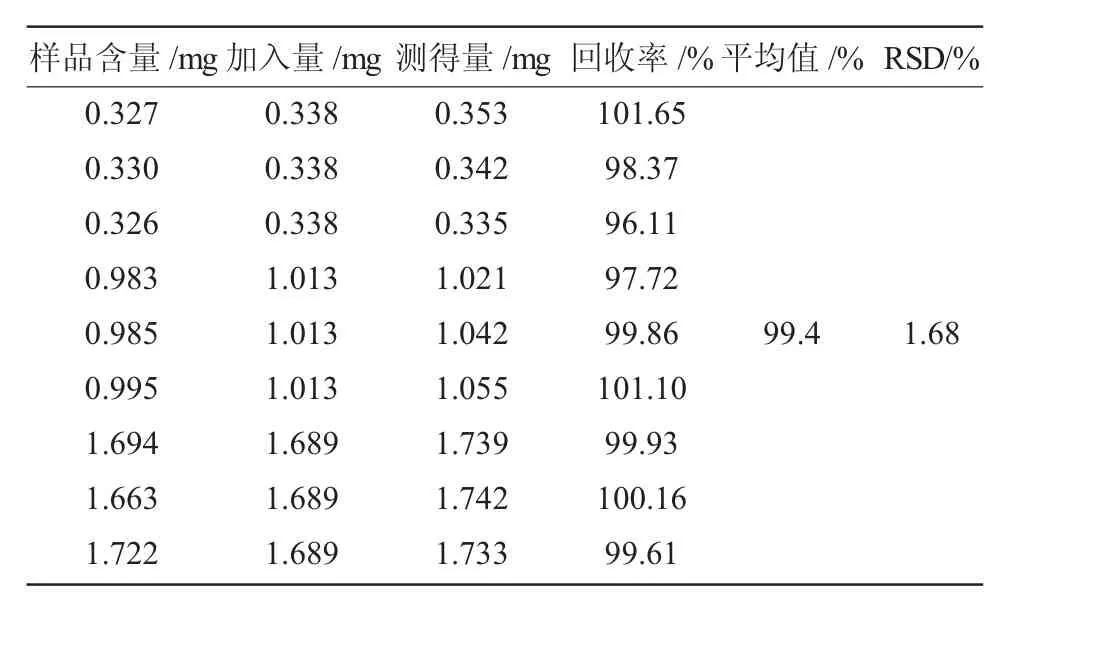
表1 回收率试验结果(n=9)Table 1 The result of recovery tests(n=9)
1.8 样品含量测定
批号为140201、140202、140203样品的含量分别为7.88、8.09、8.07mg/g。
3 结论
由于泛酸钙在水中的溶解度较大,因此我们选择水作为样品提取溶剂[9],在超声提取方面,为避免超声时间不同对泛酸提取所造成的误差影响,我们前期进行了大量的文献搜集及临床预实验,实验表明,20min可充分提取样品中的泛酸。
在流动相的选择方面,我们对目前应用较为广泛的磷酸水溶液-乙腈体系及磷酸盐缓冲溶液-乙腈体系进行了对比,并就这两种流动相的泛酸出峰时间、分离度等进行了客观评价,发现两种体系在泛酸含量的测定方面无明显差异。另有部分文献证实[10~15],磷酸水溶液-乙腈体系简便,快速并且峰形良好。因此,我们在本次的实验中,从简单实际、便捷高效的角度,选择磷酸水溶液-乙腈体系为流动相,在精简实验、节约成本方面更具优势,同时也更利于色谱柱的清洗和保护。按照该药品处方配制除该成分外的辅料空白样品,测试结果表明,辅料以及该制剂中其他成分在本试验条件下对泛酸钙含量测定无干扰。由此可见本方法精密度高、重现性及线性关系良好,回收率达标,结果准确、快速,可为该制剂的质量控制提供可靠依据。
[1] 王晞东,姚国,薛宇.泛酸与泛酸钙[J].兽药饲料添加剂, 1997,6:21~22.
[2] 王斐英,张伟,谢海蓉,等.2种不同维生素B3补充物质的理化性状及稳定性对比研究[J].中国畜牧杂志,2013,49(22):30~34.
[3] 韩秀山.D-泛酸钙生产现状及市场分析[J].精细与专用化学品,2005,13(19):28~29.
[4] 李明中.D-泛酸钙的应用与合成[J].四川化工与腐蚀控制, 1999,2(2):56~57.
[5] 郭强胜,刘明珂,禹珊,等.定量核磁共振法同时测定复合维生素B片中B1、B2、烟酰胺和泛酸钙[J].波谱学杂志,2016,33(3): 442~451.
[6] 杨艺虹,张珩,杨建设.D-泛酸钙合成技术及其进展[J].饲料工业,2004,25(6):8~11.
[7] 郭润勤.复合维生素B泛酸钙口服溶液中维生素B1和维生素B6的含量测定[J].中国药师,2009,12(1):66~68.
[8] 侯侠.高效液相色谱法测定必需磷脂注射液中右旋泛酸钙的含量[J].中外医疗,2012,31(21):120~121.
[9] 赵静,陈子龙.一种泛酸钙含量的检测方法[J].西安科技大学学报,2014,34(5):631~634.
[10] 许波,苌玲,高玲.HPLC法测定复方利血平片中维生素B1、B6、泛酸钙和氢氯噻嗪的含量[J].药物分析杂志,2008,28(11):1906~1908.
[11] 金鹏飞,夏路风,李铮,等.高效液相色谱同时测定多维元素片中的维生素B1、维生素B6、维生素C、烟酰胺和泛酸[J].药物分析杂志,2012,32(9):1606~1610.
[12] 邵生文,闻胜,聂晓明,等.高效液相色谱法测定复合维生素胶囊中泛酸含量[J].公共卫生与预防医学,2009,20(4):75~76.
[13] 盛灵慧,赵正宜,王晶,等.液相色谱法测定多元维生素片中4种水溶性维生素[J].化学分析计量,2010,19(1):30~32.
[14] 雷萍.预混合饲料中D-泛酸钙和D-生物素的UPLC测定[J].上海农业学报,2010,26(3):124~126.
[15] 石蓓佳,杨静静,张军,等.HPLC法测定克补片中6种水溶性维生素含量[J].药学与临床研究,2009,17(6):525~527.
Determination of Calcium Pantothenate Content in Multivitamins and Elements Tablets by HPLC
LI Jing-jing,FAN Fei and YANG Hui-ge
(Xi’an Institute for Food and Drug Control,Xi’an 710054,China)
A HPLC method for the determination of calcium pantothenate in multivitamins and elements tablets is established.The HPLC method is applied with a C18 column(250mm×4.6mm,5μm),and the acetonitrile-0.1%phosphate solution(v/v)(3∶97)is used as mobile phase,the flow rate is 1.0mL/min,the detection wave length is 205nm and the column temperature is set at 25℃.The linear range of calcium pantothenate sample amount is 0.68~3.38μg(R=0.9999).The average recovery is 99.4%with an RSD of 1.68%(n=9).This method is accurate,simple and feasible for quality control of calcium pantothenate.
Calcium pantothenate;HPLC;determination of content
R 927.2
B
1001-0017(2017)03-0234-03
2017-00-00
李静静(1984-)女,陕西西安人,硕士,主管药师,主要研究方向为药物分析。
