CYP11A1基因多态性与老年性骨质疏松性骨折相关性研究
2017-08-06王其飞刘正刘家帮宫雁冰吴四军姚洪春张昆薛涛张光武
王其飞 刘正 刘家帮 宫雁冰 吴四军 姚洪春 张昆 薛涛 张光武*
1. 北京大学首钢医院骨科,北京 100144 2. 北京大学首钢医院中心实验室,北京 100144
老年性骨质疏松症是原发性骨质疏松症的一种,又称为Ⅱ型骨质疏松症,为低转换型骨质疏松症,发病年龄一般在70岁以上[1]。该病受遗传因素和环境因素共同影响,其中遗传因素占80%左右[2]。目前已证实与骨质疏松症相关的候选基因有雌激素受体基因、维生素D受体基因、LRP5基因、OPG基因等。国外一项临床研究[3]发现CYP11A1基因rs900798位点多态性与芳香酶抑制剂治疗的绝经女性骨量丢失有关,说明该基因位点在骨代谢调节中有潜在作用,但尚未有关于该位点与骨代谢标志物关系的报道。本研究探讨CYP11A1基因rs900798位点与老年性骨质疏松性骨折骨转换标志物的关系,有助于从基因水平、骨代谢状况阐明老年性骨质疏松症的发病机制,为预防和治疗提供新的理论依据。
1 资料与方法
1.1 研究对象
1.1.1一般资料:研究对象为来自2015年12月至2016年7月北京大学首钢医院住院部骨科病房、内分泌病房和老年干部病房患者,共235人。老年性骨质疏松性骨折患者(骨折组)121人,其中胸椎骨折、腰椎骨折、胸腰椎骨折、股骨颈骨折、粗隆间骨折、肱骨近端骨折和桡骨远端分别为32例、40例、3例、19例、20例、4例和3例。骨折组中男性38人,女性83人;年龄65~96岁,平均(76.7±7.3)岁。老年性骨质疏松症患者(对照组)114人,其中男性41人,女性73人;年龄65~90岁,平均(72.0±7.4)岁。骨折组和对照组在性别、年龄和体重指数上差异无统计学意义(P>0.05)(表1)。研究通过医院伦理委员会批准,研究对象均签署知情同意书。
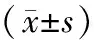
表1 研究对象基本资料Table 1 Basic characteristics of
1.1.2纳入标准:骨折组和对照组年龄≥65岁;符合骨质疏松WHO诊断标准(T≤-2.5SD);理解本研究目的及要求,同意参与本研究并签署书面知情同意书。此外,骨折组为低能量损伤导致的骨折。
1.1.3排除标准:不能签署知情同意书;近1年使用阿仑膦酸钠或唑来膦酸等双磷酸盐类药物,近6个月使用骨化三醇、雷洛昔芬、雌激素、降钙素、活性维生素D等;近3个月进行2w以上影响骨代谢药物,如类固醇类激素等;有严重肝、肾、胃肠等重要脏器疾病;患有影响骨代谢的疾病,如有糖尿病、甲状旁腺功能亢进、甲状旁腺功能减退、垂体疾病等;存在影响骨密度(bone mineral density,BMD)测量的因素,如髋部或腰椎手术史;骨折组因BMD测量困难不能完成。
1.2 研究方法
1.2.1骨密度测定:骨密度测定采用双能X线吸收仪完成,测量部位包括腰椎2-4、股骨颈和全髋。
1.2.2骨转换标志物测定:采用全自动化学发光免疫分析法检测研究组和对照组血清PINP、β-CTX浓度。
1.2.3SNP分型:清晨空腹时采集肘静脉血2ml于EDTA抗凝管中,置于-80 ℃冰箱保存。采用酚/氯仿法提取外周血白细胞DNA, -20 ℃保存。上海生物工程技术有限公司合成CYP11A1基因rs900798位点引物,上游引物:5′- CCACTCTTGGAGCCCTTCTG-3′,下游引物:5′-GAGCTGGCAATGATGTGTCC-3′。采用SNaPshot技术基因分型。核心反应(即延伸反应)体系中包含:测序酶;四种荧光标记ddNTP;紧挨多态位点5′-端的不同长度延伸引物;包含SNP位点的PCR产物模板。
1.3统计学处理
2 结果
235例研究对象SNP分型全部成功,SNP检出率为100%。两组等位基因分布符合Hardy-Weinberg平衡(P>0.05)。
骨折组G、T等位基因频率分别为40.1%、59.9%,对照组G、T等位基因频率分别为38.2%、61.8%,两组等位基因分布差异无统计学意义(P>0.05)(表2)。

表2 等位基因频率分布Table 2 Distribution of allele frequency
骨折组和对照组GG、GT、TT基因型频率分别为14.9%、50.4%、34.7%和13.2%、50.0%、36.8%,差异无统计学意义(P>0.05)(表3)。

表3 基因型频率分布Table 3 Distribution of genotype frequency
骨折组血清PINP、β-CTX均高于对照组,但差异无统计学意义(P>0.05)(表4)。

表4 两组骨转换标志物比较Table 4 Comparison of biochemical markers of bone turnover between the two groups
骨折组GT基因型血清PINP浓度大于GG基因型和TT基因型(P>0.05),骨折组3种基因型血清β-CTX浓度大小依次为TT>GT>GG(P>0.05)(表5)。

表5 骨折组各基因型骨转换标志物比较Table 5 Comparison of biochemical markers among genotypes in the fracture group
3 讨论
骨质疏松症是常见的全身性骨代谢疾病,主要特点为骨微结构破坏、骨量丢失、骨脆性增加和骨折风险增加。随着社会老龄化的发展,骨质疏松症的发病率逐年上升,预计到2050年将增加到2.1亿[1]。骨质疏松性骨折危害极大,尤其是髋部骨折致残率、致死率高,文献报道髋部骨折后患者1年内死亡率高达20%[4],引起世界各国政府的高度关注。
CYP11A1基因属于细胞色素P450超基因家族一员[5],编码胆固醇侧链裂解酶,简称为P450scc。它是生物体内类固醇激素合成第一步的限速酶[6]。P450scc在机体多个器官中表达。女性卵泡膜细胞中表达量增加,患者罹患多囊卵巢综合征风险大大增加[7]。P450scc也在脑组织中表达,当表达量下降时黄体酮水平低下,而孕烯醇酮与脑细胞生长、发育和分化有关,导致自闭症谱系障碍发生率上升[8]。关于CYP11A1基因与骨质疏松研究报道并不多,目前国内外仅有一篇相关报道。西班牙一项临床研究[3]表明CYP11A1基因与骨代谢有关。该研究在新鲜骨组织和培养的成骨细胞中检测到CYP11A基因mRNA表达,并通过蛋白质印迹法在成骨细胞中检测到CYP11A1基因编码的人胆固醇侧链裂解酶的两个亚型。这表明CYP11A基因在骨代谢调节具有潜在作用。CYP11A1基因编码P450scc催化胆固醇转化为孕烯醇酮,是性激素合成的第一步。当机体衰退老化时,CYP11A1基因表达量下降,性激素合成水平大幅度下降。雌激素或雄激素抑制破骨细胞活性、生成的功能下降,骨吸收作用加强,同时骨骼成骨作用也加强,但骨吸收作用强于骨形成作用,骨量丢失,最终导致骨质疏松[9-10]。所以在骨质疏松患者尤其发生脆性骨折的人群,CYP11A1基因表达下降,骨组织骨代谢速度加快,血清骨转换指标上升。
骨质疏松症的诊断标准依据骨密度检测结果[11],其优点为精确度高,稳定性好,但骨密度值不能反映骨代谢短期内的病理生理变化。与骨密度相比,骨转换标志物可早期评估骨质疏松治疗效果。在治疗后数1~3个月后,骨转换标志物就可发生改变。而骨密度变化一般在治疗后1年以上才有较显著的变化,可见骨密度具有明显的滞后性[12]。本研究着重从基因与骨代谢转换标志物关系进行探讨。
检测骨转换标志物可评价骨代谢状况,协助诊断代谢性骨病及分型,并可用于药物疗效的监测[13]。骨转换标志物包括骨形成标志物和骨吸收标志物两类。前者代表成骨细胞活性及骨形成状态,主要有骨钙素(OC)、骨特异性碱性磷酸酶(BALP)、Ⅰ型前胶原氨基端前肽(PINP)和Ⅰ型前胶原羧基端前肽(PICP)等。后者反映破骨细胞活性与骨吸收水平,主要包括Ⅰ型胶原羧基端肽β特殊序列(β-CTX)、吡啶啉(PYD)、脱氧吡啶啉(DPD)和抗酒石酸酸性磷酸酶-5b(TRACP5b)等。国际骨质疏松基金会推荐PICP和β-CTX作为骨质疏松疗效的检测指标。它们分别为骨形成和骨吸收的首选骨转换标志物[14]。PINP为I 型胶原合成过程中氨基端前肽切割后形成的片段。由于PINP 经过肝脏代谢,故其水平受到肝功能影响。β-CTX 是I 型胶原降解后释放入血的片段,经肾脏排出体外。
高龄、低体重指数是骨质疏松症的危险因素[15],但在本研究中人为控制研究对象一般资料,使骨折组和对照组在性别、年龄和体重指数上具有可比性。在本次研究中选择髋部或脊柱骨折患者作为研究对象,他们在骨密度测定过程中疼痛增加,给骨密度测定带来一定难度。经患者及家属同意给予肌肉注射盐酸布桂嗪注射液30min后测量,不能坚持完成骨密度测定患者不纳入本研究中。
骨折组和对照组的T等位基因频率显著大于G等位基因频率,两组等位基因频率分布差异不具有统计学意义(P>0.05)。两组基因型频率GT>TT>GG,分布差异不具有统计学意义(P>0.05)。本研究所有研究对象的G、T等位基因频率和GT、TT、GG基因型频率分别为39.1%、60.9%和14.0%、50.2%、35.7%。而在Rodríguez-Sanz研究中,G、T等位基因频率和GT、TT、GG基因型频率分别为60.4%、39.6%和37.3%、46.2%、16.5%。两个研究中该位点的等位基因频率和基因型频率分布明显不同(P<0.05),表明CYP11A1基因的rs900798位点分布具有种族、区域差异。骨折组血清骨转换标志物PINP和β-CTX浓度大于对照组(P>0.05),表明骨折组骨转换过程活跃,骨形成和骨吸收过程都加强。血清PINP、β-CTX浓度可作为骨折风险的预测指标[16-18]。骨折组GT基因型PINP浓度显著高于GG、TT基因型,表明GG基因型骨形成过程较GG、TT基因型强;而骨折组β-CTX浓度为TT>GT>GG,表明骨吸收作用依次减弱。浓度差异均不具有统计学意义(P>0.05),可能与研究的样本量较少有关。
本研究发现我国人群CYP11A1基因的rs900798位点等位基因频率和基因型频率与欧洲人群不同,说明该位点分布有种族和区域差异。但未发现老年性骨质疏松性骨折患者不同基因型的血清PINP和β-CTX浓度差异有统计学意义,这可能与纳入的研究对象较少有关。下一步笔者将扩大样本量,在不同区域进行研究,为骨质疏松症的预防和治疗提供理论依据。
