茄萼花色苷合成相关基因DFR和MYB克隆及表达分析
2017-07-31王海竹曲红云周婷婷徐启江
王海竹,曲红云,周婷婷,徐启江
茄萼花色苷合成相关基因和克隆及表达分析
王海竹1,曲红云2,周婷婷1,徐启江1
(1东北林业大学生命科学学院/林木遗传育种国家重点实验室,哈尔滨150040;2黑龙江省农业科学院园艺分院,哈尔滨 150040)
【目的】花色苷是一类通过类黄酮途径合成的水溶性次生代谢产物,既能使植物的不同器官呈现红、紫、蓝等颜色,还有利于人体健康。紫茄富含花色苷,但是有关茄萼花色苷生物合成的分子机制还不是很清楚。本研究旨在通过克隆茄萼花色苷合成相关基因和,测定其在不同发育时期不同颜色茄萼中的表达量,探究和在茄萼花色苷合成中的作用。【方法】选用绿萼和紫萼长茄(L.)果萼为试材,测定不同pH条件下茄萼花色苷含量;通过RACE方法分离克隆和cDNA全长序列,分析和的保守结构域及序列特征;分别对DFR和MYB及其同源蛋白序列进行系统进化分析,构建系统进化树来进一步分析鉴定基因;使用ExPASy网站提供的在线分析软件SOPMA预测蛋白质二级结构;利用实时荧光定量PCR方法检测目的基因在不同发育阶段果萼中的表达情况。【结果】从绿萼和紫萼长茄果萼中克隆了和片段,分别命名为、和、,GenBank登录号分别为:KX224250、KX224251和KX224253、KX224254。和全长分别为1 285 bp和1 249 bp,开放阅读框为858 bp和864 bp,分别编码285个和287个氨基酸;和全长分别为969 bp和959 bp,开放阅读框均为462 bp,编码153个氨基酸。蛋白质二级结构分析表明α-螺旋和无规则卷曲均为两个DFR蛋白和两个MYB蛋白的主要二级结构元件。序列比对表明DFR蛋白具有NADPH结构域(NADPH binding domain)和底物特异性结合结构域(Substrate specific binding domain),属于NADB-Rossmann超基因家族;MYB蛋白属于R2R3-MYB转录因子,具有R2、R3两个MYB结构域和bHLH结合域。和与和具有相对较高的同源性;和与同源性较高。花色苷含量测定显示,紫萼果茄萼花色苷含量较高且随着果实的发育成熟而逐渐增加;而绿萼茄萼几乎检测不到花色苷。荧光实时定量PCR分析表明,和在紫萼长茄果萼中表达量均远高于绿萼长茄;从初蕾期到盛花期,紫萼长茄果萼中和表达量逐渐升高,而绿萼长茄则几乎没有变化,与两个品种茄萼颜色变化相一致。【结论】和属于NADB-Rossmann超基因家族,和为典型R2R3-MYB转录因子,和在紫萼长茄果萼中表达明显高于绿萼长茄。推测和在茄萼呈色中发挥作用,并且参与花色苷生物合成。
萼片;花色苷;;;基因表达;茄
0 引言
【研究意义】茄()为茄科()茄属()一年生草本植物,是在世界范围内广泛种植的一种重要茄果类蔬菜作物[1]。紫茄富含花色苷,其浓度分别约为葡萄和洋葱的2.34和7.08倍[2]。花色苷是一种天然水溶性类黄酮物质,存在于植物的叶、花和果实中,不仅使各种蔬菜、花卉和果实呈现红色、紫色和蓝色,而且具有一定营养和药理作用,如清除自由基、预防心血管疾病、神经疾病、癌症、糖尿病、炎症等[3-4]。目前,对茄萼花色苷合成的分子调控机理知之甚少。因此,深入开展茄萼花色苷合成关键基因的研究有助于揭示茄萼与果皮花色苷合成分子调控机理的异同,为茄品质育种提供理论依据。【前人研究进展】植物花瓣、组织和果实等颜色主要由植物次生代谢产物花色苷决定,属于类黄酮物质。花色苷需要一系列酶经过3个阶段合成,目前已对如矮牵牛[5]()、玉米[6]()及金鱼草[7]()等花色苷生物合成途径有了较深入的研究。二氢黄酮醇4-还原酶(dihydroflavonol-4-reductase,DFR)是花色苷多酶合成途径中最终形成色素的关键酶,在花色苷生物合成途径的下游发挥重要作用,属于NADPH(nicotinamide adenine dinucleotide phosphate)依赖的短链还原酶家族[8],能够催化二氢黄酮醇类物质,如二氢堪非醇(dihydrokaempferol,DHK)、二氢榭皮素(dihydroquercetin,DHQ)和二氢杨梅素(dihydromyricetin,DHM),在C4位发生立体特异的还原反应,分别生成无色花葵素、无色花青素和无色翠雀素[9]。不同物种的DFR具有较高同源性,存在保守的NADPH结合域和底物特异性结合域,对底物的特异性结合通常是由第134位氨基酸残基决定[8]。在高等植物中,多数花色苷生物合成往往受诸多转录因子在不同时空上的组合调控。如R2R3-MYB转录因子、bHLH转录因子和WD40蛋白等,三者形成转录复合体MYB-bHLH-WD40(MBW)而发挥转录调控作用[10-11]。作为一种关键的转录因子,R2R3-MYB的上调能够激活参与花色苷合成的某个或多个结构基因的表达,从而使植物组织积累花色苷。该基因已从箭叶淫羊藿()[12]、梨()[13]和甜樱桃(L.)[14]等物种中克隆,并对其功能进行了解析。苹果中调控花色苷合成途径中所有结构基因的协同表达[15];‘红阳’猕猴桃中促进花色苷积累[16];过表达番茄编码MYB的,上调、、和转录水平[17]。【本研究切入点】茄从果萼和果皮颜色上划分,一般有紫色萼紫色果皮、绿色萼紫色果皮和绿色萼白色果皮3种,关于茄果皮花色苷合成分子机制已有较深入研究[18-19]。但是,有关紫萼花色苷合成的分子机制还不清楚。【拟解决的关键问题】以绿萼和紫萼长茄果萼为试验材料,通过RACE方法克隆和,并对其编码的产物进行生物信息学分析,同时运用实时荧光定量PCR技术,分析和在果萼生长过程中的表达模式,为深入阐释茄子果萼中花色苷生物合成的分子机理提供理论基础。
1 材料与方法
试验于2014—2016年在东北林业大学生命科学学院进行。
1.1 试验材料
以采摘自黑龙江省农业科学研究院园艺分院的绿萼和紫萼长茄果萼为试验材料,于2014年6月将上述两种茄子分别分成初蕾期、盛蕾期、初花期和盛花期4个时期进行取材(图1),液氮冰冻,保存于-80℃冰箱。
1.2 茄萼花色苷含量测定
参考WrolstanD等[20]的方法,采用不同pH条件下分光光度计方法测定茄萼花色苷含量。利用公式TA=A×MW×5×100×V/Ɛ;A=[A510nm(pH 1.0)-A700nm(pH 1.0)]-[A510nm(pH 4.5)-A700nm(pH 4.5)]计算花色苷的含量,其中花色苷总含量由TA表示,V代表混合液的体积(mL),摩尔吸收率26900由Ɛ表示,标准分子质量449.2由MW表示,花色苷的总含量单位为mg/100 g。
1.3 RNA提取及基因全长克隆
采用TRIzol Plant(全式金公司,北京)试剂盒提取总RNA,利用P19E(表1)和反转录试剂盒(全式金公司,北京)反转录得到cDNA,以此为模板,进行特异性扩增。

表1 绿萼和紫萼长茄果萼DFR和MYB基因克隆引物
利用cDNA末端快速扩增(rapid amplification of cDNA ends,RACE)法克隆3′-cDNA序列,登陆NCBI(http://www.ncbi.nlm.nih.gov/)参照已发表的马铃薯和番茄等基因序列设计PCR上游引物3′RACE(表1),同时找到茄科植物与花色苷合成相关基因序列信息,根据番茄、矮牵牛、马铃薯、烟草和辣椒序列,在基因DNA结合域保守区设计PCR上游引物3′RACE(表1),上述引物设计均使用Primer Premier5.0,下游引物为P18E(表1)。PCR反应体系为20 μL:10×TransTaq HiFi BufferⅡ2 μL,dNTP Mixture 2 μL(2.5 mmol·L-1),模板cDNA 1 μL,上、下游引物各0.4 μL(20 μmol L-1),TransTaq HiFi DNA聚合酶0.2 μL(5 U μL-1),其余用蒸馏水补充。反应程序:95℃预变性5 min;30个循环(94℃变性30 s,56℃()、55℃()退火30 s,72℃延伸1 min);最后72℃延伸7 min。目的条带经胶回收纯化后,连接到pEASY-T5载体(全式金,北京)上,送至北京六合华大基因科技股份有限公司测序。
根据所得的3′-cDNA序列,设计5′RACE特异性引物ou-5'RACE GSP1、ou-5'RACE GSP2、dong-5′RACE GSP1、dong-5′RACE GSP2和-5′RACE GSP1、-5′RACE GSP2、dong-5′RACE GSP2、dong- 5′RACE GSP2(表1),用于巢式PCR。利用5′RACE GSP1和锚定引物Anchor(表1)以加dA尾的cDNA为模板进行5′-RACE扩增。为保证克隆片段的特异性,再用引物5′RACE GSP2和接头引物Adaptor(表1)进行第二次5′-RACE扩增,克隆5′-cDNA序列,PCR反应体系、产物的回收纯化、克隆、测序同3′-RACE。
1.4 绿萼和紫萼长茄果萼、生物信息学分析
用ORF Finder在线工具(http://www.ncbi.nlm.nih. gov/gorf/gorf. html)查找基因开放阅读框(ORF)并推导其氨基酸序列;利用BLAST(http://blast.ncbi. nlm.nih.gov/Blast.cgi)对克隆的目的序列进行同源分析;利用DNAMAN软件进行氨基酸的多序列比对,采用MEGA6.0软件中的邻接法(Neighbor-joining,NJ)构建系统发育树;使用ExPASy网站提供的在线分析软件SOPMA预测蛋白质二级结构。
1.5 绿萼和紫萼长茄果萼、实时荧光定量分析
分别提取绿萼长茄和紫萼长茄果萼4个时期的总RNA,用PrimeScript®RT reagent Kit Perfect Real Time(宝生物,大连)试剂盒反转录合成cDNA备用。用7500 fast型实时荧光定量PCR仪和Power SYBR®Green PCR Master Mix试剂盒以上述cDNA为模板进行实时荧光定量PCR分析,所用引物如表1。20 μL反应体系:8.4 μL稀释的cDNA模板(10 μg cDNA加200 μL水稀释),上、下游引物各0.8 μL(10 μmol L-1),Power SYBR®Green PCR Master Mix(2×)10 μL。反应程序如下:95℃预变性2 min;40个循环(95℃ 10 s,60℃ 45 s)。以表达水平为内参,引物为-F:CACTTAGCACCTTCCAGCAGATGT和-R:CTACAACAGCAGACCTGAGTTCACT。每个样品设3个生物学重复,采用2–ΔΔCT法分析目的基因表达水平。

表2 绿萼和紫萼长茄萼片DFR和MYB基因表达分析引物
2 结果
2.1 果萼中花色苷含量分析
绿萼和紫萼长茄果萼的4个生长时期见图1,花色苷含量的测定结果见图2。结果表明,绿萼长茄果萼花色苷含量基本保持不变;而紫萼长茄随生长时期的推移而呈现花色苷含量增加的趋势,该变化趋势与茄萼颜色逐渐加深成正相关趋势,且在盛花期,花色苷积累更为明显,并且在该时期紫萼长茄果萼花色苷含量约是绿萼长茄的5倍。

图1 不同发育阶段的绿萼和紫萼长茄果萼

图2 绿萼和紫萼长茄果萼花色苷含量变化
2.2和的全长cDNA克隆及序列分析
克隆得到绿萼和紫萼长茄果萼(GenBank登录号为KX224250)和(GenBank登录号为KX224251)的cDNA全长序列。全长1 285 bp,开放阅读框长858 bp,编码285个氨基酸;全长1 249 bp,开放阅读框长864 bp,编码287个氨基酸。SOPMA预测的DFR蛋白二级结构预测结果(图3-A、B)表明,和编码的285和287个氨基酸残基中,α螺旋分别占31.23%和32.06%、β转角分别占11.93%和11.15%、无规则卷曲分别占35.79%和36.59%、延伸链分别占21.05%和20.21%。ouSmDFR和dongSmDFR氨基酸序列比对(图4)发现,与dongSmDFR氨基酸序列相比,ouSmDFR在C末端缺少两个氨基酸,并且在第229位氨基酸位点存在差异,但由于这些差异位点不在功能域内,因而推测不会影响二氢黄酮醇4-还原酶的功能。

a:α螺旋;b:延伸链;c:β转角;d:无规则卷曲
多重氨基酸序列比对结果(图4)表明,和基因编码的氨基酸序列一致性高达98%,此外还发现ouSmDFR和dongSmDFR蛋白是NADPH依赖型的还原酶,属于NADB-Rossmann超基因家族(NADB-Rossmann superfamily),该基因家族具有两个高度保守结构域,分别为NADPH结合结构域和底物特异性结合结构域,能将黄烷酮醇还原为无色花色素。
利用Mega6.0通过邻位相连法(Neighbor-joining,NJ)构建系统发育树(图5)。结果表明,绿萼和紫萼长茄果萼DFR蛋白与其他的茄科作物,如矮牵牛(×)、马铃薯()和烟草()亲缘关系较近,且与StDFR序列相似性达73%左右,其次是与旋花科和龙胆科植物。绿萼长茄和紫萼与StDFR和GtDFR等DFR蛋白聚为一枝。
2.3和的全长cDNA克隆及序列分析
绿萼长茄(GenBank登录号为KX224253)和紫萼长茄(GenBank 登录号为KX224254)基因cDNA全长分别为969 bp和959 bp,开放阅读框长均为462 bp,编码153个氨基酸。SOPMA预测的蛋白二级结构预测(图6-A、B)表明,和编码的153个氨基酸残基中,α螺旋均占39.22%、β转角均占9.80%、无规则卷曲均占41.83%、延伸链均占9.15%,形成螺旋-螺旋-转角-螺旋结构。

方框处分别表示NADPH结合位点和底物特异性结合位点
多重氨基酸序列比对结果(图7)表明,和基因所编码的氨基酸序列具有两个不完全重复的DNA结合结构域,分别为R2结构域和R3结构域,属于典型的R2R3-MYB转录因子。由于MYB转录因子往往与bHLH蛋白形成复合物发挥作用,因此在R3结构域内还存在一个bHLH结合结构域。
依据与DFR蛋白相同的方法构建MYB转录因子系统发育树(图8),结果表明,绿萼长茄和紫萼长茄与箭叶淫羊藿()进化关系最近,与葡萄()、草莓(x)、玉米()和马铃薯()等亲缘关系也相对较近,与拟南芥进化关系相对较远。此外,ouSmMYB和dongSmMYB与AtMYB1和MdMYB10a等11个MYB蛋白聚为一枝,而AtPAP1和AtPAP2这两个蛋白聚为另一枝。
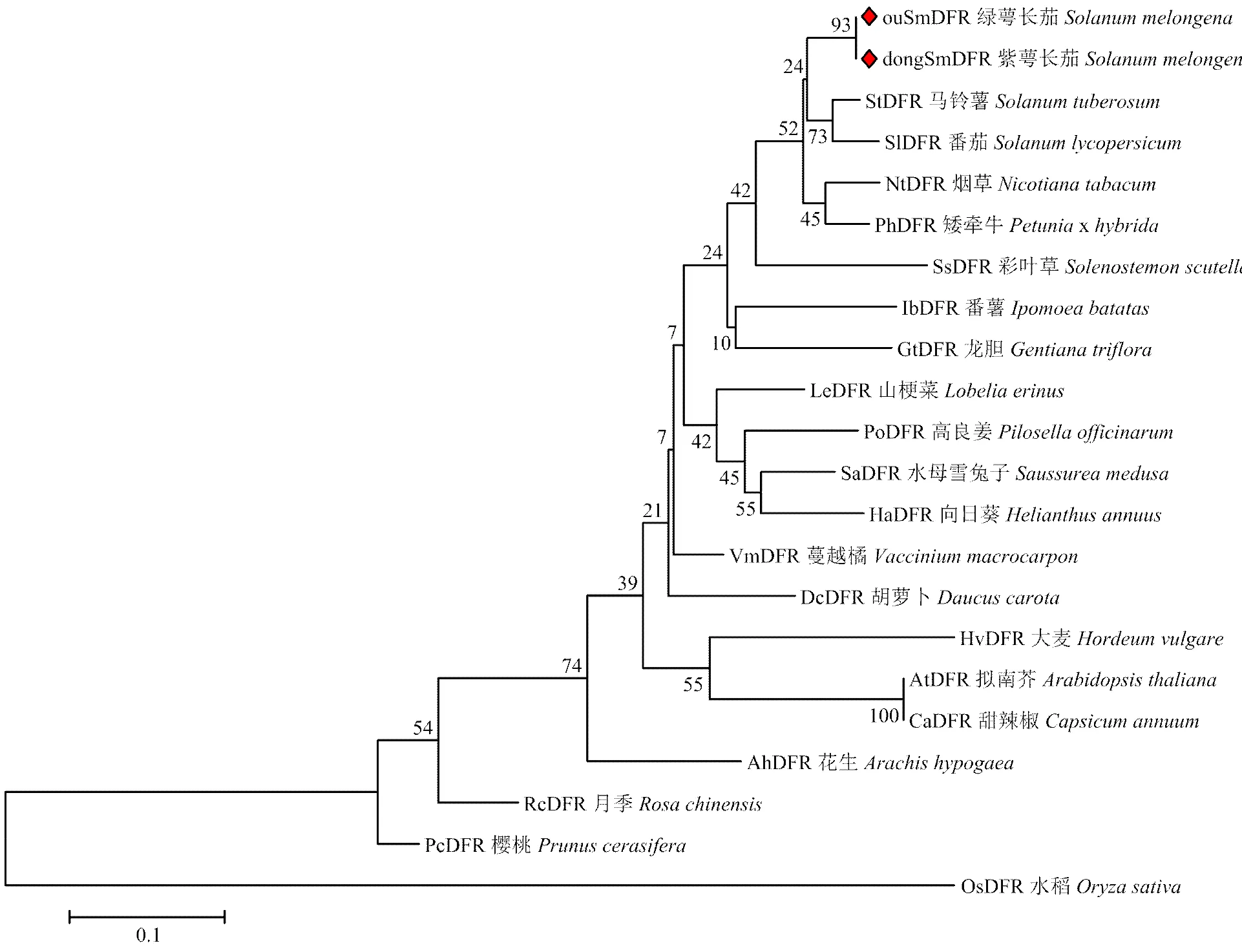
基因登录号分别是:AtDFR,NP_199094.1;StDFR,AAQ54578.1;NtDFR,ABN80437.1;PhDFR,AAF60298.1;SsDFR,ABP57077;IbDFR,BAA34637.1;GtDFR,BAA12736;LeDFR,BAF49318;PoDFR,ABF21084.1;SaDFR,ABQ97018;HaDFR,ABU93477;VmDFR,AF483835;DcDFR,AAD56578;HvDFR,AAB20555.1;CaDFR,NP_001311706.1;AhDFR,AID59206.1;RcDFR,BAH24302;PcDFR,AKV89243.1;OsDFR,AAD24584.3;SlDFR,NP_001234408.1;系统发育树树枝上面或下面的数字代表自举值

a:α螺旋;b:延伸链;c:β转角;d:不规则卷曲

直线方框处分别表示R2和R3保守结构域,虚线方框处表示bHLH结合结构域

基因登录号分别是:VvMYBA1,BAD18977.1;VvMYBA2,BAD18978.1;VvMYBA3,BAD18979.1;VvMYBPA1,CAJ90831.1;MdMYB10a,ABB84753.1;AtMYB1,AAG42001.1;AtPAP1,EFH52994.1;AtPAP2.,EFH66345.1;StMYB113,ALA13583.1;SlMYB1,AAQ55181.1;ZmMYBPL,AAA33482.1;FaMYB1,AAK84064.1;EsMYB1,AFH03053.1。系统发育树树枝上面或下面的数字代表自举值
2.4和基因的表达分析
实时荧光定量结果(图9)表明,在绿萼长茄果萼中表达量最低,并且随着生长,该基因的相对表达量几乎无变化;而在紫萼长茄果萼中,从初蕾期到盛花期,相对表达量不断增加,尤其是由初花期到盛花期生长时,增幅最为明显,并且在盛花期高峰度表达,远远高于其在绿萼长茄果萼中的表达,相对表达量约是绿萼长茄的10倍。
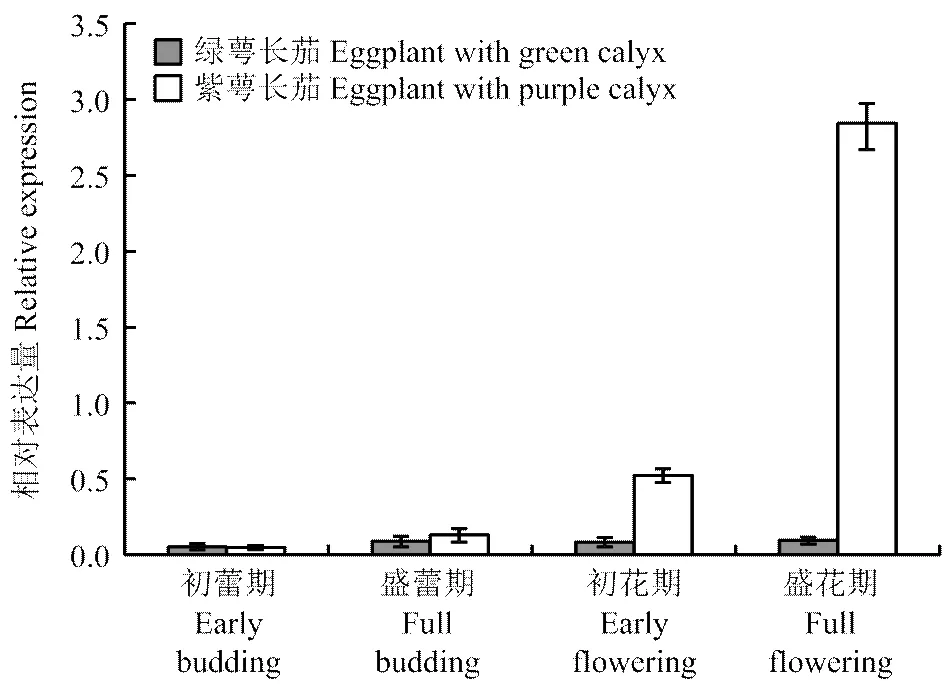
图9 ouSmDFR、dongSmDFR相对表达量
实时荧光定量结果(图10)表明,在绿萼长茄果萼前三个时期表达量几乎无变化,在第4个时期即盛花期出现小幅增加,但整体表达水平仍然较低;紫萼长茄,随着生长,果萼中相对表达量均呈上升趋势,并且从初花期到盛花期生长时,表达陡然增加,盛花期高峰度表达。此外,不论在哪个生长时期,在果萼中表达量均为紫萼长茄高于绿萼长茄,盛花期最为明显,盛花期在紫萼长茄果萼中相对表达量大约是绿萼长茄的8倍。

图10 ouSmMYB、dongSmMYB相对表达量
3 讨论
本研究克隆绿萼长茄果萼和和紫萼长茄果萼和,对和编码氨基酸序列与其他植物DFR进行多重序列比对发现均具有NADPH的结合位点和底物特异性结合位点,且高度保守,属于NADB超基因家族[17]。前人研究发现不同物种中DFR与底物结合区氨基酸序列的改变决定其底物的种类[22-23]。研究者在棉花()[24]、玫瑰()[25]和葡萄风信子()[26]等物种中克隆到同样具有上述两种结构域。进化分析表明,ouSmDFR和dongSmDFR与StDFR()和SlDFR()具有相对较高的同源性。
MYB蛋白序列分析和进化分析表明ouSmMYB和dongSmMYB转录因子与其他植物中花色苷途径相关的MYB蛋白的氨基酸序列具有较高的同源性,在其N端具有2个DNA结合域,分别为R2结合域和R3结合域,属于典型R2R3型MYB转录因子,还存在一个bHLH结合结构域[27-28],为形成MBW复合物提供bHLH转录因子结合位点[29-30]。其结构特征与月季()[31]和大豆()[32]等其他植物的具有相同性。生物信息学分析结果表明,和与()具有相对较高的同源性,推测在花色苷生物合成过程中具有相同的功能,还需通过生物工程试验深入鉴定和的生物学功能。
和表达的实时荧光定量PCR结果表明,4个时期中和在两种茄子的果萼中都有表达,且紫萼长茄高于绿萼长茄。相对表达量与呈正相关的关系,由于MYB转录因子往往是通过调控结构基因表达而影响花色苷合成,所以笔者推测MYB可能与存在相互作用,上调紫萼长茄果萼中表达,使其果萼呈现紫色。但是盛花期出现小幅增加,推测可能该基因可能还参与其他物质的合成途径。此外,参与花色苷生物合成途径的基因分前期基因和后期基因,前期基因包括PAL(苯丙氨酸裂解酶)、CHI(查尔酮异构酶)、CHS(查耳酮合酶)和F3H(黄烷酮3-羟化酶)等相关基因,后期基因除了DFR还包括ANS /LDOX(花色苷合成酶/无色花色苷双加氧酶)和UFGT(类黄酮3-O-糖基转移酶)等相关基因,两种茄子果萼颜色差异是否仅仅源于MYB转录因子对表达的调控仍需要进一步研究。‘马克斯’红洋梨的出现时因为PyMYB10正调控的表达[33];苹果MdMYB3参与调控苹果花色苷合成[34];葡萄浆果中VvMYBPA1调控表达,VvMYBA2促进表达,进而影响葡萄花色苷积累[35-36];芜菁(L.)中发现能够促进花色苷积累[37]。所以后续将克隆参与绿萼长茄和紫萼长茄果萼花色苷合成途径中所有结构基因,并对其表达进行分析,选取与表达趋势一致的结构基因进行酵母单杂交试验,确定MYB转录因子通过调控哪个或是哪几个结构基因来影响果萼中花色苷积累,为阐释绿萼长茄和紫萼长茄果萼颜色差异的分子机理奠定基础。
研究发现,茄果皮花色苷的合成除受转录因子调控外,一定程度上还受光信号的影响,‘蓝山’茄果皮为紫色,而套袋处理后其果皮呈白色,但是,果萼颜色仍为紫色[19],推测存在不同的调控机制分别调控茄果萼和果皮花色苷的生物合成,通过比较二者机制异同,完全理解花色苷合成和调节的因子以及相关酶类相互作用,为提高茄中花色苷含量、选育优质茄品种提供理论基础。
4 结论
成功克隆绿萼和紫萼长茄果萼R和的cDNA序列,其中和编码的氨基酸序列属于NADB超基因家族,而ouSmMYB和dongSmMYB则具有R2R3型MYB转录因子的典型特征,其N端具有R2、R3两个MYB结构域,C端高度特异。进化分析表明,ouSmDFR和dongSmDFR与马铃薯的DFR同源性较高;ouSmMYB和dongSmMYB与箭叶淫羊藿的MYB同源性较高。R和的表达分析推测其可能在绿萼和紫萼长茄果萼颜色差异形成中发挥作用。
References
[1] Hirakawa H, Shirasawa K, Miyatake K, Nunome T, Negoro S, Ohyama A, Yamaguchi H, Sato S, Isobe S, Tabata S, Fukuoka H. Draft genome sequence of eggplant (L.): the representative solanum species indigenous to the old world., 2014, 21(6): 649-660.
[2] Wu X, Beecher G R, Holden J M, Haytowitz D B, Gebhardt S E, Prior R L. Concentrations of anthocyanins in common foods in the United States and estimation of normal consumption., 2006, 54(11): 4069-4075.
[3] MARSZALEK K, WOZNIAK Ł, KRUSZEWSKI B, SKAPAKA S. The effect of high pressure techniques on the stability of anthocyanins in fruit and vegetables., 2017, 18(2): 277.
[4] YOUSUF B, GUL K, WANI A A, SINGH P. Health benefits of anthocyanins and their encapsulation for potential use in food systems: A review., 2016, 56(13): 2223-2230.
[5] SCHWINN K E, BOASE M R, BRADLEY J M, LEWIS D H, DEROLES S C, MARTIN C R, DAVIES K M. MYB and bHLH transcription factor transgenes increase anthocyanin pigmentation in petunia and lisianthus plants, and the petunia phenotypes are strongly enhanced under field conditions., 2014, 5: 603.
[6] IBRAHEEM F, GAFFOOR I, TAN Q, SHYU C R, CHOPRA S. A sorghum MYB transcription factor induces 3-deoxyanthocyanidins and enhances resistance against leaf blights in maize., 2015, 20(2): 2388-2404.
[7] SCHWINN K, VENAIL J, SHANG Y, MACKAY S, ALM V, BUTELLI E, OYAMA R, BAILEY P, DAVIES K, MARTIN C. A small family of-regulatory genes controls floral pigmentation intensity and patterning in the genus., 2006, 18(4): 831-851.
[8] 赵启明, 李范, 李萍. 花青素生物合成关键酶的研究进展. 生物技术通报, 2012, 28(12): 25-32.
ZHAO Q M, LI F, LI P. Research advances on core enzymes of anthocyanidin biosynthesis., 2012, 28(12): 25-32. (in Chinese)
[9] 焦淑珍, 刘雅莉, 娄倩, 姜玲. 葡萄风信子二氢黄酮醇4-还原酶基因()的克隆与表达分析. 农业生物技术学报, 2014, 22(5): 529-540.
JIAO S Z, LIU Y L, LOU Q, JIANG L. Cloning and expression analysis of dihydroflavonol 4-reductase gene () from Grape hyacinth ()., 2014, 22(5): 529-540. (in Chinese)
[10] HICHRI I, BARRIEU F, BOGS J, KAPPEL C, DELROT S, LAUVERGEAT V. Recent advances in the transcriptional regulation of the flavonoid biosynthetic pathway., 2011, 62(8): 2465-2483.
[11] BROUN P. Transcriptional control of flavonoid biosynthesis: a complex network of conserved regulators involved in multiple aspects of differentiation in., 2005, 8(3): 272-279.
[12] HUANG W, SUN W, LV H, LUO M, ZENG S, PATTANAIK S, YUAN L, WANG Y. A R2R3-MYB transcription factor fromregulates the flavonoid biosynthetic pathway., 2013, 8(8): e70778.
[13] FENG S, WANG Y, YANG S, XU Y, CHEN X. Anthocyanin biosynthesis in pears is regulated by a R2R3-MYB transcription factor PyMYB10., 2010, 232(1): 245-255.
[14] STARKEVIC P, PAUKSTYTE J, KAZANAVICIUTE V, DENKOVSKIENĖ E, STANYS V, BENDOKAS V, ŠIKŠNIANAS T, RAŽANSKIENĖ A, RAŽANSKAS R. Expression and anthocyanin biosynthesis-modulating potential of Sweet cherry (L.)andgenes., 2015, 10(5): e0126991.
[15] ESPLEY R V, HELLENS R P, PUTTERILL J, STEVENSON D E, KUTTY-AMMA S, ALLAN A C. Red colouration in apple fruit is due to the activity of the MYB transcription factor, MdMYB10., 2007, 49(3): 414-427.
[16] 满玉萍, 李刚, 刘虹, 王彦昌, 覃瑞. ‘红阳’猕猴桃基因的克隆与表达. 华中农业大学学报, 2012, 31(6): 679-685.
MAN Y P, LI G, LIU H, WANG Y C, QIN R. Cloning and expression analysis ofin‘Hong yang’., 2012, 31(6): 679-685. (in Chinese)
[17] MATHEWS H, CLENDENNEN S K, CALDWELL C G, LIU X L, CONNORS K, MATHEIS N, SCHUSTER D K, MENASCO D J, WAGONER W, LIGHTNER J, WAGNER D R. Activation tagging in tomato identifies a transcriptional regulator of anthocyanin biosynthesis, modification, and transport., 2003, 15(8): 1689-1703.
[18] ZHANG Y, HU Z, CHU G, HUANG C, TIAN S, ZHAO Z, CHEN G. Anthocyanin accumulation and molecular analysis of anthocyanin biosynthesis-associated genes in eggplant (L)., 2014, 62(13): 2906-2912.
[19] JIANG M M, REN L, LIAN H L, LIU Y, CHEN H Y. Novel insight into the mechanism underlying light-controlled anthocyanin accumulation in eggplant (L.)., 2016, 249: 46-58.
[20] Wrolstad R E, Culbertson J D, Cornwell C J, Mattick L R. Detection of adulteration in blackberry juice concentrates and wines, 1982, 65(6): 1417-1423.
[21] 朱奇朗, 李晓波, 肖向文, 李雪源, 黄先忠, 郑巨云, 艾先涛. 不同色彩矮牵牛基因的克隆与生物信息学分析. 生物技术通报, 2013, 29(9): 68-76.
ZHU Q L, LI X B, XIAO X W, LI X Y, HUANG X Z, ZHENG J Y, AI X T. Cloning and bioinformatical analysis of dihydroflavonol 4-reductase gene()fromwith different Color., 2013, 29(9): 68-76. (in Chinese)
[22] 周惠, 文锦芬, 邓明华,朱海山. 植物花青素生物合成相关基因研究进展. 辣椒杂志, 2011(4): 1-7.
ZHOU H,WEN J F,DENG M H, ZHU H S. Research progress in plant anthocyanidin biosynthesis genes., 2011(4): 1-7. (in Chinese)
[23] MIOSIC S, THILL J, MILOSEVIC M, GOSCH C, POBER S, MOLITOR C, EJAZ S, ROMPEL A, STICH K, HALBWIRTH H. Dihydroflavonol 4-reductase genes encode enzymes with contrasting substrate specificity and show divergent gene expression profiles inspecies., 2014, 9(11): e112707.
[24] WANG L, ZHU Y, WANG P, FAN Q, WU Y, PENG Q Z, XIA G X, WU J H. Functional characterization of a dihydroflavanol 4-reductase from the fiber of upland cotton ()., 2016, 21(2): 32.
[25] LUO P, NING G, WANG Z, SHEN Y, JIN H, LI P, HUANG S, ZHAO J, BAO M. Disequilibrium of flavonol synthase and dihydroflavonol- 4-reductase expression associated tightly to white vs. red color flower formation in plants., 2015, 6: 1257.
[26] 焦淑珍. 葡萄风信子基因克隆及表达分析[D]. 杨凌: 西北农林科技大学, 2014.
JIAO S Z. Cloning and expression analysis ofgenes from grape hyacinths [D]. Yangling: Northwest Agriculture and Forestry University, 2014. (in Chinese)
[27] GROTEWOLD E,SAINZ M B,TAGLIANI L,HERNANDEZ J M,BOWEN B,CHANDLER V L. Identification of the residues in theof maize C1 that specify the interaction with the bHLH cofactor R., 2000, 97: 13579-13584.
[28] STRACKE R, WERBER M, WEISSHAAR B. The R2R3-MYB gene family in., 2001, 4(5): 447-456
[29] Albert N W, Griffiths A G, Cousins G R, Verry I M, Williams W M. Anthocyanin leaf markings are regulated by a family ofgenes in the genus Trifolium., 2015, 205(2): 882-893.
[30] FELLER A, MACHEMER K, BRAUN E L, GROTEWOLD E. Evolutionary and comparative analysis of MYB and bHLH plant transcription factors., 2011, 66(1): 94-116.
[31] 赵佳, 刘荣, 杨帆, 李鑫, 刘厚生, 严倩, 肖月华. 月季花青素苷相关R2R3-MYB蛋白基因的克隆和表达分析. 中国农业科学, 2015, 48(7): 1392-1404.
ZHAO J, LIU R, YANG F, LI XIN, LIU H S, YAN Q, XIAO Y H. Cloning and expression analyses of R2R3-MYB genes related to anthocyanin biosynthesis in rose., 2015, 48(7): 1392-1404. (in Chinese)
[32] 许玲, 卫培培, 张大勇, 徐照龙, 何晓兰, 黄益洪, 马鸿翔, 邵宏波. 大豆转录因子基因的克隆及功能分析. 中国农业科学, 2015, 48(15): 3079-3089.
XU L, WEI P P, ZHANG D Y, XU Z L, HE X L, HUANG Y H,MA H X, SHAO H B. Expression and function analysis of the transcription factor, 2015, 48(15): 3079-3089. (in Chinese)
[33] WANG Z, MENG D, WANG A, LI T, JIANG S, CONG P, LI T. The methylation of thepromoter is associated with green- skinned sport in Max Red Bartlett pear., 2013, 162(2): 885-896.
[34] VIMOLMANGKANG S, HAN Y, WEI G, KORBAN S S. An apple MYB transcription factor, MdMYB3, is involved in regulation of anthocyanin biosynthesis and flower development., 2013, 13: 176-189.
[35] BOGS J, JAFFE F W, TAKOS A M, WALKER A R, ROBINSON S P. The grapevine transcription factor VvMYBPA1 regulates proanthocyanidin synthesis during fruit development., 2007, 143(3): 1347-1361.
[36] TERRIER N, TORREGROSA L, AGEORGES A, VIALET S, VERRIÈS C, CHEYNIER V, ROMIEU C. Ectopic expression ofpromotes proanthocyanidin biosynthesis in grapevine and suggests additional targets in the pathway., 2009, 149(2): 1028-1041.
[37] LIM S H, SONG J H, KIM D H, KIM J K, LEE J Y, KIM Y M, HA S H. Activation of anthocyanin biosynthesis by expression of the radish R2R3-MYB transcription factor gene., 2016, 35(3): 641-653.
(责任编辑 赵伶俐)
Cloning and Expression Analysis of Anthocyanin Biosynthesis-associatedandGenes in Calyx of Eggplant (L.)
Wang HaiZhu1, Qu HongYun2, Zhou TingTing1, Xu QiJiang1
(1College of Life Science, Northeast Forestry University/State Key Laboratory of Tree Genetics and Breeding, Northeast Forestry University, Harbin 150040;2Horticultural Branch, Heilongjiang Academy of Agricultural Sciences, Harbin 150040)
【Objective】Anthocyanins are the water-soluble secondary metabolites synthesized via the flavonoid pathway responsible for red, violet, and blue indifferent kinds of plant organs. These pigments are of benefit to human health. Eggplant is rich in anthocyanins. The molecular mechanism of anthocyanin biosynthesis in eggplant calyx is still unclear. The primary objectives of this experiment are to cloneandgenes in the eggplant, detect their expression at different developmental stages and in calyx with different colors, explore the role ofandin anthocyanin synthesis in calyx of eggplant. This work expanded our knowledge about the molecular mechanism of anthocyanin biosynthesis in eggplant peel and calyx. 【Method】Green calyx and purple calyx of eggplants were used as materials. The content of anthocyanins in the calyx was measured by spectrophotometry at different pH. cDNA sequence of theandwere isolated and cloned by using RACE techniques.Analyze theconserved domains and characteristics of DFR protein were analyzed. Phylogenetic analysis of homologous protein sequences of other plants and DFR was conducted, the phylogenetic tree was constructed to further analyze and identify genes. To predict its secondary structure, SPOMA was used on-line which provided by the ExPAsy website. The bioinformatics analysis of MYB was the same as DFR. Expression ofandgenes in calyx with different colors were investigated through quantitative real-time PCR.【Result】In this study, two full-length cDNA sequences ofwere successfully cloned and denoted asand(GenBank accession Nos KX224250 and KX224251).is 1 285 bp in cDNA length with an open reading frame of 858 bp corresponding to 285 amino acid residues.is 1 249 bp in cDNA length with an open reading frame of 864 bp, which encoding 287 amino acids. Two full-length cDNA sequences ofgene were cloned and denoted asand(GenBank accession Nos KX224253 and KX224254). The corresponding cDNAs are 969 bp and 959 bp in length and the deduced proteins contained 153 amino acids, respectively. Results of secondary structure analysis exhibited that α-Helix and random coil were primary secondary structural components of the two DFR genes and two MYB genes. Sequence analysis showed that ouSmDFR and dongSmDFR have a NADPH-binding domain and substrate specific binding domain. ouSmMYB and dongSmMYB belonged to the R2R3-MYB transcription factors, which have R2 and R3 conserved domains and a bHLH binding domain. Phylogenetic tree analysis indicated thatandhave a close relation withand,andhave the closest genetic relationship with. Results of total anthocyanins measurement showed that high contents of anthocyanins were detected in purple calyx and increased gradually, while no anthocyanins were detected in green calyx. The qRT-PCR analysis indicated that the expression ofandgenes in the purple calyx were much higher than that in the green calyx. Moreover, from early budding to full flowering,the expression ofandincreased gradually. However,andalmost had no change, which were consistented with the color variation of calyx.【Conclusion】andbelong to the NADB-Rossmann superfamily,andare typical R2R3-MYB transcription factors. The expression ofandin the purple calyx is significantly higher than that in the green calyx. Therefore, it is speculated that the DFR and MYB genes play a role in the color of eggplants’ calyx. Furthermore, DFR and MYB are involved in the process of anthocyanin biosynthesis.
calyx; anthocyanins;;; gene expression;L.
2017-01-09;接受日期:2017-03-21
国家基础科学人才培养基金(J1210053)、中央高校基本科研业务费专项资金(DL12CA10,2572014EA03)、林木遗传育种国家重点实验室创新项目(2013A06,2013B010)、黑龙江省博士后科研启动金(LBH-Q14011)
王海竹,E-mail:18686870296@163.com。通信作者徐启江,E-mail:qijiangxu@126.com
