B4C还原法制备ZrB2及其高温导电性研究
2017-07-24陈志科梁迪飞邓龙江孙东慧
陈志科,梁迪飞,邓龙江,孙东慧
(电子科技大学 微电子与固体电子学院 国家电磁辐射控制材料工程技术研究中心,四川 成都 610000)
B4C还原法制备ZrB2及其高温导电性研究
陈志科,梁迪飞,邓龙江,孙东慧
(电子科技大学 微电子与固体电子学院 国家电磁辐射控制材料工程技术研究中心,四川 成都 610000)
简要对比了几种制备ZrB2的碳/硼热还原法,其中B4C还原法原料简单、成本低廉、产物杂质易除,更容易制备高纯ZrB2。在B4C还原法的基础上研究了不同反应摩尔比和不同合成温度对产物ZrB2纯度的影响。研究表明,当B4C与ZrO2反应摩尔比为0.77、合成温度为1700 ℃时,可获得几乎无ZrO2和B2O3杂质的高纯ZrB2。最后,研究了不同反应摩尔比对ZrB2的高温电导率的影响,结果表明,随ZrB2纯度的增高,其电导率总体呈增大的趋势。
ZrB2的合成;B4C还原法;高温电导率;无压烧结;高温隐身材料;超音速
ZrB2和 HfB2一直都是航空航天领域的研究热点,它们是当今最具潜力的超高温陶瓷材料,但ZrB2又因密度更小、成本更低,从而更具吸引力和研究价值[1]。ZrB2具有熔点高(3245 ℃)、电导率高(16.6×10-5Ω·cm)、硬度高(88~91 HRA)、热导率高(20 ℃时24.3 W/(m·K))、化学稳定性好和密度小(6.085 g/cm3)等诸多优秀特性[2],在高温结构陶瓷、耐火材料、复合材料、薄膜材料和电极材料等方面应用广泛。由于ZrB2具有优秀的导电性能,近年来人们又开始尝试将其制作成超材料的形式应用在高温隐身材料领域,如超音速飞行器的隐身。
一百多年前人们便开始采用单质 Zr和 B合成ZrB2[3],经过长时间的研究,现在 ZrB2的合成方法早已相对成熟,主要分为固相法(直接合成法、碳/硼热还原法和自蔓延高温合成法等)、液相法(溶胶-凝胶法、水热法和沉淀法等)、气相法(CVD法及其类似的衍生方法)。其中,唯有碳/硼热还原法适合大规模工业化生产ZrB2粉体,常见的一些碳/硼热还原法如下[1,3,4-9]:

方法(2)、(3)都难以得到纯度较高的ZrB2,因为高温时B2O3(其中方法(2)包含方法(1)和(3)两步,B2O3为其中间产物。)属于易挥发物质,它们不易反应彻底,产物中可能残留大量难以除去的ZrO2杂质,同时,C也是一种难以除杂的物质。另外,这两个反应的合成温度也非常高(1425 ℃和1509 ℃),所以,这两种方法的缺点较为明显。方法(5)中的ZrO2、BN和C全都是难以除杂的物质,对ZrB2纯度的影响很大[10]。对于方法(4),不仅杂质硼难以除去,而且它与产物B2O3容易反应生成一系列易挥发的富硼氧化物,使得反应物B的加入量难以控制,生成的ZrB2的质量无法得到保证,同时,单质B的成本也较高,这都不利于其推广应用。只有方法(1)不仅反应物成本低廉,而且可以通过控制B4C的加入量来彻底除去 ZrO2杂质,同时在一定的范围内,B4C还不会因为过量而影响 ZrB2的纯度,因为高温低压时,它可以与 B2O3反应转变成一系列富硼氧化物(B2O2、BO等)而挥发[11-12]:

即使反应中存在少量过量的 B4C,不但很少影响ZrB2的高温性能,还通常具有增强作用。
基于 B4C还原法更容易制备高纯度 ZrB2的优点,本文将系统地研究不同反应物比例以及不同合成温度对ZrB2纯度的影响。自ZrB2这种超高温陶瓷进入高温材料领域以来,人们对它的高温力学性能和抗氧化性能的研究、开发及其应用已经相对系统、广泛且成熟,但是对于它的高电导率,不论是理论上还是实验上都鲜有研究,因此,本文还将浅谈其导电机制和在B4C还原法的基础之上研究不同反应摩尔比对其电导率的影响。
1 实验
1.1 实验原料及主要设备
实验中所用到的主要原料包括:ZrO2(纯度≥99.9%,粒径3~5 μm,广东东方锆业科技股份有限公司)、B4C(纯度≥97.97%,粒经3.5~5 μm,黑龙江省牡丹江市碳化硼厂)。所用到的主要设备包括:真空碳管烧结炉(ZT-40-20,上海晨华科技股份有限公司)、X射线衍射仪(XRD-7000,SHIMADZU CORPORATION)、扫描电子显微镜(JSM-7600f,JEOL)、薄膜变温电阻测试仪(TRT-3,武汉嘉仪通有限公司)。
1.2 实验过程
方法(1)的方程式配平时,其反应物 B4C与ZrO2的摩尔比为0.714。本实验分别按摩尔比0.714,0.73,0.75,0.76,0.77和0.78在行星球磨机中加入并混匀两种反应物,球磨时间2.5 h,转速250 r/min,料、球(ZrO2)、乙醇的质量比为 1:3:1,混匀后经80 ℃、12 h烘干。分别取少量等量上述各组分放入BN坩埚,压实后通过真空碳管烧结炉在1700 ℃进行合成,保温时间2 h,升温速率10 ℃/min,合成气氛为高纯氩气(纯度99.999%),合成的各产物在石英坩埚中破碎以作 XRD分析。另取摩尔比 0.77的组分分别在1200,1450,1700和1900 ℃合成ZrB2,保温时间都为2 h,得到的产品作SEM形貌分析和EDS元素分析。分别把按摩尔比0.714,0.73,0.75和0.77合成的ZrB2破碎成能通过80目(180 μm)滤筛的颗粒,球磨12 h,然后加入大量乙醇过滤除去B2O3,取滤纸上的产物80 ℃、12 h烘干,每种产物取2 g在液压机上压制成长条,之后在1900 ℃无压烧结,保温时间2 h,最后,测出它们的高温电阻率,测量范围0~1000 ℃,每隔50 ℃一个测量点。
2 结果与讨论
2.1 不同反应物摩尔比对ZrB2纯度的影响
图 1为 B4C与 ZrO2按不同摩尔比混料后在1700 ℃合成的ZrB2的XRD分析结果。由图可知,这几种反应物摩尔比下合成的 ZrB2的杂相峰都很少,当B4C与ZrO2摩尔比为0.714时,除了较低的ZrO2杂相峰以外就已经无其他杂相峰存在,而随着B4C与ZrO2摩尔比的增大,ZrO2的杂相峰也不断降低,据图1(b),当B4C与ZrO2摩尔比为0.76时已很难观察到杂相峰,0.77及以上则完全无法看到杂相峰,说明反应物中B4C与ZrO2的摩尔比大于0.77时,B4C可以将 ZrO2几乎完全耗尽,即产物 ZrB2中基本无ZrO2杂质。

图1 不同反应摩尔比下合成的ZrB2的XRD谱Fig.1 XRD patterns of ZrB2synthesized under different reaction molar ratios
2.2 不同合成温度对ZrB2纯度的影响
图2为B4C与 ZrO2摩尔比为 0.77时分别在1200,1450,1700和 1900 ℃合成的 ZrB2的 XRD谱。可以发现,随着温度的升高,ZrO2杂相的峰值也不断降低,说明温度越高反应(1)进行得越充分,越有利于除尽ZrO2杂质,当温度高于1700 ℃时,几乎无ZrO2杂相峰的存在,因此,当B4C与ZrO2摩尔比为0.77时,在此温度以上ZrO2杂质可以基本被完全除去。

图2 不同合成温度下制备的ZrB2的XRD谱Fig.2 XRD patterns of ZrB2prepared at different synthesis temperatures
图3与图4为B4C与ZrO2摩尔比为0.77时分别在1200,1450,1700和1900 ℃合成的ZrB2的SEM照片与EDS分析结果。可以观察到,随着温度的升高,ZrB2表面的深色黏性流体物质显著减少,最后消失,它的含氧量也明显逐渐降低。1200 ℃时,ZrB2表面几乎完全被呈黏着状的流体物质覆盖,含氧量较高,由B4C还原法的化学方程式可以确定,造成ZrB2含氧量高的物质只可能有两种:ZrO2和B2O3,根据图2中1200 ℃时的XRD分析可知,此时ZrO2的含量已经很低,不可能有其SEM照片中所观察到的那样多,而B2O3在450 ℃以上便会熔化成液态玻璃相物质,冷却后的形貌与图中的状态完全符合,因此,呈黏着状的流体物质为B2O3,不过,B2O3一般呈无定晶型,所以前面的XRD谱上观察不到其峰型。1450 ℃时,ZrB2表面的黏着状流体物质大量减少,含氧量也降低了一些。1700 ℃及其以上时,这些呈黏着状的流体物质几乎完全消失,含氧量也几乎为零,说明在此温度以上产物中的B2O3杂质可以基本完全挥发,这与B2O3的蒸气压密切相关,液相B2O3在1200 ℃时的蒸气压仅为0.5 Pa,而在1527 ℃时可以达到344 Pa[5,13-14],随温度的升高其蒸气压快速升高,故它的挥发速度随温度的升高急剧增大,到了1700 ℃以上时,较大的蒸气压完全足以使其挥发被除净。根据图5可知,0~1000 ℃之间,同一反应摩尔比下,随着温度的升高,ZrB2的电阻率线性增大,电导率与电阻率成反比关系,可知它的电导率随温度线性减小,与金属电导率的变化趋势一致。这是由ZrB2的晶体结构和成键性质所导致的,其晶体结构见图6[15]。

图3 不同合成温度下制备的ZrB2的SEM照片Fig.3 SEM photos of ZrB2prepared at different synthesis temperatures

图4 不同合成温度下制备的ZrB2的EDS谱Fig.4 EDS patterns of ZrB2prepared at different synthesis temperatures
另外,从图3中还可以得到,随着合成温度的升高,ZrO2的粒径快速增长,1200 ℃和 1450 ℃时其粒径都还很小,而温度高于1450 ℃时其粒径明显变大了很多,1450 ℃到 1700 ℃之间粒径增长十分快速,原因可能有两点:其一,温度越高材料中的原子扩散速度越快,晶界移动速度也就越快,从而加速 ZrB2粒径的长大;其二,这个温度范围内的B2O3已经全部液化,却又未来得及完全挥发,大量的液体环境起到加速传质的作用,同样可以促进ZrB2粒径的增大。
2.3 不同反应摩尔比对ZrB2电导率的影响
图5为不同反应摩尔比下制备ZrB2的电阻率。

图5 不同反应摩尔比下制备的ZrB2的电阻率Fig.5 Resistivities of ZrB2prepared by different reaction molar ratios

图6 ZrB2的结构示意图Fig.6 Structure diagram of ZrB2
ZrB2为AlB2型金属硼化物,它的每个金属原子都拥有1.33个自由电子,而密排六方晶体结构中的金属原子的排列又十分紧密,使得它具有金属一样强的导电性能,属于电子导电,其导电性满足以下公式:


式中:n指载流子数量;e指载流子电荷量;μ 指载流子迁移率;τ 指平均散射时间;me代表电子有效质量。
一般金属性导电材料的晶格震动会随温度的升高而增强,即材料的电阻由于增加了电子与声子之间的碰撞几率而升高,纯金属的电阻率通常满足布赫洛-格林艾森公式:
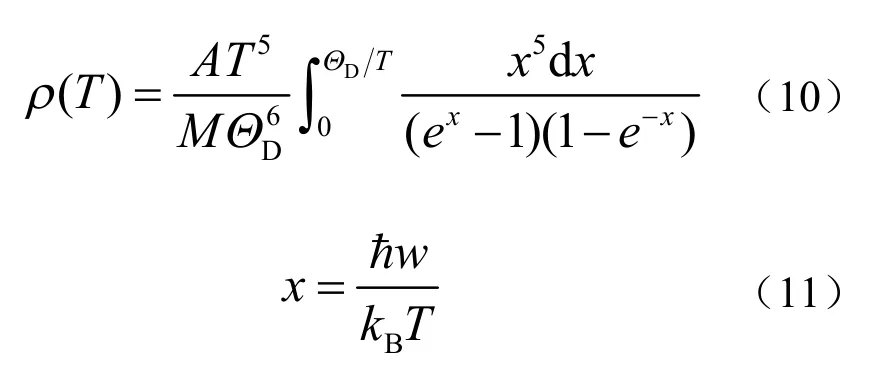
式中:M代表金属原子的质量;DΘ代表金属原子的德拜温度;A代表金属的特性常数。当体系处于高温时,,方程(10)可化为:

于是,ρ∝T。本文中研究的ZrB2用于制备高温导电涂层,适合制成高温隐身材料,故研究的温度范围是其高温区间,实验测得ZrB2的高温电阻率与温度成正比,这与金属的导电能力随温度的变化趋势一致,因此,采用金属导电理论可以预测其高温导电性能。
不过,ZrB2只是与金属单质的一些特征类似,其导电性能中还具有B环上离域大π键电子的贡献,因此,上式只适于理论上估算ZrB2的导电能力与温度的关系。根据ZrB2的晶体结构,其中的B原子形成了一种类似石墨结构的B六元环,每个B六元环构成的六中心六电子共轭大π键包含六个可以自由移动的电子,这些B环上的自由电子也极大地增强了ZrB2的导电性能。
布洛赫和布里渊为了解决金属的导电性问题,提出了能带理论,它是一种讨论晶体中电子的状态和运动的极其重要的理论,在阐明固体的导电机制、电子在晶格中的运动规律等方面取得了非常重大的成就,能带结构决定着固体的导电性。于是,还可以根据第一性原理计算来充分说明 ZrB2的导电机制,由电子结构计算软件VASP得到的ZrB2的能带结构、态密度和电荷密度分布分别如图7、图8和图9。

图7 ZrB2的能带结构分析Fig.7 Band structure of ZrB2

图8 ZrB2的态密度分析Fig.8 Density of states of ZrB2

图9 ZrB2的电荷密度分析Fig.9 Charge density of ZrB2
由ZrB2的能带结构可以发现,其价带顶与导带底之间没有能带间隙,价带顶穿越了费米能级,而对电导起作用的就是那些费米面上的电子,以上特征说明ZrB2具有金属一样的导电性,且高对称点Γ附近Zr-4d电子与B-2p电子的能量有相等的地方,由ZrB2的原子结构和晶体结构可知,其Zr-4d和B-2p自由电子可以对其导电性做出贡献,而能带图中这两种电子的能量具有相等的地方,说明在ZrB2中的这两种少数的电子还能在整个体系中自由移动,这对其导电性能也具有一定的促进作用,另外,在高对称点A处价带顶与导电底极其靠近,在一定条件下,如高温高压,价带中的电子完全可能获得能量进入空带转变成导带电子,从而进一步提高ZrB2的导电能力。根据ZrB2的态密度分析,其赝能隙处的态密度大于零,故ZrB2具有金属般的导电性,其分态密度分析还能进一步说明对导电做出贡献的是Zr-4d和B-2p电子,且Zr-4d电子的贡献更大,因为这两种电子的态密度在赝能隙处的分态密度都大于零,而 Zr-4d电子在此处的分态密度更大。ZrB2的电荷密度分析简明地呈现了其电荷的分布情况,蓝色Zr原子之间的电子区域存在相互重叠,淡黄色的环为B原子形成的六中心六电子大π键,这些大π键上的电子在B环的上下方是可以自由移动的,而Zr的电子区域与B原子大π键上的电子区域也有部分区域重合,这部分电子能够在整个ZrB2体系中自由移动,这都说明对 ZrB2的导电性做出贡献的有Zr-d电子和B-p电子。
另外,从图5中还可以发现,0~1000 ℃之间,同一温度(例如:1000 ℃)时,随反应物 B4C与ZrO2的摩尔比从0.714增大到0.77,ZrB2的高温电阻率先略微增大再剧烈减小,即ZrB2的高温电导率先略微减小再剧烈增大,且总体上随反应摩尔比呈增大的趋势,从前面 1700 ℃下的合成产物 ZrB2的XRD分析可知,反应摩尔比从0.714到0.77变化时,ZrO2杂质逐渐减少,B2O3杂质在此温度下也基本挥发完全,由此可知,随ZrB2纯度的增加,其电导率总体上呈增大的趋势。
3 结论
1700 ℃时,随反应物的摩尔比从0.714增大到0.77,产物ZrB2中的ZrO2杂质逐渐减少,摩尔比大于等于0.77时,反应物ZrO2几乎彻底被耗尽。当反应物的摩尔比为0.77,合成温度从1200 ℃逐渐升高到1900 ℃时,ZrO2杂质和B2O3杂质都逐渐减少,温度高于 1700 ℃时,ZrO2几乎被完全耗尽,B2O3基本彻底挥发而被除去。根据ZrB2的晶体结构分析和第一性原理计算可知,ZrB2具有金属一样的导电性,由实验结果得到,在0~1000 ℃范围内,其电导率随温度的增高呈线性增大的趋势,当反应物的摩尔比从0.714到0.77递增时,同一温度下,ZrB2的电导率先减后增,摩尔比为0.77时的电导率明显增大,即随ZrB2纯度的增加,其电导率先减后增,总体呈增大的趋势。
[1] GUO S Q. Densi fi cation of ZrB2-based composites and their mechanical and physical properties: a review [J]. J Eur Ceram Soc, 2009, 29(6): 995-1011.
[2] SONBER J K, SURI A K. Synthesis and consolidation of zirconium diboride: review [J]. Adv Appl Ceram, 2011,110(6): 321-334.
[3] FAHRENHOLTZ W G, HILMAS G E, TALMY I G, et al.Refractory diborides of zirconium and hafnium [J]. J Am Ceram Soc, 2007, 90: 1347-1364.
[4] ZHAO H, HE Y, JIN Z. Preparation of zirconium boride powder [J]. J Am Ceram Soc, 1995, 78(9): 2534-2536.
[5] GUO W M, ZHANG G J. Reaction processes and characterization of ZrB2powder prepared by boro/carbothermal reduction of ZrO2in vacuum [J]. J Am Ceram Soc, 2009, 92(1): 264-267.
[6] FAHRENHOLTZ W G, HILMAS G E, ZHANG S, et al.Pressureless sintering of zirconium diboride: particle size and additive effects [J]. J Am Ceram Soc, 2008, 91(5):1398-1404..
[7] GUO W M, TAN D W, ZHANG Z L, et al. Synthesis offine ZrB2powders by new borothermal reduction of coarse ZrO2powders [J]. Ceram Int, 2016, 42(13): 15087-15090.
[8] QIU H Y, GUO W M, ZOU J, et al. ZrB2powders prepared by boro/carbothermal reduction of ZrO2: the effects of carbon source and reaction atmosphere [J]. Powder Technol,2012, 217(2): 462-466.
[9] JUNG E Y, KIM J H, JUNG S H, et al. Synthesis of ZrB2powders by carbothermal and borothermal reduction [J].Cheminform, 2012, 538(42): 164-168.
[10] YAN C L, LIU R J, ZHANG C R, et al. Synthesis of ZrB2powders from ZrO2, BN, and C [J]. J Am Ceram Soc, 2016,99(1): 16-19.
[11] CAHN R W. Binary alloy phase diagrams [J]. Adv Mater,2010, 3(12): 628-629.
[12] LEE H, SPEYER R F. Pressureless sintering of boron carbide [J]. J Am Ceram Soc, 2003, 86(9): 1468-1473.
[13] RAN S, BIEST O V D, VLEUGELS J. ZrB2powders synthesis by borothermal reduction [J]. J Am Ceram Soc,2010, 93(6): 1586-1590.
[14] FAHRENHOLTZ W G. The ZrB2volatility diagram [J]. J Am Ceram Soc, 2005, 88(12): 3509-3512.
[15] LOA I, KUNC K, SYASSEN K. Crystal structure and lattice dynamics of AlB2under pressure and implications for MgB2[J]. Phys Rev, 2002(5): 1-8.
(编辑:陈丰)
Preparation of ZrB2by reduction of B4C and its high temperature conductivity
CHEN Zhike, LIANG Difei, DENG Longjiang, SUN Donghui
(National Engineering Research Center of Electromagnetic Radiation Control Materials, College of Microelectronics and Solid State Electronics, University of Electronic Science and Technology of China, Chengdu 610000, China)
Several carbon/boron thermal reduction methods for the preparation of ZrB2were briefly compared, in which, the B4C reduction method was simple, low cost, and easy to remove impurities. It can be easier to prepare pure ZrB2. The effects of different reaction molar ratios and different synthesis temperatures on the purity of ZrB2were studied based on the B4C reduction method. The results indicate that, when the reaction molar ratio of B4C to ZrO2is 0.77 and the synthesis temperature is 1700 ℃ , the pure ZrB2with almost no ZrO2and B2O3impurity can be obtained. Finally, the effect of different reaction molar ratios of ZrB2on the high temperature conductivity was studied. According to the research, the conductivity increases with the increase of the purity of ZrB2.
synthesis of ZrB2; B4C reduction method; high temperature conductivity; pressureless sintering; high temperature stealth material; supersonic
10.14106/j.cnki.1001-2028.2017.07.005
TQ174.1
A
1001-2028(2017)07-0028-06
2017-04-06
陈志科
梁迪飞(1967-),男,湖南涟源人,副教授,主要研究方向为电磁功能复合材料,E-mail:dfliang@uestc.edu.cn ;陈志科(1989-),男,四川巴中人,研究生,主要研究方向为高温吸波材料,E-mail:sankexinfeiji@163.com 。
时间:2017-06-29 10:23
http://kns.cnki.net/kcms/detail/51.1241.TN.20170629.1023.005.html
