健脾温肾方治疗腹泻型肠易激综合征临床疗效及对血清T淋巴细胞亚群的影响
2017-07-10李硕熙梁雪松李鑫峰
李硕熙,梁雪松,李鑫峰,赵 敏*
(1.黑龙江中医药大学佳木斯学院,黑龙江 佳木斯 154007;2.黑龙江中医药大学研究生院,黑龙江 哈尔滨 150040)
健脾温肾方治疗腹泻型肠易激综合征临床疗效及对血清T淋巴细胞亚群的影响
李硕熙1,梁雪松2,李鑫峰2,赵 敏1*
(1.黑龙江中医药大学佳木斯学院,黑龙江 佳木斯 154007;2.黑龙江中医药大学研究生院,黑龙江 哈尔滨 150040)
目的观察健脾温肾方对腹泻型肠易激综合征的临床疗效及对血清T淋巴细胞亚群的影响。方法将符合纳入标准的患者59例随机分为2组,其中对照组29例,治疗组30例,对照组给予匹维溴铵治疗,治疗组在对照组的基础上给予健脾温肾方治疗,2组患者疗程均为4周,并随访8周。分别观察2组治疗前后临床症状积分、大便Bristol评分、生活质量评分(IBS-QOL、SF-36)、血清T淋巴细胞亚群及随访的复发率。结果对照组总有效率为89.7%,治疗组为93.3%,两组比较差异具有统计学意义(P<0.05)。两组治疗后 Bristol评分明显降低(P<0.05),治疗后组间比较,差异具有统计学意义(P<0.05);IBS-QOL、SF-36 评分明显升高(P<0.05),治疗后组间比较,差异具有统计学意义(P<0.05);CD4+、CD4+/CD8+水平与治疗前比较均明显升高(P<0.05),治疗后组间比较,差异具有统计学意义(P<0.05);CD8+水平与治疗前比较均明显升高(P<0.05),治疗后组间比较,差异具有统计学意义(P<0.05)。对照组随访复发率为34.5%,治疗组为10%,对照组复发率明显高于治疗组(P<0.05)。结论健脾温肾方能显著缓解IBS-D患者临床症状及改善大便性质及生活质量,提高患者的免疫功能,复发率低,且无明显不良反应。
腹泻型肠易激综合征;健脾温肾方;临床疗效;T淋巴细胞亚群
腹泻型肠易激综合征(diarrhea-predominant irritable bowel syndrome,IBS-D)是临床常见的胃肠道疾病之一,其临床症状主要表现为频繁的腹痛、腹胀和便溏,同时无形态学、生化学异常改变和其他明显原因可以解释上述症状的产生[1]。目前对于IBS-D的药物治疗存在诸多不足之处,如止泻药洛哌丁胺并不能明显缓解IBS-D的腹痛症状,5-羟色胺受体拮抗剂阿洛司琼只限于女性重度、难治性IBS-D患者的使用[2]。另外,如三环类的抗抑郁药物,由于其报道的不良反应多,限制其在临床的应用,尤其是对于老年腹泻型肠易激综合征患者[3]。匹维溴铵片属于钙拮抗剂,是目前最常用的治疗IBS-D的药物,虽然可以高度选择性地作用于肠道的平滑肌细胞,阻滞肠道的过度收缩,缓解肠道的痉挛,改善患者的腹泻和腹痛症状,但是其临床单独运用时疗效欠佳[4]。在临床实践中,笔者通过运用健脾温肾方联合匹维溴铵治疗IBS-D临床疗效显著,现将有关研究结果报道如下。
1 资料与方法
1.1 一般资料
所有59例IBS-D患者均为黑龙江中医药大学第一附属医院2015年11月至2016年8月门诊就诊患者,按照就诊顺序采用随机数字表法,分为治疗组30例、对照组29例。其中治疗组男16例,女14 例,平均年龄(38.6±16.7)岁,病程 1.5~10.5 年,平均(5.7±2.3)年;对照组男 14 例,女 15 例,平均年龄(40.2±17.5)岁,病程 2.3~10.2 年,平均(5.3±2.1)年。两组治疗前一般资料比较,差异无统计学意义(P>0.05)。
1.2 病例选择
1.2.1 西医诊断标准 参照罗马Ⅲ中IBS-D的标准[5]:反复发作的腹痛或者腹部不适,近3个月内,每个月至少有3 d出现以上症状,同时伴有以下2项或2项以上者:(1)发作时伴有大便性状的改变:小于25%的时间大便成形,大于25%的时间大便松散(水样便或糊状便);(2)发作时伴有排便频率改变;(3)排便后腹痛或者腹部不适症状改善。以上症状至少存在6个月,近3个月满足上述标准。
1.2.2 中医诊断标准 参考2010年的 《肠易激综合征中医诊疗共识意见》[6]中脾肾阳虚证的诊断标准:(1)晨起即腹痛腹泻;(2)腹部冷痛,得温后痛减;(3)形寒畏冷。 次症:(1)不思饮食;(2)腰膝酸软;(3)舌淡胖,苔白滑;(4)脉沉细。 凡具备 2 项主症及2项或以上次症即可诊断为脾肾阳虚证。
1.2.3 纳入标准 (1)符合IBS-D中医辨证分型诊断标准和西医诊断标准;(2)年龄在18~65岁之间;(3)同意并签署知情同意书。
1.2.4 排除标准 (1)合并炎症性肠病、消化性溃疡、消化道肿瘤、糖尿病、甲状腺功能亢进症者;(2)目前正在服用解痉药、抗胆碱药、抗抑郁药、促动力药等;(3)合并严重心、肺、肝、肾、血液、内分泌等系统原发疾病或肿瘤者;(4)妊娠或哺乳妇女;(5)有妇科盆腔疾病史。
1.2.5 剔除及脱落标准 剔除标准:(1)患者依从性差,自行加药或停药者;(2)资料不全影响疗效,影响安全性者。脱落标准:(1)患者在临床试验中因各种原因而不愿意继续者;(2)发生严重的并发症,不宜继续参加本试验者;(3)中途失访。
1.3 治疗方法
对照组给予匹维溴铵片(得舒特,进口药物注册 证 号 :H20120127,Abbott Products SAS,50 mg/粒),50 mg,日3次口服;治疗组在对照组的基础上给予健脾温肾方 (药物组成:黄芪30 g,炒白术20 g, 补骨脂 15 g,吴茱萸 10 g,肉豆蔻 10 g,五味子 15 g,陈皮 15 g,木香 10 g,升麻 10 g,炙甘草10 g,由本院煎药机统一煎煮,每剂250 mL×2袋),250 mL早晚温服。两组患者疗程均为4周,并随访8周。
1.4 观察指标
1.4.1主要症状积分
标准参照 《中药新药临床研究指导原则》(试行)[7],主要症状包括腹部冷痛、晨起腹泻、腰膝酸软、形寒肢冷、不思饮食,按无、轻度、中度、重度4级评分,分别计0、1、2、3分。以临床症状总积分的减分率判定其疗效。减分率=[(治疗前积分-治疗后积分)÷治疗前积分]×100%。痊愈:治疗后临床症状和体征完全消失,且减分率≥95%;显效:治疗后临床症状和体征得到明显的改善,并且减分率在70%~95%之间;有效:治疗后症状和体征得到改善,并且减分率在35%~69%之间;无效:治疗后临床症状和体征没有得到明显的改善,减分率<35%。
1.4.2 大便性状评分 粪便性状采用Bristol的粪便量表[8]进行评分,并按照粪便性状的分型(1~7型)分别记为1~7分。
1.4.3 生活质量评价 分别采用IBS生活质量评价量表(IBS quality of life questionnaire,IBS-QOL)[9]及SF-36生活质量量表(the MOS item short from health survey,SF-36)[10]评估两组患者生活质量变化。
1.4.4 血清T淋巴细胞亚群水平 分别于治疗前、后空腹采血,运用流式细胞术检测患者CD4+和CD8+T淋巴细胞分布百分率,具体按照试剂和仪器说明操作。
1.5 统计分析
运用SPSS 18.0软件进行统计分析。计数资料以频数和率进行描述,采用χ2检验;计量资料以“±s”表示,组间比较运用独立样本的t检验,组内比较采用配对样本的t检验。P<0.05表示差异具有统计学意义。
2 结果
2.1 两组患者临床疗效的比较
治疗组的总有效率为93.3%,对照组总有效率为89.7%,两组差异具有统计学意义(P<0.05)。见表1。
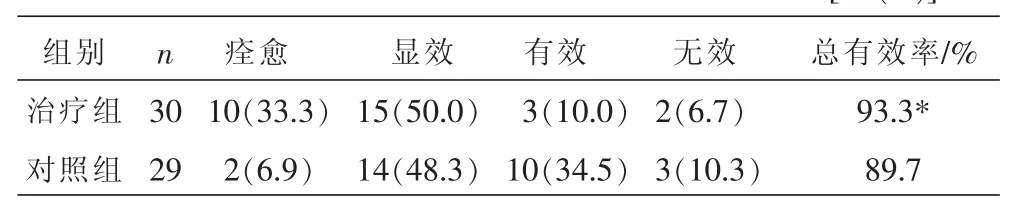
表1两组临床疗效比较 [例(%)]
2.2 两组Bristol评分及生活质量评分比较
两组患者治疗后大便Bristol评分与治疗前比较均明显降低(P<0.05),治疗后组间比较,差异具有统计学意义(P<0.05);两组治疗后 IBS-QOL、SF-36生活质量评分与治疗前比较明显升高(P<0.05),治疗后组间比较,差异具有统计学意义(P<0.05)。见表2。
表2两组Bristol评分及生活质量评分比较 (分,±s)

表2两组Bristol评分及生活质量评分比较 (分,±s)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05。
SF-36治疗前 治疗后治疗组对照组组别 n Bristol scale治疗前 治疗后IBS-QOL治疗前 治疗后30 29 6.52±0.38 6.47±0.41 4.73±0.61*#5.12±0.57*512.31±78.32 522.21±88.31 732.75±65.51*#657.69±79.42*338.49±42.78 346.61±46.92 625.47±51.27*#499.68±56.78*
2.3 两组T细胞亚群水平变化
两组患者治疗后CD4+、CD4+/CD8+水平与治疗前比较均明显升高(P<0.05),治疗后组间比较,差异具有统计学意义(P<0.05);两组患者治疗后 CD8+水平与治疗前比较均明显降低(P<0.05),治疗后组间比较,差异具有统计学意义(P<0.05)。见表3。
表 3.两组 T 细胞亚群 CD4+、CD8+水平及 CD4+/CD8+比较 (%,±s)

表 3.两组 T 细胞亚群 CD4+、CD8+水平及 CD4+/CD8+比较 (%,±s)
注:与治疗前比较,*P<0.05;与对照组比较,#P<0.05。
CD4+/CD8+治疗前 治疗后治疗组对照组组别 n CD4+治疗前 治疗后CD8+治疗前 治疗后30 29 19.34±1.17 20.32±1.38 38.22±2.15*#31.54±1.94*39.44±1.72 38.77±1.43 23.15±0.91*#27.11±1.12*0.49±0.28 0.51±0.19 1.47±0.31*#0.86±0.28*
2.4 不良反应和随访情况
两组治疗过程中均无病例退出、失访,治疗组中未出现与药物相关的不良反应,对照组出现恶心1例、轻度皮疹1例,疗程结束后症状自行消失。对照组随访复发10例,复发率为34.5%,治疗组随访复发3例,复发率为10%,对照组复发率明显高于治疗组(P<0.05)。
3 讨论
IBS是临床上常见的一种功能性胃肠病,全球发病率具有逐年增高之趋势,调查研究发现,该病在全球的患病率为11.2%左右[11]。我国IBS的发病率低于欧美国家的平均水平,但是在不同地区IBS的发病率在5%~10%之间[12]。随着IBS病程的迁延,对患者的生活质量造成了严重影响,IBS的患者比非IBS的患者更为频繁地表现出就医的要求和药物的使用需求,甚至常常导致不必要的手术需求,给患者和社会医疗造成巨大的经济负担[13]。
根据RomeⅢ的诊断标准,IBS分以为4个亚型,分别为腹泻型 IBS(IBS-D)、便秘型 IBS(IBSC)、混合型 IBS(IBS-M)和不确定型 IBS(IBS-U)[14]。在以上4个亚型中,IBS-D患者粪便呈稀水样或者糊状,每日3~5次,有的多达十余次,甚至呈黏液样便。然而目前尚不完全清楚IBS的基本病因、发病机制,一般认为该病与胃肠动力、内脏敏感性、脑-肠轴、神经-内分泌-免疫网络等功能异常及肠道菌群失调、肠道感染等众多因素有关。T细胞亚群可以反映IBS的免疫状态,在细胞的免疫应答中,T淋巴细胞各亚群各自发挥着相应的作用,如CD4+细胞能够促进T细胞、B细胞等相关免疫细胞的增殖及分化,促进淋巴因子的生成和活化,在协调免疫细胞相互间起着关键的作用[15]。CD8+细胞按照其作用可以分为杀伤性T细胞(Tc)和抑制性T细胞(Ts),长期病原刺激可以反复激活肠黏膜的CD8+细胞活化及免疫球蛋白分泌增多,激活CD8+细胞后,Ts能够抑制T细胞对自身抗原的增殖反应和抑制活化B细胞产生相关的免疫球蛋白,而Tc的异物排斥反应和抗原微生物免疫也将随之增强[16]。
IBS-D属于中医“腹痛、泄泻”范畴,《素问·灵兰秘典论》有言“大肠者,传导之官,变化出焉”,因此中医认为本病病位在肠,且与肝、脾、肾关系密切。脾主运化,饮食不节、过食生冷,则易伤脾胃,脾损日久及肾,致命门火衰;脾失温煦,无权运化无权水谷而反为“湿”与“滞”,清浊不分,水谷并走肠间,泄泻乃作[17]。健脾温肾方是由黄芪、炒白术、补骨脂、吴茱萸、肉豆蔻、五味子等中药组成,具有健脾益气、温阳补肾、涩肠止泻之功效。方中黄芪味甘微温,入脾肺经,补脾益气,炒白术味苦甘而温,补脾燥湿以治土虚,两药共为君药;《素问·举痛论篇》中曰:“寒邪客于小肠,小肠不得成聚,故后泄腹痛”,故以辛苦大温之补骨脂补命门之火以温养脾土,吴茱萸温肝脾肾以散阴寒,肉豆蔻温脾暖肾、涩肠止泻,以上三药共为臣药。有实验研究表明补骨脂-肉豆蔻醇提物可降低结肠中P物质、降钙素基因相关肽及促肾上腺皮质激素释放因子及受体的含量,从而作用内脏初级传入神经纤维从而降低内脏高敏感性[18]。五味子固肾益气、涩肠止泻,陈皮理气燥湿、醒脾和胃,木香理气醒脾,散寒止痛,使补而不碍胃,以上三药共为佐药;升麻引阳明清气上升,炙甘草缓急止痛、调和诸药为使药。本研究发现,治疗组与对照组比较,不仅能够明显改善大便Bristol评分、IBS-QOL及SF-36生活质量评分,还能够明显调整血清CD4+、CD8+、CD4+/CD8+水平,临床总有效率为93.3%,显著高于对照组89.7%,差异具有统计学意义(P<0.05)。
综上所述,健脾温肾方能显著缓解IBS-D患者临床症状及改善大便性质及生活质量,提高患者的免疫功能,复发率低,且无明显不良反应,值得临床广泛推广应用。
[1]马宝璋,齐聪.中医妇科学[M].新世纪第3版.北京:中国中医药出版社,2012:226.
[2]李景轩,童 英,陈 冰,等.宫腔镜联合腹腔镜治疗输卵管性不孕的临床研究[J].现代生物医学进展,2016,16(12):2316.
[3]陈志霞,陈桂芳,黄健玲.黄健玲教授治疗输卵管阻塞性不孕经验[J].湖南中医药大学学报,2016,36(3):53.
[4]腾秀香.柴松岩辩证治疗阻塞性不孕经验附验案一则[J].中国临床医生,2011,39(4):63.
[5]刘 丽,寇媛媛,李世大,等.“活血化瘀,行气止痛”大法治疗气滞血瘀型输卵管炎性不孕的临床观察[J].辽宁中医杂志,2016,43(10):2096.
[6]张声生,李乾构,魏 玮,等.肠易激综合征中医诊疗共识意见[J].中华中医药杂志,2010,25(7):1062-1065.
[7]郑筱萸.中药新药临床研究指导原则(试行)[S].北京:中国医药科技出版社,2002:139-143.
[8]Riegler G,Esposito I.Bristol scale stool form.A still valid help in medical practice and clinical research[J].Techniques in Coloproctology,2001,5(5):163-164.
[9]Francis CY,Morris J,Whorwell PJ.The irritable bowel severity scoring system:a simple method of monitoring irritable bowel syndrome and its progress[J].Alimentary Pharmacology&Therapeutics,1997,11(2):395-402.
[10]Ware JE,Snow KK,Kesinski M,et al.SF-36 health survey manual:an interpretation guide[S].Boston:New England Medical Center the Health Institute,1993:1-12.
[11]Lovell RM,Ford AC.Global prevalence of and risk factors for irritable bowel syndrome:a meta-analysis[J].Clinical Gastroenterology&Hepatology,2012,10(7):712-721(e4).
[12]何宛蓉,张法灿,梁列新.肠易激综合征流行病学研究现状与进展[J].胃肠病学和肝病学杂志,2012,21(1):83-88.
[13]Nellesen D,Yee K,Chawla A,et al.A systematic review of the economic and humanistic burden of illness in irritable bowel syndrome and chronic constipation.[J].Journal of Managed Care Pharmacy Jmcp,2013,19(9):755-674.
[14]刘新光.肠易激综合征与罗马Ⅲ诊断标准[J].胃肠病学,2006,11(12):736-738.
[15]常 东,李 健,冯春霞,等.易激灵2号方对大肠湿热型肠易激综合征T细胞亚群的影响[J].中国中西医结合消化杂志,2014,22(4):182-184.
[16]林少民.局部晚期直肠癌术前放疗的临床研究 [J].山东医药,2011,51(8):89-90.
[17]张 卓.理中丸联合得舒特治疗腹泻型肠易激综合征临床疗效观察[J].湖南中医药大学学报,2013,34(6):31-32+43.
[18]宋俊梅,王 婷,高家荣,等.补骨脂-肉豆蔻醇提物治疗肠易激综合征大鼠的内脏高敏感[J].中成药,2016,38(9):1881-1886.
(本文编辑 马 薇)
Effect of Jianpi Wenshen Decoction on Clinical Symptoms and Serum T Lymphocyte Subsets in Patients with Diarrhea-Predominant Irritable Bowel Syndrome
LI Shuoxi1,LIANG Xuesong2,LI Xinfeng2,ZHAO Min1*
(1.Jiamusi College,Heilongjiang University of Chinese Medicine,Jiamusi,Heilongjiang 154007,China;2.Graduate School,Heilongjiang University of Chinese Medicine,Harbin,Heilongjiang 150040,China)
ObjectiveTo observe the effect of Jianpi Wenshen (invigorating spleen and warming kidney)decoction on clinical symptoms and serum T lymphocyte subsets in patients with diarrhea-predominant irritable bowel syndrome.MethodsThe 59 cases of patients were randomly divided into 2 groups according to the diagnostic criteria and inclusion criteria,including 29 cases in the control group and 30 cases in the treatment group.The control group was treated with pinaverium bromide and the treatment group was
with Jianpi Wenshen decoction on the basis of control group.Both groups were treated for 4 weeks and followed up for 8 weeks.The clinical symptom score,Bristol score,quality of life score (IBS-QOL,SF-36),serum T lymphocyte subsets and recurrence rate.ResultsThe total effective rate of control group was 89.7%,the total effective rate of treatment group was 93.3%,differences between the two groups were statistically significant(P<0.05).Bristol scores were significantly improved compared with before treatment in both groups(P<0.05),and the difference was statistically significant between the two groups (P<0.05).IBS-QOL and SF-36 scores were significantly improved compared with before treatment (P<0.05),there was significant difference between the two groups (P<0.05).The CD4+and CD4+/CD8+levels significantly increased compared with before treatment (P<0.05),the difference was statistically significant between the two groups(P<0.05).The CD8+level was significantly higher than before treatment(P<0.05),the difference was statistically significant between the two groups (P<0.05).The recurrence rate of the control group was 34.5%,the treatment group was 10%,the recur-rence rate of the control group was significantly higher than that of the treatment group,the difference was statistically significant (P<0.05).ConclusionJianpi Wenshen decoction could significantly relieve the clinical symptoms,improve the quality of stool,quality of life and the immune function,and the recurrence rate was low with no significant adverse reaction.
diarrhea-predominant irritable bowel syndrome;Jianpi Wenshen decoction;clinical efficacy;T lymphocyte subsets
R256.34;R574.62
B
10.3969/j.issn.1674-070X.2017.07.023
本文引用:李硕熙,梁雪松,李鑫峰,赵 敏.健脾温肾方治疗腹泻型肠易激综合征临床疗效及对血清T淋巴细胞亚群的影响[J].湖南中医药大学学报,2017,37(7):785-788.
2017-02-20
李硕熙,男,在读博士研究生,主治医师,助教,研究方向:中医药治疗内科疾病。
* 赵 敏,女,副教授,E-mail:583772956@qq.com。
