改进双氢青蒿素哌喹片中双氢青蒿素的溶出度测定方法Δ
2017-07-07重庆市食品药品检验检测研究院重庆401121
张 勉,李 超(重庆市食品药品检验检测研究院,重庆 401121)
·药物分析与检定·
改进双氢青蒿素哌喹片中双氢青蒿素的溶出度测定方法Δ
张 勉*,李 超(重庆市食品药品检验检测研究院,重庆 401121)
目的:改进双氢青蒿素哌喹片中双氢青蒿素的溶出度测定方法。方法:采用桨法进行溶出试验,以0.1mol/L盐酸溶液为溶出介质,溶出介质体积为500m L,转速为75 r/m in,取样时间为45m in;样品前处理中加入3.6%氢氧化钠溶液的体积由原来的5 m L改为20m L,加入磷酸的体积由原来的0.2m L改为0.7m L。采用高效液相色谱法测定制剂中双氢青蒿素的溶出度:色谱柱为YMC-Pack ODS-A,流动相为0.02mol/L磷酸氢二钠溶液(用磷酸调节pH为2.4)-乙腈(65∶35,V/V),流速为1.0m L/m in,检测波长为237 nm,柱温为30℃,进样量为20μL。结果:双氢青蒿素检测质量浓度线性范围为7.802~117.03μg/m L(r=0.999 9);定量限为2.0 ng,检测限为0.6 ng;精密度、重复性试验的RSD<1.0%;回收率为99.18%~100.46%(RSD=0.45%,n=9)。3批样品中双氢青蒿素的平均溶出度分别为94.9%、77.9%、89.6%。结论:改进后的方法提高了其灵敏度、溶出度以及检测结果的准确性。
双氢青蒿素哌喹片;双氢青蒿素;溶出度测定;方法改进
双氢青蒿素哌喹片为双氢青蒿素和磷酸哌喹的复方制剂。双氢青蒿素为青蒿素的衍生物[1-2],能迅速控制症状和杀灭疟原虫[3]。磷酸哌喹是一种长效抗疟疾药物[4],能使滋养体食物泡膜和线粒体肿胀,导致其生理功能的破坏,从而杀死疟原虫[5]。体外药效学研究显示,双氢青蒿素与磷酸哌喹合用具有协同作用[6],可延缓疟原虫抗药性的产生[7]。双氢青蒿素哌喹片质量标准收载于2010年版《中国药典》(第一增补本)[8]。但在实际操作中发现,双氢青蒿素测定回收率偏低,溶出度测定结果也偏低。根据国家药典委员会下达的全球基金项目国家药品标准提高课题任务以及药品生产企业对双氢青蒿素哌喹片公示标准的反馈意见,为了更好地控制和评价企业产品质量,本课题组经试验研究,通过在样品前处理中增加3.6%氢氧化钠溶液和磷酸的体积,使溶液中双氢青蒿素衍生更加完全,以达到提高回收率和溶出度测定结果的目的。本研究改进的方法已收载于2015年版《中国药典》(二部)[9],现将有关情况报道如下。
1 材料
1.1 仪器
AT 7smart型溶出仪,包括CY7-50活塞泵及C613收集器(瑞士SOTAX公司);ZKT-18型真空脱气机(天津天大天发科技有限公司);e2695型高效液相色谱(HPLC)仪,包括2489型紫外-可见吸收检测器及Empower工作站(美国Waters公司);KQ5200型超声波清洗器(昆山市超声仪器有限公司,功率:200W,频率:40 kHz);BSA224S-CW型万分之一电子天平及ME215S型十万分之一电子天平(德国Sartorius公司)。
1.2 药品与试剂
双氢青蒿素哌喹片(华立岩康制药有限公司,批号:010212、011110、010512,规格:每片含双氢青蒿素40 mg、磷酸哌喹320mg);双氢青蒿素对照品(中国食品药品检定研究院,批号:100184-201202,纯度:99.94%);乙腈为色谱纯,其余试剂均为分析纯,水为纯化水。
2 方法与结果
2.1 色谱条件
色谱柱:YMC-Pack ODS-A(250mm×4.6mm,5μm);流动相:0.02mol/L磷酸氢二钠溶液(用磷酸调节pH为2.4)-乙腈(65∶35,V/V);流速:1.0m L/min;检测波长:237 nm;柱温:30℃;进样量:20μL。
2.2 溶液的制备
2.2.1 对照品溶液 取双氢青蒿素对照品20mg,置于50m L量瓶中,加乙醇溶解并定容,摇匀,精密量取适量,置于10m L量瓶中,用0.1mol/L盐酸溶液稀释至刻度,于37℃保温45 m in,放冷至室温,即得质量浓度为390.1μg/m L的对照品贮备液。取上述对照品贮备液5 m L,置于25m L量瓶中,用3.6%氢氧化钠溶液稀释至刻度,摇匀,置于60℃水浴中反应30m in,取出放冷至室温,精密加入磷酸0.7m L,摇匀,经0.45μm微孔滤膜滤过,取续滤液,即得。
2.2.2 供试品溶液 取样品适量,采用2010年版《中国药典》(二部)附录ⅩC“溶出度测定”第二法(桨法),以0.1mol/L盐酸溶液为溶出介质,溶出介质体积为500 m L,转速为75 r/min,依法操作,于45min时取溶出液适量,作为供试品贮备液。取上述供试品贮备液5m L,置于25m L量瓶中,用3.6%氢氧化钠溶液稀释至刻度,摇匀,置于60℃水浴中反应30min,取出放冷至室温,精密加入磷酸0.7m L,摇匀,经0.45μm微孔滤膜滤过,取续滤液,即得。
2.2.3 阴性对照溶液 按样品的处方称取辅料(含磷酸哌喹)适量,再按“2.2.2”项下方法制备阴性对照溶液。
2.3 系统适用性试验
精密量取“2.2”项下对照品溶液、供试品溶液和阴性对照溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。由图1可知,在该色谱条件下,各成分均能达到基线分离,分离度>2.0;理论板数以双氢青蒿素衍生物1峰计>3 000,保留时间为4.65m in。结果表明,其他成分对测定无干扰。
2.4 线性关系考察
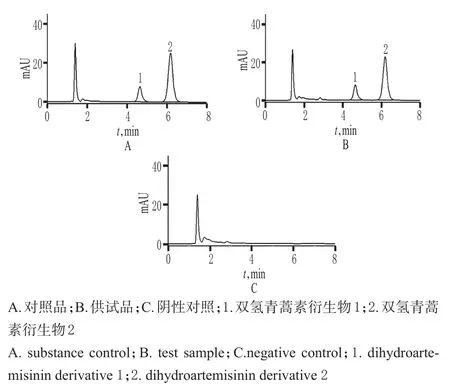
图1 高效液相色谱图Fig 1 HPLC chromatograms
精密量取“2.2.1”项下对照品贮备液1.0、2.5、5.0、7.5、10.0、12.5、15.0 m L,各置于50 m L量瓶中,用0.1 mol/L盐酸溶液稀释至刻度,于37℃保温45m in,放冷至室温,即得系列对照品溶液。精密量取上述系列对照品溶液各20μL,按“2.1”项下色谱条件进样测定,记录峰面积。以双氢青蒿素质量浓度(x,μg/m L)为横坐标、峰面积(y)为纵坐标进行线性回归,得回归方程为y=0.000 03x-0.023 1(r=0.999 9)。结果表明,双氢青蒿素检测质量浓度线性范围为7.802~117.03μg/m L。
2.5 定量限与检测限考察
取“2.2.1”项下对照品溶液适量,倍比稀释,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。当信噪比为10∶1时,得定量限(LOQ);当信噪比为3∶1时,得检测限(LOD)。结果,双氢青蒿素的LOQ为2.0 ng,LOD为0.6 ng。
2.6 精密度试验
取“2.2.1”项下对照品溶液适量,按“2.1”项下色谱条件连续进样测定6次,记录峰面积。结果,双氢青蒿素峰面积的RSD=0.20%(n=6),表明仪器精密度良好。
2.7 重复性试验
取“2.2.2”项下供试品溶液(批号:010212)适量,按“2.1”项下色谱条件进样测定,记录峰面积并计算含量。结果,双氢青蒿素峰面积的RSD=0.46%(n=6),表明本方法重复性良好。
2.8 回收率试验
取低、中、高质量的双氢青蒿素对照品适量,共9份,再按样品的处方比例加入空白辅料(含磷酸哌喹)适量,分别置于500m L量瓶中,加乙醇溶解并定容,摇匀,各取适量,按“2.1”项下色谱条件进样测定,记录峰面积并计算回收率,结果见表1。
2.9 溶出介质的选择
取样品(批号:010212)适量,分别以水、0.1mol/L盐酸溶液、pH 4.0醋酸盐缓冲液和pH 6.8磷酸盐缓冲液为溶出介质,溶出介质体积为500m L,转速为75 r/m in,于5、15、30、45、60m in时取样(同时补充相应的溶出介质10m L),按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,考察样品在4种溶出介质中的平均累积溶出度,结果见图2。由图2可知,样品在4种溶出介质中的溶出行为均相似。但是在0.1mol/L盐酸溶液中的各溶出时间点的平均累积溶出度均较高,因此选择0.1mol/L盐酸溶液为溶出介质。
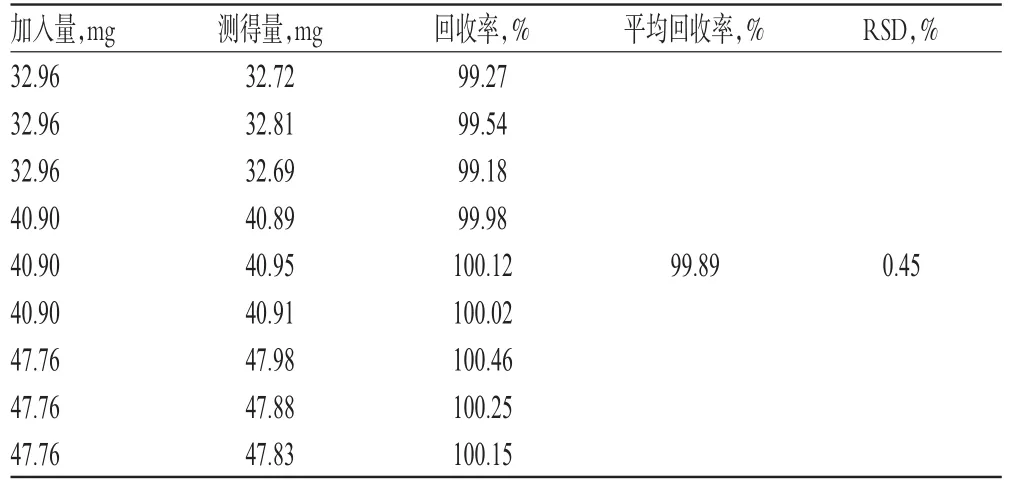
表1 回收率试验结果(n=9)Tab 1 Resultsof recovery tests(n=9)

图2 样品在4种溶出介质中的溶出曲线Fig 2 Dissolution curvesof samples in 4 kindsof dissolutionmediums
2.10 转速的确定
取样品(批号:010212)适量,以0.1mol/L盐酸溶液为溶出介质,溶出介质体积为500m L,转速分别为50、75 r/min,于5、15、30、45、60min时取样(同时补充相应的溶出介质10m L),并按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,考察样品在不同转速、不同时间点的平均累积溶出度,结果见表2。由表2可知,75 r/min转速的平均累积溶出度较好,因此选择75 r/min为本试验的转速。

表2 样品在不同转速及不同时间点的平均累积溶出度(n=6,%)Tab 2 Average accumulative dissolution of samplesat different rotation speeds and different time points(n=6,%)
2.11 取样时间的确定
取样品(批号:010212)适量,共6份,以0.1mol/L盐酸溶液为溶出介质,溶出介质体积为500m L,转速为75 r/m in,于5、15、30、45、60m in时取样(同时补充相应的溶出介质10m L),按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,考察样品在不同时间点的平均累积溶出度,结果见图3。由图3可知,样品在45 min时溶出曲线达到平台期。

图3 样品在不同时间点的溶出曲线(n=6)Fig 3 Dissolution curves of samples at different time points(n=6)
2.12 滤膜吸附试验
取“2.2.1”项下滤过前和滤过后的对照品溶液各适量,按“2.1”项下色谱条件进样测定,记录峰面积并计算吸附量。结果,0.45μm微孔滤膜对双氢青蒿素的吸附量<2.0%(n=6),符合规定[10]。
2.13 样品溶出度测定
取3批样品各适量,按“2.2.2”项下方法制备供试品溶液,按“2.1”项下色谱条件进样测定,用外标法以峰面积计算溶出度(要求≥标示量的70%);同时,以2010年版《中国药典》(第一增补本)的方法测定溶出度,结果见表3。
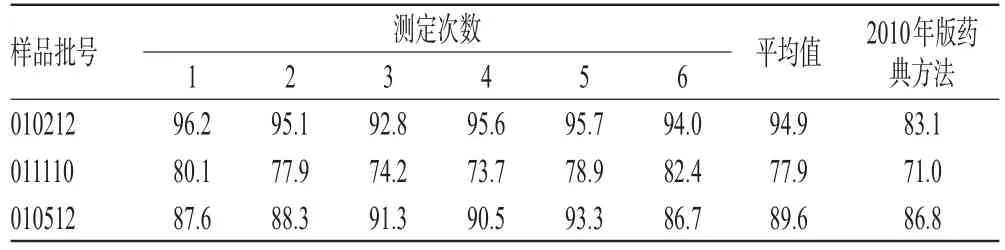
表3 样品溶出度测定结果(n=6,%)Tab 3 Results of dissolution determ ination of samples(n=6,%)
3 讨论
本课题组曾取“2.2.2”项下供试品溶液(批号:010212)适量,分别于室温下放置0、1、2、4、6、8、12 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果显示,供试品溶液在室温下放置2 h后,其中的双氢青蒿素峰面积呈显著递减趋势,因此本试验制备的供试品溶液应在2 h内完成测定。
因为双氢青蒿素存在α和β两种差向异构体,在不同溶剂中溶解两种异构体可能会相互转换且双氢青蒿素中无共轭结构和发色基团,不宜用分光光度法和HPLC法直接测定。考虑到双氢青蒿素含内酯结构,在碱性条件下易水解,能得到更加稳定和紫外吸收更强的衍生物(双氢青蒿素衍生物1和2)。故本试验将样品前处理中加入3.6%氢氧化钠溶液体积由5 m L改为20 m L,加入磷酸的体积由0.2m L改为0.7m L,使其衍生更加完全,使其定量更准确;且所有方法学验证试验均按外标法以双氢青蒿素衍生物1和2的峰面积之和计算结果。
按2010年版《中国药典》(第一增补本)[8]方法测定,3批样品的平均溶出度分别为83.1%、71.0%、86.8%;而按本试验方法测定,3批样品的平均溶出度分别为94.9%、77.9%、89.6%,溶出度测定结果显示灵敏度明显提高。
综上所述,改进后的方法提高了其灵敏度、溶出度以及检测结果的准确性。
[1] 韦国峰,何有成,黄祖良.双氢青蒿素的制备及其含量测定[J].右江民族医学院学报,2011,23(5):691-692.
[2] 王满元.青蒿素类药物的发展历史[J].自然杂志,2012,34(1):44-47.
[3] 常明,张相林,刘晓,等.双氢青蒿素人体药动学及生物等效性研究[J].中国药房,2006,17(14):1086-1088.
[4] 刘昌辉,黄天来,洪馨,等.高效液相色谱法测定人血浆中磷酸哌喹[J].药物分析杂志,2007,27(1):63-65.
[5] 周琳.HPLC测定双氢青蒿素哌喹片中的磷酸哌喹及有关物质[J].华西药学杂志,2015,30(5):610-612.
[6] 朱凯,范琦,张小松,等.HPLC测定双氢青蒿素哌喹片中磷酸哌喹的含量[J].中国药学杂志,2008,43(9):713-714.
[7] 韩韬,代勇.简述使用青蒿素联合西药治疗疟疾的研究进展[J].当代医药论丛,2015,13(6):10-11.
[8] 国家药典委员会.中华人民共和国药典:第一增补本[S].2010年版.北京:中国医药科技出版社,2012:271.
[9] 国家药典委员会.中华人民共和国药典:二部[S].2015年版.北京:中国医药科技出版社,2015:95.
[10] 国家食品药品监督管理局.普通口服固体制剂溶出度试验技术指导原则[S].2009.
Improvement of Determ ination Method for the Dissolution of Dihydroartem isinin in Dihydroartem isinin and Piperaquine Phosphate Tablets
ZHANG M ian,LIChao(Chongqing Institute for Drug and Food Control,Chongqing 401121,China)
OBJECTIVE:To improve the detection method for the dissolution of dihydroartem isinin in Dihydroartem isinin and piperaquine phosphate tablets.METHODS:The dissolution experiment adopted paddlemethod using 0.1mol/L hydrochloric acid solution 500m L as solventw ith rotating speed of 75 r/m in and sampling time of 45m in.In sample pre-treatment,the volume of 3.6% sodium hydroxide solution was increased from 5 m L to 20 m L,and that of phosphoric acid was increased from 0.2 m L to 0.7 m L. HPLC was adopted to determ ine the dissolution of dihydroartem isinin.The determ ination was performed on YMC-Pack ODS-A column w ith mobile phase consisted of 0.02 mol/L disodium hydrogen phosphate solution(pH adjusted to 2.4 using phosphoric acid)-acetonitrile(65∶35,V/V)at the flow rate of 1.0m L/min.The detection wavelength was set at 237 nm,and column temperature was 30℃.The sample size was 20μL.RESULTS:The linear range of dihydroartem isinin were 7.802-117.03μg/m L(r=0.999 9).The limit of quantitation was2.0 ng,and the limit of detection was 0.6 ng.RSDsof precision and reproducibility testswere all lower than 1.0%.The recoverieswere 99.18%-100.46%(RSD=0.45%,n=9).Average dissolutionsof dihydroartem isinin in 3 batchesof sampleswere 94.9%,77.9%,89.6%,respectively.CONCLUSIONS:Improved method enhance the accuracy for the lim it of sensitivity,dissolution and detection results.
Dihydroartem isinin and piperaquine phosphate tablets;Dihydroartem isinin;Dissolution determ ination;Method improvement
R 927.2
A
1001-0408(2017)15-2086-04
2016-05-31
2016-11-30)
(编辑:刘 柳)
全球基金项目国家药品标准提高课题(No. GF2012.39)
*主管药师。研究方向:药物分析。电话:023-86072743。E-mail:7183503@qq.com
DOI 10.6039/j.issn.1001-0408.2017.15.20
