苏萸痛风胶囊重复给药毒性试验研究
——对SD大鼠肝脏的影响*
2017-07-03王红平武志强曾统英宋英刘莉荣祖元
王红平 武志强 曾统英 宋英 刘莉 荣祖元△
(1.四川省食品药品检验检测院,四川 成都 610097;2.成都中医药大学附属医院,四川 成都 610072)
苏萸痛风胶囊重复给药毒性试验研究
——对SD大鼠肝脏的影响*
王红平1武志强1曾统英1宋英2刘莉2荣祖元1△
(1.四川省食品药品检验检测院,四川 成都 610097;2.成都中医药大学附属医院,四川 成都 610072)
目的:分析苏萸痛风胶囊在重复给药毒性试验中对SD大鼠肝脏的影响,评价其安全性,为临床应用提供参考。方法:取健康SD大鼠120只,按性别、体重随机分为溶剂对照组(0.5%羧甲基纤维素钠水溶液)和苏萸痛风胶囊高、中、低剂量组(3.732 g·kg-1、1.866 g·kg-1、0.933 g·kg-1),每组30只,雌雄各半。连续给药3个月,停药恢复1个月,于给药末期和恢复期,分别采用戊巴比妥钠麻醉,腹主动脉采血,放血处死动物,进行血液生化学检测和组织病理学等检查。结果:给药末期中、高剂量组动物肝脏的脏体指数均有显著性升高(P<0.01),停药后1个月基本恢复正常,病理结果提示:给药末期高剂量组可能会引起大鼠肝细胞的弥漫性正常增生。结论:苏萸痛风胶囊在拟定的人体临床应用剂量范围内较安全,但长期大剂量使用可能会导致肝细胞的弥漫性正常增生,建议长期用药患者应定期监测肝功能指标。
苏萸痛风胶囊;重复给药毒性;肝脏
苏萸痛风胶囊内容物为黄色粉末,由吴茱萸、木瓜、薏苡仁、肉桂四味中药组成,有止痛、利湿、消肿的功效,临床用于治疗急慢性痛风关节炎。吴茱萸在方中所占比重最大,发挥主要功效,历代文献均有记载其“小毒”或“有毒”,近期有研究显示[1-2],肝脏可能为吴茱萸的毒性靶器官,故本次研究在进行大鼠重复给药毒性试验时,重点关注与肝功能相关的血液生化指标,结合脏器指数和组织病理学检查综合评价苏萸痛风胶囊安全性,为临床应用提供数据支持。
1 材料与方法
1.1 材料
1.1.1 药物
苏萸痛风胶囊,批号:20150701,由成都中医药大学附属医院提供,临床拟用剂量(生药量):7.5 g·d-1。
1.1.2 动物
SD大鼠,SPF级,北京维通利华实验动物技术有限公司提供,实验动物生产许可证号:SCXK(京)2012-0001,实验动物质量合格证号:11400700119621。本研究严格遵循本单位有关实验动物保护与使用的准则。
1.1.3 仪器
c501全自动生化分析仪,Roche;SORVAN ST16R高速冷冻离心机,Thermo;ASP300S全自动真空组织脱水机,德国徕卡(Leica)仪器有限公司;EG1160包埋机,德国徕卡(Leica)仪器有限公司;RM2245组织切片机,德国徕卡(Leica)仪器有限公司;HI1210组织摊片机,德国徕卡(Leica)仪器有限公司;ST5010全自动染色机,德国徕卡(Leica)仪器有限公司;DM2000显微镜,德国徕卡(Leica)仪器有限公司;TYMR-Ⅲ血液混匀器,姜堰市天仪电子仪器有限公司。
1.2 方法
取健康合格SD大鼠120只,按性别、体重随机分为溶剂对照组(0.5%羧甲基纤维素钠水溶液),苏萸痛风胶囊高、中、低剂量组(3.732 g·kg-1、1.866 g·kg-1、0.933 g·kg-1),每组30只,雌雄各半。每周连续灌胃给药6天,1次·d-1,给药体积为15 ml·kg-1,连续3个月(按13周计),停药恢复1个月(4周)。每天观察动物的外观体征,给药末期(第13周)和恢复期(第17周)采用戊巴比妥钠麻醉,腹主动脉采血,放血处死动物,进行包括总蛋白(Total protein,TP)、谷草转氨酶(Aspertate aminotransferase,AST)、谷丙转氨酶(Alanine aminotransferase,ALT)、白蛋白(Albumin,ALB)、总胆红素(Total bilirubin,TBIL)、碱性磷酸酶(Alkaline phosphatase,ALP)等与肝功能密切相关的血液生化学指标检测和组织病理学等检查[3-5]。
1.3 统计与分析

2 结果
2.1 相关血液生化学指标
给药末期结果显示,与同期溶剂对照组比较,雌性大鼠低、中、高剂量组ALT(谷丙转氨酶)显著性降低(P<0.01),高剂量组AST(天冬氨酸氨基转移酶)显著性降低(P<0.05);雄性大鼠低、中、高剂量组ALT显著性降低(P<0.01或P<0.05),见表1。
恢复期结果显示,与同期溶剂对照组比较,雌性大鼠低、中、高剂量组TBIL(血清总胆红素)显著性降低(P<0.01或P<0.05),高剂量组ALT显著性降低(P<0.01),见表2。
2.2 肝脏脏器指数
表3、4结果显示,给药末期中、高剂量组动物肝脏的脏体指数均显著性升高(P<0.01),恢复期高剂量组动物肝脏脏体指数未见异常,中剂量组雄性动物肝脏脏体指数仍见升高(P<0.01),但肝脏与大脑的脏脑指数结果显示:恢复期溶剂对照组与中剂量组相比较并无显著性差异,说明恢复期雄性大鼠中剂量组肝脏脏体指数的改变与动物体重有关。
表1 连续3个月经口灌服苏萸痛风胶囊对SD大鼠给药末期血液生化学的影响( ±SD,n=10)
注:与溶剂对照组比较,*P<0.05,**P<0.01。
表1 连续3个月经口灌服苏萸痛风胶囊对SD大鼠给药末期血液生化学的影响( ±SD,n=10)(续)
注:与溶剂对照组比较,*P<0.05,**P<0.01。

表2 连续3个月经口灌服苏萸痛风胶囊对SD大鼠恢复期血液生化学的影响±SD,n=5)
注:与溶剂对照组比较,*P<0.05,**P<0.01。

表2 连续3个月经口灌服苏萸痛风胶囊对SD大鼠恢复期血液生化学的影响±SD,n=5)(续)
注:与溶剂对照组比较,*P<0.05,**P<0.01。
2.3 肝脏组织病理检查结果
病理检查结果表明,与溶剂对照组比较,高剂量组肝细胞平均直径显著性升高(P<0.01),高剂量组肝细胞均数有升高的趋势。以上结果提示高剂量组可能会导致肝细胞弥漫性增生,但增生的肝细胞为正常肝细胞,停药一个月后,能恢复正常,见表5。

表3 连续3个月经口灌服苏萸痛风胶囊对SD大鼠给药末期肝脏指数的影响±SD,n=10)
注:与溶剂对照组比较,*P<0.05,**P<0.01。

表4 连续3个月经口灌服苏萸痛风胶囊对SD大鼠恢复期肝脏指数的影响±SD,n=5)
注:与溶剂对照组比较,*P<0.05,**P<0.01。
表5 肝细胞直径统计结果表
注:与溶剂对照组比较,*P<0.05,**P<0.01。
溶剂对照组与高剂量组肝脏均出现空泡样改变,见图1。
3 讨论
随着社会的发展,人民生活水平的提高,饮食结构的不合理现象日趋严重,痛风性关节炎的患者也越来越多,西药治疗痛风性关节炎多选用非甾类抗炎药、秋水仙碱、糖皮质激素、促进尿酸排泄药物等药物。由于用药时间久,且不能根治,给痛风性关节炎患者带来了巨大的经济负担和心理负担。因此越来越多的医护人员把治疗痛风性关节炎的目光投向传统中医药[6]。苏萸痛风胶囊具有止痛、利湿、消肿的功效,临床上主要用于治疗急慢性痛风关节炎。方中木瓜主治关节肿痛、脚气转筋,薏苡仁有利水消肿、清热排脓之功,肉桂具有散寒止痛之功,吴茱萸,除散寒止痛外,还具有疏肝下气之功,能够引诸药直达病所,现代药理学研究表明:吴茱萸[7-8]具有抗炎镇痛作用,可以迅速缓解痛风性关节炎患者的疼痛。但高剂量的吴茱萸次碱及吴茱萸醇提物具有明显的肝毒性:体外试验发现吴茱萸次碱可升高肝细胞上清液中的AST、ALP、LDH,但光镜下未见细胞形态发生改变[9];SD大鼠经口一次灌胃给予吴茱萸醇物,出现血清转氨酶及肝脏系数增加,肝脏出现中央静脉及小叶下静脉周围肝细胞疏松等病理性改变[1];SD大鼠连续28天经口重复给予吴茱萸醇提物,出现TBIL升高,肝脏肥大,肝脑比呈剂量依赖性升高,电镜下肝细胞变性肿胀、炎细胞浸润,恢复期缓解[2]。
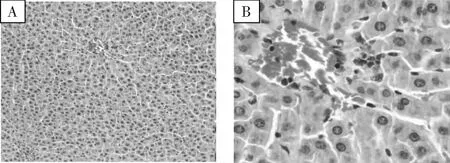
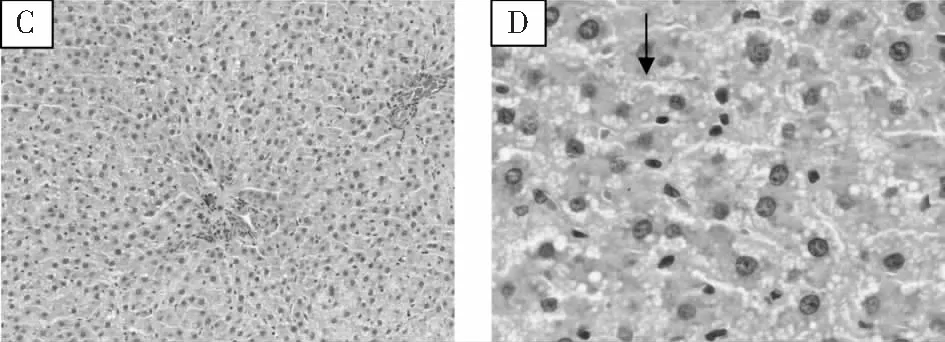
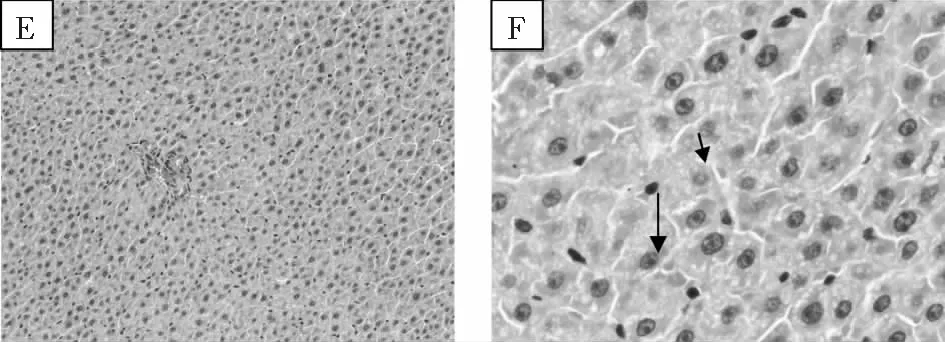
图1 SD大鼠重复给药毒性试验典型肝脏组织病理照片注:A~B:肝脏,A: HE×100,B: HE×400,正常;C~D:给药末期对照组肝脏,C: HE×100,D4: HE×400,肝细胞空泡样变(黑色箭头所示);E~F:给药末期高剂量组肝脏,E:HE×100,F:HE×400,肝细胞空泡样变(黑色箭头所示)
本研究依据前期急毒试验结果设定本次试验中各测试组的给药剂量,分别为临床剂量的60倍、30倍、15倍,结果显示,给药末期与同期溶剂对照组比较,雌性大鼠低、中、高剂量组ALT(谷丙转氨酶)显著性降低,高剂量组AST(天冬氨酸氨基转移酶)显著性降低,雄性大鼠低、中、高剂量组ALT显著性降低。恢复期与同期溶剂对照组比较,雌性大鼠低、中、高剂量组TBIL(血清总胆红素)显著性降低,高剂量组ALT显著性降低,其余生化指标均无异常,说明该样品在本次试验条件下未对肝脏相关血液生化指标产生影响。给药末期中、高剂量组动物肝脏脏体指数均有不同程度的升高,恢复期高剂量动物肝脏脏体指数未见异常,中剂量组雄性动物肝脏脏体指数仍见升高,但
恢复期溶剂对照组与中剂量组的肝脏脏脑指数比较并无显著性差异,说明恢复期雄性大鼠中剂量组肝脏脏体指数的改变与动物体重有关。肝脏组织病理学检查发现,本次试验动物肝脏主要病变为肝细胞的空泡样变和肝细胞增生。肝细胞的空泡样变为大鼠常见自发病,本次试验供试品低、中、高各剂量组与溶剂对照组比较,无论是病变程度或病变发生率均无显著性差异,且各组别病变发生率均在本中心自发病变范围内,因此推测肝细胞空泡样变为动物的自发病变。针对给药末期中、高剂量组肝脏脏体指数的升高,而镜下观察肝脏结构和细胞形态均正常,推测肝细胞可能有弥漫性增生,因此进行了肝细胞直径测量和数量计数。结果,高剂量组雌、雄动物的肝细胞直径比溶剂对照组大,且与溶剂对照组相比均出现极显著性差异;各组肝细胞数量在400倍放大图片中,均值在50~70个之间,且雌、雄统计结果相反,雌性大鼠低、中剂量组数量均值比溶剂对照组小,且有统计学意义,高剂量组雌性均值较对照组大,但无统计学意义;而雄性动物数量均值高剂量组比溶剂对照组大,且有统计学意义,因此肝细胞计数结果表明高剂量组的雌、雄数量均比溶剂对照组高。综合分析,高剂量出现的肝脏脏体指数的升高可能为肝细胞弥漫性增生引起,但增生的肝细胞为正常肝细胞,停药1个月后,恢复正常。
本研究表明,长期大剂量使用苏萸痛风胶囊可能会引起SD大鼠肝细胞弥漫性正常增生,具有可逆性,而与肝脏功能相关的血液生化指标并无异常,故苏萸痛风胶囊在拟定的人体临床应用剂量范围内较安全,但肝肾功能异常者及长期大剂量使用者应监测肝功能指标。
1 李波,李莉,赵军宁,等. 吴茱萸乙醇提取物对大鼠急性毒性及肝毒性的影响[J].中药药理与临床, 2013, 29(2): 120-124.
2 刘颖,杨润芳,夏祺悦,等. 吴茱萸醇提物重复给药的靶器官毒性研究[J]. 现代预防医学, 2015, 42(14): 2600-2644.
3 侯志勇,王立强,韩静,等. 肾茶胶囊对大鼠脏器长期毒性的实验研究[J]. 中国医药科学, 2011, 1(12): 16-17.
4 张淑香,王萌影,刘学伟,等. 复方灵芝降糖胶囊大鼠给药长期毒性研究[J]. 中国实验方剂学杂志, 2015, 21(17): 146-151.
5 国家食品药品监督管理局. 药物重复给药毒性试验技术指导原则[S]. 2014.
6 王新宇. 中医治疗痛风性关节炎的近况研究[J]. 内蒙古中医药, 2014, 33(13): 109-110.
7 张璐,冯育林,王跃生,等. 吴茱萸现代研究状况[J]. 江西中医学院学报, 2010, 22(2): 78-82.
8 宋英,盛蓉,李涓,等. 吴茱萸碱治疗痛风的药效学研究[J]. 中药药理与临床, 2011, 27(6): 17-18.
9 张茜,周绮,金若敏,等. 吴茱萸次碱对肝肾毒性的初步研究[J]. 中国实验方剂学杂志, 2011, 17(8): 221-224.
Repeated dose toxicity test of Su Yu gout capsule——influence of it on SD rat liver function
Wang Hong-ping1, Wu Zhi-qiang1, Zeng Tong-ying1, Song Ying2, Liu Li2, Rong Zu-yuan1△
(1.Sichuan Institute for Food and Drug Control, Sichuan Chengdu 610097;2.Affiliated Hospital of Chengdu University of TCM, Sichuan Chengdu 610072)
Objective:To study the effect of Su Yu gout capsule on SD rat liver function, to evaluate the safety of its repeated dose toxicity test, and hope the date can provide the evidence for the doses and parameters in clinical test. Methods:A total of 120 SD rats, half male and half female, were randomly divided into solvent control (0.5% sodium carboxymethyl cellulose solution) group and Su Yu(3.732 g·kg-1, 1.866 g·kg-1and 0.933 g·kg-1) treated group. All drugs were administered by intragastric administration (i.g.) for 3 months. After 4 weeks of recovery, the rats were sacrificed, blood samples were obtained from all rats for hematological and serum chemistry analysis and histopathologic examination were done for all rats. Results: Compared with the control group, relative organ weight of the liver was significantly higher in 3.732 g·kg-1and 1.866 g·kg-1treated group after administration (P<0.01). All of them were almost returned normal for 1 month. Histopathological examination showed the diffuse proliferation of liver cell in the Su Yu 3.732 g·kg-1group after administration. Conclusion:Su Yu gout capsule possesses a good opportunity for clinical use. However related with the period of using Su Yu may lead to diffuse proliferation of liver cell, we recommend that patients monitor hepatic function at regular intervals.
Su Yu gout capsule; Repeated dose toxicity; Liver
四川省科技厅科技支撑计划(编号:2014SZ0140)
王红平,女,主管中药师,主要从事中药药理学研究,Email:54whpcn@163.com。
△通讯作者:荣祖元,男,研究员,主要从事药理毒理学研究,Email:304240183@qq.com。
2017-2-24)
