热处理对Ca-乳清浓缩蛋白纳米纤维起泡性的影响
2017-06-23王楠楠徐红华董世荣谢明明
王楠楠,徐红华,董世荣,谢明明
(东北农业大学食品学院,黑龙江哈尔滨 150030)
热处理对Ca-乳清浓缩蛋白纳米纤维起泡性的影响
王楠楠,徐红华,董世荣,谢明明
(东北农业大学食品学院,黑龙江哈尔滨 150030)
通过向乳清浓缩蛋白纳米纤维中添加一定量的氯化钙后热处理不同时间(0、1、2、3、4、5 h),研究不同热处理时间对Ca-WPC纳米纤维聚合物起泡性的影响。结果表明Ca-WPC纳米纤维聚合物的起泡能力在热处理3 h时达最大值96.00%±0.02%,是对照组Ca-WPC常规聚合物热处理3 h时的2.13倍;Ca-WPC常规聚合物在不同热处理时间后其泡沫稳定性均为零,而Ca-WPC纳米纤维聚合物随着热处理时间延长其泡沫稳定性先增加后减小,热处理3 h时达到最大值为62.38%±1.51%,即热处理一定时间可以显著提高Ca-WPC纳米纤维聚合物的起泡性。
乳清浓缩蛋白,钙,Ca-乳清浓缩蛋白纳米纤维,热处理,起泡性
泡沫是以气泡的形式分散在液体或者固体连续介质中的一种气体分散系,而蛋白质的起泡性是食品功能性质测定的重要指标。目前卵清蛋白、乳清分离蛋白均可作为表面活性剂广泛应用于调和蛋白、牛轧糖、人造奶油等发泡性食品中[1],虽然其结构复杂但仍能通过疏水基团作用,降低表面张力均匀吸附在空气-水界面,在起泡过程中蛋白结构发生局部展开或部分变性,一些极性基团和非极性基团分别暴露在液相和气相中[2],并与相邻的蛋白分子通过氢键、疏水相互作用甚至共价键在表面形成更加稳定的界面膜[3-5]。起泡能力和泡沫稳定性是评价起泡性的两个主要技术参数[6],其中泡沫稳定性是决定起泡性好坏的关键[7]。乳清浓缩蛋白纳米纤维是一种在变性条件下(低pH、低离子强度、高温长时间加热[8-9])通过自组装方式形成的无分支杆状聚合物,与传统蛋白质聚合不同的是其主要是通过疏水相互作用、静电作用等形成的[10-12],而且加入一定钙离子可以改变纤维的形态和柔性[9,13],提高自组装速率[14-15],有学者报道乳清浓缩蛋白纳米纤维适宜的长宽比可能对起泡性有利,但其在食品体系中并没有达到人们预期,一些研究表明适当温度下对乳清浓缩蛋白(WPC)进行热处理会提高其起泡性,然而热处理不当便会降低起泡性[16]。本课题研究目的是通过向WPC纳米纤维聚合物中加入一定量氯化钙,比较不同热处理时间对Ca-WPC纤维聚合物起泡性的影响,并通过测定表面疏水性和透射电镜观察,研究蛋白质结构与起泡性的关系,进一步拓展单一蛋白质或者多种蛋白混合物作为大分子表面活性剂的应用领域。
1 材料与方法
1.1 材料与仪器
乳清浓缩蛋白WPC-80 美国HILMAR公司;尿素 西陇化工股份有限公司;8-苯氨基-1-萘磺酸(ANS) Sigma公司;DTNB MERCK公司;溴甲酚绿、甲基红 天津迪博化工公司;硫酸铜、硫酸钾、磷酸氢二钠、甘氨酸、硼酸、氢氧化钠、磷酸二氢钠、乙二胺四乙酸(EDTA)、盐酸、氯化钙 天津市力天化学公司。
GL-21M型离心机 上海精密仪器研究所;pHS-3C型精密PH计 梅特勒-托利多仪器(上海)有限公司;LNK-872型多功能快速消化器 江苏省宜兴市科教仪器研究所;KDN-102C半自动定氮仪 上海纤检仪器有限公司;JEM-1200EX透射电子显微镜 日本日立公司;UV-240IPC紫外可见分光光度计 日本岛津公司;F-4500荧光分光光度计 日本日立F-4500。
1.2 实验方法
1.2.1 WPC纳米纤维的制备 20.00 g乳清浓缩蛋白用去离子水定容至500 mL,调pH至2.0,4 ℃、12500 r/min离心20 min,吸取中层清液消化、定氮,稀释样品终浓度为2.0 wt%后调pH至2.0,90 ℃加热10 h,样品于4 ℃冰箱保存[8-9]。对照组Ca-WPC常规聚合物除在离心前和加热前调pH至6.5以外,其余步骤与WPC纳米纤维制备方法相同。
1.2.2 氯化钙添加 根据前期研究结果[17],取3.125 mmol/L氯化钙溶液10 mL加到1.2.1的实验组和对照组溶液中搅拌均匀,分别调溶液pH至2.0和6.5,室温放置30 min。
1.2.3 热处理 将1.2.2中室温放置30 min后的溶液于90 ℃[18]下分别加热不同时间(0、1、2、3、4、5 h)进行指标测定。
1.2.4 起泡性测定 蛋白质溶液的起泡能力(FC)和泡沫稳定性(FS)测定参考Motoi[19]等人方法并加以改进。将1.2.3热处理后的溶液用0.01 mol/L、pH7.0的磷酸缓冲液稀释至0.1 wt%,室温下用组织捣碎机10000 r/min均质1 min,测定搅打后的泡沫体积V0,再测定放置30 min后的泡沫体积Vt,通过相对溢出量与静止后稳定的泡沫体积比来评价样品的起泡能力(FC)和泡沫稳定性(FS),具体计算方法如下:
起泡能力(%)=V0/Vi×100
泡沫稳定性(%)=Vt/V0×100
式中:V0-起泡0 min时的泡沫体积;Vt-起泡t min后的泡沫体积;Vi-起泡前最初液体的体积
1.2.5 表面疏水性的测定 参照Ni Y Z Wen[20]ANS荧光探针法并加以改进。用0.01 mol/L的磷酸缓冲液(pH7.0)将1.2.3热处理后的溶液稀释蛋白浓度为1.0 wt%,加入20 μL的ANS(8 mmol/L,溶于0.01 mol/L的磷酸缓冲液,pH7.0)荧光探针,混匀后在室温下避光15 min,用荧光分光光度计于激发波长390 nm,发射波长470 nm、狭缝宽度5 nm的条件下,进行425~600 nm波段扫描。
1.2.6 透射电镜观察(TEM) 参考Mark[21]等人的方法并加以改进。将1.2.3热处理后的溶液稀释成蛋白浓度为0.325 wt%的待测样品,取两滴稀释液滴于透射电镜专用铜网上吸附15 min后,室温下放置20 min,采用80 kv电压下观察样品的微观结构。
1.3 统计方法
采用Origin 8.0和SPSS Statistics 8.1软件对实验数据进行统计分析,其中每组实验均做3个平行,表中数据均以平均值±标准差表示(n=3)。
2 结果与分析
2.1 起泡性
2.1.1 起泡能力 由图1实验结果可知,随着热处理时间的延长,Ca-WPC常规聚合物的起泡能力逐渐降低最后基本保持不变,热处理3 h时其起泡能力为45.00%±0.01%,热处理4 h和5 h时分别降为40.00%±0.03%和40.00%±0.06%;而Ca-WPC纳米纤维聚合物的起泡能力随着热处理时间延长呈现出先降低后升高再降低的趋势,热处理3 h时达到最大值为96.00%±0.02%,是Ca-WPC常规聚合物热处理3 h的2.13倍。这一结果可能是由于经过不同热处理时间后WPC常规聚合物与Ca之间的钙桥作用被破坏,因此其起泡能力随着热处理时间延长不断下降;而WPC纳米纤维是一种具有特殊三维立体网状结构的聚合物[9],钙离子加入后与WPC纳米纤维通过热处理作用形成更加稳定的聚合结构,有效提高其起泡能力。
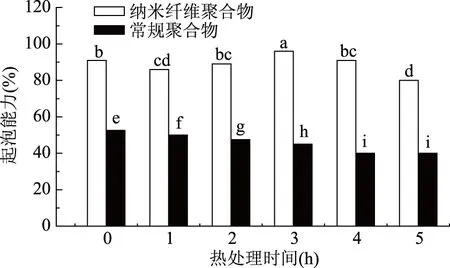
图1 热处理时间对起泡能力的影响Fig.1 Effect of the different heating time on foam-ability 注:不同字母表示样品经不同热处理时间后起泡能力差异显著(p<0.05)。
2.1.2 泡沫稳定性 由图2实验结果可知,Ca-WPC常规聚合物在不同热处理时间后其泡沫稳定性均为零,而Ca-WPC纳米纤维聚合物随着热处理时间延长其泡沫稳定性呈现先增加后减小的趋势,热处理3 h时达到最大值为62.38%±1.51%,同其起泡能力规律大致相同。由图3热处理3 h时分别测定放置0、5、10、15、20、25、30 min后泡沫体积的实验结果可知,Ca-WPC常规聚合物的泡沫在均质1 min后不断凝聚消散,直至放置5 min时泡沫体积为零,而Ca-WPC纳米纤维聚合物随着放置时间的延长,泡沫体积也会有所下降,但下降速度缓慢。热处理后通过测定Ca-WPC常规聚合物和Ca-WPC纳米纤维聚合物起泡性可知,Ca-WPC纳米纤维聚合物的起泡能力和泡沫稳定性均好于Ca-WPC常规聚合物,且热处理3 h时Ca-WPC纳米纤维聚合物的起泡能力和泡沫稳定性达到最高。
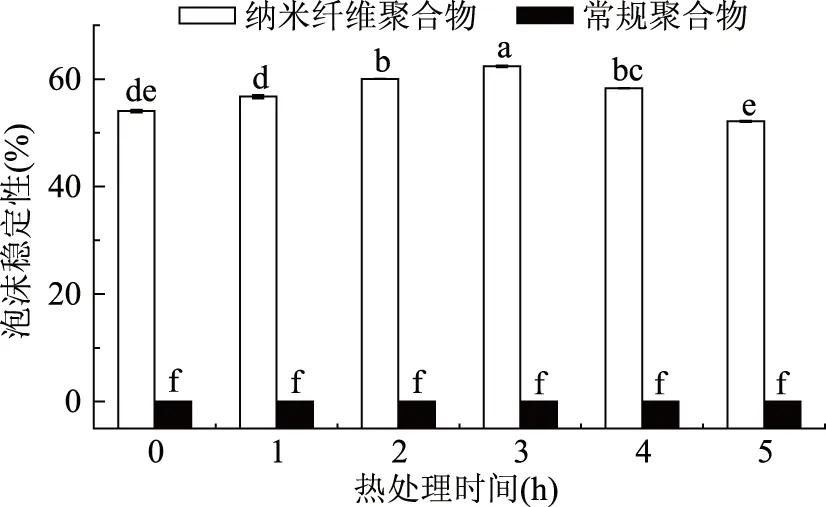
图2 不同热处理时间对泡沫稳定性的影响Fig.2 Effect of the different heating time on foam stability注:不同字母表示样品经不同热处理时间后泡沫稳定性差异显著(p<0.05)。
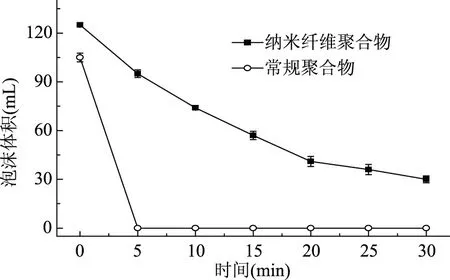
图3 热处理3 h时泡沫体积的变化Fig.3 Change of foam volume of samples at heating for three hours
2.2 表面疏水性
热处理3 h时,Ca-WPC纳米纤维聚合物与Ca-WPC常规聚合物的起泡性都表现出极大差异,这可能是由于蛋白质分子一旦吸附于界面,分子随即展开,内部疏水基暴露,表面张力下降所导致[22]。因此将重点研究热处理3 h时两种聚合物表面疏水性的变化(见图4)。
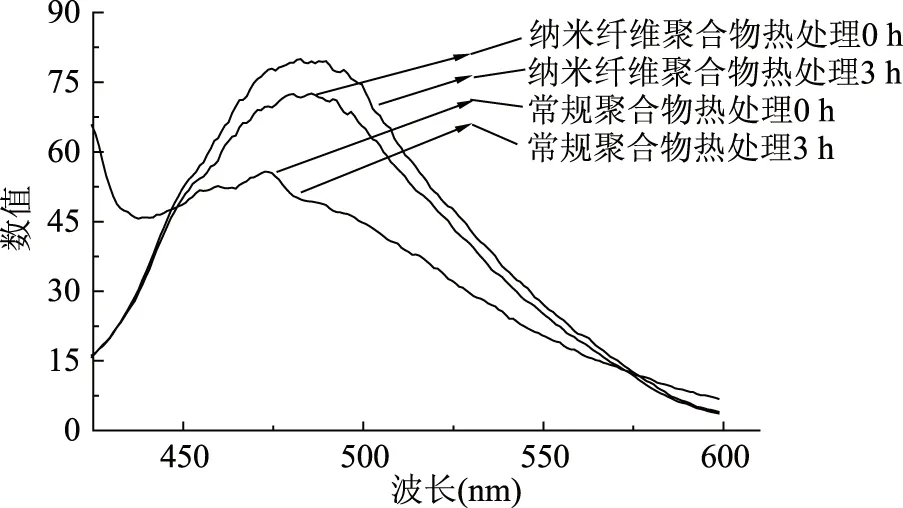
图4 热处理0、3 h时表面疏水性的变化Fig.4 Surface hydrophobic changes with heating for 0 h and 3 h
由图4实验结果可知,Ca-WPC纳米纤维聚合物和Ca-WPC常规聚合物热处理3 h较热处理0 h其表面疏水性均有所升高,Ca-WPC常规聚合物表面疏水性提高了1.08%,Ca-WPC纳米纤维聚合物表面疏水性提高了13.28%,Ca-WPC纳米纤维聚合物具有更高的表面疏水性,导致这种显著性差异的原因是Ca-WPC纳米纤维聚合物与Ca-WPC常规聚合物的聚合方式不同。Ca-WPC纳米纤维聚合物在形成过程中表面疏水作用占主导地位,而Ca-WPC常规聚合物在聚合过程中表面疏水作用较弱,较高的表面疏水性可以有效改善蛋白质的起泡性[23-25],因此Ca-WPC纳米纤维聚合物表现出更好的起泡性。
2.3 透射电镜(TEM)
不同热处理时间对Ca-WPC纳米纤维聚合物起泡性的影响程度与蛋白质结构变化密切相关,因此通过透射电镜观察比较Ca-WPC纳米纤维聚合物与Ca-WPC常规聚合物热处理0、1、3、5 h后微观结构的变化(见图5)。
由图5实验结果可知,Ca-WPC纳米纤维聚合物在热处理3 h时纤维细丝结构明显且可看到黑色的钙离子与纤维丝紧密缠绕在一起,分枝较少,结构更加紧密有序,热处理1、5 h时纤维细丝明显变粗,分枝较多,柔性降低。Ca-WPC常规聚合物在热处理0、1、3、5 h时聚合结构遭到破坏,且破坏程度逐渐增加。这一结果表明Ca-WPC纳米纤维聚合物对热处理有一定的耐受力,而Ca-WPC常规聚合物在热处理后由有序网状结构变成无序松散结构。起泡性的好坏取决于蛋白质-蛋白质之间的相互作用和蛋白质链的柔韧性[26]。热处理使Ca-WPC纳米纤维聚合物形成了更加稳定的聚合结构,提高了纤维细丝的柔韧性,因此具有更好的起泡性。在Ca-WPC常规聚合物形成过程中二硫键占主导作用,并通过钙桥进行连接,经热处理后这种聚合结构不稳定,导致其起泡性随着热处理时间的延长不断下降。
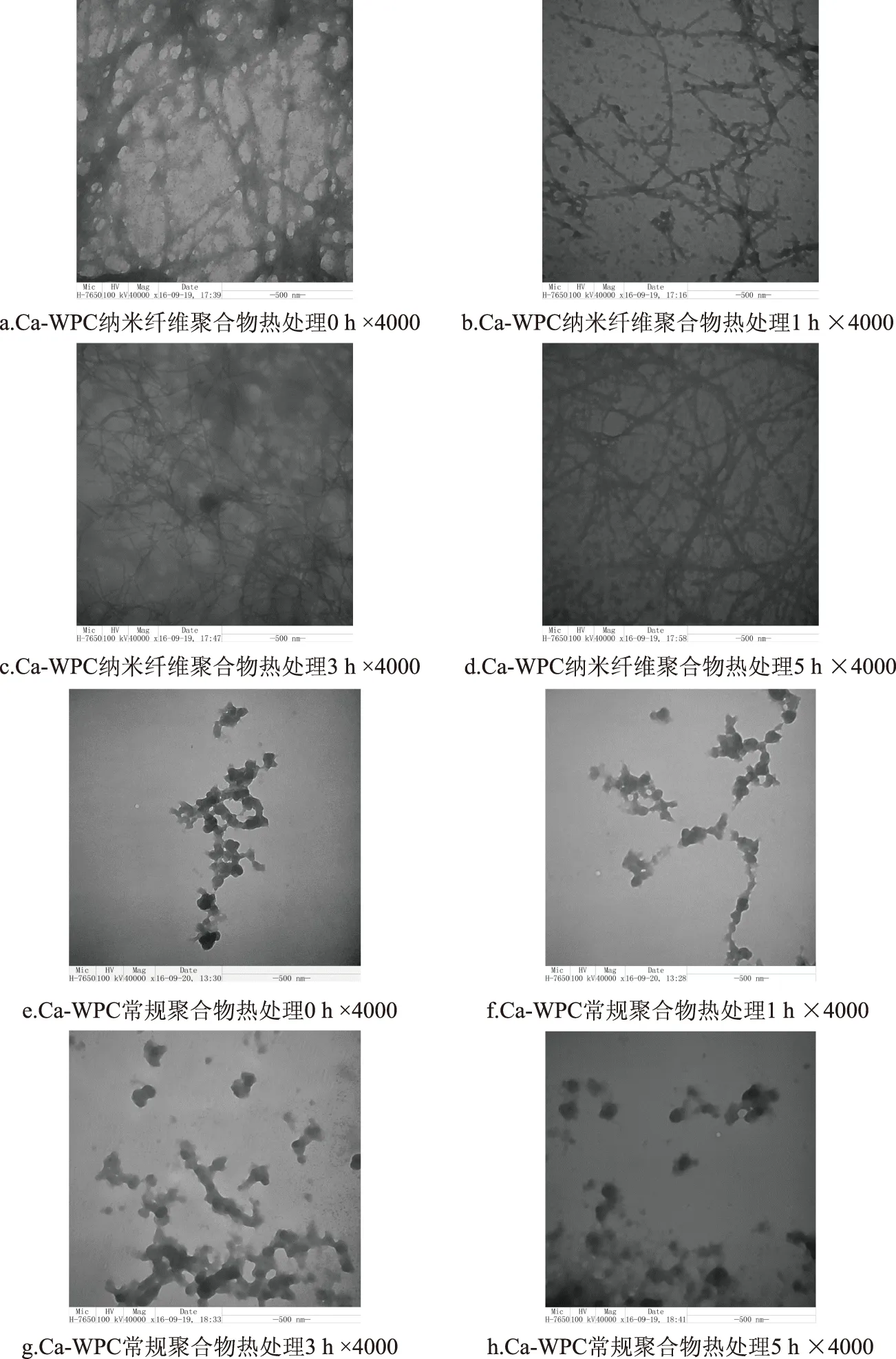
图5 不同蛋白聚合物的透射电镜图Fig.5 The TEM pictures of different protein aggregates
3 结论
与Ca-WPC常规聚合物相比,Ca-WPC纳米纤维聚合物的起泡性在热处理3 h时明显提高。这一结果可能是因为热处理3 h时Ca-WPC纳米纤维聚合物的表面疏水性大幅度升高,疏水基团暴露,WPC纳米纤维与Ca通过吸附或者镶嵌的方式形成更加稳定的Ca-WPC纳米纤维聚合物,这种新型聚合物对热的耐受能力较强,且分子柔性较高,从而提高了起泡性。而Ca-WPC常规聚合物主要通过钙桥这种较弱的非共价键作用,在经过热处理后其结构被破坏,导致起泡性变差。
[1]Nicrescu I,Vial C,Talansier E,et al. Comparative effect of thermal treatment on the physicochemical properties of whey and egg white protein foams[J]. Food Hydrocolloid,2011,25:797-808.
[2]Zayas J F. Foaming properties of proteins in functionality of proteins in food[J]. Berlin:Springer-Verlag,1997,12:260-309.
[3]Croguennec T,Renault A,Beaufils S,et al. Interfacial properties of heat-treated ovalbumin[J]. Journal of Colloid and Interface Science,2007,315:627-636.
[4]Damodaran S,Anand K,Razumovsky L. Competitive adsorption of egg white proteins at the air-water interface:direct evidence for electrostatic complex formation between lysozume and other egg proteins at the interface[J]. Journal of the Science of Food and Agriculture,1998,46:872-876.
[5]Wierenga P A,Kosters H,Egmond M R,et al. Importance of physical vs. chemical interations in surface shear rheology[J]. Advances in Colloid and Interface Science,2006,119:131-139.
[6]Raikos V,Campbell L,Euston S R. Effects of sucrose and sodium chloride on foaming properties of egg white proteins[J]. Food Research International,2007,40:347-355.
[7]Ercelebi E A,Ibanoglu E. Effects of ionic strength on the foaming properties of whey protein isolate and egg white in the presence of polysaccharides[J]. Journal of Food Processing and Preservation,2009,33:513-526.
[8]Bolder S G,Vasbinder A J,Sagis L M C. Heat-induced whey protein isolate fibrils conversion,hydrolysis,and disulphide bond formation. Int.Dairy[J].2007,17:846-853.
[9]Loveday S M,Wang X L,Rao M A,et al. Factors affecting rheological characteristics of fibril gels:The case ofβ-Lactoglobulin andα-Lactalbumin. Int.Dairy[J].2010,20:571-579.
[10]Loveday S M,Wang X L. Effect of calcium on morphology and functionality of whey protein nanofibrils[J]. American Chemical Society,2011,12:3780-3788.
[11]Durand D,Gimel J. Aggregation,gelationand phase separation of heat denatured globular proteins[J].Physica A,2002,304:253-265.
[12]Langton M,Hermansson A M. Fine-stranded and particulate gels ofβ-lactoglobulin and whey-protein at varying pH[J]. Food Hydrocolloids,1992,5:523-539.
[13]Bolder S G,Sagis L M C,Venema P. The critical aggregation concentration ofβ-Lactoglobulin-Based fibril formation[J]. Agric Food Chem,2007,55:5661-5669.
[14]Loveday S M,Wang X L,Rao M A,et al. Effect of pH,NaCl,CaCl2and Temperature on Self-Assembly ofβ-Lactoglobuliin into Nanofibrils:A Central Composite Design Study[J]. Agric Food Chem,2011,59:8467-8474.
[15]Loveday S M,Wang X L,Rao M A,et al.β-Lactoglobulin nanofibrils:Effect of temperature on fibril formation kinetics,fibril morphology and therheological properties of fibril dispersions. Food Hydrocolloids,2012,27(1):242-249.
[16]Richert S H,Morr C V,Cooney C M. Effect of heat and other factors upon foaming properties of whey protein concentrates[J]. Food Sci,1974,39:42-48.
[17]高育哲.结构修饰对乳蛋白纤维聚合物形成的影响及其机理的研究[D]. 哈尔滨:东北农业大学,2014.
[18]李波杨,徐红华,王楠楠,等.纳米纤维对乳清浓缩蛋白凝胶形成的诱导作用[D]. 哈尔滨:东北农业大学,2016.
[19]Stiegr M,Richtering W,Pedersen J S,et al. Small-angle neutron scattering study of structural changes in temperature sensitive microgel colloids[J]. The Journal of chemical physics,2004,120:61-97.
[20]Ni Y Z,Wen L J,Wang L,et al. Effect of temperature calcium and protein concentrate on aggregation of whey protein isolate:Formation of gel-like micro-particles[J].International Dairy Journal,2015,51:8-15.
[21]Krebs M R H,Devlin G L,Donald A M. Amyloid fibril-like structure underlies the aggregate structure across the pH range forβ-lactoglobulin[J]. Biophysical Journal,2009,96(12):5013-5019.
[22]赵新淮,徐红华,姜毓君,等. 食品蛋白质:结构,性质与功能[M]. 北京:科学出版社,2009.
[23]Forgeding E A,Luck P,Davis J. Factors determining the physical properties of protein foams[J]. Food Hydrocolloids,2006,20:284-292.
[24]Nakai S,Ho L,Helbig N,et al. Relationship between hydrophobicity and emulsifying properties of some plant proteins[J].Can Inst. Food Sci Technol,1980,13:23.
[25]Townsend A,Nakai S. Relationships between hydrophobicity and foaming characteristics of food proteins[J]. Journal of Food Science,1983,48:588.
[26]Kato A,Ibrahim H R.,Watanabe H,et al. New approach to improve the gelling and surface functional properties of dried egg white by heating in dry state[J]. Joural of Agricutural and Food Chemistry,1989,37:433-437.
Effect of heat treatment on the foaming properties of Ca-whey protein concentrate nanofibrils
WANG Nan-nan,XU Hong-hua,DONG Shi-rong,XIE Ming-ming
(College of Food Science,Northeast Agricultural University,Harbin 150030,China)
The effect of different heating time(0,1,2,3,4,5 h)on the foaming properties of Ca-namofibrils polymer was investigated in this paper. The results showed that the foaming ability of Ca-namofibrils polymer reached a maximum value of 96.00%±0.02% at heating 3 h,the foaming ability of Ca-namofibrils polymer was 2.13 times that of Ca-WPC polymer. The foam stability of Ca-WPC polymer after the heat treatment were zero.While the foam stability of Ca-namofibrils polymer was increased and then decreased with the increasing of heating time and reached a maximum value of 62.38%±1.51% at heating 3 h.So heating a certain time can significantly improve the foaming properties of Ca-namofibrils polymer.
whey protein concentrate;calcium;Ca-namofibrils polymer;heat treatment;foaming properties
2016-12-27
王楠楠(1991-),女,硕士, 研究方向:食品科学方向,E-mail:15114501270@163.com。
*通讯作者:徐红华(1969-),女,博士,教授,研究方向:食品科学与营养方向,E-mail:xhh316@126.com。
国家自然基金项目(31471682)。
TS201.1
A
1002-0306(2017)11-0092-05
10.13386/j.issn1002-0306.2017.11.009
