全湿法短流程高纯银的制备工艺
2017-06-15汪秋雨胡意文黄绍勇吕喜聪孙敬韬
汪秋雨,何 强,胡意文,王 日,黄绍勇,吕喜聪,孙敬韬,蔡 琥
全湿法短流程高纯银的制备工艺
汪秋雨1, 3,何 强1,胡意文1,王 日1,黄绍勇2,吕喜聪2,孙敬韬2,蔡 琥3
(1. 江西铜业集团公司江西铜业技术研究院有限公司,南昌 330096;2. 江西铜业集团公司贵溪冶炼厂,贵溪 335424;3. 南昌大学化学学院,南昌 330031)
以铜阳极泥中间物料分金渣为原料,提出一种“亚钠分银−酸化沉银−净化除杂−银粉还原”的全湿法短流程制备高纯银粉的新工艺。对工艺的机理及最佳工艺条件进行研究,在最佳工艺条件下,银的浸出率达到98.4%,粗氯化银中杂质元素Pb和Te的脱除率分别为97.7%和96.7%,银的直收率到达98.1%。采用OES、XRD、SEM检测方法对产物的化学成分、表观形貌和晶体结构分析。结果表明:制备出颗粒均匀的99.995%高纯银粉。
铜阳极泥;分金渣;全湿法;短流程;高纯银粉
白银是高新技术产业所必须的基础材料之一,广泛应用于超导体材料、导电架料、复合材料、催化剂、医药、抗菌材料等众多领域[1−2]。我国98%的白银是从各类有色金属矿冶炼阳极泥中回收,铜阳极泥是铜电解精炼过程中主要副产品,是提取贵金属银的最主要原料之一,采用清洁环保、高效、低成本的工艺回收铜阳极泥中的有价资源意义重大。国内外工业化应用的铜阳极泥处理工艺主要有3大类[3]:一是以火法为主,湿法、火法相结合的火法工艺;二是全湿法工艺;三是以湿法为主,火法、湿法相结合的(半)湿法工艺。国外多以波立登火法冶炼工艺处理阳极泥,而我国多采用“硫酸化焙烧−水浸分铜−碱浸分碲−氯化分金−亚钠分银−甲醛还原−银电解精炼”的半湿法工艺。
随着矿产资源的日趋短缺,低品位矿、复杂铜矿、废杂铜等被作为铜冶炼原料使用,使得铜阳极泥成分日趋复杂,我国现有半湿法铜阳极泥处理工艺对原料适应性差的问题日渐凸显,其中金属银因Te、Pb等杂质元素含量超标,而导致1号银锭达标率不到25%的问题尤为突出[4]。造成上述问题的主要原因是铜阳极泥预处理工艺、银分离提取和银电解精炼工艺难以满足成分日趋复杂铜阳极泥的处理要求[5−8]。现有铜阳极预处理工艺对Cu、Sb、Bi、As、Se等元素的分离提取效果明显。但铜阳极泥中的Pb没有实现开路处理,主要以硫酸铅和氯化铅的形式存在于铜阳极泥处理的整个工艺过程中,严重影响了银产品质量。此外现有碱浸分碲的工艺受到回转窑焙烧工艺的影响严重,Te的浸出率一般不到60%,大量碲残留在分碲渣中,最终导致银阳极板中Te杂质含量高。电解银粉的质量主要受阳极板质量影响[9],银阳极板中铅和碲等杂质元素过高时,容易造成电解银粉中Te和Pb杂质含量超标。此外,现有半湿法工艺的银提取分离及电解精炼工艺生产周期长,易造成资金积压;银阳极板熔铸和银电解能耗量大,硝酸银电解液制备成本高;硝酸银电解过程中容易发生副反应生成二氧化氮的棕红色有毒气体,环保污染严重。
针对我国半湿法铜阳极泥处理工艺中银提取、提纯存在的问题,研制出一种“亚钠分银−酸化沉银−净化除杂−银粉还原”高纯银粉的新工艺,以铜阳极泥处理中间物料分金渣为原料,全湿法短流程直接制备4N5级高纯银粉,为取消银电解精炼工艺,解决现有铜阳极泥处理工艺中存在的原料适应性差、银一级品率低、银电解工艺能耗大、生产周期长、环境污染等问题提供实验和理论依据。
1 实验
1.1 原料
分金渣主要化学成分如表1所列,主要含有银、铅、锡、钡以及少量的碲、锑、铜等其他元素,XRD谱(见图1)显示银主要以AgCl存在、铅主要以PbSO4以及少量的PbCl2形式存在,由于Te的含量只有0.98%,难以观察其在分金渣中的物相。
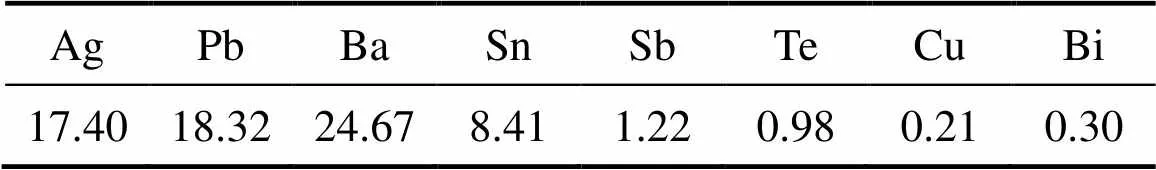
表1 分金渣化学成分
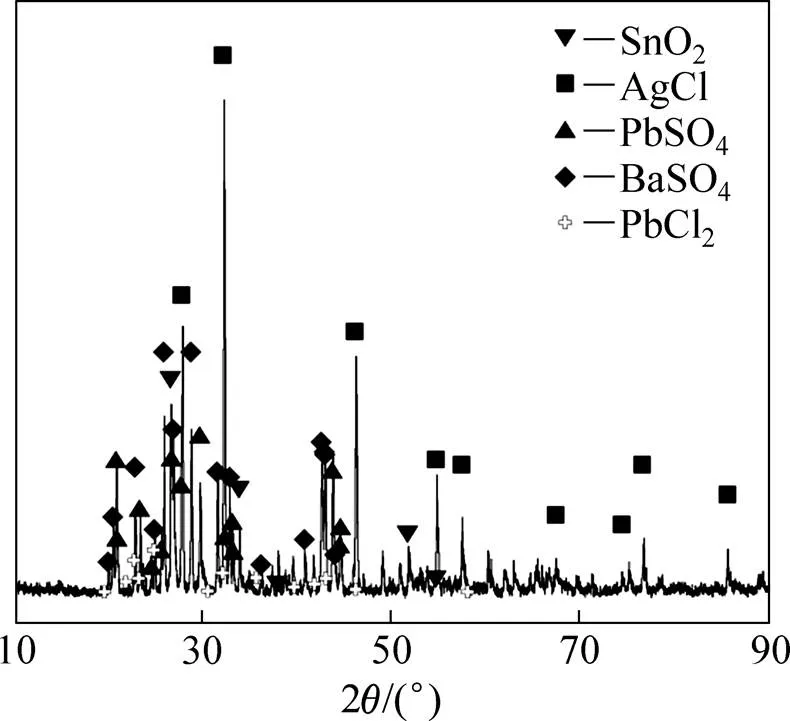
图1 分金渣XRD谱
1.2 主要设备
实验中用到的检测设备:原子发射光谱仪(SPECTROLAB M11),电感耦合等离子光谱分析仪(5100 ICP-OES),X射线衍射光谱仪(XRD, Rigaku, D/max-RB),扫描电子显微镜(JSM-6510)。实验设备:恒温水浴锅(HH-S1),电动搅拌机(JB-90D),实验室用烘箱(DHG-9023A),真空泵等。
1.3 试验方法
用70 ℃的热水将分金渣清洗至洗液pH终点为7,烘干磨粉备用。取5 kg分金渣,配制250 g/L亚硫酸钠溶液(pH=8.0),控制液固比为8:1(8 L:1 kg),反应温度为40 ℃,搅拌转速为300 r/min的条件下反应2 h,反应结束后过滤分离得到分银液和分银渣,并对其进行化学成分分析,计算银的浸出率;取分银液为原料,加入分析纯硫酸调整溶液pH沉淀氯化银,过滤分离获得粗氯化银和沉银后液,对沉银后液进行成分分析;取粗氯化银为原料,控制液固比、净化剂加入量、初始酸度、反应温度、反应时间等条件对氯化银净化除杂;精制氯化银在液固比为4:1,碱溶度为40 g/L的碱液中用水合肼直接还原成银粉,银粉热水洗涤至中性,烘干后进行成分分析。
2 结果与讨论
2.1 亚钠分银和酸化沉银
从含氯化银物料中分离提取银的主要湿法工艺有氨浸法[10−11]、碳酸钠转型−氨浸法[12]、硫代硫酸钠 法[13]、亚钠分银法[14]。采用氨浸法分离提取银的同时,分金渣中的铅会消耗大量氨、粗银粉铅含量高纯度仅为99%左右,需要电解精炼工艺提纯;“碳酸钠转 型−氨浸法”是在氨浸分离提取银之前,采用碳酸钠将硫酸铅转型成碳酸铅,再进行氨浸分银解决铅消耗氨的问题,但该工艺流程长,银氨溶液储存过程中易生成不稳定易爆炸的雷银,分离后的铅化合物需另外处理,银纯度依然达不到99.99%;硫代硫酸钠法存在选择性差、设备复杂、银杂质含量高,需要电解精炼工艺才能获得高纯银。亚硫酸钠分银工艺是较为理想的分银工艺,具有银浸出率高、选择性好、操作条件环保等优点。目前工业上分金渣中银的分离提取工艺是“亚钠分银−甲醛还原”工艺,存在氯离子未实现开路处理,还原后液(亚硫酸钠溶液)循环浸出氯化银的过程中,溶液中不断积累的氯离子导致浸银效率逐渐变差[15]的问题。
本文作者提出的“亚钠分银”和“酸化沉银”相结合工艺,实现分金渣中氯化银的高效浸出分离,Cl−实现开路而不在亚硫酸钠溶液中富集,亚硫酸钠溶液能够多次循环使用。控制亚硫酸钠溶液pH为8.0浸出分金渣,发生如反应式(4)~(6)的正反应,分金渣中的氯化银与亚硫酸钠络合生成亚硫酸银离子,亚硫酸银络合离子和氯离子一同进入溶液(分银液),而Pb、Te等杂质不与亚硫酸钠发生络合反应,实现银的选择性浸出;取分银液为原料,加入硫酸控制分银液的pH值,发生如化学反应式(1)和(2)的逆反应发生,溶液中SO32−浓度降低,促使分银液中[Ag(SO3)]−、[Ag(SO3)2]3−、[Ag(SO3)3]5−分解,发生反应式(3)~(6)的逆反应,游离态的Ag+由与分银液中的Cl−生成AgCl沉淀析出,过滤分离得到粗氯化银和沉银后液;沉银后液加入液碱调整pH至8.0,发生反应式(2)正向反应,再生亚硫酸钠循环使用。
SO2+H2OHSO3−+H+(1)
HSO3−SO32−+H+(2)
AgClAg++Cl−(3)
Ag++SO32−[Ag(SO3)]−(4)
Ag++2SO32−[Ag(SO3)2]3−(5)
Ag++3SO32−[Ag(SO3)3]5−(6)
表2所列为分银液的主要化学成分,银离子的浓度为21.4 g/L,根据分银液体积和银离子浓度,计算出银的亚硫酸钠浸出率为98.4%。

表2 分银液化学成分
图2所示为分银液中银离子浓度与溶液pH值的关系,分银液初始pH值为8.0,银含量为21.4g/L。随着溶液pH的降低银离子含量呈递减的规律,当 5.0<PH<7.2时,溶液中银离子浓度快速降低;当 pH<4.0时,溶液中银离子浓度下降趋势减缓;溶液pH越低银离子沉淀越完全。因为亚硫酸钠溶液中存在SO2、HSO3−和SO32−的可逆反应(反应式(1)和(2)),当PH<1.9时,主要以SO2的形式稳定存在;当1.9< pH<7.2时,主要以HSO3−的形式稳定存在;当溶液中的PH>7.2时,主要以SO32−的形式稳定存在[16]。因此,当分银液pH<7.2时,H2O-SO32−系中溶液的稳定区域由SO32−移至HSO3−区域,络合物释放出大量的银离子,与溶液中过量的氯离子生成氯化银沉淀,使溶液中银离子浓度快速降低,当pH低至4.0后溶液中的银离子基本沉淀完全。

图2 银离子浓度与溶液pH的关系
取分银液加入硫酸分别控制溶液终点pH分别为4.0、3.5和3.0进行3组酸化沉银试验,对沉银后液中银离子浓度进行检测,其结果表明溶液中的银离子浓度都小于10 mg/L,银的沉淀率达到99.9%以上。分银液的pH过低容易生成SO2气体造成环境污染,为了保证溶液中银离子完全沉淀同时不出现SO2气体,酸化沉银的终点pH值选择控制在3.0~4.0之间。
图3所示为酸化沉银后产物的XRD谱,结果表明产物为氯化银,表3所列为氯化银的化学成分,氯化银的平均纯度达到99.939%,但Pb、Te等杂质元素含量都较高,若直接用水合肼还原成金属银,将达不到1号银锭(国标IC—Ag99.99)标准,因此,必须进一步净化脱杂。

图3 氯化银XRD谱
2.2 净化除杂和银粉还原
目前,工业上多采用银电解精炼工艺[17−19],先还原制备银粉浇铸成银阳极板,再经电解精炼获得到高纯银,存在生产周期长、原料适应性差、资金积压、环境污染等问题[20−21]。新工艺采取对氯化银进行净化除杂先制备出高纯氯化银,然后直接还原制备4N5级高纯银粉,不再经过银电解精炼提纯。根据AgCl在盐酸介质中稳定性(sp=1.8×10−10,=25 ℃)好的特点,采用在盐酸介质下添加净化剂对AgCl进行净化除杂处理。净化剂在盐酸介质中具有强氧化性,可将AgCl中其中杂质元素M被氧化成MCl可溶性氯化物,从而实现杂质脱除的目的。氯化银中难以深度脱除的杂质主要是Te和Pb元素,净化除杂的过程中Te及其化合物能够被氧化溶解在盐酸溶液而被除去,根据PbCl2随着盐酸溶度和高温升高溶解度增大的特点,控制反应在一定的酸度和温度下,就能够实现Pb的深度脱除,达到净化提纯AgCl。新工艺具有原料适应性强、生产周期短、清洁环保、产品为4N5级高纯银粉的 优点。

表3 氯化银化学成分
以粗氯化银为原料,其化学成分如表3所示,控制液固比为5:1,研究净化剂加入量、初始酸度、反应温度、反应时间条件对氯化银净化除杂效率的影响,确立最佳的净化条件。根据原料成分、浸出液成分及体积,按照式(7)计算Te和Pb的浸出率:
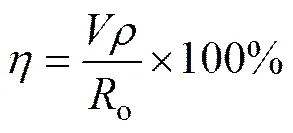
式中:为浸出率;o为原料中元素的含量;为浸出液体积;为浸出液中元素的质量浓度。
控制液固比为5:1、初始酸度为3.0 mol/L、反应温度为70 ℃、反应时间为3.0 h时,考察初净化剂加入量对杂质Pb和Te的脱除效果和溶液中银离子浓度变化,其结果如图4所示。净化剂加入量对Pb和Te的脱除效果影响较大,随着净化剂量的增加,净化剂浓度从2.5 g/L提高至10 g/L时,溶液中Pb和Te的溶度分别从51 mg/L和6 mg/L提高至65 mg/L和28 mg/L,净化剂浓度达到10 g/L以后趋于平缓。根据浸出率计算式(7),计算出当净化剂浓度为10 g/L时,Pb和Te的脱除率分别达到91.8%和92.7%,而银离子的浓度小于10 mg/L,为保证杂质脱除的同时尽量降低净化剂用量,认为最佳净化剂浓度为10 g/L。
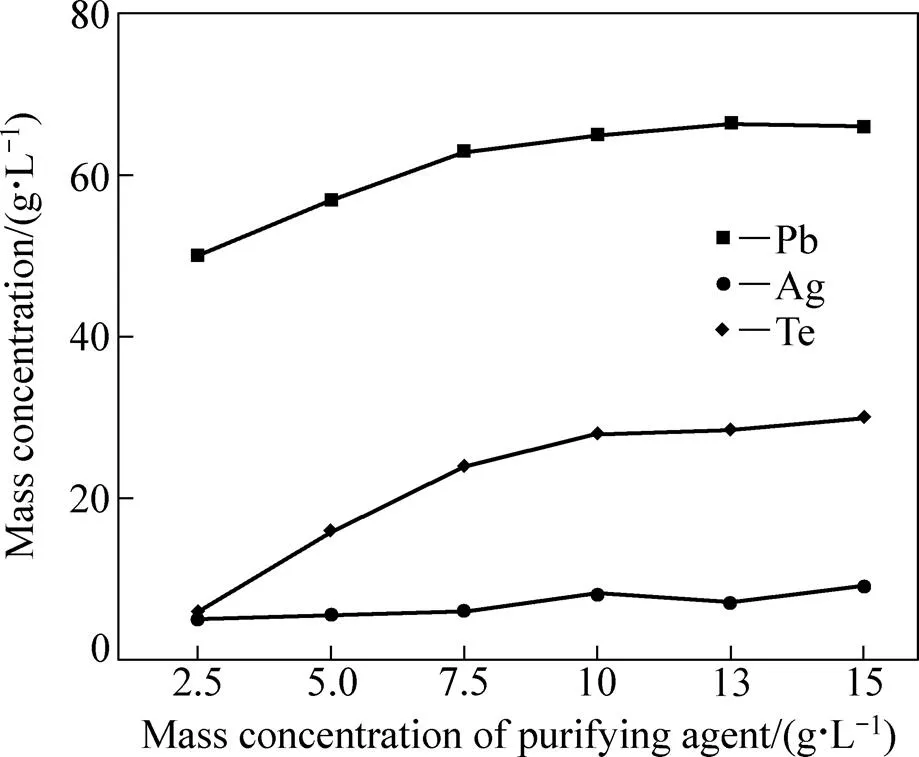
图4 净化剂与Pb、Te和Ag质量浓度的关系
控制液固比为5:1、净化剂浓度为10 g/L、反应温度为70 ℃、反应时间为3.0 h时,考察初始酸度对浸出率的影响。铅离子(Pb2+)和银离子(Ag+)与氯离子存在一系列的络合反应[22−23],Pb2++Cl−=PbCl2−n(=1,2,3,…),Ag++Cl−=AgCl1−n(=1,2,3,…),氯离子浓度越高,铅转化成可溶性络合离子的量就越多。盐酸作用是提供了Cl−和H+,因此,高浓度的盐酸有利于Pb脱除,但过高的Cl−会使银被络合进入溶液造成银的损失。图5结果显示,盐酸浓度达到3.5 mol/L时,铅的溶度为67 mg/L,而此时银离子浓度也达到23 mg/L。在保证银回收率的前提下,尽可能地提高盐酸的浓度,以达到Pb和Te脱除目的。选择控制溶液中盐酸的浓度为3.0 mol/L较为合理,溶液中铅和碲的浓度分别为63 mg/L和29.4 mg/L,此时溶液中银离子浓度只有8.5 mg/L,银的损失量较低。
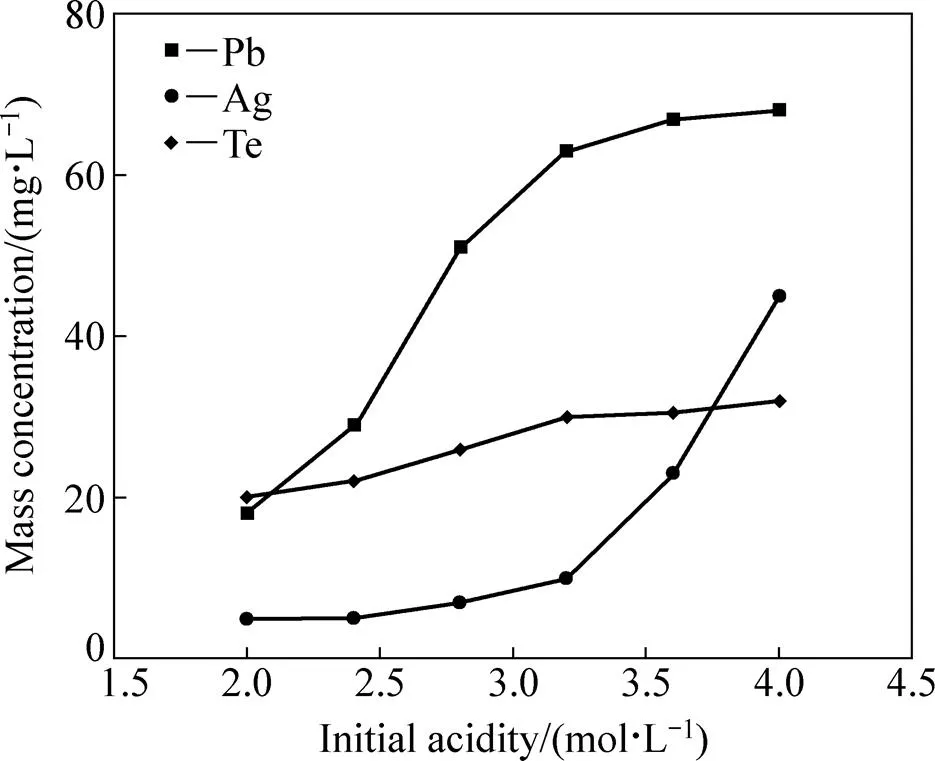
图5 初始酸度与Pb、Te和Ag质量浓度的关系
控制液固比为5:1、净化剂浓度为10 g/L、初始酸度为3.0 mol/L、反应时间为3.0 h,考察反应温度对浸出率的影响。图6所示为反应温度从60 ℃至70 ℃范围内溶液中Pb、Te浓度呈递增趋势,温度达到70 ℃以后Te浓度基本稳定,而铅浓度依然在升高直至80 ℃才趋于稳定,结果表明在反应温度70 ℃时,Te就能够基本被脱除,而Pb需要温度达到80 ℃才能基本被脱除完全,温度对银的损失影响不大。主要由于净化剂氧化性受溶液温度和酸度影响,在一定酸度条件下随着温度的升高其氧化性越强,反应温度达到70 ℃净化剂就达到了理想氧化脱Te效果,温度再高对Te脱除效果不明显,而氯化铅的溶解度随着温度的变化较大,温度越高其溶解度越大,越有利于铅的脱除,认为合理的反应温度为80 ℃。

图6 反应温度与Pb、Te和Ag质量浓度的关系
控制液固比为5:1、净化剂浓度为10 g/L,初始酸度为3.0 mol/L、反应温度为80 ℃,考察反应时间对浸出率的影响。图4所示为反应时间对净化除杂影响不大,当反应达到1.5h以后,Pb、Te和Ag离子浓度都趋于稳定,此时,Pb和Te离子浓度分别为65.4和28.1 mg/L,根据浸出率计算式(7),计算出Pb和Te浸出率分别为92.4%和93.0%。为了保证杂质元素彻底脱除,认为较为合理的反应时间为2 h。
根据以上研究结果确定净化除杂最佳工艺条件:净化剂浓度为10 g/L、初始酸度为3 mol/L、反应温度80 ℃、浸出反应时间2.0 h。
氯化银的还原剂包括水合肼、甲醛、活性金属 等[24],甲醛为有毒物质存在环境污染的问题,活性金属置换容易引入杂质元素,水合肼具有还原效率高、反应时间短、清洁环保、不引入其它杂质等优点,因此新工艺选用水合肼为还原剂,其反应机理如化学式(8)所示。
4AgCl+N2H4+4NaOH→4Ag↓+N2↑+4NaCl+4H2O (8)
宋裕华等[25]研究水合肼还原氯化银提取银的方法,本文作者在此基础上确定水合肼还原氯化银的最佳反应条件:NaOH的浓度为40 g/L,水合肼用量为理论量的1.1~1.2倍,反应时间45 min,氯化银的还原率达到99.9%以上。

图7 反应时间与Pb、Te和Ag质量浓度的关系
2.3 优化试验
取酸化沉淀的粗氯化银为原料,原料成分如表3所示,控制净化剂的浓度为10 g/L、初始酸度3 mol/L、液固比为5:1、反应温度为80 ℃、反应时间为2 h,反应结束后用80 ℃蒸馏水过滤洗涤氯化银,洗液至终点pH为7.0。精制氯化银在水合肼浓度为70 g/L,液固比为4:1,碱浓度为40 g/L,反应时间为45 min的条件下还原。表4为高纯银粉的化学成分检测结果,6组试验银的主品位含量都达到99.995%以上,各杂质含量都达到国家标准IC—Ag99.99(1号银锭),1号银锭达标率为100%。根据6组实验数据,计算出Pb和Te的平均浸出率分别为97.7%和96.7%,银的平均直收率达到98.1%。
对制备的产品进行了晶型结构和表观形貌的表征,图8所示为银粉经水洗、烘干后产物的XRD谱和SEM像。由图8(a)可看出,银粉的产物为单质Ag;银粉颗粒均匀平均粒径5 μm左右,说明制备出高纯银粉颗粒均匀,也进一步地验证了“亚钠分银−酸化沉银−净化除杂−银粉还原”的全湿法短流程高纯银粉制备新工艺可行性。
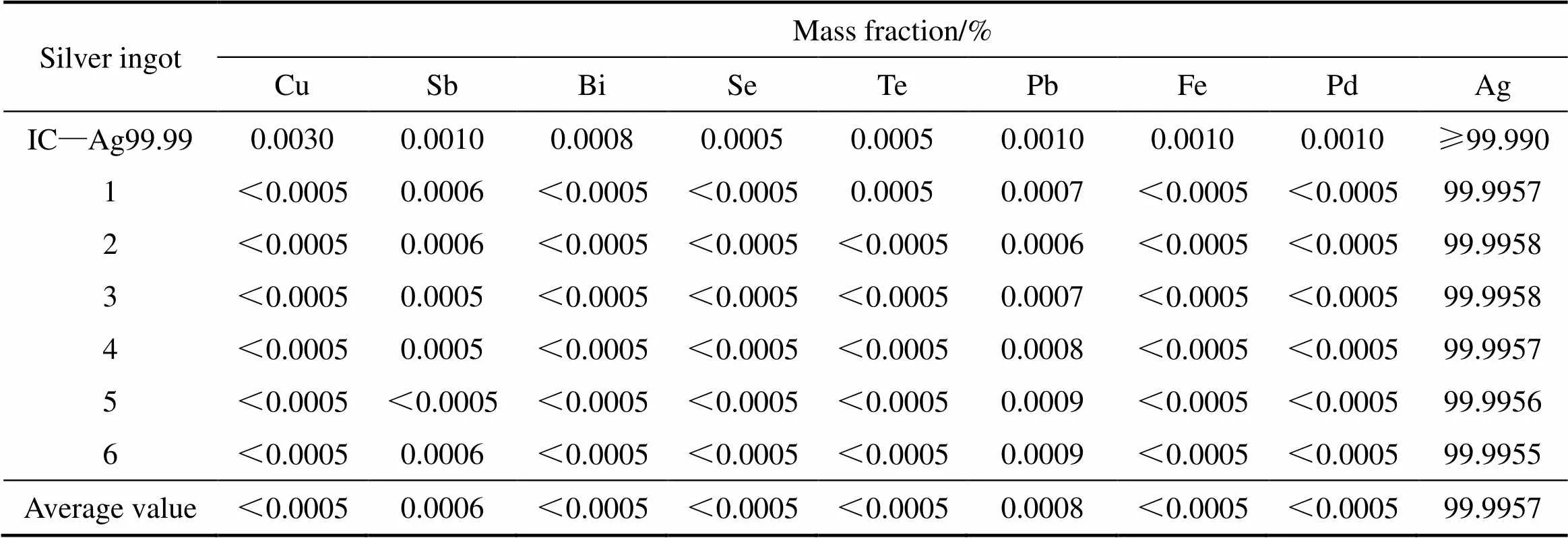
表4 高纯银粉化学成分
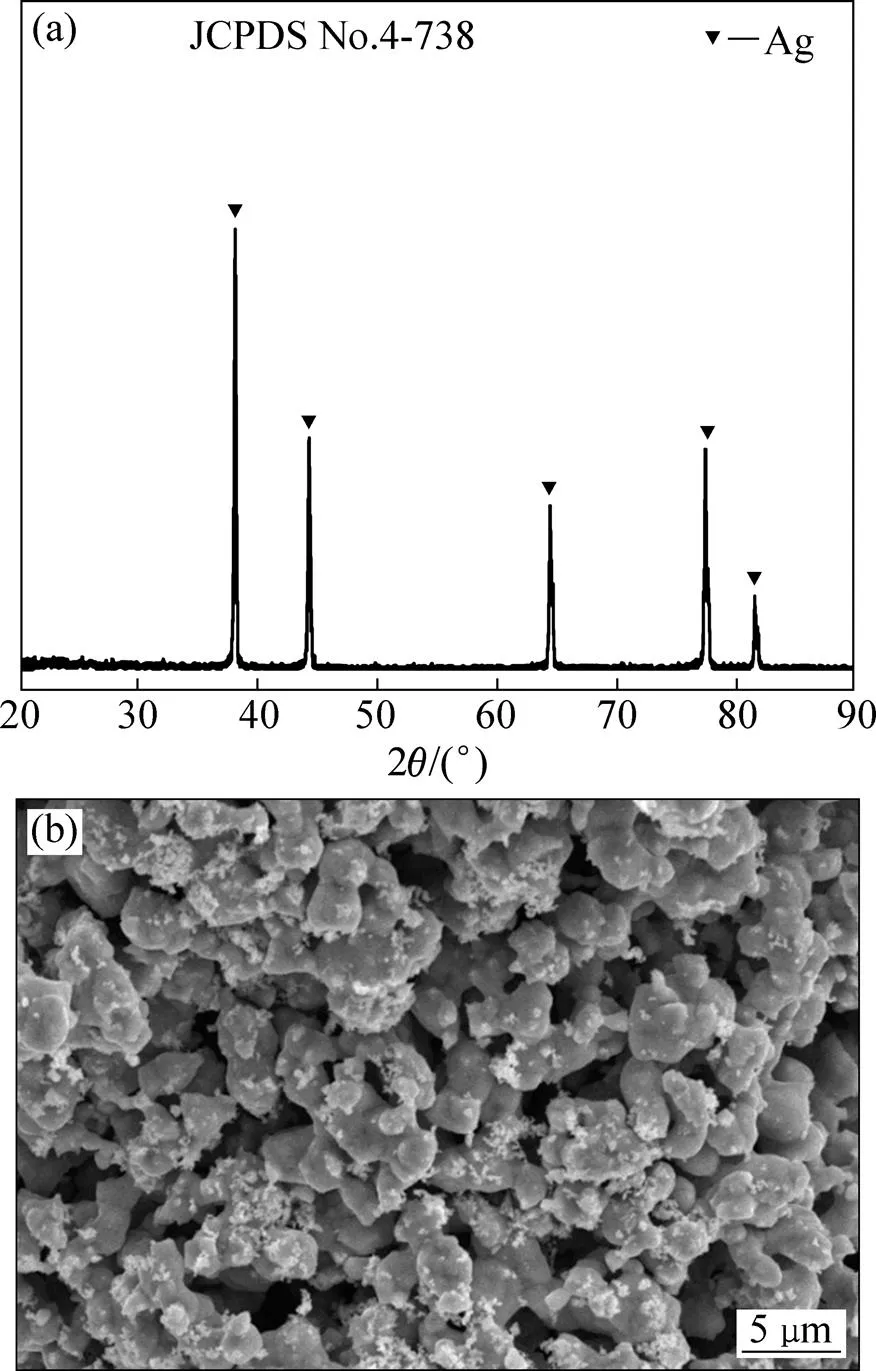
图8 银粉的XRD谱和SEM像
以高纯银粉制备新工艺取代现有“亚钠分银—甲醛还原—银阳极浇铸—银电解”的银提取提纯工艺,优化现有铜阳极泥处理工艺,银提取提纯的生产周期能够由6 d缩短至2 d,铜阳极泥总生产周期缩短1/3,由原来的12 d减为8 d,可以解决银电解精炼工艺生产周期长、工艺能耗大、环境污染严重的问题,实现不经过电解精炼工艺可直接制备4N5级高品质银粉。
3 结论
1) 提出一种“亚钠分银−酸化沉银−净化除杂−银粉还原”全湿法短流程直接制备4N5级高纯银粉新工艺,对工艺的机理及最佳工艺参数进行了研究,验证工艺的可行性。
2) 采用“亚钠分银”和“酸化沉银”相结合工艺,分金渣中银的浸出率为98.4%,控制分银液溶液pH值在3.0~4.0之间,银的沉淀率达到99.9%,沉银后液中银残留浓度低于10 mg/L,沉银后液加入液碱控制pH值为8.0可再生亚硫酸钠溶液循环使用。
3) 最佳净化除杂工艺条件下:净化剂浓度为 10 g/L、初始酸度为3 mol/L、反应温度80 ℃、浸出反应时间2.0 h,粗氯化银中杂质Pb和Te的脱除率分别为97.7%和96.7%,采用水合肼还原净化后的氯化银,制备的银纯度达到99.995%以上,银的直收率达到98.1%,且各杂质元素含量都达到国家标准 IC—Ag99.99,1号银锭达标率为100%。
4) 若以高纯银粉制备新工艺取代银电解工艺,优化现有铜阳极泥处理工艺,银提纯提取的生产周期由6 d缩短至2 d,铜阳极泥总生产周期缩短1/3,同时降低阳极泥处理工艺成本,提高对原料的适应性和银 品质。
REFERENCES
[1] 赵怀志. 银的主要应用领域和发展现状[J]. 云南冶金, 2002, 31(3): 118−123. ZHAO Huai-zhi. Main application fields of silver and current status of development[J]. Yunnan Metallurgy, 2002, 31(3): 118−122.
[2] 何发泉, 李勇军. 银粉的用途和制备[J]. 中国粉体技术, 2001, 7(3): 45−47. HE Fa-quan, LI Yong-jun. Application and preparation of silver powder[J]. China Powder Science and Technology, 2001, 7(3): 45−47.
[3] 王小龙, 张昕红. 铜阳极泥处理工艺的探讨[J]. 矿冶, 2005, 14(2): 46−48. WANG Xiao-long, ZHANG Xin-hong. Discussion on process for treating copper anode slime[J]. Mining and Metallurgy, 2005, 14(2): 46−48.
[4] 李建春. 提高银锭一级品率的技术实践[J]. 铜业工程, 2004(2): 31−33. LI Jian-chun. To improve the rate of the grade one silver ingot[J]. Copper Engineering, 2004(2): 31−33.
[5] 郑雅杰, 汪 蓓, 史建远, 孙召明, 刘昭成. 铜阳极泥预处理富集金银的研究[J]. 中南大学学报(自然科学版), 2010, 41(3): 865−870. ZHENG Ya-jie, WANG Bei, SHI Jian-yuan, SUN Zhao-ming, LIU Zhao-cheng. Pretreatment of copper anode slime for concentrating gold and silver[J]. Journal of Central South University (Science and Technology), 2010, 41(3): 865−870.
[6] 金哲男, 马致远, 杨洪英, 刘新建. 铜阳极泥全湿法处理过程中贵贱金属的行为[J]. 东北大学学报(自然科学版), 2015, 36(9): 1305−1309. JIN Zhe-nan, MA Zhi-yuan, YANG Hong-ying, LIU Xin-jian. Behaviors of precious and base metals in process of copper anode slime hydrometallurgical treatment[J]. Journal of Northeastern University (Natural Science), 2015, 36(9): 1305−1309.
[7] 郭学益, 肖彩梅, 钟菊芽, 田庆华. 铜阳极泥处理过程中贵金属的行为[J]. 中国有色金属学报, 2010, 20(5): 990−998. GUO Xue-yi, XIAO Cai-mei, ZHONG Ju-ya, TIAN Qing-hua. Behaviors of precious metals in process of copper anode slime treatment[J]. The Chinese Journal of Nonferrous Metals, 2010, 20(5): 990−998.
[8] 刘伟锋, 杨天足, 刘又年, 陈 霖, 张杜超, 王 安. 脱除铜阳极泥中贱金属的预处理工艺[J]. 中南大学学报(自然科学版), 2013, 44(4): 1332−1333. LIU Wei-feng, YANG Tian-zu, LIU You-nian, CHEN Lin, ZHANG Du-chao, WANG An. Pretreatment process for removing base metals from copper anode slime[J]. Journal of Central South University (Science and Technology), 2013, 44(4): 1332−1333.
[9] 浦忠民. 银电解精炼工艺研究[J]. 有色金属(冶炼部分), 2005(5): 41−42. PU Zhong-min. Study on Silver Electrolysis Refining Process[J].Nonferrous Metals (Extractive Metallurgy), 2005(5): 41−42.
[10] 蒙星辉, 柯家骏. 氨性溶液中Ag氧化浸取动力学研究[J]. 金属学报, 1987, 23(2): 190−197. MENG Xing-hui, KE Jia-jun. Kinetics of oxidation leaching of Ag in ammoniacal solutions[J]. Acta Metallurgica Sinica, 1987, 23(2): 190−197.
[11] 耿桂秀, 李 勤, 周晓勇, 高武成. 亚硫酸钠分银与氨浸分银工业实验[J]. 化学工程师, 2013(1): 63−66. GENG Gui-xiu, LI Qin, ZHOU Xiao-yong, GAO Wu-cheng. Industrial experiments of silver extraction by sodium sulfite and ammonia leaching[J]. Chemical Engineer, 2013(1): 63−66.
[12] 张小林, 李 伟, 宁 瑞. 用Na2SO3与NH3分银实验研究[J]. 有色金属科学与工程, 2014, 5(1): 63−67. ZHANG Xiao-lin, LI Wei, NING Rui. Siler separation by using Na2SO3and NH3[J]. Nonferrous Metals Science and Engineering, 2014, 5(1): 63−67.
[13] 张钦发, 龚竹青, 陈白珍, 李景升. 用硫代硫酸钠从分银渣中提取银[J]. 贵金属, 2003, 24(1): 5−9. ZHANG Qin-fa, GONG Zhu-qing, CHEN Bai-zhen, LI Jing-sheng. Extracting Ag from residue containing silver with Na2S2O3[J]. Precious Metals, 2003, 24(1): 5−9.
[14] 李义兵, 陈白珍, 龚竹青, 邓 川. 用亚硫酸钠从分银渣中浸出银[J]. 湿法冶金, 2003, 22(1): 34−38. LI yi-bing, CHEN Bai-zhen, GONG Zhu-qing, DENG Chuan. Leaching of Ag from residue containing silver with sodium sulfite[J]. Hydrometallurgy of China, 2003, 22(1): 34−38.
[15] 张杜超, 杜新玲, 杨天足, 杜作娟, 窦爱春. 氯化银在含氯离子的亚硫酸钠溶液中的浸出研究[J]. 贵金属, 2007, 28(3): 10−14. ZHANG Du-chao, DU Xin-ling, YANG Tian-zu, DU Zuo-juan, DOU Ai-chun. Study on leaching of silver chloride in sodium sulfite solution containing chloride ions[J]. Precious Metals, 2007, 28(3): 10−14.
[16] 陈小红, 赵祥麟, 楚 广, 周兆安, 杨天足, 苏 莎. 用亚硫酸钠从分银渣中浸出银[J]. 中南大学学报(自然科学版), 2014, 45(2): 356−360. CHEN Xiao-hong, ZHAO Xiang-lin, CHU Guang, ZHOU Zhao-an, YANG Tian-zu, SU Sha. Leaching of Ag from residue containing silver with sodium sulfite[J]. Journal of Central South University (Science and Technology), 2014, 45(2): 356−360.
[17] 王 日, 黄绍勇, 聂华平. 无铜离子电解制备高纯银新技术[J]. 湿法冶金, 2013, 32(5): 323−325. WANG Ri, HUANG Shao-yong, NIE Hua-ping. New technology for preparation of high purity silver by electrolysis using copper-ions free electrolyte[J]. Hydrometallurgy of China, 2013, 32(5): 323−325.
[18] 刘 丹, 李轶韬, 贺 昕, 熊晓东. 超高纯银的制备研究[J]. 贵金属, 2015, 36(3): 37−41. LIU Dan, LI Yi-tao, HE Xin, XIONG Xiao-dong. Study on preparation of super-pure silver[J]. Precious Metals, 2015, 36(3): 37−41.
[19] 刘晓刚, 甘卫平, 杨 超, 林 涛, 黎应芬. 太阳能电池用微细银粉的制备[J]. 中国有色金属学报, 2014, 24(4): 987−992. LIU Xiao-gang, GAN Wei-ping, YANG Chao, LIN Tao, LI Ying-fen. Preparation of ultra-fine silver powder utilized in solar cells[J]. The Chinese Journal of Nonferrous Metals, 2014, 24(4): 987−992.
[20] 刘 超, 王光忠, 赵红浩. 银电解车间酸雾治理研究与槽体设计[J]. 中国有色冶金, 2015(3): 57−59. LIU Chao, WANG Guang-zhong, ZHAO Hong-hao. Acid mist treatment and cell body design of silver electrolysis workshop[J]. China Nonferrous Metallurgy, 2015(3): 57−59.
[21] 万 斯, 陈 伟, 黄顺红, 王 兵, 李 倩, 朱安玲. 银电解精炼的清洁生产的实践[J]. 湖南有色金属, 2013, 29(1): 61−64. WAN Si, CHEN Wei, HUANG Shun-hong, WANG Bing, LI Qian, ZHU An-ling. Practice of clean production on electrolytical refinement of silver[J]. Hunan Nonferrous Metals, 2013, 29(1): 61−64.
[22] 刘云霞. PbCl2在不同盐酸浓度、Sb3+浓度和温度条件下溶解度的研究[J]. 稀有金属, 2000, 24(4): 270−272. LIU Yun-xia. Study on PbCl2solubility under different conditions of HCl concentration, Sb3+concentration and temperature[J]. Chinese Journal of rare metals, 2000, 24(4): 270−272.
[23] 郑蒂基, 傅崇说. 关于铅−氯离子−水系在高离子强度及升温条件下的平衡研究[J]. 中南矿冶学院学报, 1981(4): 1−9. ZHENG Di-ji, FU Chong-yue. Equilibrium study on the lead-chloride ion-water system at high ionic strength and elevated temperature[J]. Journal of Central South Institute of Mining and Metallurgy, 1981(4): 1−9.
[24] 贺小塘. 氯化银还原精炼技术[J]. 黄金, 1998, 19(2): 36−38. HE Xiao-tang. Technique of reducing refining of silver chloride[J]. Gold, 1998, 19(2): 36−38.
[25] 宋裕华, 王维国. 从氯化银中提取银的方法[J]. 黄金, 2013, 34(6): 57−59. SONG Yu-hua, WANG Wei-guo. Silver recovery from silver chloride[J]. Gold, 2013, 34(6): 57−59.
(编辑 李艳红)
Preparation technology of hydrometallurgical process high purity sliver powder
WANG Qiu-yu1, 2, HE Qiang1, HU Yi-wen1, WANG Ri1, HUANG Shao-yong2, LÜ Xi-cong2, SUN Jing-tao2, CAI Hu3
(1. Jiangxi Copper Technology Research Institute Co., Ltd., Jiangxi Copper Corporation, Nanchang 330096, China;2. Guixi Smelter, Jiangxi Copper Corporation, Guixi 335424, China;3. College of Chemistry, Nanchang University, Nanchang 330031, China)
The copper anode slime intermediate material gold separating residue was used as raw material and a new hydrometallurgical process of high purity sliver powder preparation was proposed, the process comprising following steps: sodium sulfite leaching silver, acidification deposit silver, purification and sliver reduction. The reaction mechanism and optimum conditions of process were investigated. Under the optimum conditions, the leaching rate of silver reaches 98.4%, the removal rates of impurity element Pb and Te in silver chloride reach 97.2% and 96.7%, respectively, and the direct recovery rate of Ag reaches 98.1%. The chemical composition, morphology and crystal structure of product were analyzed by optical emission spectrometry (OES), scanning electron microscopy (SEM) and X-ray diffractometry (XRD), respectively. The results show that high purity 99.995% silver powder with uniform morphology and particle is prepared.
copper anode slime; gold separating residue; full hydrometallurgy; short process; high purity sliver powder
Project(2012CBA01204) supported by the National Key Basic Research Special Foundation of China
2016-04-21; Accepted date: 2016-09-30
WANG Qiu-yu; Tel: +86-791-88196433; E-mail: wangqy_27@163.com
10.19476/j.ysxb.1004.0609.2017.05.022
1004-0609(2017)-05-1037-08
TF83
A
国家重点基础研究发展计划资助项目(2012CBA01204)
2016-04-21;
2016-09-30
汪秋雨,工程师,博士;电话:0791-88196433;E-mail:wangqy_27@163.com
