急诊经皮冠状动脉介入术后心肌灌注对心肌收缩功能恢复的预测价值
2017-06-01杨亚娟
杨亚娟
王 飞WANG Fei
莫 展MO Zhan
吴仰帆WU Yangfan
陈火梅CHEN Huomei
刘晓丹LIU Xiaodan
赖玉琼LAI Yuqiong
急诊经皮冠状动脉介入术后心肌灌注对心肌收缩功能恢复的预测价值
杨亚娟YANG Yajuan
王 飞WANG Fei
莫 展MO Zhan
吴仰帆WU Yangfan
陈火梅CHEN Huomei
刘晓丹LIU Xiaodan
赖玉琼LAI Yuqiong
目的探讨急诊经皮冠状动脉介入术(PPCI)后心肌微循环灌注水平对心肌收缩功能恢复程度的预测价值,以早期发现心肌无复流,改善患者不良预后。资料与方法选取49例接受PPCI治疗的急性心肌梗死(AMI)患者为研究对象,术后1周内行二维应变成像(2DS)、静息定性心肌声学造影(MCE)检查,术后3个月复查2DS。应用2DS测量各节段心肌收缩期纵向峰值应变(LPSS),并根据LPSS牛眼图彩色编码将左心室心肌分为收缩功能正常(红色)、收缩功能受损(浅红色、蓝色)心肌。应用MCE目测半定量法对各节段心肌进行灌注评分(MPS),并根据MPS将收缩功能受损心肌分为灌注良好、灌注减少、灌注缺失心肌。比较各灌注水平间△LPSS(3个月各节段心肌LPSS与术后1周的差值),同时将MPS分别与术后1周、术后3个月LPSS行相关性分析。结果△LPSS的组间比较为灌注良好心肌>灌注减少心肌>灌注缺失心肌[(-5.78±6.23)%比(-4.37±6.60)%比(-1.21± 4.77)%,P<0.05];PPCI术后1周心肌MPS与术后1周、术后3个月LPSS均呈正相关(r=0.47、0.58,P<0.001);2名评估者对心肌灌注评分一致性较好(Kappa=0.785,P<0.05)。结论AMI患者PPCI术后心肌灌注水平与心肌收缩功能相关,可预测心肌收缩功能恢复程度。
心肌梗死;急性病;血管成形术,经腔,经皮冠状动脉;超声心动描记术;造影剂;心肌再灌注;心肌收缩
急诊经皮冠状动脉介入术(primary percutaneous coronary intervention,PPCI)可及时开通梗死相关动脉(infarct-related artery,IRA),是治疗急性心肌梗死(acute myocardial infarction,AMI)的首选治疗措施[1]。然而,冠状动脉造影显示IRA的成功再通并不一定代表心肌水平的灌注恢复[2]。研究显示,PPCI术后心肌微循环灌注情况与心肌收缩功能恢复密切相关[3]。若能在PPCI术后早期对心肌微循环灌注进行评估,对患者制订临床决策、改善临床预后有重要指导意义。
心肌声学造影(myocardial contrast echocardiography,MCE)是一项评估心肌微循环灌注功能的无创超声心动图新技术,可充分反映局部心肌微循环灌注水平。二维应变成像(two-dimensional strain,2DS)可以更加客观、精确地定量评价局部心肌收缩功能。本研究应用静息定性MCE评价AMI患者心肌灌注水平,并用2DS对心肌收缩功能进行定量追踪复查,探讨AMI患者PPCI术后应用MCE预测心肌收缩功能恢复程度的可行性及应用价值,为PPCI术后治疗效果及远期预后提供预测价值。
1 资料与方法
1.1 研究对象 选取2013年1月—2014年6月入住佛山市第一人民医院心血管重症监护室的AMI患者49例,男43例,女6例;年龄42~80岁,平均(61.2±10.2)岁。纳入标准:①发病时间<12 h,有ST段抬高并行PPCI的AMI患者;②经冠状动脉造影术确诊冠状动脉至少1支主干75%以上狭窄,并在狭窄处成功实施冠状动脉支架置入,且术后IRA远端血流达到心肌梗死溶栓治疗(thrombolysis in myocardial infarction,TIMI)血流分级3级;③MCE检查能完整、清晰地显示左心室壁各节段心肌灌注情况;④图像质量好,斑点追踪心肌成功并获取2DS牛眼图。排除标准:①陈旧性心肌梗死、心肌纤维化形成、严重瓣膜病变、先天性心脏病伴心内分流、心肌病、心律失常、严重肺动脉高压、严重心外疾病;②食物、药物、白蛋白和其他血制品过敏;③PPCI术后IRA远端血流未达到TIMI 3级。所有患者均签署知情同意书。
1.2 仪器与方法 采用GE vivid E9超声诊断仪,探头M5S,频率1.5~4.3 MHz,具备心脏超声造影条件及自动功能成像功能(automated function imaging,AFI)。对AMI患者PPCI术后1周内及术后3个月行2DS检查。根据主动脉瓣血流频谱确定瓣口开放、关闭时间点,采集心尖左心室长轴切面、四腔心切面、二腔心切面各3个心动周期,启用AFI功能获取左心室收缩期纵向峰值应变(longitudinal peak systolic strain,LPSS)牛眼图。根据美国超声心动图协会推荐,将左心室壁分为17个节段,记录左心室各节段LPSS。根据各节段心肌在牛眼图所对应的彩色编码,将左心室心肌分为收缩功能正常心肌(红色)及收缩功能受损心肌(浅红色、蓝色)。LPSS数值为负值,负值越大代表心肌应变越大及收缩功能越好,目前对于正常心肌LPSS尚无统一标准[4]。本研究将LPSS≤-20%考虑为正常心肌,根据各节段心肌LPSS数值将收缩功能受损心肌进一步划分为轻度受损(≤-10%)、中度受损(-10%~0)、重度受损(>0%)。
超声造影剂选用Bracco SonoVue,用5 ml 生理盐水稀释,混合后用力振摇20 s,得到乳白色六氟化硫悬乳液,每次取2.5 ml 肘静脉推注,快速推注0.5 ml,剩余0.2 ml于2 min 内匀速推注,用5 ml 生理盐水以同样速度冲管。待造影剂在左心室心肌达到饱和状态时,按心尖四腔观、左心室长短轴等顺序扫查17节段,所有图像记录于磁光盘上,供进一步分析。由2名副主任医师应用双盲目测半定量法对心肌灌注进行评分(myocardial perfusion scores,MPS),当评分结果不一致时请上级主任医师进行评分使结果达成一致, 1分:心肌显影均匀增强;2分:心肌显影减少/不均/心内膜下心肌显影缺失;3分:心肌显影完全或大部分缺失。根据MPS将收缩功能受损心肌分为灌注良好(1分)、灌注减少(2分)、灌注缺失(3分)心肌[2]。
1.3 统计学方法 采用SPSS 17.0软件。所有计量资料经统计学分析均符合正态分布,2名评估者对心肌灌注评分结果的一致性采用Kappa检验;术后1周、术后3个月各计量资料比较采用配对设计t检验。灌注良好、灌注减少、灌注缺失3组心肌LPSS在术后1周、术后3个月差值(△LPSS)的组间比较采用单因素方差分析,两两比较采用LSD法。MPS与LPSS相关性采用Spearman秩相关分析。P<0.05表示差异有统计学意义。
2 结果
2.1 冠状动脉造影结果 所有患者于PPCI术后1周内,平均(2.92±1.41)d完成2DS、MCE检查。49例患者中,单支血管病变24例,双支血管病变19例,多支血管病变6例。所有患者均行PPCI,共置入支架67枚,其中前降支(left anterior descending,LAD)29枚、回旋支(left circum fl ex,LCX)13枚、右冠状动脉(right coronary artery,RCA)25枚;IRA 70支,经PPCI治疗后,所有IRA均为TIMI 3级(表1)。

表1 患者一般资料与冠状动脉造影结果
2.2 静息定性MCE对心肌收缩功能恢复程度的预测2.2.1 不同灌注水平组LPSS组内比较 2DS牛眼图显示收缩功能受损心肌共676个节段,其中灌注良好心肌416个节段(61.5%),灌注减少心肌157个节段(23.2%),灌注缺失心肌103个节段(15.2%)。PPCI术后3个月灌注良好心肌、灌注减少心肌、灌注缺失心肌LPSS均较术后1周提高(P<0.05),见表2、图1。2名评估者对心肌灌注评分一致性较好(Kappa=0.785,P<0.05)。
表2 PPCI术后1周、术后3个月LPSS比较(±s,%)
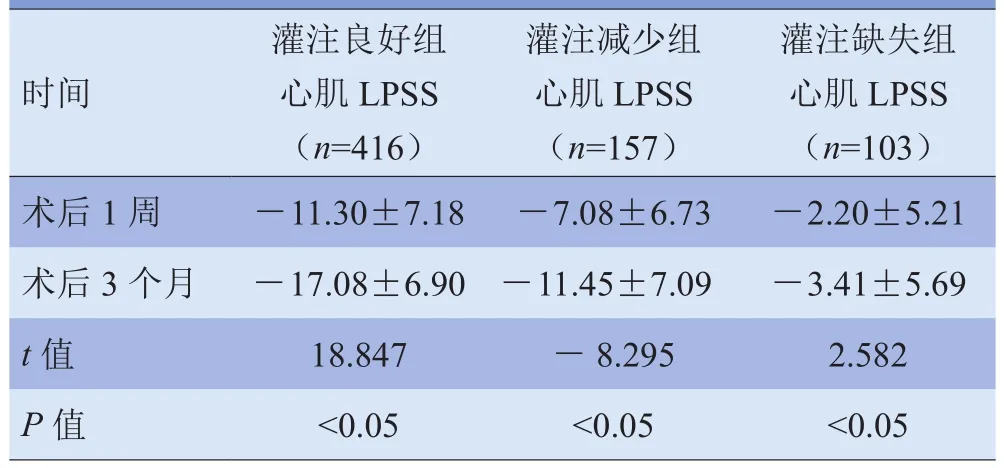
表2 PPCI术后1周、术后3个月LPSS比较(±s,%)
时间灌注良好组心肌LPSS(n=416)灌注减少组心肌LPSS(n=157)灌注缺失组心肌LPSS(n=103)术后1周-11.30±7.18-7.08±6.73-2.20±5.21术后3个月-17.08±6.90-11.45±7.09-3.41±5.69t值18.847-8.2952.582P值<0.05<0.05<0.05
2.2.2 各灌注水平组间△LPSS比较 术后3个月与术后1周△LPSS组间比较,差异有统计学意义(F=23.263,P<0.0001),各组心肌△LPSS比较,结果灌注良好心肌>灌注减少心肌>灌注缺失心肌[(-5.78±6.23)%比(-4.37±6.60)%比(-1.21±4.77)%,P<0.05],见图2。
2.2.3 不同程度收缩功能受损心肌3组间△LPSS比较将收缩功能受损心肌进一步划分为轻度受损(373个节段,55.2%)、中度受损(187个节段,27.6%)、重度受损(116个节段,17.2%),比较组内各灌注水平的△LPSS,结果显示组内各灌注水平差异有统计学意义(F=18.565、20.611、15.957,P<0.0001)。进一步将组内各灌注水平心肌△LPSS进行两两比较,结果当收缩功能轻、重度受损时,灌注良好心肌>灌注减少心肌>灌注缺失心肌(P<0.05);当收缩功能中度受损时,灌注良好心肌、灌注减少心肌>灌注缺失心肌(P<0.05),灌注良好心肌与灌注减少心肌差异无统计学意义(P>0.05),见表3。
2.3 心肌灌注与心肌收缩功能的相关性 PPCI术后1周内、术后3个月各灌注水平组心肌LPSS组间比较,差异有统计学意义(F=81.238、179.037,P<0.0001),进一步将各灌注水平组心肌LPSS进行两两比较,结果在术后1周内、术后3个月均为灌注良好心肌≥灌注减少心肌≥灌注缺失心肌(P均<0.001),见图3;且MPS与术后1周内、术后3个月LPSS呈正相关(r=0.47、0.58,P<0.001),见图4。
3 讨论
及时开通AMI患者IRA可挽救濒死的心肌、改善AMI患者的预后。研究显示,IRA经皮冠状动脉介入的开放率为75%[5]。当微循环完整性受损时,微血管痉挛、血栓栓塞、炎症细胞及坏死组织均可能导致微血管血流减少,这种现象称为无复流,PPCI中无复流发生率高达30%[6]。无复流现象是影响PPCI近期预后和远期心源性死亡及心脏不良事件发生的独立危险因素[7]。
目前临床工作中诸多检查可以评估心肌微循环灌注,如单光子发射计算机断层成像、心脏MRI、多层螺旋CT等[8];MCE相对于以上检查有许多潜在优势,因其具有无电离辐射、有良好的空间分辨率及时间分辨率、可重复进行、价格相对低廉等诸多优点在临床上广泛应用。
MCE是利用微气泡作造影剂反映某一区域心肌微循环的灌注情况,可用于检测存活心肌与坏死心肌,从而预测该区域心肌收缩功能恢复的潜能。大量研究显示MCE在评价AMI后心肌存活及预测局部与整体心肌收缩功能恢复中起着重要作用。Liu等[9]研究显示AMI患者行PCI后无论心肌灌注与否可以反映心肌收缩功能恢复的倾向;Kang等[10]对98例急性冠脉综合征患者研究发现MCE比心肌核素显像更能精确地诊断心肌缺血,可以更好地评价患者预后。
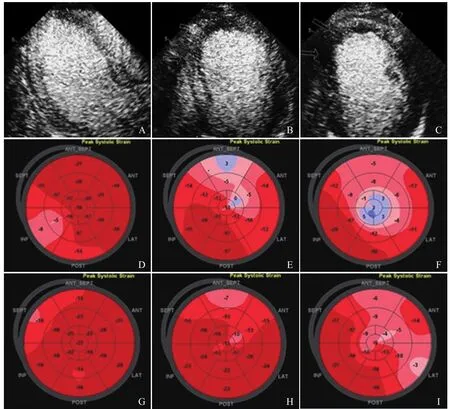
图1 心肌灌注对PPCI术后心肌收缩功能恢复的影响。灌注良好心肌(A)术后3个月(G)心肌收缩功能较术后1周(D)明显恢复;灌注减少心肌(B)术后3个月(H)心肌收缩功能较术后1周(E)明显恢复;灌注缺失心肌(C)术后3个月(I)心肌收缩功能较术后1周(F)部分恢复

图2 △LPSS组间比较
表3 不同程度收缩功能受损心肌△LPSS组间比较(±s,%)
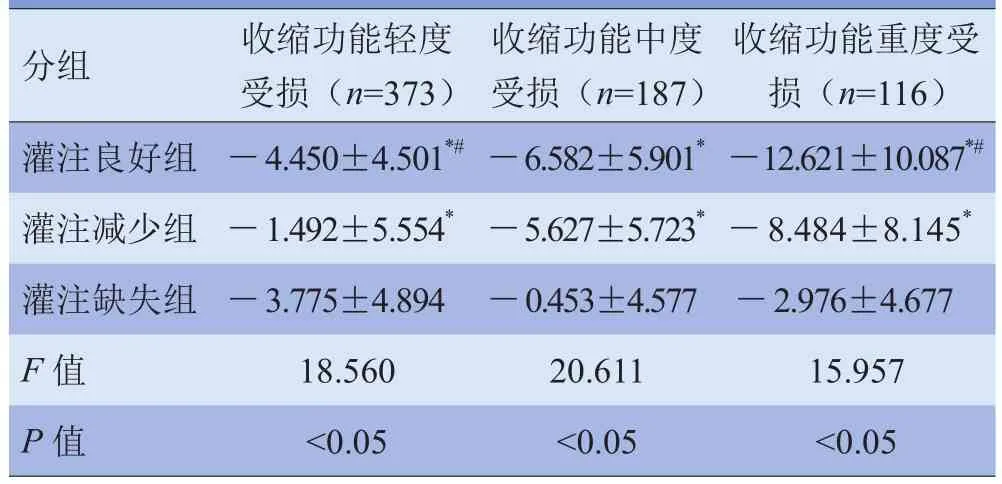
表3 不同程度收缩功能受损心肌△LPSS组间比较(±s,%)
注:与灌注缺失组比较,*P<0.05;与灌注减少组比较,#P<0.05
分组收缩功能轻度受损(n=373)收缩功能重度受损(n=116)灌注良好组-4.450±4.501*#-6.582±5.901*-12.621±10.087*#灌注减少组-1.492±5.554*-5.627±5.723*-8.484±8.145*灌注缺失组-3.775±4.894-0.453±4.577 -2.976±4.677F值18.56020.611 15.957P值<0.05<0.05<0.05收缩功能中度受损(n=187)
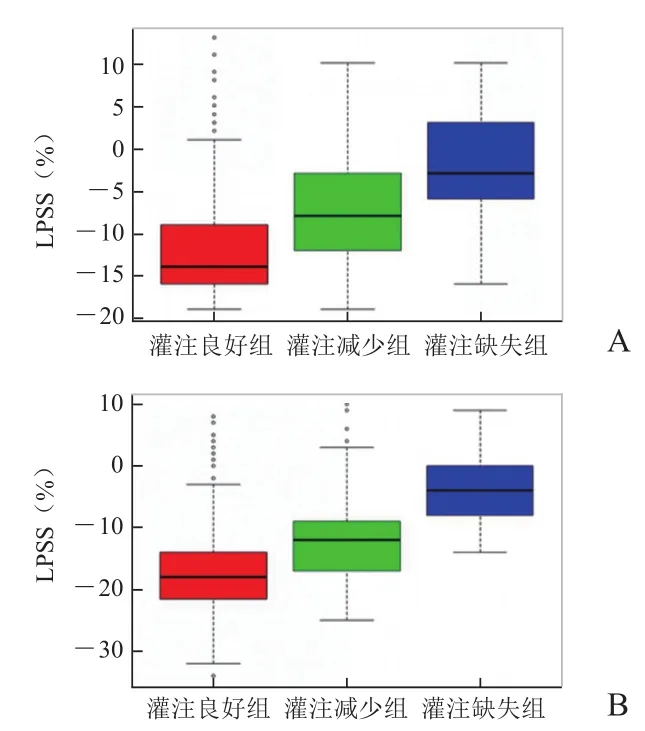
图3 PPCI术后1周、术后3个月各组心肌LPSS组间比较。术后1 周(A),术后3个月(B)
二维应变利用斑点追踪技术能够敏感地反映血流灌注减少引起的局部心肌收缩功能下降[11],其不受声束方向和室壁运动方向间夹角的影响,且与组织多普勒频移无关[12],因此用二维应变评价局部心肌收缩功能更加客观、准确。

图4 PPCI术后3个月,MPS与LPSS的相关性。术后1周(A),术后3个月(B)
本研究结果显示,灌注良好、灌注减少心肌PPCI术后收缩功能有所改善,与晋军等[13]的研究结果相符,但本研究同时发现,即使灌注缺失心肌,术后收缩功能亦存在一定程度的提高,与既往较多研究结果不符,如Galiuto等[14]提示灌注缺失心肌微血管完整性遭受破坏,心肌坏死不可避免,不具备收缩功能恢复潜能;钱建芬等[3]研究结果则表明灌注缺失组心肌术后3个月收缩功能有降低趋势,Maria等[15]研究表明无复流心肌提示左心室将重塑、左室收缩功能下降及预后较差。分析其原因可能有以下几点:①既往研究评估左室心肌收缩功能变化多采用左室射血分数、组织多普勒技术及室壁运动分析指数评价,而本研究采用二维斑点追踪技术,其评价局部心肌收缩功能更加客观、精确;②生理学上,再灌注区的血流不均匀,并随时间动态变化,在心肌损伤或坏死伴有微血管完整性破坏并且MCE显示无造影增强的区域内,仍可能存在血流正常心肌;③有研究提示,PCI术后无复流大部分是短暂性的,短暂的无复流不会导致不利的左室重塑[16];④缺血心肌区域侧支循环的建立及药物的作用也可能对心肌收缩功能恢复起作用。综上,本研究提示灌注缺失心肌并不等同于心肌坏死,即使PPCI术后缺血心肌无复流,仍可能具备收缩功能恢复潜能。
由于AMI患者PPCI术后1周收缩功能异常心肌受损程度不同,为探讨PPCI术后心肌灌注水平与心肌收缩功能恢复程度之间的变化趋势,本研究进一步将3组心肌术后3个月与术后1周△LPSS进行组间比较,结果发现随着术后1周心肌灌注水平的减少,△LPSS值下降。为减少心肌收缩功能受损程度对结果的影响,本研究继续将术后1周收缩功能受损心肌分为轻度、中度、重度受损3组,结果仍然基本一致。提示灌注缺失心肌虽术后3个月心肌收缩功能较前有所恢复,但恢复程度较小,与预期结果相符。提示AMI患者术后心肌灌注水平是决定心肌收缩功能恢复程度的关键。另外,本研究同样发现MCE心肌灌注指标与心肌收缩功能在术后1周及术后3个月存在相关,术后灌注水平越好,收缩功能恢复程度越高。
因此,本研究认为AMI患者PPCI术后评价梗死区域内心肌灌注具有重要临床指导意义,灌注水平直接影响患者心肌收缩功能恢复;虽然无复流心肌仍具备收缩功能恢复潜能,但程度轻微,仍是导致PPCI术后患者不良预后的关键所在,故早期发现无复流现象,及早进行药物干预等治疗,是改善患者预后的主要治疗方法。
本研究不足之处在于:①由于MCE定量法评价心肌灌注复杂、耗时、数据分析较困难,故应用MCE目测半定量法评价心肌灌注,对操作者有一定的主观性及经验依赖性,且干扰因素较多,如患者年龄、体型、透声条件等,结果显示心肌内无明显造影剂充盈,但仍可能有少量存活心肌;②本研究样本量较少,既往大量研究认为PPCI术后无复流患者心脏不良事件的发生率明显增加,本研究结果提示无复流心肌同样有心肌收缩功能恢复潜能,仅恢复程度较灌注良好及灌注减少心肌小,因此灌注缺失心肌是否等同于坏死心肌、PPCI术后无复流区域是否预后不佳仍需大样本临床试验及追踪复查才能得出结论。
总之,AMI患者PPCI术后心肌灌注水平与心肌收缩功能恢复程度密切相关,术后灌注水平越好,收缩功能恢复程度越高,联合运用两种技术能够更精确地评价PPCI术后治疗效果,指导临床治疗并为患者远期预后提供预测参考。
[1] O'Gara PT, Kushner FG, Ascheim DD, et al. 2013 ACCF/AHA guideline for the management of ST-elevation myocardial infarction: executive summary: a report of the american college of cardiology foundation/american heart association task force on practice guidelines: developed in collaboration with the american college of emergency physicians and society for cardiovascular angiography and interventions. Catheter Cardiovasc Interv, 2013, 82(1): E1-E27.
[2] Abdelmoneim SS, Martinez MW, Mankad SV, et al. Resting qualitative and quantitative myocardial contrast echocardiographyto predict cardiac events in patients with acute myocardial infarction and percutaneous revascularization. Heart Vessels, 2015, 30(1): 45-55.
[3] 钱建芬, 汤裕华, 林银康. 实时心肌超声造影结合二维应变评价经皮冠状动脉重建术后心肌灌注与收缩功能改变. 中华医学超声杂志(电子版), 2012, 9(5): 30-33.
[4] Orde SR, Pulido JN, Masaki M. Outcome prediction in sepsis:speckle tracking echocardiography based assessment of myocardial function. Crit Care, 2014, 18(4): R149.
[5] Michaels AD, Gibson CM, Barron HV. Microvascular dysfunction in acute myocardial infarction: focus on the roles of platelet and inflammatory mediators in the no-reflow phenomenon. Am J Cardiol, 2000, 85(5A): 50B-60B.
[6] Salinas P, Jimenez-Valero S, Moreno R, et al. Update in pharmacological management of coronary no-reflow phenomenon. Cardiovasc Hematol Agents Med Chem, 2012, 10(3): 256-264.
[7] Jeong YH, Kim WJ, Park DW, et al. Serum B-type natriuretic peptide on admission can predict the 'no-re fl ow' phenomenon after primary drug-eluting stent implantation for ST-segment elevation myocardial infarction. Int J Cardiol, 2010, 141(2): 175-181.
[8] Salerno M, Beller GA. Noninvasive assessment of myocardial perfusion. Circ Cardiovasc Imaging, 2009, 2(5): 412-424.
[9] Liu R, Deng Y, Bi X, et al. Assessment of myocardial perfusion and systolic function in patients with coronary artery disease after coronary artery bypass surgery by myocardial contrast echocardiography and two-dimensional strain echocardiography. J Huazhong Univ Sci Technol Med Sci, 2009, 29(5): 664-668.
[10] Kang SJ, Kang DH, Song JM, et al. Comparison of myocardial contrast echocardiography versus rest sestamibi myocardial perfusion imaging in the early diagnosis of acute coronary syndrome. J Cardiovasc Ultrasound, 2010, 18(2): 45-51.
[11] Joyce E, Hoogslag GE, Al Amri I, et al. Quantitative dobutamine stress echocardiography using speckle-tracking analysis versus conventional visual analysis for detection of signi fi cant coronary artery disease after ST-Segment elevation myocardial infarction. J Am Soc Echocardiogr, 2015, 28(12): 1379-1389.
[12] Liu YJ, Leng XP, Du GQ, et al. Two-dimensional longitudinal strains and torsion analysis to assess the protective effects of ischemic postconditioning on myocardial function: a speckle tracking echocardiography study in rabbits. Ultrasonics, 2015, 56: 344-353.
[13] 晋军, 王红, 黄岚, 等. 急性心肌梗死患者心肌灌注状况对经皮冠状动脉介入术后心功能的影响. 中华老年多器官疾病杂志, 2010, 9(5): 421-424.
[14] Galiuto L, Locorotondo G, Paraggio L, et al. Characterization of microvascular and myocardial damage within perfusion defect area at myocardial contrast echocardiography in the subacute phase of myocardial infarction. Eur Heart J Cardiovasc Imaging, 2012, 13(2): 174-180.
[15] Pontecorvo ML, Spaziani C, Montone RA, et al. Myocardial no-re fl ow phenomenon: recent knowledges. Recenti Prog Med, 2011, 102(2): 53-57.
[16] Chan W, Stub D, Clark DJ, et al. Usefulness of transient and persistent no reflow to predict adverse clinical outcomes following percutaneous coronary intervention. Am J Cardiol, 2012, 109(4): 478-485.
(本文编辑 张晓舟)
Prediction of Myocardial Systolic Function Recovery with Myocardial Perfusion After Primary Percutaneous Coronary Intervention
Myocardial infarction; Acute disease; Angioplasty, transluminal, percutaneous coronary; Echocardiography; Contrast media; Myocardial reperfusion; Myocardial contraction
中山大学附属佛山市第一人民医院超声诊疗中心 广东佛山 528000
赖玉琼
Department of Ultrasonic Diagnosis and
Treatment Center, the First People's Hospital of Foshan, Sun Yat-sen University, Foshan 528000, China
Address Correspondence to:LAI Yuqiong
E-mail: yukinglai@tom.com
广东省科技计划项目(2013B021800034)。
R542.2+2
2016-12-09
修回日期:2017-01-30
中国医学影像学杂志
2017年 第25卷 第5期:377-382
Chinese Journal of Medical Imaging
2017 Volume 25 (5): 377-382
10.3969/j.issn.1005-5185.2017.05.013
【Abstrac】PurposeTo explore the predictive value of myocardial perfusion in assessing myocardial systolic function recovery after primary percutaneous coronary intervention (PPCI), in order to improve poor prognosis by early detection of myocardial no-reflow.Materials and MethodsForty nine patients with acute myocardial infarction (AMI) who had received PPCI were chosen as subjects. All the patients underwent two-dimensional strain (2DS) images and resting real-time myocardial contrast echocardiography (MCE) within one week after surgery, and 2DS measurement was repeated after three months. 2DS imaging was used to acquire longitudinal peak systolic strain (LPSS) at all myocardial segments. Based on the graphs of LPSS, left ventricular myocardium was divided into normal contractile function myocardium (red) and impaired contractile function myocardium (light red, blue). According to the myocardial perfusion scores (MPS) qualitatively assessed by MCE visual interpretation, the myocardia with impaired systolic function were categorized into three groups with different perfusion level. The changes of LPSS within one week and three months after surgery (△LPSS) among the three groups were analyzed. The correlation between MPS and LPSS within one week and three months after PPCI was also analyzed respectively.ResultsThe △LPSS increased signi fi cantly among the three groups with the improvement of myocardial perfusion level [(-5.78±6.23)%vs. (-4.37±6.60)%vs. (-1.21±4.77)%, allP<0.05]. The MPS measured one week after PPCI was both positively correlated with the LPSS detected within one week after surgery and that after three months (r=0.47,0.58,P<0.001). The consistence of myocardial perfusion scores given by two evaluators was good (Kappa=0.785,P<0.05).ConclusionThe level of myocardial perfusion after PPCI in patients with AMI is closely related to regional myocardial systolic function, and the improvement of myocardial perfusion can forecast the recovery of regional systolic function.
