脓毒症患者二尖瓣舒张早期峰流速与二尖瓣环舒张早期运动速度比值对预后的评估价值
2017-05-25夏嘉鼎段立娟苏震刘畅秦诗阳
夏嘉鼎,段立娟,苏震,刘畅,秦诗阳
(承德医学院附属医院,河北承德067000)
脓毒症患者二尖瓣舒张早期峰流速与二尖瓣环舒张早期运动速度比值对预后的评估价值
夏嘉鼎,段立娟,苏震,刘畅,秦诗阳
(承德医学院附属医院,河北承德067000)
目的 观察脓毒症患者二尖瓣舒张早期峰流速与二尖瓣环舒张早期运动速度比值(E/e′)的变化,探讨其对脓毒症预后的评估价值。方法 将82例脓毒症患者根据住院28 d内是否存活分为存活组59例和死亡组23例。分别于入ICU第1、3、7天行经胸壁超声心动图检查,应用组织多普勒成像(DTI)技术测定E/e′。应用多因素Logistic回归分析E/e′与脓毒症患者28 d病死率的相关性,利用受试者工作者特征曲线(ROC)分析E/e′对脓毒症患者28 d病死率的预测价值。结果 死亡组E/e′入ICU第3、7天均高于第1天(P均<0.05),第3天与第7天比较差异无统计学意义(P>0.05)。存活组E/e′入ICU第3天高于第1天(P<0.05);第7天较第3天降低(P<0.05),与第1天比较差异无统计学意义(P>0.05)。死亡组E/e′在第1、3、7天均较存活组明显增高(P均<0.05)。Logistic回归分析显示,E/e′与脓毒症患者28 d病死率显著相关(P<0.05),ROC分析显示,E/e′第1、3、7天评估脓毒症患者28 d病死率的曲线下面积分别为0.72、0.84、0.80,以第3天的E/e′值11.3为截点值,其预测28 d病死率的敏感度为73.9%、特异度为72.9%。结论 E/e′是脓毒症患者28 d死亡的独立预测指标,有助于评估脓毒症患者的预后。
脓毒症;左心室舒张功能障碍;二尖瓣舒张早期峰流速;二尖瓣环舒张早期运动速度
脓毒症是感染导致的失控性全身性炎症反应,具有高发病率和高病死率的特点,是重症医学领域的严重问题[1]。心功能不全是脓毒症最严重的并发症之一。脓毒症患者常发生重度心肌损伤和心肌抑制[2],心肌抑制可导致心脏收缩、舒张功能障碍,约44%的脓毒症患者存在左心室舒张功能障碍[3]。研究显示,伴有左心室舒张功能障碍的脓毒症患者死亡风险显著增加,预后不良[4]。采用经胸壁超声心动图测定二尖瓣舒张早期峰流速与二尖瓣环舒张早期运动速度比值(E/e′),可准确评价左心室舒张功能。目前,国内尚缺乏E/e′评估脓毒症患者预后的相关报道。本研究以E/e′评价脓毒症患者的左心室舒张功能,观察其在脓毒症发展过程中的变化,分析E/e′与脓毒症预后的关系。
1 资料与方法
1.1 临床资料 选择2014年10月~2016年10月我院ICU收治的脓毒症患者82例。入选标准参照2012年拯救脓毒症运动(SSC)国际指南定义的脓毒症诊断标准[5],患者存在感染灶或有明确的细菌学检查结果,发病至入选时间<24 h。其中肺部感染24例,消化系统及腹腔感染30例,血液感染9例,其他部位感染8例,感染灶不明11例。排除肿瘤、糖尿病、器质性心脏病、急性脑血管病、肝肾功能不全、年龄<18岁的患者及孕妇。入选患者均给予病因处理、抗感染、留取病原学标本、液体平衡管理、监测血流动力学及血乳酸变化、改善心肌细胞代谢等治疗。根据预后将患者分为存活组(住院28 d内存活)和死亡组(住院28 d内死亡)。存活组59例,男41例、女18例,年龄(60.3±10.8)岁,体温(37.9±1.0)℃,呼吸(23.1±5.3)次/min,心率(100.5±15.0)次/min,平均动脉压(77.4±12.9)mmHg,氧合指数(190.9±60.3)mmHg,血乳酸[4.2(1.02,11.65)]mmol/L,APACHEⅡ评分(20.4±8.1)分;死亡组23例,男16例、女7例,年龄(62.4±10.9)岁,体温(37.8±1.2)℃,呼吸(23.9±5.1)次/min,心率(99.2±15.6)次/min,平均动脉压(75.7±11.0)mmHg,氧合指数(179.2±72.6)mmHg,血乳酸[7.7(3.11,11.87)]mmol/L,APACHEⅡ评分(29.2±7.0)分。两组年龄、性别、体温、呼吸、心率、平均动脉压、氧合指数比较差异均无统计学意义,死亡组血乳酸水平及APACHEⅡ评分高于存活组(P均<0.05)。本研究经我院伦理委员会批准,患者或其家属签署知情同意书。
1.2 E/e′检测 由同一位超声科医师于入ICU第1、3、7天使用床旁超声仪测定二尖瓣舒张早期E峰流速(E),使用组织多普勒成像(DTI)测定二尖瓣环舒张早期运动速度(e′),计算E/e′。应用M型超声心动图测定左心室射血分数(LVEF)。同一时间点连续测定三次取平均值。

2 结果
2.1 两组入ICU第1、3、7天E/e′比较 死亡组入ICU后第1、3、7天E/e′均较存活组升高(P均<0.05)。死亡组E/e′入ICU第3、7天均高于第1天(P均<0.05),第3天与第7天比较差异无统计学意义(P>0.05);存活组E/e′入ICU第3天高于第1天(P<0.05),第7天较第3天降低(P<0.05),与第1天比较差异无统计学意义(P>0.05)。见表1。
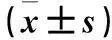
表1 两组入ICU第1、3、7天E/e′比较
注:与存活组同期比较,aP<0.05;与同组第1天比较,bP<0.05;与同组第3天比较,cP<0.05。
2.2 影响脓毒症患者病死率的相关因素 单因素分析显示,脓毒症患者28 d病死率与E/e′、血乳酸及APACHEⅡ评分相关(P均<0.05);与年龄、性别、氧合指数、体温、心率、平均动脉压及不同部位感染无关(P均>0.05)。以E/e′、血乳酸、APACHEⅡ评分为自变量,以28 d病死率为因变量,Logistic回归分析结果显示,E/e′、血乳酸、APACHEⅡ评分与脓毒症患者28 d病死率均呈独立相关。见表2。

表2 影响脓毒症患者28 d病死率的多因素Logistic回归分析结果
2.3 E/e′对脓毒症预后的评估价值 以入ICU第1、3、7天E/e′和28 d病死率作ROC分析,第1、3、7天E/e′的ROC曲线下面积分别为0.72、0.84、0.80,P均<0.05,提示E/e′对预测脓毒症患者28 d死亡有较高的预测价值。其中ROC曲线上敏感度、特异性均较高的临界点为第3天,以11.3为截点值,预测死亡的敏感度和特异度分别为73.9%、72.9%。见图1。

图1 E/e′评估脓毒症患者28 d死亡的ROC曲线
3 讨论
脓毒症患者病情危重,可迅速进展为严重脓毒症及脓毒性休克,是导致危重症患者死亡的重要原因。研究显示,脓毒症患者左心室舒张功能障碍的发生率很高[6,7]。脓毒症患者常在起病初期即存在心肌损伤和心肌抑制,进而发展为心脏收缩及舒张不全,导致临床结局更加恶化,患者死亡风险明显增高[4]。既往检测左心室舒张功能的“金指标”为心导管检查,但作为一种有创性操作,其临床应用受到限制。经胸壁超声心动图是目前临床最常用的无创性检测心功能的方法,二尖瓣环舒张早期E峰流速与A峰流速比值(E/A)作为传统的评价左心室舒张功能的指标,其敏感性较高,但诊断中有假性正常化和超正常化的可能,降低了诊断的特异性和应用价值[8]。应用DTI测定e′相对不依赖前负荷,通过计算E/e′可使左心室主动松弛力和年龄影响被消除,随着左心室舒张功能障碍的加重,E/e′呈稳定性升高,是评估左心室舒张功能更可靠的指标[9]。本研究将E/e′作为评估左心室舒张功能的手段,一定程度上避免了左心房顺应性、心肌松弛状态、容量负荷及瓣膜反流等干扰因素,提高了评估左心室舒张功能的准确性。
本研究显示,脓毒症患者E/e′在入ICU第1天即出现升高,第3天升至最高;其中存活组经抗感染、改善心肌细胞代谢及液体出入平衡管理等干预措施下E/e′显著下降,于第7天恢复至第1天水平,提示左心室舒张功能明显改善;而死亡组在入ICU后各时间点E/e′均明显高于存活组,直至第7天仍未恢复至初始水平。Mahjoub等[10]对83例机械通气的脓毒症患者给予液体管理及脏器功能支持治疗后,发现存在心脏舒张功能障碍的患者临床症状明显改善,机械通气时间缩短,证实脓毒症患者左心室舒张功能障碍存在可逆性。而具有高死亡风险的脓毒症患者,其心脏舒张功能受损更为严重,且恢复过程缓慢,可逆性差。
本研究应用多因素Logistic回归分析显示,E/e′与脓毒症患者28 d病死率独立显著相关。分析原因,E/e′是评估左心室舒张功能的重要指标,脓毒症患者心肌组织遭受打击,由于心肌抑制因子增多、心肌细胞内钙超载、氧化应激等因素造成心脏顺应性减退,心肌松弛障碍,左心室舒张末压升高,导致左心室舒张功能障碍,临床状况恶化,患者病死率增加[11,12]。此外,死亡组血乳酸水平及APACHEⅡ评分均显著高于存活组。同时多因素Logistic回归分析提示血乳酸水平及APACHEⅡ评分均与28 d病死率显著相关。研究显示,早期动态监测脓毒症患者血乳酸变化可评估其严重程度及预后[13];而APACHEⅡ评分系统作为评价危重症患者严重程度的标准,被广泛用来评估脓毒症患者的病情和预后,APACHEⅡ评分与患者的病死率呈正相关,分值越高,病情越危重,病死率越高[14,15]。本研究证实,E/e′可作为脓毒症患者28 d死亡的独立预测指标,且血乳酸水平及APACHEⅡ评分越高,其预后越差。根据ROC测得入ICU第3天应用E/e′评估脓毒症患者28 d病死率的效能最高,以11.3为截点值,曲线下面积为0.84,可作为预测死亡的临界点,对预后有诊断价值。临床上在入ICU第3天对E/e′≥11.3的脓毒症患者应更加关注左心室舒张功能异常变化,及时采取相应的预防和治疗措施,避免心功能不全加重。
综上所述,脓毒症患者早期即可出现左心室舒张功能障碍,随病情进展明显加重,且高死亡风险脓毒症患者心脏舒张功能恢复更加缓慢。E/e′与脓毒症患者28 d病死率独立显著相关,有利于评估脓毒症预后。
[1] 中华医学会重症医学分会.中国严重脓毒症/脓毒性休克治疗指南(2014)[J].中华内科杂志,2015,54(6):365-367.
[2] Mourad M, Chow-Chine L, Faucher M, et al. Early diastolic dysfunction is associated with intensive care unit mortality in cancer patients presenting with septic shock[J]. Br J Anaesth, 2014,112(1):102-109.
[3] Price LC, Wort SJ, Finney SJ, et al. Pulmonary vascular and right ventricular dysfunction in adult critical care :Current and emerging options for management : A systematic literature review[J]. Crit Care, 2010,14(5): R169.
[4] Landesberg G , Gilon D, Meroz Y, et al. Diatolic dysfunction and mortality in severe sepsis and septic shock[J]. Eur Heart J, 2012,33(7):895-903.
[5] Dellinger RP, Levy MM, Rhodes A, et al. Surviving Sepsis Campaign: international guidelines for management of severe sepsis and septic shock, 2012[J]. Intensive Care Med, 2013,39(2):165-228.
[6] Pulido JN, Afessa B, Masaki M ,et al. Clinical spectrum, frequency, and significance of myocardial dysfunction in in severe sepsis and septic shock[J]. Mayo Clin Proc, 2012,87(7):620-628.
[7] Sturgess DJ, Marwick TH, Joyce C, et al. Prediction of hospital outcome in septic shock: a prospective comparison of tissue Doppler and cardiac biomarker[J]. Crit Care, 2010,14(2):R44.
[8] 郭继鸿.舒张性心衰的新理念[J].临床心电学杂志,2009,18(3):209-221.
[9] Veselka J. Role of Doppler echocardiogram in the diagnostics and therapy of hypertrophic cardiomyopathy[J]. Cas Lek Cesk, 2006,145(4):279-283.
[10] Mahjoub Y, Benoit-Fallet H, Airapetian, et al. Improvement of left ventricular relaxation as assessed by tissue Doppler imaging in fluid-responsive critically ill septic patients[J]. Intensive Care Med, 2012,38(9):1461-1470.
[11] Zanotti-Cavazzoni SL, Hollenberg SM. Cardiac dysfunction in severe sepsis and septic shock[J]. Curr Opin Crit Care, 2009,15(5):392-397.
[12] Hassoun SM, Marechal X, Montaigne D, et al. Prevention of endotoxin-induced sarcoplasmic reticulum calcium leak improves mitochondrial and myocardial dysfunction[J]. Crit Care Med, 2008,36(9):2595-2596.
[13] Shapiro NI, Howell MD, Talmor D, et al. Serum lactate as a predictor of mortality in emergency department patients with infection[J]. Ann Emerg Med, 2005,45(5):524-528.
[14] 谭兰婷,桂海波,胡春林,等.心肌损伤标志物联合APACHE-Ⅱ评分在感染性休克患者预后判断中的价值[J].中国急救医学,2015,35(7):34-36.
[15] Carcillo JA, Kuch BA, Han YY, et al. Mortality and functional morbidity after use of PALS/APLS by community physicians[J]. Pediatrics, 2009,124(2): 500-508.
河北省科技支撑计划项目(152777205)。
10.3969/j.issn.1002-266X.2017.06.021
R63
B
1002-266X(2017)06-0062-03
2016-11-15)
