配位不饱和金属-有机骨架材料吸附CO2的研究进展
2017-05-15赵倩冯东汪洋赵文波
赵倩,冯东,汪洋,赵文波
(昆明理工大学化学工程学院,云南 昆明 650500)
配位不饱和金属-有机骨架材料吸附CO2的研究进展
赵倩,冯东,汪洋,赵文波
(昆明理工大学化学工程学院,云南 昆明 650500)
配位不饱和金属-有机骨架(MOFs)材料是一种极具潜力的小分子气体吸附分离储存材料。本文回顾了近几年MOFs材料在捕集CO2领域的发展状况,对近年来研究比较集中的几种金属配位不饱和MOFs材料进行了详细的介绍与比较,如MIL系列、Cu-BTC系列及MOF-74等。该工作为系统地认识MOFs和拓展其未来在CO2吸附分离领域的应用提供了帮助。本文同时也进一步指出不饱和金属配位的存在对多孔MOFs材料的吸附性能起着重要作用。在多孔MOFs材料对CO2捕集效果仍不能满足工业需求的现状下,预测合理设计MOFs的金属配位中心且通过活化处理调控MOFs中金属的配位状况,甚至对其孔道表面功能化修饰将是该类型材料的发展方向,并在最后从制备方法、金属中心的选择与表面改性3方面作了总结。
配位不饱和;金属-有机骨架;多孔MOFs材料;CO2捕集;吸附;表面改性
随着社会快递地发展,化石燃料能源消耗的急剧增加导致环境污染与温室效应日益严重。为了减缓全球变暖的速度,满足节能减排的环保要求,对CO2进行有效捕集及储存迫在眉睫。由于传统化学溶剂吸收法存在吸收/解吸过程中能耗高、吸收剂损耗严重、再生过程会对环境有二次污染等问题,利用固体吸附材料渐渐受到关注。金属-有机骨架(MOFs)固体材料具有明确的次级结构单元(SBUs)及属于它自身独特的物理与化学性能优势,对分离储存小分子气体有潜在利用价值[1]。特别是配位不饱和MOFs,在吸附CO2气体方面相较其他固体材料,其具有以下3个特性:①对CO2选择性吸附能力强,吸附容量大;②具有稳定的刚性结构,可进行吸附/解吸循环操作;③结构柔韧性好,可在分子水平的基础上进行微调和化学功能化修饰,因此成为迄今为止符合CO2理想吸附剂要求的多孔固体材料之一[2-3]。
目前,虽有关于配位不饱和MOFs的综述性研究,但大都只关注于其配位中心或应用方面,而在吸附CO2方面未作全面性的总结。本文将从结构、吸附机理及性能影响因素3方面对目前应用于吸附CO2研究较为成熟的配位不饱和MOFs材料进行总结,为未来MOFs能成功用于吸附CO2指明其可能发展的方向。
1 配位不饱和MOFs的结构
由于金属中心和有机配体的不同,MOFs的结构、吸附性能也各不相同。按结构的不同,其可划分为多种不同系列,如MIL、PCN、ZIF等系列。其中配位不饱和的MOFs材料有:UiO-66、MIL-53、MIL-88、MIL-100、MIL-101、MIL-127、HKUST-1、MOF-74、MOF-505、UTSA-20、BTT、MFU-1/2等,涉及的配位不饱和金属中心有Cr3+、Fe2+/3+、Al3+、Sc3+、V3+、Mn2+、Co2+、Cu1+/2+、Zn2+、Mg2+、Ni2+等。掌握配位不饱和MOFs的结构是理解其对二氧化碳吸附机理的基础,将其结构认识到位才能把握吸附剂与吸附质的相互作用。对CO2表现出较高吸附性能的配位不饱和MOFs主要是以下几种,结构介绍如下。
1.1 HKUST-1(Cu-BTC)的结构
均苯三甲酸铜(HKUST-1,通常又表示为Cu-BTC)是一类独特的具有孔笼-孔道结构的MOFs材料,是众多MOFs材料中非常具有代表性的一种。与具有不饱和金属配位但没有孔笼的MOFs材料相比,其对CO2表现出较好的吸附选择性及较高的吸附容量。Cu3(BTC)2的主要结构特点是相邻的两个铜离子之间会形成铜二聚体,其间距为0.263nm。每个Cu2+和均苯甲酸(TMA)上的一个羧基中的两个氧原子配位,每个二聚体和来自4个均苯三甲酸上的4个羧基以及两个水分子中的羟基氧配位。其中羧酸上的氧原子位于同一平面,而两个羟基氧位于轴向,便形成了类似桨轮结构的次级结构单元,如图1(a);每个TMA配体和3个次级结构单元相连构成含有近八面体结构的孔笼,孔笼间相互连接构成含有空腔的Cu-BTC晶体。每个孔笼有4个窗口孔道,连接到三维正交孔道,其孔隙大小呈双峰分布;正交孔道间也相互连接,形成似正方形的接口,其口径因配体的不同而不同[5],该骨架的比表面积达1500m2/g,孔隙率约为40.7%[6]。金属中心的终端水分子通过真空高温处理去除,可在金属中心形成具有路易斯酸性质的不饱和金属配位点[7][图1(b)],利于提高对小分子气体的吸附选择性。
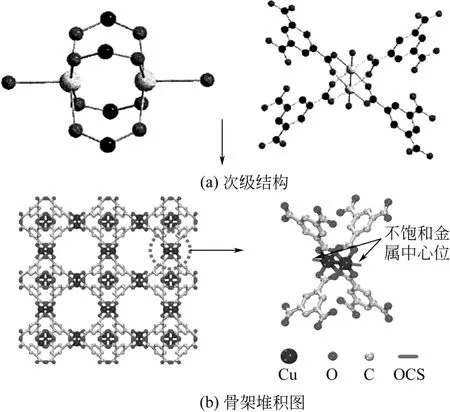
图1 HKUST-1的次级结构单元及骨架堆积图[4]
1.2 MIL系列的结构
MIL(materials of institut lavoisier)由法国凡尔赛大学Ferey课题组研究合成,是MOFs材料中比较著名的一类。目前,在所合成的MIL系列材料中具有不饱和配位金属中心的有MIL-53、MIL-100/101、MIL-127等,以MIL-53/100/101较为典型。
在MIL-100/101中,带有金属离子的无机基团与二羧酸配体形成超四面体次级结构单元[M3O(F/OH)(H2O)],这些结构单元又通过与氧原子间的共价键相连在三维空间上形成更大的拓扑结构。在该材料中有两种孔径的孔结构:由29~34Å的六边形孔面形成的介孔和由25~29Å的五边形孔面形成的微孔[8-9],如图2。这两种材料同时具有超大的比表面积(4100m2/g±200m2/g;5900m2/g± 300m2/g)和大量潜在的不饱和金属位(约3.0mmol/g),如图2、图3。经真空高温处理去除铬三聚物簇终端的水分子后会产生约为1.1~2.6mmol/g的配位不饱和金属位(如图3中a、b、c),并且可经螯合作用引入多电子官能团或氨基功能化修饰[10],如图3中d。
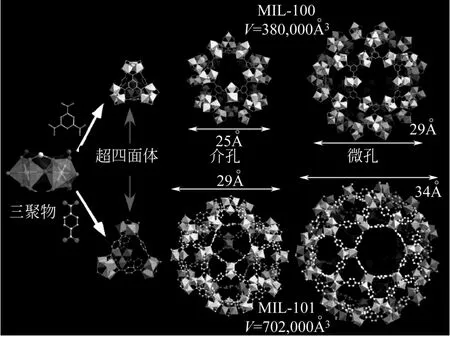
图2 MIL-100(Cr)(上)和MIL-101(Cr)(下)的次级结构单元图[9]

图3 MIL-101中产生不饱和金属位及氨功能化修饰的过程[10]
其次是MIL-53,该金属有机骨架是由八面体的MO4(OH)2次级结构单元组成,其中M=Al、Cr、Fe、Sc等金属。在MO4(OH)2的次级结构单元中,金属中心分别与4个不同苯二甲酸配体中的氧原子和2个羟基氧相连,每个次级结构单元由羟基氧连接,最后与有机配体相互连接构成一维菱形孔道,如图4[11-12]。孔的大小会随温度的不同而变化,高温下孔径约为8.5Å×8.5Å(1Å=10–1nm),低温下约为2.6Å×13.6Å,孔变窄,即所谓的“呼吸现象”[11]。
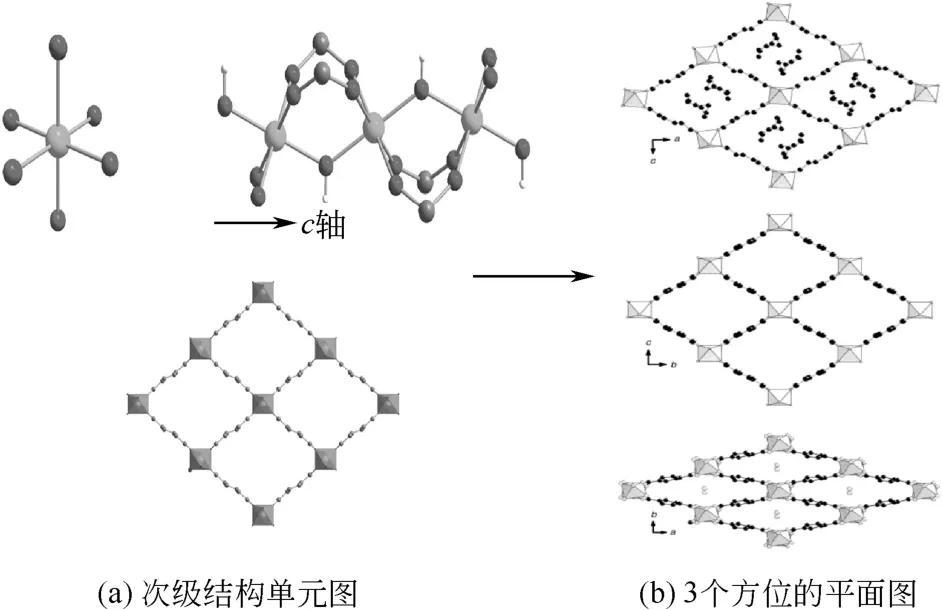
图4 MIL-53的次级结构单元图[12]与3个方位的平面图[11]
1.3 MOF-74系列的结构
与MIL-100/101和HKUST-1相比,MOF-74的结构性能更稳定。前者在金属离子中心发生改变时,它们结构的刚性强度容易受到影响,对小分子气体的吸附量会减少,甚至在吸附过程中有杂质存在时,结构会出现坍塌现象。但MOF-74的结构并不会受到影响,且随着金属中心性质的不同,其力学性能和吸附性能反而会表现的更独特。
MOF-74的结构是由二维六方孔道构成的三维类蜂巢状骨架,孔径为1.1~1.2nm,在蜂巢交叉口是由八面体配位的金属与氧缩合形成的螺旋链,其中一个金属原子与来自溶剂水分子中的6个氧原子配位形成金字塔构形的六环螯合物,其中金属中心占据顶点,如图5。通过在真空中热处理去除金属中心终端水分子,其会形成约2.9~3.4mmol/g[14]的具有路易酸性质的不饱和金属位[13],如2016年,KATZ等[15]制备出的特殊桨轮结构Cu-MOF-74(也被称为Cu-COP-27)通过热处理后每个Cu2+可以提供5个不饱和金属配位。在MOF-74系列中由于金属离子的不同,其如孔隙率、比表面积、孔容等结构性能参数也不同。
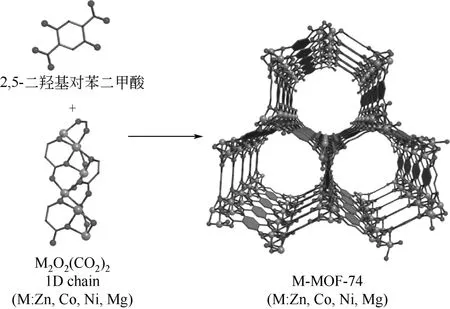
图5 M-MOF-74的次级单元及骨架结构图[13]
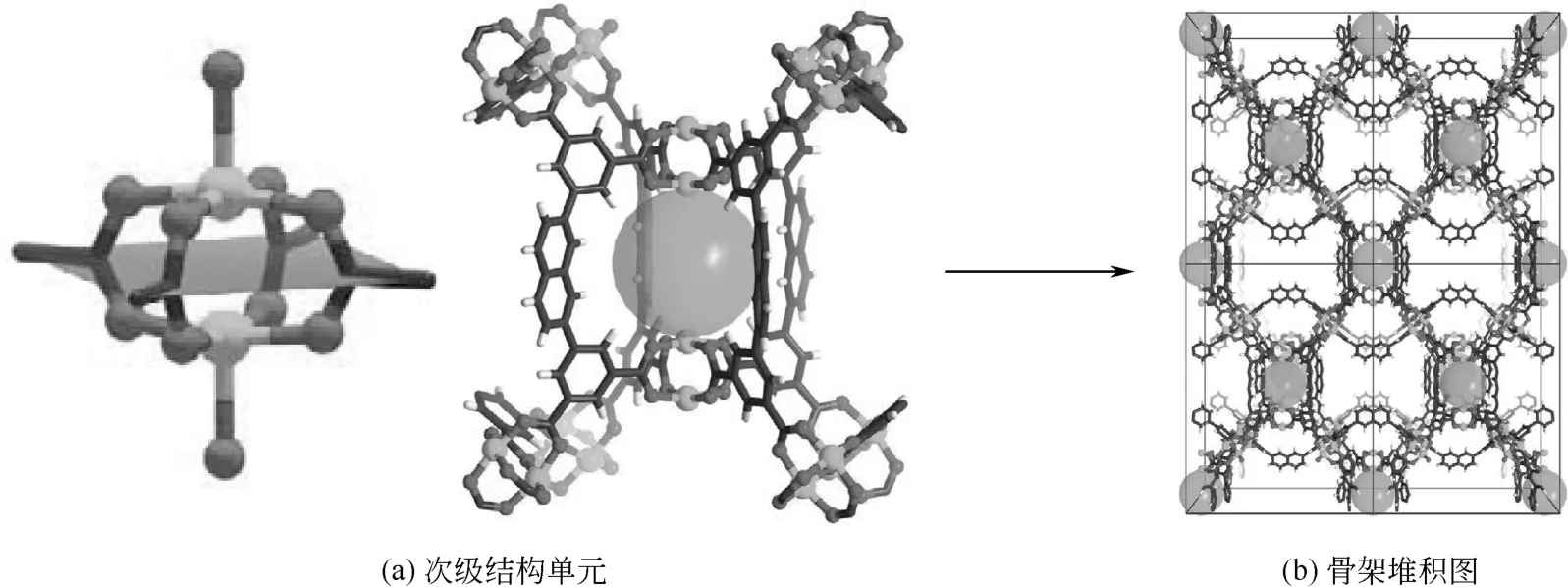
图6 PCN-88的次级结构单元和骨架堆积图[16]
1.4 PCN系列的结构
PCN(porous coordination network)也是一类具有孔笼-孔道结构的MOFs,其中PCN-16 、PCN-88、PCN-305的研究比较集中。目前由于PCN-88中具有高密度的铜金属不饱和位,对CO2气体具有特殊的选择性。在该结构中每两个铜离子与4个α-羧酸中的氧原子相连,形成灯笼形的四面体,然后由附加的β-羧酸相连形成四棱柱形的次级结构单元。每个次级结构单元通过金属与氧原子相连形成三维构型,如图6。通过热处理后,在铜离子中心可产生不饱和金属位,其孔隙率可达73.7%,比表面积为3308~3845m2/g[16]。
1.5 UTSA系列的结构
UTSA-50是UTSA系列中结构较为特殊的一种,它具有双核金属的桨轮结构,虽类似于HKUST-1,却又有别于它。在该结构中,8个相邻的Cu核与吡啶二甲酸(PDC)有机配体连接,其中Cu1和水分子连接,通过热处理可产生不饱和金属位,而Cu2与有机配体中的4个氧原子及1个氮原子配位连接,形成1个金字塔构型的次级结构单元。由于吡啶二甲酸配体中有两种不同的配位点,因此构成了两种类型孔结构。孔隙率可达57.1%,比表面积约为933m2/g,对CO2的吸附量可达100.1cm3/g[17],如图7。除此,该系列的UTSA-20/60也是比较典型配位不饱和MOF材料,具有不同的拓扑结构[18-19]。
1.6 UiO系列的结构
UiO系列材料是一类基于金属锆(Zr)的新型MOF材料。其中以UiO-66最为典型,它在CO2/CH4吸附试验中对CO2表现出良好的选择性和吸附容量[20]。在该材料的结构中,6个锆原子形成一个六核金属簇,每相邻的3个锆原子通过一个μ3-O相连,每两个相邻的锆原子再和一个二酸(BDC)配体上的羧基氧相连,通过这种方式,6个锆原子同8个μ3-O或μ3-OH、12个BDC配体上的12个羧基相连,构成一个六核的正八面体次级结构单元[Zr6O4(OH)4],如图8(a)。然后该八面体与12个对苯二酸(BDC)有机配体相连,形成包含八面体中心孔笼(11Å)和8个四面体角笼(约8Å)的三维微孔结构(图8),这两种孔笼间通过三角窗口相连(约6Å)。在合成过程中,合理设计反应物的比例使金属中心锆处缺失部分有机配体,产生高密度的不饱和金属位[21-22],而且有研究还表明引入官能团—SO3H和—CO2H后会进一步提高UiO-66对CO2的捕集效果[23]。同时UiO-66由于特殊的结构而成为目前报道的MOFs材料中稳定性最好的系列材料之一[24]。
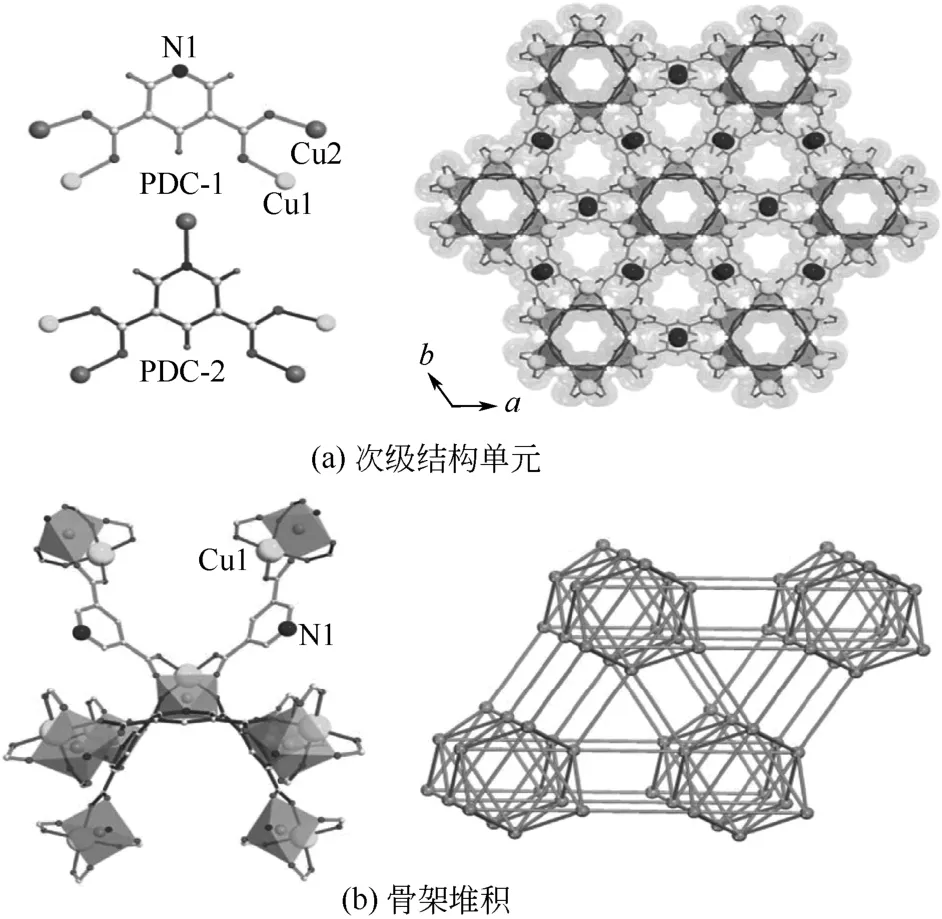
图7 UTSA-50的次级结构单元和骨架堆积图[17]
在混合气体吸附分离领域,上述的6种配位不饱和MOF材料均对CO2表现出较好的吸附选择性。从结构方面分析可以看出这6种吸附材料有各自的特点:首先,每个结构中都有明确几何构型的次级结构单元(SBU),如MIL-100/101中的超四面体结构单元[M3O(F/OH)、MIL-53和UiO-66的八面体结构单元[MaOb(OH)n],HKUST-1和PCN-88的四棱柱形次级结构单元,MOF-74和UTSA-50的金字塔形结构单元等;其次是虽然UTSA-50、HKUST-1和UiO-66次级结构单元不同,但整体结构却都是具有多核金属簇的孔笼-孔道结构;最后是这几类材料经高温或其他处理后,均能产生4~6个不饱和金属位,使得这6种材料在吸附CO2时表现出相似的吸附性能。
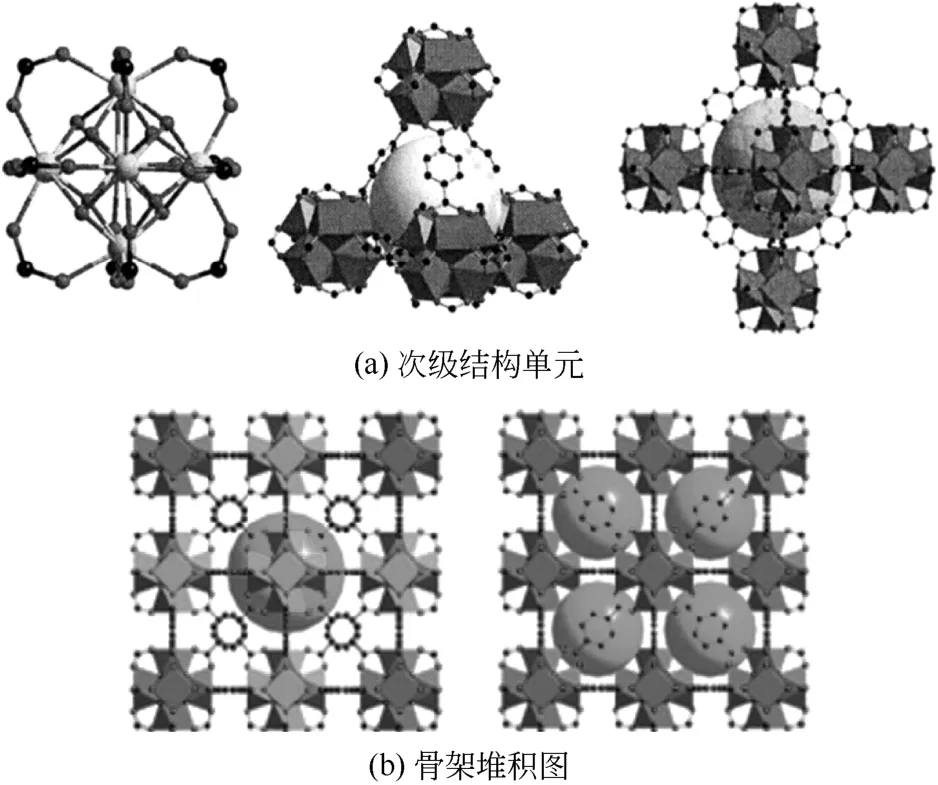
图8 UiO-66的结构图[20]
2 配位不饱和MOFs对CO2的吸附机理
金属中心、有机配体的多种改变使得MOFs材料的结构特性与功能特性也越来越多样化,也使其在小分子气体分离储存的材料领域占有了一定优势。掌握MOFs的吸附机理是改进其在吸附领域的核心,许多研究者在挖掘新型MOFs材料的同时,也在完善已有MOFs材料对小分子气体的吸附机理,但并未做全面的总结,如对CO2的吸附。近几年,研究者利用理论与实践的结合验证了MOFs材料与吸附质CO2的相互作用主要有静电吸附作用、氢键作用及与金属配位等。材料不同,吸附机理也不尽相同,其主要取决于吸附材料的金属中心、孔表面的官能团及孔径大小。
对于大部分配位不饱和MOF材料,如MIL-100/101和MOF-74,对CO2的吸附作用位主要有两种:一种是在配位不饱和金属中心,CO2与具有路易酸性质的阳离子中心相互作用生成端点加合物O=C=O…Mn+;另一种是孔表面,CO2与孔表面上有机配体中的某些官能团通过库仑力或范德华力相互作用。2008年,LLEWELLYN等[9]的实验表明,CO2与MIL-100/101的主要相互作用形式是:①在主体配位不饱和的金属中心形成O=C=O…Cr3+;②与孔表面形成微弱的相互作用力。与配位饱和多孔固体吸附材料相比,配位不饱和金属位会增加该材料对小分子气体的吸附选择性,使吸附剂与CO2相互作用位增加,其吸附量可高达40mmol/g。同时该材料结构中与不饱和金属位相邻的氧原子数和碱性位点也会影响其对CO2的吸附量。2016年,ZHANG等[12]的研究完善了CO2与孔表面的相互作用,结果表明在金属中心配位饱和的情况下,CO2主要与孔表面即有机配体中的官能团相互作用,如MIL-53配体中的羟基官能团,如图9。对于MOF-74,CHO等[13]的研究表明其与MIL系列的吸附机理相同。在吸附过程中,CO2先与MOF-74中的不饱和金属中心Co相互作用,再通过范德华力和扩散吸附与孔表面相互作用。当配位不饱和金属中心Co的金属位达到饱和时,孔表面吸附便成为之后的吸附控制步骤,CO2吸附量的增加速度会减慢[13];同样,NIJEM[25]和TIAN[26]等的研究也进一步表明,CO2中的碳原子与配位不饱和金属中心Mg2+/Ni2+和孔表面上有机配体中的碳原子以范德华力相互作用,如图10。由于不饱和金属位的存在,Mg-MOF-74对CO2的吸附容量可达37.9%(质量分数)[27]。
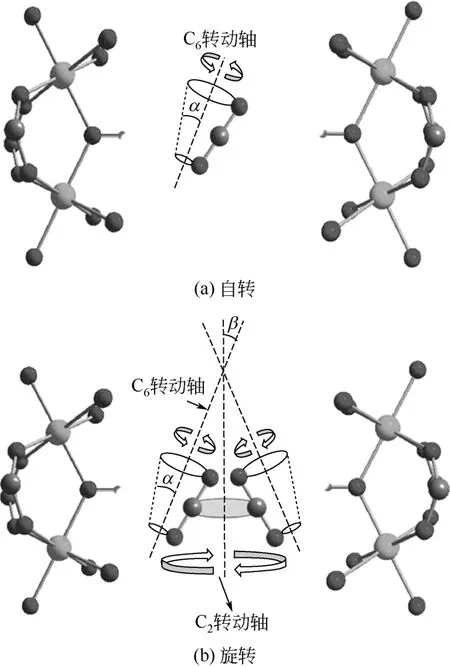
图9 在MIL-53孔表面的吸附位:CO2在相邻位间的自转和旋转[12]
对于具有特殊孔结构的MOFs材料,相互作用位就会变复杂。如研究表明由于Cu-BTC材料特殊的孔笼-孔道结构,其对CO2的吸附作用位主要有3种。2010年,KARRA等[28]的实验初步表明HKUST-1材料的孔径、不饱和金属位和孔表面的官能团是HKUST-1选择性吸附的关键影响因素,并未详细指出吸附剂与吸附质间具体的作用点。2013年,RUBEŠ等[29]研究表明这3种相互作用位分别是不饱和金属位(CUS)、孔中心吸附位(CTR)和孔窗吸附位(WIN),如图11。其中配位不饱和金属位主要是通过吸附质与Cu2+间的电子转移而形成共价键相互作用,而孔中心吸附与孔窗处的吸附主要是由吸附质与有机配体间的范德华力控制。2014年,GRAJCIAR研究组[30]在微观层面上利用密度泛函理论精确计算CO2与CUS的相互作用,对宏观的实验现象做出合理解释。
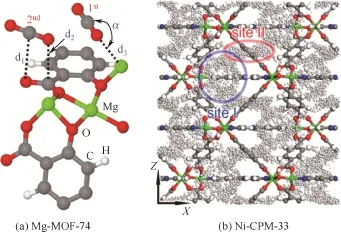
图10 Mg-MOF-74和Ni-CPM-33对CO2吸附的主/次吸附位[25]
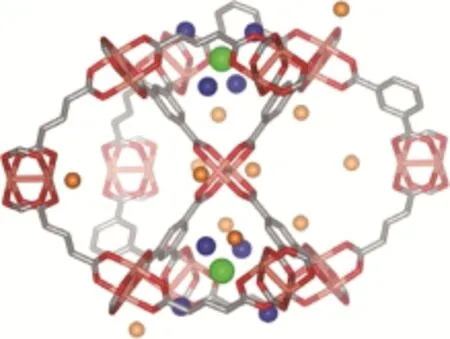
图11 Cu-BTC的对CO2吸附的3种吸附位[29]橘黄色—不饱和金属位;绿色—孔中心;蓝色—孔窗)
3 影响配位不饱和MOFs 吸附CO2的主要因素
在MOFs的结构与吸附机理的基础上,清楚了吸附材料的吸附位、比表面积、孔容积等参数会决定吸附材料对小分子气体吸附的选择性及容量。总结近些年的研究,影响这些参数的主要因素如下。
3.1 金属中心
金属中心物理性质和化学性质的差异导致同系列的MOFs材料尽管骨架结构相同,但它的孔径、孔表面积、与吸附质间的相互作用却有很大区别,对小分子气体的吸附选择性和吸附性能也不尽相同。通过热处理、酸处理、配体取代等手段,使有机金属骨架的金属中心处产生路易斯酸位,对小分子气体的吸附位增加,进而影响该材料对吸附质的吸附容量。
2014年,EUBANK等[31]指出当金属离子不同时,金属离子是影响该类型吸附剂吸附性能的主要因素;当金属离子相同时,MOFs的结构和不饱和金属位则是主要影响因素。在金属中心不同的MOFs材料中,MOF-74系列的研究比较全面与系统,其中涉及的金属中心有Mg、Ni、Co、Zn等。中心金属离子性质的不同使同系列MOF-74结构中不饱和金属位的密度和比表面积都不同,对CO2的吸附能力也不同。M-MOF-74(M=Mg、Ni、Co)在一定条件下,Mg2+与CO2间的相互作用较其他离子强,其中Mg-MOF-74对CO2的吸附性能最好,其吸附量依次分别为261.1mg/g、179.1mg/g和123.8mg/g;2011年,GLOVER课题组[32]的研究完善了不同金属中心MOF-74的性能参数,Mg-MOF-74的比表面积最大(其他比表面积参数见表1),也诠释了金属中心为镁的MOF-74材料对CO2具有较高的吸附量的原因。另外Mg-MOF-74与MIL系列和Cu-BTC系列相比,其优势还表现在其吸附氨后仍能保留原有对CO2的吸附性能,并推测其对CO2吸附量会增加。在MOF-74吸附小分子气体的研究历程中,有研究者发现除了单金属MOF-74对NH3、CO、CO2等表现出良好的吸附性能外,多金属MOF-74的吸附性能也很突出。2015年,ORCAJO等[33]制备出了多金属配位不饱和MOF-74,在低温和室温条件下对氢气表现出良好的吸附效果,如Ni50Co-MOF-74。由此可推测多金属中心会对MOFs的吸附性能存在一定影响。那么将单金属中心换为与CO2相互作用较强的多金属中心,其吸附能力应该会有所改变。同年,WONGSAKULPHASATCH等[34]在MIL-127结构的基础上采用次级结构单元法制备出基于铁离子的混合价态多金属MOFs材料MOF-Fe(Ⅲ)/M(Ⅱ)(M=Ni、Co、Mg),结构如图5,并将其用于CO和CO2二元混合气体吸附实验。研究表明随着二价金属的改变,该材料对CO的吸附选择性有明显变化:Ni2+>Co2+>Fe2+>Mg2+,而CO2的吸附能力几乎不受影响。因此从实验结果中可以推断MOF-Fe(Ⅲ)/Mg(Ⅱ)应用于混合气体选择性吸附CO2将占一定优势。2016年,ZHANG等[12]利用13C、17O固体核磁(SSNMR)进一步研究MIL-53系列的金属中心和氨官能团对MOFs吸附CO2的影响,结果表明MIL-53-NH3(Al)>MIL-53-NH3(Ga)>MIL-53(Al)>MIL-53(Ga)。研究者表示由于金属中心原子不同,原子半径不同,其可能影响金属-氧之间的键长和键角,同时还可能影响CO2与孔表面即配体间的相互作用强度。

表1 不同金属中心的MOF-74的比表面积[32]
3.2 客体分子或官能团
在具有配位不饱和金属中心的基础上,对MOFs材料进行表面功能化修饰会使其对吸附质的吸附能力明显增加。KITAGAWA及其研究人员曾提出通过固定不饱和金属配位(CUSs)[35]和引入有机官能团[36]修饰多孔配位聚合物孔表面的概念。其中官能团主要是含氮的有机官能团或其他极性官能团,如—NH2、—F、—Br、—Cl、—OH、—COOH、—NO2等,—NH2的研究最为集中。
究其原因,有研究者提出孔容积被划分[37]和吸附位被分割[26]两种概念。经GCMC和DFT计算模拟和实验研究表明,这两个概念并不矛盾,而是相辅相成。插入的客体分子将金属中心吸附位分割为两个独立的对称吸附位,使每个金属中心可吸附两个CO2分子,如图12。同时,配体中的—COOH分子内会形成氢键,并极化相邻的—OH,使得其与CO2分子间的相互作用增强,如图13[25]。除此,研究者发现氨基官能团有着同样的影响作用。
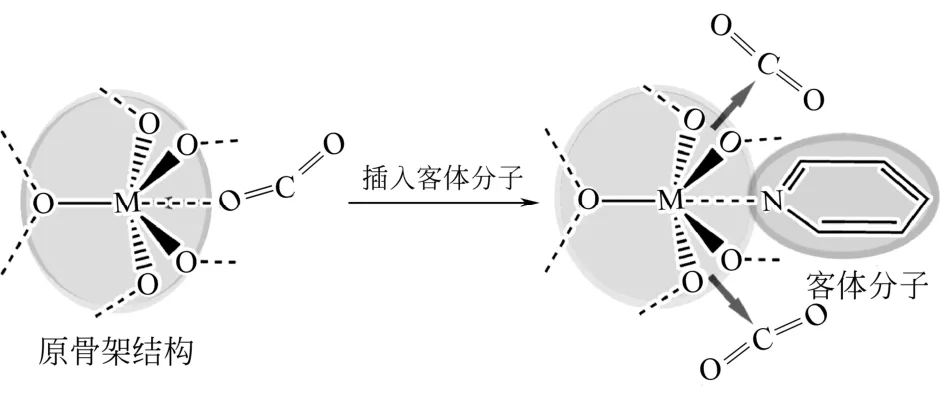
图12 客体分子的插入将不饱和金属位分割为两个对称的吸附位[25]
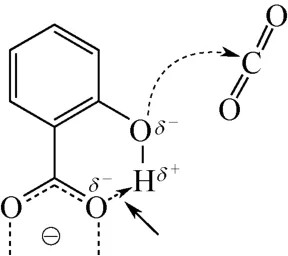
图13 有机配体中羧基对相邻羟基的影响[25]
在2005—2011年期间,研究者针对MIL-53(Al)及其氨功能化修饰后对CO2吸附性能进行研究。研究结果均推测NH2-MIL-53(Al)中的—NH2官能团可能与CO2直接相互作用,或影响配体中—OH官能团的酸性,进而影响MIL-53(Al)的CO2吸附性能[38]。有实验表明低温相MIL-53(Al)经氨基功能化修饰后,对CO2的吸附量会由为10%增至12%~30%(质量分数)[39-41]。2015年,SERRA-CRESPO等[42]结合实验与理论模拟进一步验证了NH2-MIL-53(Al)对变压气体体系下的CO2具有较好的吸附选择性和性能。2016年,ZHANG等[12]的研究进一步完整地解释了—NH2官能团使配体羟基中的H原子与CO2中的C原子间偶极耦合作用增强,进而使CO2与孔表面的相互作用增加。除此,MCDONALD等[43]研究也指出氨基功能化修饰的Mg-MOF-74系列,相对于传统的胺类硅酸盐、胺类水溶液,在低压低温(40℃)的条件下对空气与烟道气中CO2的吸附选择性高,且吸附能力大。
3.3 水分
由于MOFs材料中的有机配体多为亲水基,且同时水分子与不饱和金属位也会强烈结合,导致在有水蒸气存在的混合气体体系中,MOFs材料的结构会发生变化且不饱和金属吸附位被占用。理论上,不饱和金属位被水分子占用后,与CO2的相互作用位会减少,进而吸附量减少,然而实验验证值却并非如此。
2009年,YAZAYDIN等[44]曾发现微量水分的存在对HKUST-1吸附CO2是有利的,且存在4%(质量分数)水时,HKUST-1对CO2的吸附含量可增加45%,而2010年,LIANG等[45]实验表明在水分存在的混合体系中,Cu-BTC的吸附性能会降低,吸附能力相对干燥环境会降低30%,并推断该材料吸附含水体系中CO2气体会受到限制。因此2012年,SOUBEYRAND-LENOIR等[46]在此基础上开展了实验对水分存在的影响进行详细研究。结果表明,在相对湿度为3%时CO2的吸附量为35mg/g,10%RH时为52mg/g,之后随着湿度的增加,CO2的吸附量开始下降,增至20% RH时,吸附量降为41mg/g,当相对湿度增加至40%时,吸附含量低于20mg/g。推测该原因是由于水分子中的羟基会与CO2相互作用,在低湿度的环境中,虽然水分子会占用金属吸附位,但它不会使CO2的吸附量降低,反而增加;然而大量水蒸气存在时会导致HKUST-1的结构出现坍塌损坏[47],使吸附量降低。对于MIL-100,在吸附含有水蒸气的混合气中的CO2时也出现了类似的情况。2012年,SOUBEYRANDLENOIR等[46]在低压(0.2bar,1bar=105Pa)条件下,用MIL-100(Fe)吸附不同相对湿度(3%、20%、40%)环境中得CO2,结果表明,在3% RH时吸附量为26mg/g,20% RH时为66mg/g,40% RH时为105mg/g,吸附量约增加了5倍,且循环2~3次的情况下其吸附量仍不变。2016年,ZÁRATE等[48]研究MIL-53系列材料吸附CO2时水分的影响,结果表明MIL-53(Al)的水稳性要比NH2-MIL-53(Al)的水稳性好,且在不同湿度的环境中,MIL-53(Al)都能始终保持较好的吸附性能。在30℃、相对湿度为5%的条件下,MIL-53(Al)对CO2的最大吸附量将近6%(质量分数),约为无水条件下吸附量的1.7倍,然而NH2-MIL-53(Al)的对CO2的吸附性能却大幅度降低[48],原因同HKUST-1类似。
对于MOF-74,研究者也做过相关的研究,但不是很完整。2010年,LIU等[49]针对水对CPO-27材料CO2吸附性能的影响研究,只是发现混合气中含有一定量水分时对DOBDC(Ni-COP-74)吸附CO2并不会有很大影响。因此推测MOF-74与MIL系列和Cu-BTC相比,用于有水蒸气的混合气体体系吸附CO2会具有更强的优势。然而实验也表明湿度较高时,同样会有不利影响,水分子会与未被有机配体中氧原子配位的金属中心键合,而CO2则会与该水分子通过氢键相互作用,因而低湿度时吸附量增加。但与M—O之间的键能相比,氢键的键能较低,进而高湿度时CO2的吸附量降低[50],如图14。
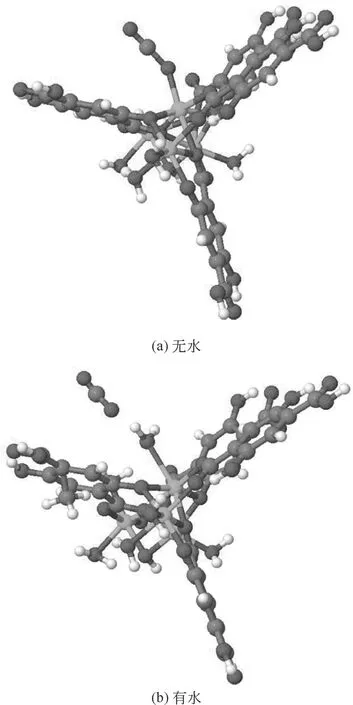
图14 水分子对Mg-MOF-74吸附性能的影响[50]
3.4 合成方法及合成条件的影响
合成方法及合成条件主要影响MOFs的晶形、孔表面、孔径等结构性能。2008年,HARTMANN等[51]分别采用热液合成法、常压合成法和电化学合成法制备Cu3(BTC)2,并用于CO2吸附。结果表明合成方法不同,该材料的表面积、孔容积及吸附性能会有差异。特别是在常压下,采用乙醇回流方法制备的Cu3(BTC)2具有较高的孔隙率(VP=0.62cm3/g)与表面积(S=1624m2/g)(其他方法的数据见表2)。2009年[52]HONG等[52]采用水热法和微波辐射合成法两种方法制备MIL-101。和水热法相比,微波合成法的制备时间大大缩短,且MIL-101的晶体粒度均一,便于控制,如图15。同时该研究也表明了当合成方法相同时,合成条件的影响以温度和时间为主,溶剂浓度与活化处理方法为辅。2012年,CHO等[13]同样利用溶剂热法和微波加热法制备Co-MOF-74,产物在合成所需时间、结构性能与吸附性能方面的区别很大。采用溶剂热合成法制备单晶需要24h,且颗粒大小长约为300μm,宽约为70μm,而微波加热法的合成时间则仅需1h,且颗粒要小得多,长约50μm,宽约8μm(如图16,其他性能参数见表3),进一步表明微波热法相对更具有优势,该法制备的Co-MOF-74对CO2的吸附量相较于其他增至288mg/g,对CO2表现出高的吸附选择性。另外,经此方法合成的Co-MOF-74经过8次吸附/解吸循环后,其吸附能力未有很大变化,对CO2的吸附量仍可达210mg/g。
另外对于不同的MOFs材料,制备方法的不同除了影响该材料结构、吸附性能,还会影响它的热稳定性。2012年,LEE等[53]在Mg-MOF-74结构的低稳定性问题的基础上,通过晶种层层包覆和第二次生长的方法制备出Ni-MOF-74膜,在高温高压的条件下可表现出极好的热稳定性;而在2016年,SORRIBAS等[54]利用二次生长法制备出的MIL-53(Al)由于稳定性差而不能用于循环吸附,导致其应用受到限制。
除了以上主要影响因素外,吸附初始条件对吸附材料的吸附性能也有一定影响,如温度、压力、混合气中CO2的浓度等,在此不作详细介绍。
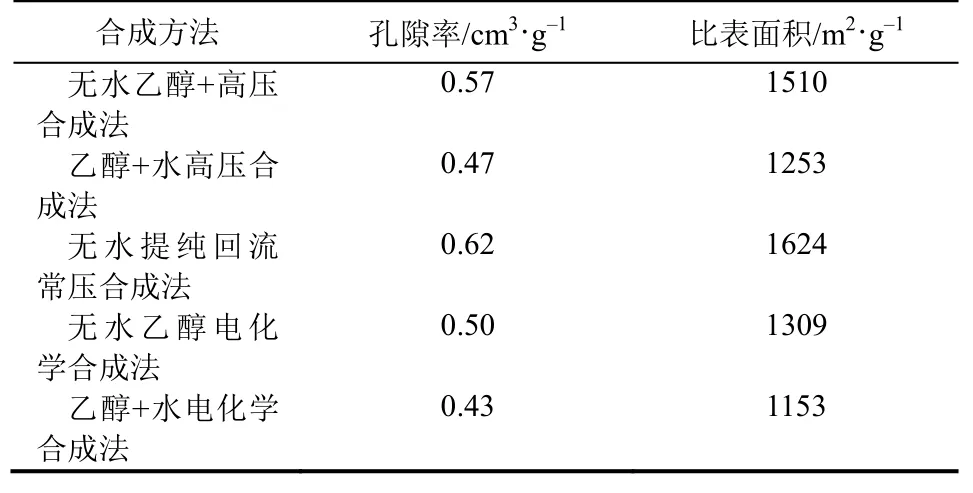
表2 不同方法制备出的Cu3(BTC)2的结构性能[51]

图15 MIL-101的电镜扫描图[52]

图16 Co-MOF-74的电镜扫描图[13]

表3 Co-MOF-74的结构性能[14]
4 结语
综上所述,MOFs材料由于具有多样的拓扑结构和优越的吸附性能而被广为关注,通过合理设计、活化处理产生不饱和金属位和表面功能化修饰后更拓展了其在吸附分离方面的应用领域。本篇文章旨在总结具有不饱和金属位MOFs材料的结构、对CO2的吸附机理及吸附性能的影响因素,为设计最佳吸附CO2的MOFs材料奠定理论基础,也预测了未来MOFs发展的几个方向:①选择合适高效的制备方法合成MOFs;②选择物理性质与化学性质较优的、与CO2相互作用力强的金属离子与有机配体,合成具有不饱和金属位的MOFs类似物,如过渡金属、镧系元素金属、含有两个或两个以上路易斯酸位的多金属化合物和多核金属簇;③引入亲CO2的含氮或极性较强的官能团,如氨基、羟基、羧基等。面对如今捕集CO2技术的挑战,新型的配位不饱和MOFs材料将有广阔的发展前景。
[1] SEO Y K,YOON J W,LEE J S,et al. Energy-efficient dehumidification over hierachically porous metal–organic frameworks as advanced water adsorbents[J]. Advanced Materials,2012,24(6):806-810.
[2] MA S,ZHOU H C. Gas storage in porous metal-organic frameworks for clean energy applications[J]. Chemical Communications,2010,46(1):44-53.
[3] SUMIDA K,ROGOW D L,MASON J A,et al. Carbon dioxide capture in metal–organic frameworks[J]. Chemical Reviews,2011,112(2):724-781.
[4] JEONG N C,SAMANTA B,LEE C Y,et al. Coordination-chemistry control of proton conductivity in the iconic metal-organic framework material HKUST-1[J]. Journal of the American Chemical Society,2011,134(1):51-54.
[5] 仲崇立,刘大欢,阳庆元,著. 金属有机骨架材料的构效关系及设计[M] 北京:科学出版社,2013. ZHONG C L,LIU D H,YANG Q Y. Structure-activity relationship and design of metal organic framework materials [M] Beijing:Science Press,2013.
[6] CHUI S S Y,LO S M F,CHARMANT J P H,et al. A chemically functionalizable nanoporous material [Cu3(TMA)2(H2O)3]n[J]. Science,1999,283(5405):1148-1150.
[7] SCHLICHTE K,KRATZKE T,KASKEL S. Improved synthesis,thermal stability and catalytic properties of the metal-organic framework compound Cu3(BTC)2[J]. Microporous and Mesoporous Materials,2004,73(1):81-88
[8] FÉREY G,MELLOT-DRAZNIEKS C,SERRE C,et al. A chromium terephthalate-based solid with unusually large pore volumes and surface area[J]. Science,2005,309(5743):2040-2042.
[9] LLEWELLYN P L,BOURRELLY S,SERRE C,et al. High uptakes of CO2and CH4in mesoporous metal-organic frameworks MIL-100 and MIL-101[J]. Langmuir,2008,24(14):7245-7250.
[10] HWANG Y K,HONG D Y,CHANG J S,et al. Amine grafting on coordinatively unsaturated metal centers of MOFs:consequences for catalysis and metal encapsulation[J]. Angewandte Chemie International Edition,2008,47(22):4144-4148.
[11] LOISEAU T,SERRE C,HUGUENARD C,et al. A rationale for the large breathing of the porous aluminum terephthalate(MIL-53)upon hydration[J]. Chemistry——A European Journal,2004,10(6):1373-1382.
[12] ZHANG Y,LUCIER B E G,HUANG Y. Deducing CO2motion,adsorption locations and binding strengths in a flexible metal-organic framework without open metal sites[J]. Physical Chemistry Chemical Physics,2016,18(12):8327-8341.
[13] CHO H Y,YANG D A,KIM J,et al. CO2adsorption and catalytic application of Co-MOF-74 synthesized by microwave heating[J]. Catalysis Today,2012,185(1):35-40.
[14] PALOMINO C C,GÓMEZ-POZUELO G,NACHTIGALL P,et al. Metal Organic Frameworks M-MOF-74 and M-MIL-100:comparison of textural,acidic and catalytic properties[J]. ChemPlusChem,2016,81(8):828-835.
[15] KATZ M J,HOWARTH A J,MOGHADAM P Z,et al. High volumetric uptake of ammonia using Cu-MOF-74/Cu-CPO-27[J]. Dalton Transactions,2015,45(10):4150-4153.
[16] LI J R,YU J,LU W,et al. Porous materials with pre-designed single-molecule traps for CO2selective adsorption[J]. Nature Communications,2013,4:1538.DOI:10.1038/ncomms2552.
[17] XU H,HE Y,ZHANG Z,et al. A microporous metal-organic framework with both open metal and Lewis basic pyridyl sites for highly selective C2H2/CH4and C2H2/CO2gas separation at room temperature[J]. Journal of Materials Chemistry A,2013,1(1):77-81.
[18] GUO Z,WU H,SRINIVAS G,et al. A metal-organic framework with optimized open metal sites and pore spaces for high methane storage at room temperature[J]. Angewandte Chemie International Edition,2011,50(14):3178-3181.
[19] WEN H M,LI B,WANG H,et al. A microporous metal-organic framework with rare lvt topology for highly selective C2H2/C2H4separation at room temperature[J]. Chemical Communications,2015,51(26):5610-5613.
[20] YANG Q,JOBIC H,SALLES F,et al. Probing the dynamics of CO2and CH4within the porous zirconium terephthalate UiO-66(Zr):a synergic combination of neutron scattering measurements and molecular simulations[J]. Chemistry——A European Journal,2011,17(32):8882-8889.
[21] VALVEKENS P,VERMOORTELE F,DE Vos D. Metal-organic frameworks as catalysts:the role of metal active sites[J]. Catalysis Science & Technology,2013,3(6):1435-1445.
[22] VANDICHEL M,HAJEK J,VERMOORTELE F,et al. Active site engineering in UiO-66 type metal–organic frameworks by intentional creation of defects:a theoretical rationalization[J]. CrystEngComm,2015,17(2):395-406.
[23] YANG Q,WIERSUM A D,LLEWELLYN P L,et al. Functionalizing porous zirconium terephthalate UiO-66(Zr) for natural gas upgrading:a computational exploration[J]. Chemical Communications,2011,47(34):9603-9605.
[24] VALENZANO L,CIVALLERI B,CHAVAN S,et al. Disclosing the complex structure of UiO-66 metal organic framework:a synergic combination of experiment and theory[J]. Chemistry of Materials,2011,23(7):1700-1718.
[25] NIJEM N,CANEPA P,KONG L,et al. Spectroscopic characterization of van der Waals interactions in a metal organic framework with unsaturated metal centers:MOF-74-Mg[J]. Journal of Physics:Condensed Matter,2012,24(42):424203.
[26] TIAN Z,DAI S,JIANG D. Site partition:turning one site into two for adsorbing CO2[J]. The Journal of Physical Chemistry Letters,2016.
[27] CASKEY S R,WONG-Foy A G,MATZGER A J. Dramatic tuning of carbon dioxide uptake via metal substitution in a coordination polymer with cylindrical pores[J]. Journal of the American Chemical Society,2008,130(33):10870-10871.
[28] KARRA J R,WALTON K S. Molecular simulations and experimental studies of CO2,CO,and N2adsorption in metal-organic frameworks[J]. The Journal of Physical Chemistry C,2010,114(37):15735-15740.
[29] RUBEŠ M,WIERSUM A D,LLEWELLYN P L,et al. Adsorption of propane and propylene on Cu-BTC metal-organic framework:combined theoretical and experimental investigation[J]. The Journal of Physical Chemistry C,2013,117(21):11159-11167.
[30] GRAJCIAR L,NACHTIGALL P,BLUDSKÝ O,et al. Accurate ab initio description of adsorption on coordinatively unsaturated Cu2+and Fe3+sites in MOFs[J]. Journal of Chemical Theory and Computation,2014,11(1):230-238.
[31] EUBANK J F,WHEATLEY P S,LEBARS G,et al. Porous,rigid metal (III)-carboxylate metal-organic frameworks for the delivery of nitric oxide[J]. APL Materials,2014,2(12):124112.
DOI:10.1063/1.4904069.
[32] GLOVER T G,PETERSON G W,SCHINDLER B J,et al. MOF-74 building unit has a direct impact on toxic gas adsorption[J]. Chemical Engineering Science,2011,66(2):163-170.
[33] ORCAJO G,VILLAJOS J A,MARTOS C,et al. Influence of chemical composition of the open bimetallic sites of MOF-74 on H2adsorption [J]. Adsorption,2015,21(8):589-595.
[34] WONGSAKULPHASATCH S,NOUAR F,RODRIGUEZ J,et al. Direct accessibility of mixed-metal (Ⅲ/Ⅱ)acid sites through the rational synthesis of porous metal carboxylates[J]. ChemicalCommunications,2015,51(50):10194-10197.
[35] KITAGAWA S,NORO S,NAKAMURA T. Pore surface engineering of microporous coordination polymers[J]. Chemical Communications,2006(7):701-707.
[36] HASEGAWA S,HORIKE S,MATSUDA R,et al. Three-dimensional porous coordination polymer functionalized with amide groups based on tridentate ligand:selective sorption and catalysis[J]. Journal of the American Chemical Society,2007,129(9):2607-2614.
[37] ZHENG S T,BU J T,LI Y,et al. Pore space partition and charge separation in cage-within-cage indium-organic frameworks with high CO2uptake[J]. Journal of the American Chemical Society,2010,132(48):17062-17064.
[38] STAVITSKI E,PIDKO E A,COUCK S,et al. Complexity behind CO2capture on NH2-MIL-53 (Al)[J]. Langmuir,2011,27(7):3970-3976.
[39] BOURRELLY S,LLEWELLYN P L,SERRE C,et al. Different adsorption behaviors of methane and carbon dioxide in the isotypic nanoporous metal terephthalates MIL-53 and MIL-47[J]. Journal of the American Chemical Society,2005,127(39):13519-13521.
[40] ARSTAD B,FJELLVÅG H,KONGSHAUG K O,et al. Amine functionalised metal organic frameworks (MOFs) as adsorbents for carbon dioxide[J]. Adsorption,2008,14(6):755-762.
[41] COUCK S,DENAYER J F M,BARON G V,et al. An amine-functionalized MIL-53 metal− organic framework with large separation power for CO2and CH4[J]. Journal of the American Chemical Society,2009,131(18):6326-6327.
[42] SERRA-CRESPO P,BERGER R,YANG W,et al. Separation of CO2/CH4mixtures over NH2-MIL-53-an experimental and modelling study[J]. Chemical Engineering Science,2015,124:96-108.
[43] MCDONALD T M,LEE W R,MASON J A,et al. Capture of carbon dioxide from air and flue gas in the alkylamine-appended metal-organic framework mmen-Mg2(dobpdc)[J]. Journal of the American Chemical Society,2012,134(16):7056-7065.
[44] YAZAYDIN A O,BENIN A I,FAHEEM S A,et al. Enhanced CO2adsorption in metal-organic frameworks via occupation of open-metal sites by coordinated water molecules[J]. Chemistry of Materials,2009,21(8):1425-1430.
[45] LIANG Z,MARSHALL M,CHAFFEE A L. CO2adsorption-based separation by metal organic framework(Cu-BTC)versus zeolite(13X)[J]. Energy & Fuels,2009,23(5):2785-2789.
[46] SOUBEYRAND-LENOIR E,VAGNER C,YOON J W,et al. How water fosters a remarkable 5-fold increase in low-pressure CO2uptake within mesoporous MIL-100(Fe)[J]. Journal of the American Chemical Society,2012,134(24):10174-10181.
[47] GUL-E-NOOR F,JEE B,PÖPPL A,et al. Effects of varying water adsorption on a Cu3(BTC)2metal–organic framework(MOF)as studied by1H and13C solid-state NMR spectroscopy[J]. Physical Chemistry Chemical Physics,2011,13(17):7783-7788.
[48] ZÁRATE A,PERALTA R A,BAYLISS P A,et al. CO2capture under humid conditions in NH2-MIL-53(Al):the influence of the amine functional group[J]. RSC Advances,2016,6(12):9978-9983.
[49] LIU J,WANG Y,BENIN A I,et al. CO2/H2O adsorption equilibrium and rates on metal-organic frameworks:HKUST-1 and Ni/DOBDC[J]. Langmuir,2010,26(17):14301-14307.
[50] PENTYALA V,DAVYDOVSKAYA P,ADE M,et al. Carbon dioxide gas detection by open metal site metal organic frameworks and surface functionalized metal organic frameworks[J]. Sensors and Actuators B:Chemical,2016,225:363-368.
[51] HARTMANN M,KUNZ S,HIMSL D,et al. Adsorptive separation of isobutene and isobutane on Cu3(BTC)2[J]. Langmuir,2008,24(16):8634-8642.
[52] HONG D Y,HWANG Y K,SERRE C,et al. Porous chromium terephthalate MIL-101 with coordinatively unsaturated sites:surface functionalization,encapsulation,sorption and catalysis[J]. Advanced Functional Materials,2009,19(10):1537-1552.
[53] LEE D J,LI Q,KIM H,et al. Preparation of Ni-MOF-74 membrane for CO2separation by layer-by-layer seeding technique[J]. Microporous and Mesoporous Materials,2012,163:169-177.
[54] SORRIBAS S,ZORNOZA B,SERRA-CRESPO P,et al. Synthesis and gas adsorption properties of mesoporous silica-NH2-MIL-53(Al)core–shell spheres[J]. Microporous and Mesoporous Materials,2016,225:116-121.
Research progress of CO2adsorption using coordinatively unsaturated MOFs materials
ZHAO Qian,FENG Dong,WANG Yang,ZHAO Wenbo
(Faculty of Chemical Engineering,Kunming University of Science and Technology,Kunming 650500,Yunnan,China)
MOFs are a kind of potentially ideal adsorbents with coordinative unsaturated metal sites(UMSs). It can be used to separate and store small molecule gas. This article reviewed the development of MOFs materials in CO2capture in recent years. We summarized some typical coordinatively unsaturated metal-organic materials,such as MIL series,Cu-BTC,MOF-74 and so on,which are suitable for capturing CO2. This work would help us to understand the metal-organic porous materials and expand their application in CO2capture in the future. At the same time,this paper also pointed out that open metal sites play an important role on the adsorption performance of the porous MOFs materials. At present,the efficiency of porous MOFs materials for CO2capture is far from the industrial requirement,so reasonable design of MOFs metal center,activating treatment after syntheses and the functionalized modifications on the pore channel surface would be the development directions for these type materials. At the end,we made the conclusions from the aspect of the preparation methods,the metal centers and surface modification.
coordinatively unsaturated metal sites;MOFs;porous MOFs material;CO2capture;adsorption;surface modification
TB34
:A
:1000–6613(2017)05–1771–11
10.16085/j.issn.1000-6613.2017.05.027
2016-08-22;修改稿日期:2017-01-12。
云南省自然科学基金(2014FB118)及国家自然科学基金(21306071,21666011)项目。
赵倩(1990—),女,硕士研究生,主要从事金属有机骨架多孔材料吸附CO2。E-mail:845651208@qq.com。联系人:赵文波,博士,副教授,主要从事有机碳酸酯合成研究。E-mail:wenshuixing@126.com。
