丘脑底核脑深部电刺激术联合药物治疗帕金森病有效性和安全性的Meta分析
2017-05-15王海姣陈邓朱丽娜谭戈徐达刘凌
王海姣 陈邓 朱丽娜 谭戈 徐达 刘凌
·循证神经病学·
丘脑底核脑深部电刺激术联合药物治疗帕金森病有效性和安全性的Meta分析
王海姣 陈邓 朱丽娜 谭戈 徐达 刘凌
目的评价丘脑底核脑深部电刺激术联合药物治疗帕金森病的有效性和安全性。方法以subthalamic nucleus、deep brain stimulation、DBS、STN、Parkinson disease、random等英文检索词,计算机检索1980年1月1日-2016年10月1日美国国立医学图书馆生物医学信息检索系统、荷兰医学文摘、Cochrane图书馆等数据库收录的关于丘脑底核脑深部电刺激术联合药物治疗帕金森病的随机对照临床试验,采用Jadad量表、Cochrane系统评价手册和Rev Man 5.2统计软件进行文献质量评价和Meta分析。结果共获得3245篇文献,经剔除重复和不符合纳入标准者,最终纳入6项高质量(Jadad评分≥4分)临床试验共958例帕金森病患者。Meta分析显示:与单纯药物治疗相比,丘脑底核脑深部电刺激术联合药物治疗可以显著降低帕金森病患者服药(SMD=⁃0.570,95%CI:⁃0.710~⁃0.430;P=0.000)和未服药(SMD=⁃1.170,95%CI:⁃1.500~⁃0.850;P=0.000)状态下统一帕金森病评价量表第三部分(UPDRSⅢ)评分,以及UPDRSⅠ评分(SMD=⁃0.150,95%CI:⁃0.290~⁃0.010;P=0.030)和39项帕金森病调查表评分(SMD=⁃0.510,95%CI:⁃0.660~⁃0.370;P=0.000);但增加严重不良事件(RD=0.140,95%CI:0.090~0.190;P=0.000)和构音障碍不良事件(RD=0.070,95%CI:0.010~0.120;P=0.020)发生率,而减少运动障碍不良事件发生率(RR=0.450,95%CI:0.330~0.620;P=0.000)。结论丘脑底核脑深部电刺激术联合药物治疗能够显著改善帕金森病患者运动功能、精神状态和生活质量,但术后发生严重不良事件和构音障碍不良事件的风险增加,应引起临床医师的重视。
帕金森病;丘脑底核;深部脑刺激法;药物疗法;Meta分析
帕金森病(PD)是常见于中老年人群的神经变性病,以静止性震颤、运动迟缓、肌强直和姿势步态异常为主要临床特征。除运动症状外,嗅觉减退、便秘、睡眠障碍和抑郁症状等非运动症状(NMS)也是其重要临床特征,严重影响帕金森病患者生活质量[1]。脑深部电刺激术(DBS)是一种通过影像学方法(CT或MRI)立体定位靶点,手术植入微电极并予以电刺激,从而改善运动症状和减少左旋多巴剂量的治疗技术[2],其刺激靶点主要是丘脑底核(STN)、苍白球内侧部(GPi)、丘脑腹中间核(Vim)和脚桥核(PPN),尤以丘脑底核是最常见的脑深部电刺激术靶点,而脚桥核尚未被美国食品与药品管理局(FDA)批准,但已提议作为潜在刺激靶点改善帕金森病患者姿势步态异常[3]。丘脑底核脑深部电刺激术对改善静止性震颤、肌强直、运动迟缓和异动症等运动症状疗效显著,已广泛应用于帕金森病中晚期治疗[4],但对非运动症状的疗效尚不确定,缺乏循证医学证据的支持[5],且丘脑底核脑深部电刺激术联合药物治疗后常见不良事件类型和发生风险尚不明确,本文旨在系统评价丘脑底核脑深部电刺激术联合药物治疗帕金森病的随机对照临床试验,以探讨其有效性和安全性。
资料与方法
一、文献检索
参照PRISMA原则,采用预先设计的文献检索策略,分别以subthalamic nucleus、deep brain stimulation、DBS、STN、Parkinson disease、random等英文词汇为检索词,计算机检索美国国立医学图书馆生物医学信息检索系统(Pub Med)、荷兰医学文摘(EMBASE/SCOPUS)、Cochrane图书馆等数据库收录的关于丘脑底核脑深部电刺激术联合药物治疗帕金森病的随机对照临床试验,同时查阅纳入研究的参考文献以补充可能遗漏的相关临床研究。检索时间为1980年1月1日-2016年10月1日。
二、纳入与排除标准
1.纳入标准(1)研究类型:丘脑底核脑深部电刺激术联合药物治疗帕金森病的随机对照临床试验。(2)研究对象:所纳入的研究对象性别、年龄不限,均符合英国帕金森病学会脑库帕金森病临床诊断标准(包含静止性震颤、肌强直、运动迟缓中至少2项)[6];有独立能力并签署知情同意书;排除继发性帕金森综合征、阿尔茨海默病(AD)、精神病、头部手术史、严重肝肾功能障碍和严重营养不良患者。(3)干预措施:试验组为丘脑底核脑深部电刺激术联合药物治疗帕金森病组(STN⁃DBS+BMT组),对照组为最佳药物治疗组(BMT组),药物均为左旋多巴。(4)结局指标:各项研究中均报道或4项及其以上研究报道的指标,对运动症状、精神状态和日常生活质量进行评价;严重不良事件(SAE):符合国际医学用语词典(Med DRA)的定义,系临床试验过程中发生的需住院治疗、延长住院时间、伤残、影响工作能力、危及生命或死亡、导致先天性畸形等事件;其他不良事件:各项研究中均报道或3项及以上研究报道的发生率超过1%的不良事件。
2.排除标准(1)非随机对照临床试验、动物实验、综述和个案报道等。(2)研究对象的纳入与排除标准不明确或不合理。(3)失访率过高或随访时间不符合研究设计。(4)干预措施虽是脑深部电刺激术,但刺激靶点不是丘脑底核或刺激靶点不详的研究。(5)结局指标不明确或为非量化指标如图像等。
三、文献筛选及数据提取
由两位相互独立的评价者根据纳入与排除标准,分别对文献进行筛选。首先,通过阅读文题和摘要,剔除重复和不符合纳入标准者;其次,对可能纳入的文献进一步阅读全文并交叉核对结果;最后,对存在异议的文献,由两位评价者共同讨论协商,仍不能取得一致意见时,请第三位评价者进一步评价。对资料存疑或资料缺失的文献,通过与作者或通讯作者联系,尽可能获得确认或补充。对符合纳入标准的文献提取以下数据资料:(1)一般资料,包括文题、作者、来自国家或地区、发表日期等。(2)研究特征,包括研究对象的一般资料、各组基线可比性如患病时间、干预措施、随访时间等。(3)结局指标,疗效指标,采用统一帕金森病评价量表第三部分(UPDRSⅢ)[7]评价运动功能,统一帕金森病评价量表第一部分(UPDRSⅠ)[7]评价精神状态,39项帕金森病调查表(PDQ⁃39)[8]评价生活质量(评分越高、生活质量越差);严重不良事件,符合国际医学用语词典的定义;其他不良事件。
四、文献质量评价
1.Jadad量表评价文献质量参照Jadad量表[9]质量评价标准对文献质量进行评价,如果一项试验经过补充资料多次发表,则选择资料最全的一次。(1)随机分组序列的产生方法:通过计算机产生的随机分组序列或随机数字表法产生的序列,2分;试验提及随机分配,但文中未交待随机序列的产生方法,1分;半随机或准随机试验,采用交替分配病例的方法,如按照入院顺序、出生日期单双号,0分。(2)随机化隐藏:由医疗中心或药房控制分配方案、采用编号一致的容器、现场计算机控制、采用密封不透光的信封或其他使临床医师或受试者无法预知分配序列的方法,2分;仅表明采用随机数字表法或其他随机分配方案,1分;交替分配、系列号、系列编码信封,以及任何不能阻止分组可预测性的措施或未采用随机化隐藏,0分。(3)双盲法:描述实施双盲的具体方法并认为是恰当的,如采用完全一致的安慰剂,2分;文献仅提及双盲但方法不恰当,1分;文献未提及盲法,0分。(4)退出与失访:对退出与失访病例数和退出理由进行详细描述,1分;未提及退出或失访,0分。总评分为7分,评分≥4分者为高质量文献、评分<4分者为低质量文献。
2.Cochrane系统评价手册评价文献偏倚参照Cochrane系统评价手册5.0.1[10]中的偏倚分析方法,分别对文献的选择偏倚、实施偏倚、失访偏倚、选择性报告等进行评价,包括随机序列产生方法、分配隐藏方法、受试者、研究人员和结局测量者设盲情况、结局数据完整性、选择性结局报告及其他偏倚情况。如果一项研究上述7个方面中的1个或多个方面存在较高的偏倚风险,则该项研究判定为高偏倚风险;相反,如果一项研究上述7个方面均为低偏倚风险,则判定为低偏倚风险;如果一项研究上述7个方面中1个或多个方面的偏倚风险不清楚,则判定为偏倚风险不清楚。
五、统计分析方法
采用Cochrane协作网提供的RevMan 5.2软件进行Meta分析。计数资料以Mantel⁃Haensze(lM⁃H)模型计算相对危险度(RR),若结果中含零,则计算率差(RD);计量资料采用倒方差法,以标准化均数差(SMD)表示,效应量的检验水准为α=0.05。根据Higgins等[11]的方法,各项研究之间的异质性检验采用χ2检验,当P>0.100和I2≤50.000%,无异质性,采用固定效应模型进行合并效应分析;当P≤0.100和I2>50.000%时,存在异质性,分析其异质性来源,采用随机效应模型进行合并效应分析。采用敏感性分析评价Meta分析结果的稳定性,将固定效应模型与随机效应模型相互转换,统计量值RD和RR变换为比值比(OR)、SMD变换为均数差(MD)重新计算95%CI,若转换后的研究结论一致则表明Meta分析结果稳定,反之则不稳定。
结果
一、文献检索结果
经初步检索共获得相关英文文献3245篇,阅读文题和摘要,剔除重复和不符合纳入标准的文献3230篇,进一步阅读全文剔除文献9篇,最终共纳入6项质量较高(Jadad评分≥4分)的随机对照临床试验[12⁃19]共958例帕金森病患者,其中Deuschl等[14]和Witt等[17]报告的是同一项随机对照临床试验(试验编号:NCT00196911),Charles等[12]和Tramontana等[19]报告的是同一项随机对照临床试验(试验编号:NCT00282152)。文献检索流程参见图1,所纳入临床试验的基线资料和质量评价参见表1和图2。
二、Meta分析结果
1.丘脑底核脑深部电刺激术联合药物治疗帕金森病的有效性分析(1)运动功能:共计5项临床试验[12⁃14,16,18]报道丘脑底核脑深部电刺激术联合药物治疗前后UPDRSⅢ评分变化,以服药(“开”期)和未服药(“关”期)状态下UPDRSⅢ评分为评价指标,对治疗前后帕金森病患者运动功能进行评价,其中,在服药状态下,共计815例帕金森病患者完成UPDRSⅢ评分,各项研究之间无异质性(P=0.160,I2=39.000%),故采用固定效应模型进行合并效应分析,结果显示:在服药状态下,STN⁃DBS+BMT组与BMT组患者治疗前后UPDRSⅢ评分差异有统计学意义(SMD=⁃0.570,95%CI:⁃0.710~⁃0.430,P=0.000;图3a),提示丘脑底核脑深部电刺激术联合药物治疗较单纯药物治疗更能改善帕金森病患者服药期间的运动功能;在未服药状态下,共计774例帕金森病患者完成UPDRSⅢ评分,各项研究之间有异质性(P=0.004,I2=74.000%),故采用随机效应模型进行合并效应分析,结果显示:在未服药状态下,STN⁃DBS+BMT组与BMT组患者治疗前后UPDRSⅢ评分差异具有统计学意义(SMD=⁃1.170,95%CI:⁃1.500~⁃0.850,P=0.000;图3b),提示丘脑底核脑深部电刺激术联合药物治疗较单纯药物治疗更能改善帕金森病患者未服药期间的运动功能。(2)精神状态:有5项临床试验[12⁃14,16,18]报道丘脑底核脑深部电刺激术联合药物治疗前后UPDRSⅠ评分变化,共计827例帕金森病患者,以UPDRSⅠ评分为评价指标,对治疗前后帕金森病患者精神状态进行评价,各项研究之间无异质性(P=0.910,I2=0.000%),故采用固定效应模型进行合并效应分析,结果显示:STN⁃DBS+BMT组与BMT组患者治疗前后UPDRSⅠ评分差异有统计学意义(SMD=⁃0.150,95%CI:⁃0.290~⁃0.010,P=0.030;图4),提示丘脑底核脑深部电刺激术联合药物治疗较单纯药物治疗更能改善帕金森病患者精神状态。(3)日常生活质量:有5项临床试验[12,14⁃16,18]报道丘脑底核脑深部电刺激术联合药物治疗前后PDQ⁃39评分变化,其中1项[15]提供的数据为中位数和四分位数间距,经与原作者联系仍未获得均数和标准差,予剔除,最终纳入4项试验[12,14,16,18],共计709例帕金森病患者,以PDQ⁃39评分为评价指标,对治疗前后帕金森患者生活质量进行评价,各项研究之间无异质性(P=0.220,I2=32.000%),故采用固定效应模型进行合并效应分析,结果显示:STN⁃DBS+BMT组与BMT组治疗前后PDQ⁃39评分差异具有统计学意义(SMD=⁃0.510,95%CI:⁃0.660~⁃0.370,P=0.000;图5),提示丘脑底核脑深部电刺激术联合药物治疗较单纯药物治疗更能改善帕金森病患者生活质量。

图1 文献检索流程图Figure 1 Flow chart of screening literatures.
2.丘脑底核脑深部电刺激术联合药物治疗帕金森病的安全性分析(1)严重不良事件发生率:5项临床试验[12⁃14,16,18]均报道丘脑底核脑深部电刺激术联合药物治疗后严重不良事件发生率,主要包括颅内出血(0.5%)、自杀(1.3%~1.6%)、肺部感染(1.3%)等原因导致的死亡,植入部位感染(2.0%~2.6%)、癫发作(1%)等手术相关不良事件,肢体灵活性下降(3.8%~4.0%)等药物或帕金森病相关不良事件,各项研究之间无异质性(P=0.110,I2= 47.000%),故采用固定效应模型进行合并效应分析,结果显示:STN⁃DBS+BMT组与BMT组患者治疗后严重不良事件发生率差异有统计学意义(RD= 0.140,95%CI:0.090~0.190,P=0.000;图6),提示丘脑底核脑深部电刺激术联合药物治疗较单纯药物治疗发生严重不良事件的风险更大。(2)抑郁不良事件发生率:有5项临床试验[12⁃16]均报道丘脑底核脑深部电刺激术联合药物治疗后抑郁不良事件发生率,各项研究之间无异质性(P=0.150,I2= 41.000%),故采用固定效应模型进行合并效应分析,结果显示:STN⁃DBS+BMT组与BMT组患者治疗后抑郁不良事件发生率差异无统计学意义(RD= 0.020,95%CI:⁃0.040~0.080,P=0.570;图7),提示丘脑底核脑深部电刺激术联合药物治疗并不增加抑郁不良事件的风险。(3)构音障碍不良事件发生率:有3项临床试验[13⁃14,16]均报道丘脑底核脑深部电刺激术联合药物治疗后构音障碍不良事件发生率,各项研究之间有异质性(P=0.120,I2=54.000%),故采用随机效应模型进行合并效应分析,结果显示:STN⁃DBS+BMT组与BMT组患者治疗后构音障碍不良事件发生率差异有统计学意义(RD=0.070,95%CI:0.010~0.120,P=0.020;图8),提示丘脑底核脑深部电刺激术联合药物治疗可以增加构音障碍不良事件的风险。(4)运动障碍不良事件发生率:有3项临床试验[13⁃14,16]均报道丘脑底核脑深部电刺激术联合药物治疗后运动障碍不良事件发生率,各项研究之间有异质性(P=0.330,I2=10.000%),故采用固定效应模型进行合并效应分析,其结果显示:STN⁃DBS+BMT组与BMT组患者治疗后运动障碍不良事件发生率差异有统计学意义(RR=0.450,95%CI:0.330~0.620,P=0.000;图9)。提示丘脑底核脑深部电刺激术联合药物治疗可以减少运动障碍不良事件的风险。(5)其他不良事件发生率:3项试验[13⁃14,16]共同报道的不良事件为皮下血肿(RD= 0.020,95%CI:⁃0.010~0.040;P=0.190)、认知功能障碍(RD=0.020,95%CI:⁃0.010~0.040;P=0.150)、精神障碍(RD=⁃0.020,95%CI:⁃0.090~0.040;P= 0.500)、睡眠障碍(RD=0.020,95%CI:⁃0.040~0.080;P=0.490)和步态障碍(RD=0.020,95%CI:⁃0.030~0.070;P=0.480),其发生率差异无统计学意义,提示丘脑底核脑深部电刺激术联合药物治疗并不增加皮下血肿、认知功能障碍、精神障碍、睡眠障碍和步态障碍等不良事件的风险。
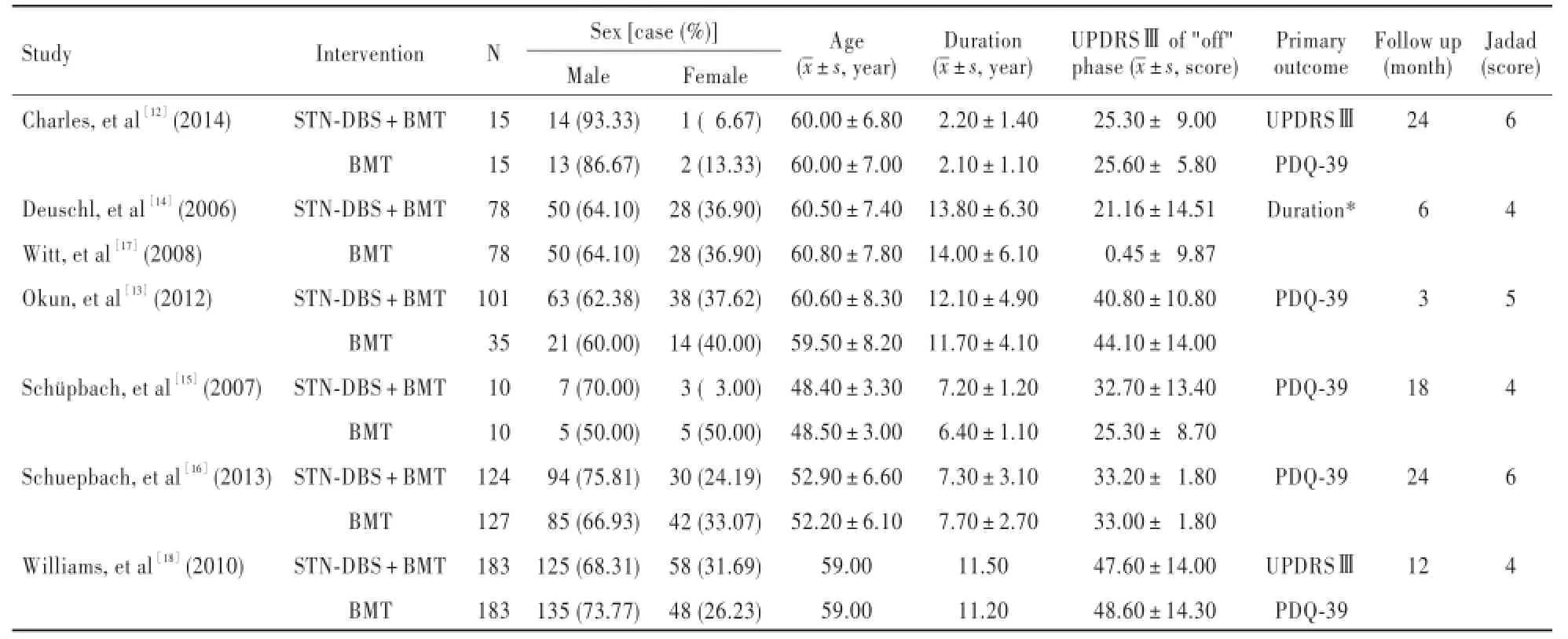
表1 所纳入6项临床试验的基线资料和质量评价Table 1.Baseline materials and quality assessment of 6 included clinical trials
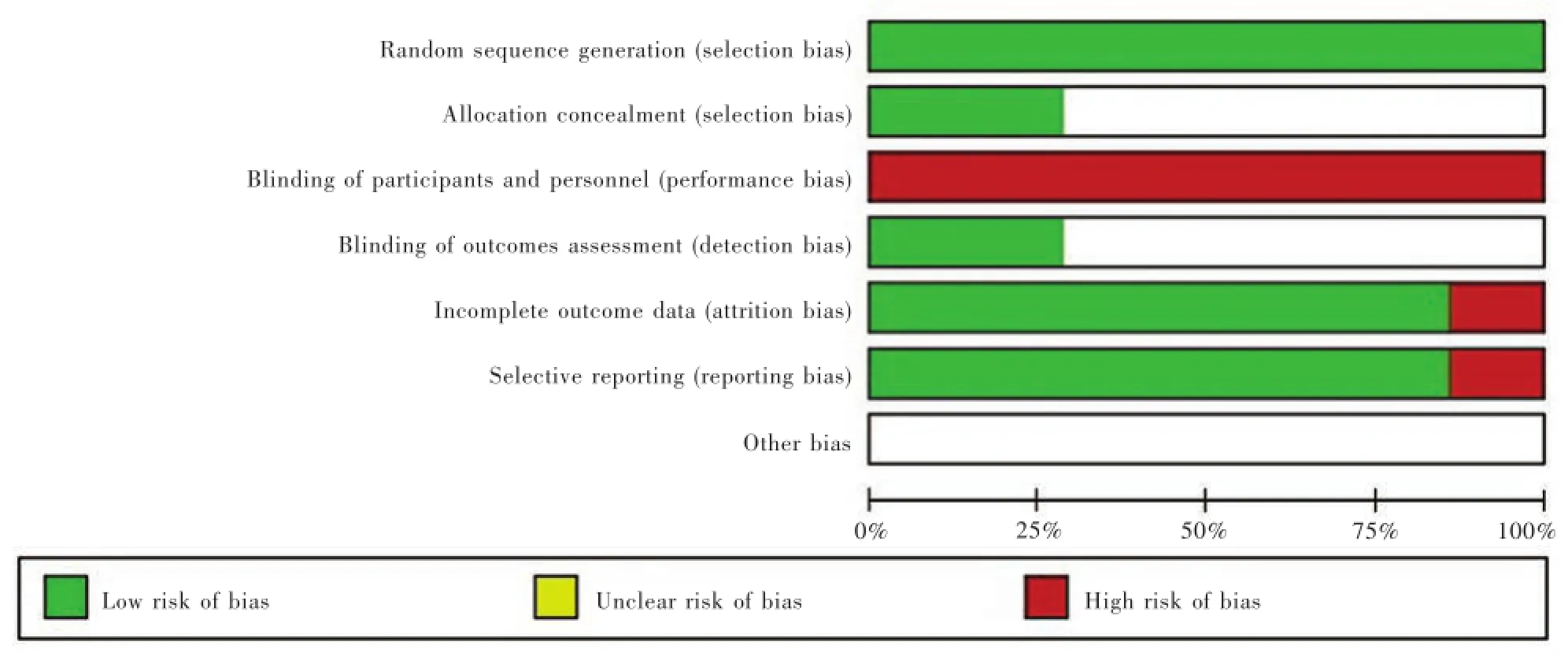
图2 文献偏倚图Figure 2 Risk of bias.

图3 STN⁃DBS+BMT组与BMT组患者治疗前后UPDRSⅢ评分比较的森林图3a“开”期3b“关”期Figure 3 Forest plot for comparison of UPDRSⅢscore before and after treatment between STN⁃DBS+BMT group and BMT group."On" phase(Panel 3a)."Off"phase(Panel 3b).

图4 STN⁃DBS+BMT组与BMT组患者治疗前后UPDRSⅠ评分比较的森林图Figure 4 Forest plot for comparison of UPDRSⅠscore before and after treatment between STN⁃DBS+BMT group and BMT group.
三、敏感性分析
将丘脑底核脑深部电刺激术联合药物治疗帕金森病的有效性和安全性评价结果中固定效应模型与随机效应模型相互转换、RD值和RR值与OR值变换或SMD值与MD值变换,精神障碍不良事件发生率于转换模型后研究结论改变,提示精神障碍不良事件发生率的Meta分析结果不稳定,解释该结果时需谨慎,其他研究结论均一致,表明Meta分析结果稳定(表2)。
讨论
本研究通过系统评价丘脑底核脑深部电刺激术联合药物治疗帕金森病的随机对照临床试验,探讨其有效性和安全性,Meta分析结果显示,丘脑底核脑深部电刺激术联合药物治疗可以显著改善帕金森病患者运动功能和生活质量,与既往研究相一致[20⁃21],而与文献报道的丘脑底核脑深部电刺激术联合药物治疗帕金森病神经精神症状结果存有较大差异[5],其中抑郁是最常见的帕金森病非运动症状之一[22]:有文献报道,丘脑底核脑深部电刺激术联合药物治疗可以改善抑郁症状[23],但也可能无影响甚至加重抑郁症状[22];研究显示,丘脑底核脑深部电刺激术联合药物治疗可以改善冲动控制障碍及相关疾病,但也可能无影响或恶化,甚至引起冲动控制障碍[24]。然而,本Meta分析显示丘脑底核脑深部电刺激术联合药物治疗可以改善帕金森病患者精神状态,且敏感性分析显示结果稳定、可靠,故尚待更多的证据验证。
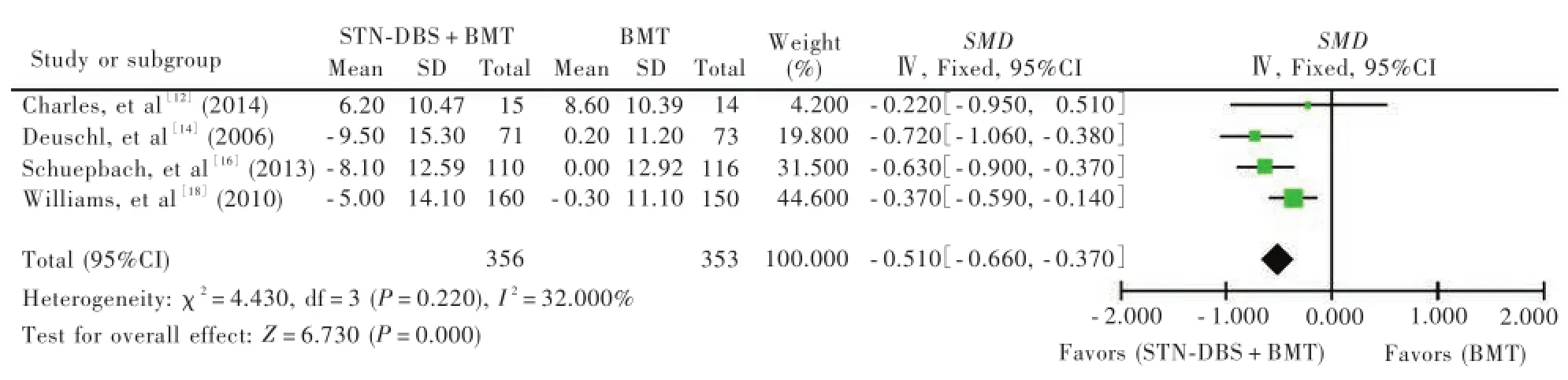
图5 STN⁃DBS+BMT组与BMT组患者治疗前后PDQ⁃39评分比较的森林图Figure 5 Forest plot for comparison of PDQ⁃39 score before and after treatment between STN⁃DBS+BMT group and BMT group.

图6 STN⁃DBS+BMT组与BMT组患者治疗后严重不良事件发生率比较的森林图Figure 6 Forest plot for comparison of the incidence rate of severe adverse events after treatment between STN⁃DBS+BMT group and BMT group.
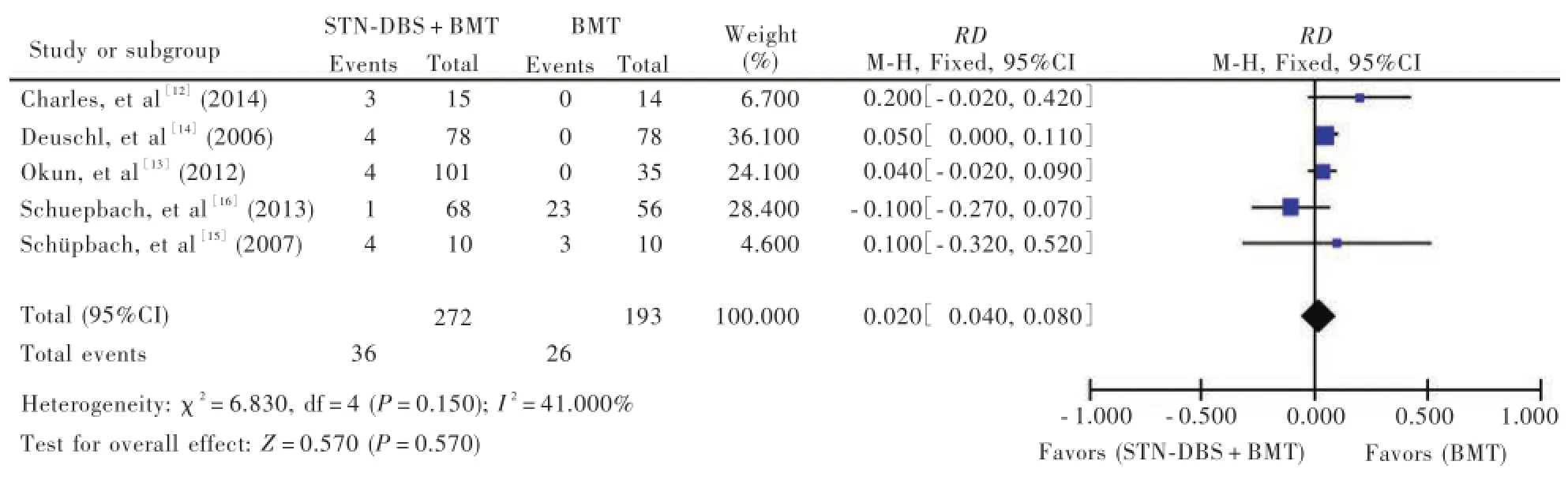
图7 STN⁃DBS+BMT组与BMT组患者治疗后抑郁不良事件发生率比较的森林图Figure 7 Forest plot for comparison of the incidence rate of depression after treatment between STN⁃DBS+BMT group and BMT group.
本Meta分析以UPDRSⅢ量表评价未服药状态下丘脑底核脑深部电刺激术联合药物治疗对帕金森病患者运动功能的疗效,各项研究之间存在异质性,其异质性来源可能是各项研究的纳入对象患病时间存在明显差异,Charles等[12]的研究对象均为早期帕金森病患者,Schuepbach等[16]的研究对象均为伴早期运动并发症的帕金森病患者,而其他临床试验的研究对象是晚期帕金森病患者,但是所纳入的文献较少不足以进行亚组分析。此外,Okun等[13]的STN⁃DBS+BMT组的干预措施是采用恒定电流刺激,BMT组也进行脑深部电刺激术但是术后3个月内并不给予电刺激,而其他临床试验STN⁃DBS+ BMT组的干预措施均采用恒定电压刺激,且BMT组未进行脑深部电刺激术,这有可能给研究结果带来一定的异质性。

图8 STN⁃DBS+BMT组与BMT组患者治疗后构音障碍不良事件发生率比较的森林图Figure 8 Forest plot for comparison of the incidence rate of dysarthria after treatment between STN⁃DBS+BMT group and BMT group.

图9 STN⁃DBS+BMT组与BMT组患者治疗后运动障碍不良事件发生率比较的森林图Figure 9 Forest plot for comparison of the incidence rate of dyskinesia after treatment between STN⁃DBS+BMT group and BMT group.
本Meta分析结果显示,STN⁃DBS+BMT组较BMT组发生严重不良事件和构音障碍不良事件的风险更高,其中严重不良反应主要包括颅内出血(0.5%)、自杀(1.3%~1.6%)、肺部感染(1.3%)等原因导致的死亡,植入部位感染(2.0%~2.6%)、癫发作(1%)等手术相关不良事件,以及肢体灵活性下降(3.8%~4.0%)等药物或帕金森病相关不良事件,其中颅内出血发生率远低于既往随访研究[25⁃29],且自杀发生率亦低于文献报道[30]。观察性研究和病例报告提示脑深部电刺激术可以增加自杀风险[30⁃32],而一项随机对照临床试验结果不支持脑深部电刺激术与自杀之间存在直接联系[33],因此尚待更多的证据验证。有文献报道,丘脑底核脑深部电刺激术可以加重构音障碍[28⁃29,34⁃35],其原因可能是手术过度刺激靶点横断面附近的皮质脊髓束[29]。除上述不良事件外,本Meta分析纳入的个别研究报道的常见不良事件,包括跌倒(8.9%)[13]、体重改变(12%)[16]、疼痛(15%)[16]等,与一些队列研究所报道的不良事件相似[25⁃29,32,36⁃37],但不同的随访时间导致不良事件发生率存在差异。Williams等[18]仅报告严重不良事件,并未报告其他不良事件,故该随机对照临床试验在研究不良事件时存在一定的局限性。
本Meta分析所纳入对象的基线资料存在患病时间、病情严重程度不同,以及随访时间和各医疗中心急诊条件不同,均可造成研究结果的偏倚;所纳入的临床试验根据随机对照原则,对照组最好是进行假手术,但是因为假手术违背道德伦理学要求,故纳入的6项随机对照临床试验[12⁃16,18]对照组干预措施均为最佳药物治疗,因此难以做到对患者和研究人员的双盲,故均未采用双盲,这可能给研究结果带来一定的偏倚,将在以后的研究中改进设计方法。

表2 效应模型相互转换和统计量值变换后的敏感性分析Table 2.Sensitivity analysis of interconversion between fixed effects model and random effects model,and exchange of statistical values
目前关于丘脑底核脑深部电刺激术治疗早期帕金森病和帕金森病早期运动并发症的研究较少,尚待更多高质量大样本多中心随机对照临床试验加以验证,目前美国食品与药品管理局已批准一项随机对照试验(试验编号:IDE#G050016)用于评价脑深部电刺激术治疗早期帕金森病的有效性,而且另一项非随机对照临床试验(试验编号:NCT01922388)正在招募中,旨在证明早期进行丘脑底核脑深部电刺激术对伴运动并发症的帕金森病患者更有利。
结论
与单纯药物治疗相比,丘脑底核脑深部电刺激术联合药物治疗能够显著改善帕金森病患者运动功能、精神状态和生活质量,但术后严重不良事件和构音障碍不良事件风险增加,应引起临床医师的重视。因此,术前应详细告知患者术后可能发生的不良事件,权衡利弊考虑手术,并在术后注意预防和及时处理不良事件。
[1]Ray Chaudhuri K,Rojo JM,Schapira AH,Brooks DJ,Stocchi F,Odin P,Antonini A,Brown RG,Martinez⁃Martin P.A proposal for a comprehensive grading of Parkinson's disease severity combining motor and non⁃motor assessments:meeting an unmet need.PLo S One,2013,8:E57221.
[2]Limousin P,Krack P,Pollak P,Benazzouz A,Ardouin C, Hoffmann D,Benabid AL.Electrical stimulation of the subthalamic nucleus in advanced Parkinson's disease.N Engl J Med,1998,339:1105⁃1111.
[3]Verhagen Metman L,Pal G,Slavin K.Surgical treatment of Parkinson's disease.Curr Treat Options Neurol,2016,18:49.
[4]Study Group of Parkinson's Disease and Movement Disorders, Chinese Society of Neurology,Chinese Medical Association. Guidelines for treatment of Parkinson's disease in China(third edition).Zhonghua Shen Jing Ke Za Zhi,2014,47:428⁃433[.中华医学会神经病学分会帕金森病及运动障碍学组.中国帕金森病治疗指南(第三版).中华神经科杂志,2014,47:428⁃433.]
[5]Gao DD,Tao YQ.Advances of deep brain stimulation in the treatment of non⁃motor symptoms of Parkinson's disease. Zhonghua Shen Jing Wai Ke Za Zhi,2015,31:419⁃421.[高丹丹,陶英群.脑深部电刺激术治疗帕金森病非运动症状的研究进展.中华神经外科杂志,2015,31:419⁃421.]
[6]Gelb DJ,Oliver E,Gilman S.Diagnostic criteria for Parkinson disease.Arch Neurol,1999,56:33⁃39.
[7]Movement Disorder Society Task Force on Rating Scales for Parkinson's Disease.The Unified Parkinson's Disease Rating Scale(UPDRS):status and recommendations.Mov Disord, 2003,18:738⁃750.
[8]Jenkinson C,Fitzpatrick R,Peto V,Greenhall R,Hyman N. The Parkinson's Disease Questionnaire(PDQ⁃39):development and validation of a Parkinson's disease summary index score. Age Ageing,1997,26:353⁃357.
[9]Jadad AR,Moore RA,Carroll D,Jenkinson C,Reynolds DJ, Gavaghan DJ,McQuay HJ.Assessing the quality of reports of randomized clinical trials:is blinding necessary?Control Clin Trials,1996,17:1⁃12.
[10]Higgins JP,Green S.Cochrane handbook for systematic reviews of interventions:version 5.0.1.2011⁃05⁃30[2016⁃10⁃11].http:// handbook.cochrane.org/.
[11]Higgins JP,Thompson SG,Deeks JJ,Altman DG.Measuring inconsistency in meta⁃analyses.BMJ,2003,327:557⁃560.
[12]Charles D,Konrad PE,Neimat JS,Molinari AL,Tramontana MG,Finder SG,Gill CE,Bliton MJ,Kao C,Phibbs FT,Hedera P,Salomon RM,Cannard KR,Wang L,Song Y,Davis TL. Subthalamic nucleus deep brain stimulation in early stage Parkinson's disease.Parkinsonism Relat Disord,2014,20:731⁃737.
[13]Okun MS,Gallo BV,Mandybur G,Jagid J,Foote KD,Revilla FJ,Alterman R,Jankovic J,Simpson R,Junn F,Verhagen L, Arle JE,Ford B,Goodman RR,Stewart RM,Horn S,Baltuch GH,Kopell BH,Marshall F,Peichel D,Pahwa R,Lyons KE, Troster AI,Vitek JL,Tagliati M;SJM DBS Study Group. Subthalamic deep brain stimulation with a constant⁃current device in Parkinson's disease:an open⁃label randomised controlled trial.Lancet Neurol,2012,11:140⁃149.
[14]Deuschl G,Schade⁃Brittinger C,Krack P,Volkmann J,Schafer H,Botzel K,Daniels C,Deutschlander A,Dillmann U,Eisner W,Gruber D,Hamel W,Herzog J,Hilker R,Klebe S,Kloss M, Koy J,Krause M,Kupsch A,Lorenz D,Lorenzl S,Mehdorn HM,Moringlane JR,Oertel W,Pinsker MO,Reichmann H, Reuss A,Schneider GH,Schnitzler A,Steude U,Sturm V, Timmermann L,Tronnier V,Trottenberg T,Wojtecki L,Wolf E, Poewe W,Voges J;German Parkinson Study Group, Neurostimulation Section.A randomized trial of deep⁃brain stimulation for Parkinson's disease.N Engl J Med,2006,355: 896⁃908.
[15]Schüpbach WM,Maltête D,Houeto JL,du Montcel ST,Mallet L,Welter ML,Gargiulo M,Béhar C,Bonnet AM,Czernecki V, Pidoux B,Navarro S,Dormont D,Cornu P,Agid Y. Neurosurgery at an earlier stage of Parkinson disease:a randomized,controlled trial.Neurology,2007,68:267⁃271.
[16]Schuepbach WM,Rau J,Knudsen K,Volkmann J,Krack P, Timmermann L,Halbig TD,Hesekamp H,Navarro SM,Meier N,Falk D,Mehdorn M,Paschen S,Maarouf M,Barbe MT,Fink GR,Kupsch A,Gruber D,Schneider GH,Seigneuret E,Kistner A,Chaynes P,Ory⁃Magne F,Brefel Courbon C,Vesper J, Schnitzler A,Wojtecki L,Houeto JL,Bataille B,Maltete D, Damier P,Raoul S,Sixel⁃Doering F,Hellwig D,Gharabaghi A, Kruger R,Pinsker MO,Amtage F,Regis JM,Witjas T,Thobois S,Mertens P,Kloss M,Hartmann A,Oertel WH,Post B, Speelman H,Agid Y,Schade⁃Brittinger C,Deuschl G; EARLYSTIM Study Group.Neurostimulation for Parkinson's disease with early motor complications.N Engl J Med,2013, 368:610⁃622.
[17]Witt K,Daniels C,Reiff J,Krack P,Volkmann J,Pinsker MO, Krause M,Tronnier V,Kloss M,Schnitzler A,Wojtecki L, Botzel K,Danek A,Hilker R,Sturm V,Kupsch A,Karner E, Deuschl G.Neuropsychological and psychiatric changes after deep brain stimulation for Parkinson's disease:a randomised, multicentre study.Lancet Neurol,2008,7:605⁃614.
[18]Williams A,Gill S,Varma T,Jenkinson C,Quinn N,Mitchell R,Scott R,Ives N,Rick C,Daniels J,Patel S,Wheatley K;PD SURG Collaborative Group.Deep brain stimulation plus best medical therapy versus best medical therapy alone for advanced Parkinson's disease(PD SURG trial):a randomised,open⁃label trial.Lancet Neurol,2010,9:581⁃591.
[19]Tramontana MG,Molinari AL,Konrad PE,Davis TL,Wylie SA, Neimat JS,May AT,Phibbs FT,Hedera P,Gill CE,Salomon RM,Wang L,Song Y,Charles D.Neuropsychological effects of deep brain stimulation in subjects with early stage Parkinson's disease in a randomized clinical trial.J Parkinsons Dis,2015,5: 151⁃163.
[20]Chinese Expert Group on Deep Brain Stimulation for Treating Parkinson's Disease.Chinese expert consensus on deep brain stimulation for treating Parkinson's disease.Zhonghua Shen Jing Wai Ke Za Zhi,2012,28:855⁃857.[中国帕金森病脑深部电刺激疗法专家组.中国帕金森病脑深部电刺激疗法专家共识.中华神经外科杂志,2012,28:855⁃857.]
[21]Benabid AL,Chabardes S,Mitrofanis J,Pollak P.Deep brain stimulation of the subthalamic nucleus for the treatment of Parkinson's disease.Lancet Neurol,2009,8:67⁃81.
[22]Mosley PE,Marsh R.The psychiatric and neuropsychiatric symptoms after subthalamic stimulation for Parkinson's disease. J Neuropsychiatry Clin Neurosci,2015,27:19⁃26.
[23]Voon V,Kubu C,Krack P,Houeto JL,Troster AI.Deep brain stimulation:neuropsychological and neuropsychiatric issues. Mov Disord,2006,21 Suppl 14:305⁃327.
[24]Broen M,Duits A,Visser⁃Vandewalle V,Temel Y, Winogrodzka A.Impulse control and related disorders in Parkinson's disease patients treated with bilateral subthalamic nucleus stimulation:a review.Parkinsonism Relat Disord,2011, 17:413⁃417.
[25]Beric A,Kelly PJ,Rezai A,Sterio D,Mogilner A,Zonenshayn M,Kopell B.Complications of deep brain stimulation surgery. Stereotact Funct Neurosurg,2001,77(1⁃4):73⁃78.
[26]Kondziolka D,Whiting D,Germanwala A,Oh M.Hardware⁃related complications after placement of thalamic deep brain stimulator systems.Stereotact Funct Neurosurg,2002,79(3/4): 228⁃233.
[27]Oh MY,Abosch A,Kim SH,Lang AE,Lozano AM.Long⁃term hardware⁃related complications of deep brain stimulation. Neurosurgery,2002,50:1268⁃1274.
[28]Romito LM,Scerrati M,Contarino MF,Bentivoglio AR,Tonali P,Albanese A.Long⁃term follow up of subthalamic nucleus stimulation in Parkinson's disease.Neurology,2002,58:1546⁃1550.
[29]Umemura A,Oka Y,Yamamoto K,Okita K,Matsukawa N, Yamada K.Complications of subthalamic nucleus stimulation in Parkinson's disease.Neurol Med Chir(Tokyo),2011,51:749⁃755.
[30]Burkhard PR,Vingerhoets FJ,Berney A,Bogousslavsky J, Villemure JG,Ghika J.Suicide after successful deep brain stimulation for movement disorders.Neurology,2004,63:2170⁃2172.
[31]Funkiewiez A,Ardouin C,Caputo E,Krack P,Fraix V,Klinger H,Chabardes S,Foote K,Benabid AL,Pollak P.Long term effects of bilateral subthalamic nucleus stimulation on cognitive function,mood,and behaviour in Parkinson's disease.J Neurol Neurosurg Psychiatry,2004,75:834⁃839.
[32]Krack P,Batir A,Van Blercom N,Chabardes S,Fraix V, Ardouin C,Koudsie A,Limousin PD,Benazzouz A,LeBas JF, Benabid AL,Pollak P.Five⁃year follow⁃up of bilateral stimulation of the subthalamic nucleus in advanced Parkinson's disease.N Engl J Med,2003,349:1925⁃1934.
[33]Weintraub D,Duda J,Carlson K,Luo P,Sagher O,Weaver F. Suicide ideation and behaviors after deep brain stimulation for Parkinson's disease:results from a randomized controlled trial. Mov Disord,2012,27:291.
[34]Burghaus L,Hilker R,Thiel A,Galldiks N,Lehnhardt FG,Zaro⁃Weber O,Sturm V,Heiss WD.Deep brain stimulation of the subthalamic nucleus reversibly deteriorates stuttering in advanced Parkinson's disease.J Neural Transm(Vienna),2006,113:625⁃631.
[35]Zhang JG,Ma Y,Hu WH.Present study on deep brain stimulation in the treatment of Parkinson disease and dyskinetic diseases.Zhongguo Xian Dai Shen Jing Ji Bing Za Zhi,2007,7: 22⁃24[.张建国,马羽,胡文瀚.帕金森病及运动障碍性疾病的脑深部电刺激术治疗研究现状.中国现代神经疾病杂志, 2007,7:22⁃24.]
[36]Kenney C,Simpson R,Hunter C,Ondo W,Almaguer M, Davidson A,Jankovic J.Short⁃term and long⁃term safety of deep brain stimulation in the treatment of movement disorders. J Neurosurg,2007,106:621⁃625.
[37]Wu X,Chen JC,Wang WL,Hao B,Chen X,Hu XW.Long⁃term follow⁃up study on the safety of deep brain stimulation for treating Parkinson's disease.Zhongguo Xian Dai Shen Jing Ji Bing Za Zhi,2015,15:790⁃794[.吴曦,陈剑春,王万璐,郝斌,陈鑫,胡小吾.帕金森病脑深部电刺激术安全性长期随访研究.中国现代神经疾病杂志,2015,15:790⁃794.]
Efficacy and safety of subthalamic nucleus deep brain stimulation combined with drug therapy for treating Parkinson's disease:a Meta⁃analysis
WANG Hai⁃jiao,CHEN Deng,ZHU Li⁃na,TAN Ge,XU Da,LIU Ling
Department of Neurology,West China Hospital,Sichuan University,Chengdu 610041,Sichuan,China Corresponding author:LIU Ling(Email:zjllxx1968@163.com)
ObjectiveTo evaluate the efficacy and safety of subthalamic nucleus deep brain stimulation(STN⁃DBS)combined with drug therapy for treating Parkinson's disease(PD).MethodsRetrieve relevant randomized controlled trials(RCTs)from online databases(January 1,1980-October 1, 2016)as PubMed,EBMASE/SCOPUS and Cochrane Library with key words:subthalamic nucleus,deep brain stimulation,DBS,STN,Parkinson disease,random.Selection of studies was performed according to pre⁃designed inclusion and exclusion criteria.Quality of studies was evaluated by using Jadad Scale and Cochrane Handbook for Systematic Reviews of Interventions.All data were pooled by Rev Man 5.2 software for Meta⁃analysis.ResultsThe research enrolled 3245 articles,from which 6 studies with Jadad score≥4 were chosen after excluding duplicates and those not meeting the inclusion criteria.A total of 958 PD patients were included.Meta⁃analysis showed that comparing with best medical treatment(BMT),STN⁃DBS combined with drug therapy significantly reduced the scores of Unified Parkinson's Disease Rating Scale (UPDRS)Ⅲin the"on"phase(SMD=⁃0.570,95%CI:⁃0.710-⁃0.430;P=0.000)and in the"off"phase (SMD=⁃1.170,95%CI:⁃1.500-⁃0.850;P=0.000),UPDRSⅠscore(SMD=⁃0.150,95%CI:⁃0.290-⁃0.010;P=0.030),and 39⁃Item Parkinson's Disease Questionnaire(PDQ⁃39)score(SMD=⁃0.510,95%CI:⁃0.660-⁃0.370;P=0.000).But it can increase the occurrence of severe adverse events(RD=0.140,95%CI:0.090-0.190;P=0.000)and dysarthria(RD=0.070,95%CI:0.010-0.120;P=0.020),while decrease the occurrence of dyskinesia(RR=0.450,95%CI:0.330-0.620;P=0.000).ConclusionsSubthalamic nucleus deep brain stimulation combined with drug therapy could greatly improve motor function,mental status and quality of life of PD patients,however,clinicians should pay more attention to the increased risk of severe adverse events and dysarthria after operation.
Parkinson disease;Subthalamic nucleus;Deep brain stimulation;Drug therapy; Meta⁃analysis
2016⁃12⁃28)
10.3969/j.issn.1672⁃6731.2017.02.006
610041成都,四川大学华西医院神经内科
刘凌(Email:zjllxx1968@163.com)
