荧光探针检测水中F-研究
2017-05-11刘倩白星星
刘倩,白星星
(商洛学院化学工程与现代材料学院/陕西省尾矿资源综合利用重点实验室,陕西商洛 726000)
氟化物可以用于牙齿保健、治愈骨质疏松症以及制备化学试剂,因此它在生物、医学和化学进程中发挥着重要作用。但是人体氟过量会导致氟中毒,轻者造成氟斑牙,重者引起氟骨症,甚至完全丧失劳动和生活自理能力。且氟中毒一旦患上即永远成疾[1-3]。因此,近年来,氟离子的检测越来越受到人们的关注。荧光分析法因其具有操作简便、选择性好、灵敏度高、取样量少、线性范围宽等优点,在药物分析、DNA排序、食品的微量和痕量分析以及生物科学等领域得到了广泛的应用[4-6]。近年来,人们尝试将荧光探针应用于药物分析、临床诊断、遗传分析、细胞检测、环境监测等方面,并取得了显著成果。目前,用于检测氟离子的荧光探针已有大量文献进行报道,主要基于以下几种反应机理:断裂Si-O键;断裂Si-C键;基于氟离子诱导Si-O键断裂合环反应;与有机硼化合物相互作用等[7-9]。基于氟离子对硅具有很强的亲和力,诱导硅醚键断裂的原理。本文设计、合成一种新型F-荧光探针1-(2-叔丁基二甲基氯化硅烷基-4-吡咯基)-苯乙烯基丙二腈(PB-1),利用叔丁基二甲基氯化硅化合物对化合物的羟基进行保护,从而抑制激发态分子内质子转移(ESIPT)过程。而加入氟离子后,氟离子选择性地切割探针中的叔丁基二甲基硅基,释放出羟基,ESIPT过程恢复,从而实现对氟离子的检测。本文还考查了该荧光探针对F-的识别能力,包括反应时间、灵敏度、选择性及pH的影响。并讨论它对水中F-检测的可能性。
1 实验部分
1.1 实验试剂和仪器
间氯苯酚、三氯氧磷、二甲基甲酰胺、氯仿、吡咯烷、二甲基亚砜、碳酸钾、三乙胺、叔丁基二甲基氯硅烷、丙二腈、哌啶、二氯甲烷、无水乙醇、氢氧化钾、硝酸。
紫外可见分光光度计、F4600荧光分光光度计、磁力搅拌器、电子分析天平、旋转蒸发仪、电子分析天平。
1.2 实验原理
荧光探针1-(2-叔丁基二甲基氯化硅烷基-4-吡咯基)-苯乙烯基丙二腈,简称PB-1,结构如图1所示。探针PB-1中的羟基被叔丁基二甲基氯硅烷保护后,激发态分子内质子转移(ESIPT)过程被抑制,荧光很弱,而加入F-后可以选择性的断裂硅醚键,生成的氧负离子与邻位的α,β-不饱和腈分子发生分子内的1,2-亲核加成反应,生成异香豆素类化合物,使ESIPT过程恢复,荧光增强,如图2所示。
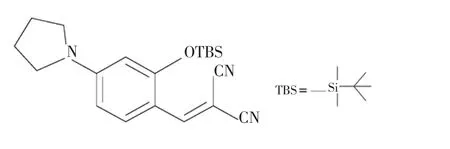
图1 PB-1的分子结构式
1.3 PB-1合成路线
PB-1的合成路线如图3所示。
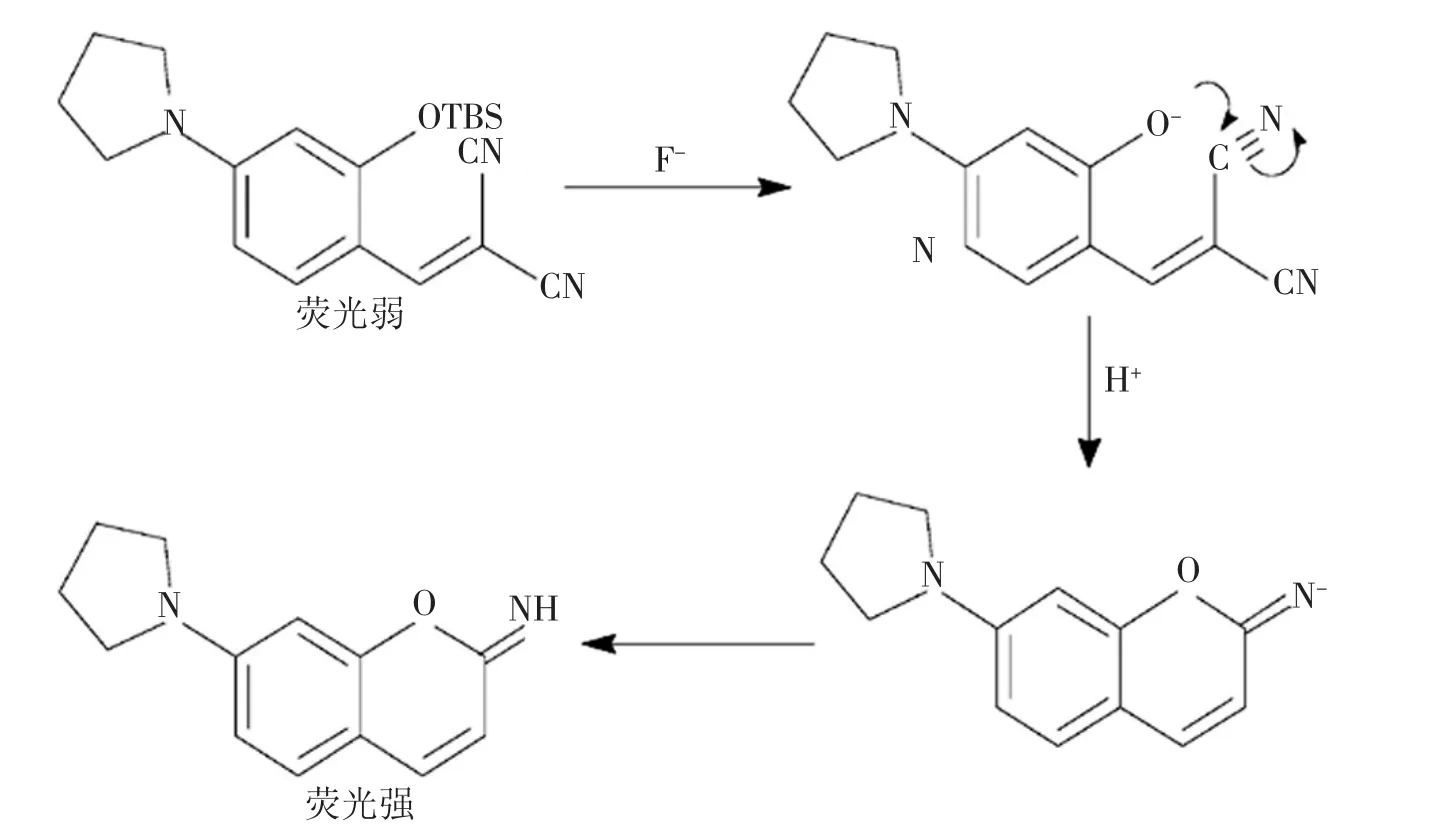
图2 PB-1与F-反应的原理图
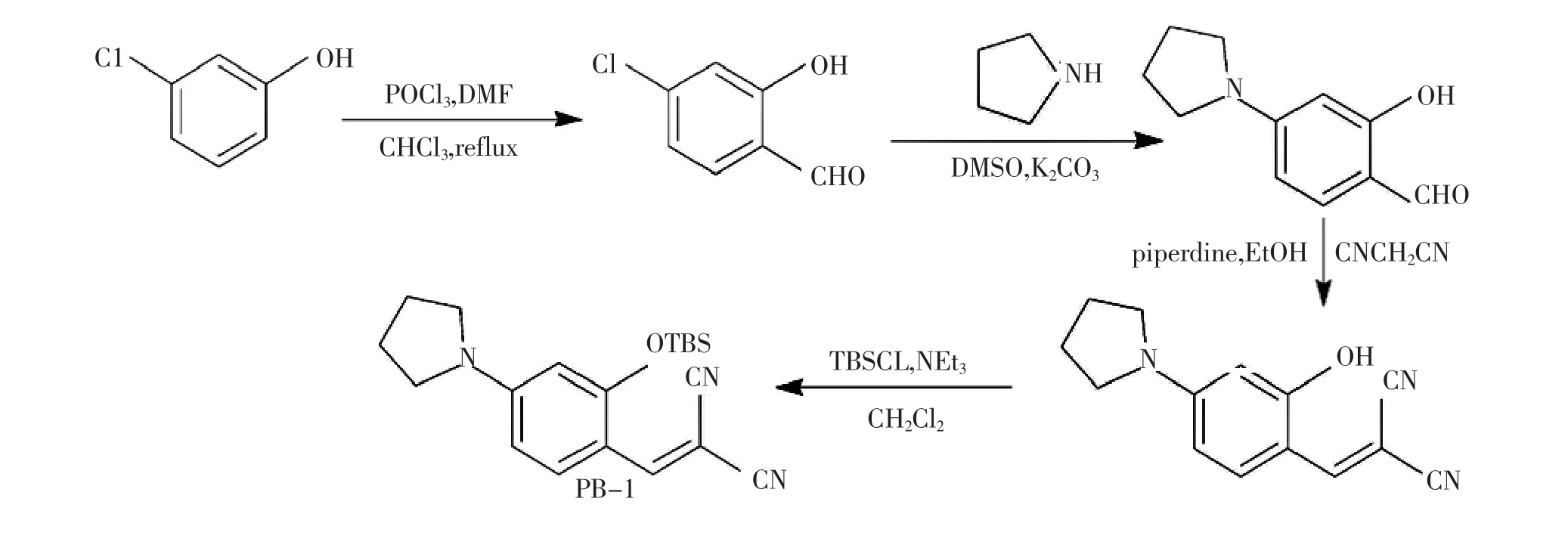
图3 荧光探针PB-1的合成路线
1.4 实验检测条件
称取适量的探针PB-1进行真空干燥后溶于乙腈溶液中,定容至100 mL,配制成测试所需要的合适浓度。各种常见物质(Br-,I-,NO2-,NO3-,CO32-,ClO4-,Cl-,SO42-,H2PO4-,SCN-,Cys,AcO-,GSH,Hcy,F-)配制成测试所需浓度的水溶液。测试体系:乙腈-HEPES 缓冲液,20 mol·mL-1,pH=7.4,v/v=4:1。荧光分光光度计参数如下:λex=445 nm,Em的狭缝宽度为5.0 nm,激发电压为700 v。
2 结果与分析
2.1 紫外、荧光光谱分析
2.1.1 紫外可见吸收光谱
实验分别测试了荧光探针PB-1(10 μmol·L-1)及PB-1与F-(v/v=1:1,10 μmol·L-1)反应40min后的紫外-可见吸收光谱图,结果如图4所示。由图4可知,PB-1在435 nm处有一个宽的收峰处,当它与同体积同浓度的F-反应40 min后,最大吸收峰红移至445 nm处,且吸光度减弱。表明F-诱导探针PB-1中的硅醚键断裂,发生了羟基脱保护反应,生成的氧负离子与邻位的α,β-不饱和腈分子发生分子内的1,2-亲核加成反应,生成了亚胺阴离子中间产物,该中间产物又迅速从溶液中得到质子而形成了新的物质,此现象与原理所述一致。
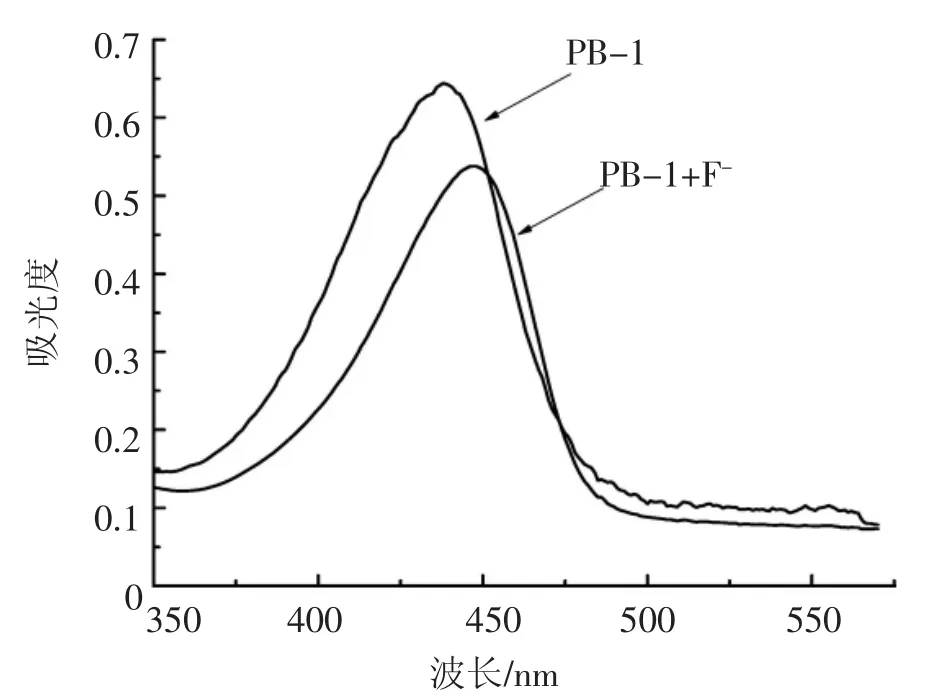
图4 紫外-可见吸收光谱图
2.1.2 荧光发射光谱
1)荧光光谱与时间的关系
实验考察了时间与荧光强度的关系,将荧光探针PB-1与F-(v/v=1:1,10 μmol·L-1)混合,每隔10 min测试荧光强度,一直测到反应后1 h,荧光强度随时间变化的曲线如图5、图6所示。
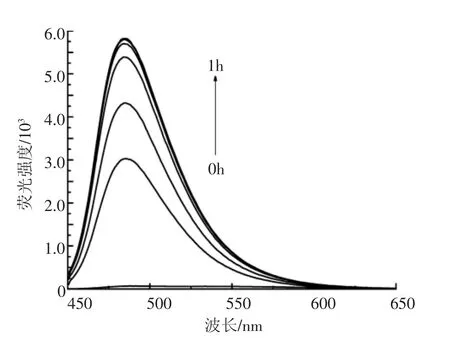
图5 荧光发射光谱随时间的变化
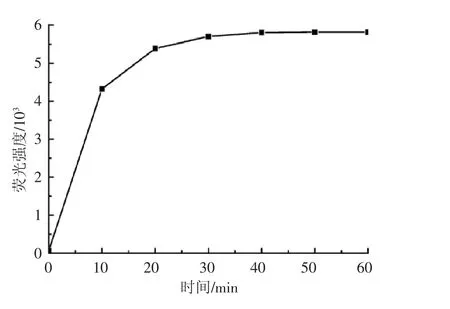
图6 荧光强度在最大发射波长处(488 nm)随时间的变化
由图5和图6可以看出,荧光探针PB-1与F-反应后生成的化合物在488 nm处吸收强度达到最大,PB-1与F-反应时间在20 min内,荧光强度增加较迅速,20~40 min增加较缓慢,40 min后荧光强度不再增加,趋于稳定。即反应达到饱和的时间为40 min。
2)荧光光谱与浓度的关系
将荧光探针 PB-1(10 μmol·L-1)与不同浓度(0、3、6、9、12、15、18、21、24、27、30、33、36、39 μmol·L-1)的 F-反应 40 min,荧光强度的变化如图7所示。由图7可以看出,F-的浓度为0时,荧光强度很弱,随着F-的浓度不断增大,在488 nm处出现最大发射峰且荧光强度不断增强,当 F-的浓度达到 27μmol·L-1时,即探针 PB-1的 2.7倍时,荧光强度达到饱和,不在随着F-浓度的增大而增加,最大增强为荧光探针PB-1的108倍。在紫外灯的照射下,探针呈现出较强的黄绿色荧光。
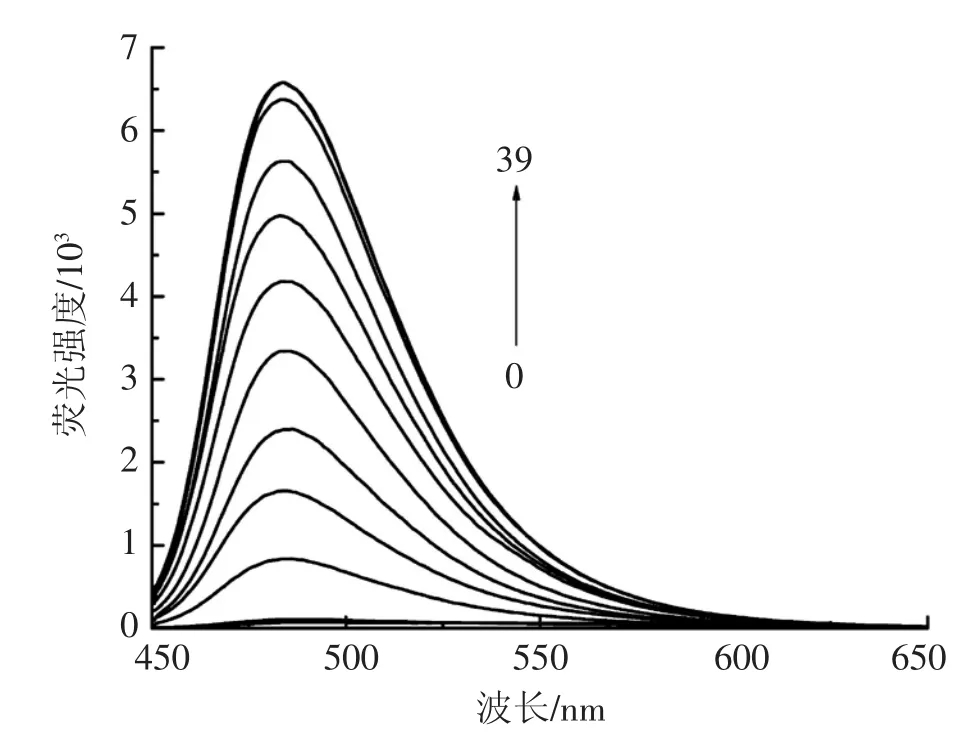
图7 荧光强度随F-浓度增加的变化
由图 8 可知,当 F-的浓度为 0~24 μmol·L-1,荧光探针PB-1浓度为10 μmol·L-1时,荧光强度与F-的浓度有较好的线性关系。线性方程为y=266.8x+71.588,其拟合常数R为0.9988。F-的检测下限达到10 μmol·L-1,显示了较高的检测灵敏度。

图8 荧光强度与F-浓度的线性关系
2.2 其他离子干扰测试分析
将荧光探针 PB-1(10 μmol·L-1)分别与20 倍的 Br-,I-,NO2-,NO3-,CO32-,ClO4-,Cl-,SO42-,H2PO4-,SCN-,Cys,AcO-,GSH,Hcy 反应40 min后的荧光强度如图9所示。可以看出,只有加入F-,荧光强度才会显著增加,是未加物质空白溶液的108倍。而加入其它阴离子及巯基化合物后,荧光强度并未增加或增加很小(可忽略),说明荧光探针PB-1对F-有较好的选择性。
为了进一步探讨该方法测定F-的可行性,实验考察了共存物质对F-测定的影响,如图10所示,加入浓度为PB-1 200倍的共存物质对2.7倍的F-几乎没有干扰。这表明F-仍能选择性的脱去PB-1中的叔丁基二甲基硅基官能团,探针PB-1可以实现复杂样品中F-的检测。
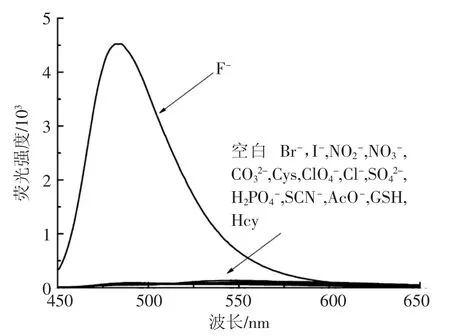
图9 加入不同阴离子及巯基化合物后荧光强度的变化
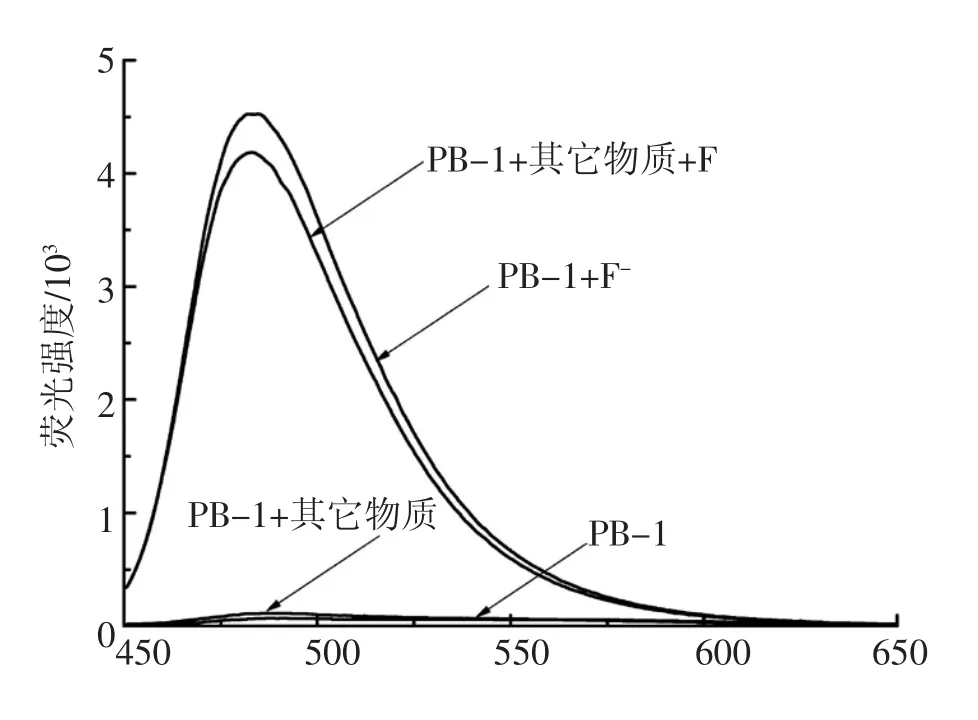
图10 干扰物质与F-共存时对PB-1的发射光谱的影响
2.3 pH值的影响
实验考察了加入F-前后,pH对PB-1荧光强度的影响,利用KOH和HNO3将溶液调制成pH=4,5,6,7,8,9 的测试体系,将探针 PB-1 配置成浓度为 1×10-5mol·L-1的溶液并测试其荧光强度,且分别往里面加入相同体积相同浓度的F-,反应40 min后,测试其荧光强度,如图11所示。
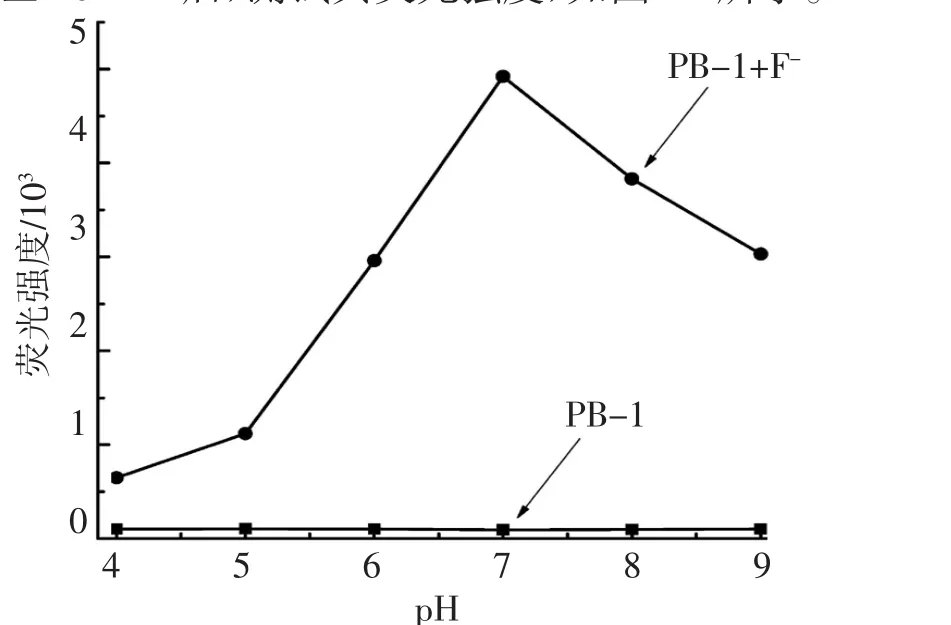
图11 加入F-前后不同pH条件下的荧光强度
由图11可以看出,pH在4.0~9.0,探针PB-1荧光强度保持不变,说明探针PB-1可以在较宽的pH值范围内稳定存在,而加入F-后,荧光强度都会增加,表明PB-1可以在较宽的pH值范围内检测F-。但在pH为4、5时,荧光强度增加比较小,在 pH 为 6、7、8、9 时,荧光强度增加比较大,尤其在pH为7时,荧光强度增加最为显著。因此,pH为7作为最佳测试条件。
3 结论
本文基于氟离子对硅具有很强的亲和力,可以诱导硅醚键断裂的原理。设计并合成一种新型的F-荧光探针PB-1,实验对其光谱性质、选择性、pH等进行研究,发现加入F-后,光谱性质变化明显,紫外可见吸收波长由435 nm红移到445 nm;并且荧光光谱在波长为488 nm处强度不断增强,最大增强为108倍。通过对pH和选择性的测试,发现它可以在不受其它离子干扰的情况下,在一个较宽的pH范围内检测F-。且测试体系中有机溶剂的含量仅为5%,因此,PB-1可用于水中F-的检测。
参考文献:
[1]BAO Y,LIU B,WANG H,et al.A"naked eye"and ratiometric fluorescent chemosensor for rapiddetection of F based on combination of desilylation reaction and excited -state proton transfer [J].Chemical Communications,2011,47(13):3957-3959.
[2]宋萍,氟对机体健康影响与危害[J].化学工程与装备,2010,6(4):20-23.
[3]HOU P,CHEN S,WANG H,et al.An aqueous red emitting fluorescent fluoride sensing probe exhibiting a large Stokes shift and its application in cell imaging[J].Chemical Communications,2014,50(3):320-322.
[4]SWAMY K M K,LEE Y J,LEE H N,et al.A new fluorescein derivative bearing a boronic acidgroup as a fluorescent chemosensor for fluoride ion[J].The Journal of Organic Chemistry,2006,71(22):8626-8628.
[5]KIM S H,KIM J S,PARK S M,et al.Hg2+-selective OFFON and Cu2+-selective ON-OFF type fluoroionophore based upon cyclam[J]Organic Letters,2006,8(3):371-374.
[6]YANG Z,ZHANG K,GONG F,et al.A highly selective fluorescent sensor for fluoride anion based on pyrazole derivative:naked eye"no-yes"detection[J].Journal of Photochemistry and Photobiology A:Chemistry,2011,217(1):29-34.
[7]马文辉,彭孝军,徐群,等.香豆素类荧光传感器[J].化学进展,2007,19(9):5012-5016.
[8]SUN H,DONG X,LIU S,et al.Excellent BODIPY dye containing dimesitylboryl groups as pet based fluorescent probes for fluoride [J].The Journal of Physical Chemistry C,2011,115(40):19947-19954.
[9]WU M Y,LI K,HOU J T,et al.A selective colorimetric and ratiometric fluorescent probe for hydrogen sulfide[J].Organic&Biomolecular Chemistry,2012,10(41):8342-8347.
