比索洛尔对大鼠肝微粒体细胞色素P450酶含量及其不同亚型活性的影响
2017-05-10刘明远赵可欣赵锦程张明远朱秋双杨光远
刘明远 李 萌 赵可欣 韩 梅 赵锦程 张明远 朱秋双 杨 玉 白 雪 杨光远
(佳木斯大学基础医学院药理学教研室,黑龙江 佳木斯 154007)
比索洛尔对大鼠肝微粒体细胞色素P450酶含量及其不同亚型活性的影响
刘明远 李 萌 赵可欣 韩 梅1赵锦程 张明远 朱秋双 杨 玉 白 雪 杨光远
(佳木斯大学基础医学院药理学教研室,黑龙江 佳木斯 154007)
目的 探讨比索洛尔对大鼠肝微粒体细胞色素P450酶 (CYP450) 含量及CYP1A2、CYP2C9、CYP2C19、CYP2D6和CYP3A4活性的影响。方法 生理盐水为对照,大鼠灌胃给予0.9 mg·kg-1·d-1的比索洛尔,连续7 d,然后测定其肝微体中CYP450含量及CYP1A2、CYP2C9、CYP2C19、CYP2D6和CYP3A4活性。结果 与对照组比较,比索洛尔组CYP450含量和CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP3A4活性的差异无统计学意义(P>0.05)。结论 比索洛尔对CYP450含量和CYP1A2、CYP2C9、CYP2C19、CYP2D6、CYP3A4活性无影响。
比索洛尔;CYP450;CYP1A2;CYP2C9;CYP2C19;CYP2D6;CYP3A4
比索洛尔为选择性β1-受体阻断剂〔1〕,主要用于高血压、心绞痛、心律失常及心力衰竭等心血管系统疾病的治疗〔2〕,也可辅助用于甲亢治疗。临床上常与其他抗心血管药物及抗甲状腺功能亢进药物联合应用。肝细胞色素P450 (CYP450) 为Ⅰ相药物代谢酶,是参与外源性物质生物转化的重要酶系。多种化学物质对CYP450酶可产生诱导或抑制作用,因而改变CYP450 酶的含量或活性,并进一步影响CYP 450 酶对其底物的生物转化〔3〕。多种药物联合应用在临床很常见,但因此而产生的药物之间的相互作用(DDI)也随之增长〔4〕。研究发现,两种药物合用发生DDI的风险为13%,若同时服7种或以上药物,则DDI发生率将会上升到82%〔5〕。长期用药对CYP450酶的抑制或诱导是DDI的重要机制之一。关于比索洛尔直接给药对CYP450酶各亚型的作用国内外文献鲜见报道。本实验旨在探讨比索洛尔对肝CYP450酶的影响及其DDI的临床意义。
1 材料与方法
1.1 材料 动物:清洁级雄性Wistar大鼠,体重200~250 g〔购自哈尔滨医科大学实验动物学部,合格证号:SCXK-(黑)2013-001)〕。主要试剂与仪器:富马酸比索洛尔(批号:100711-200401,含量>98%,中国食品药品检定研究院);非那西丁、对乙酰氨基酚、甲苯磺丁脲、美芬妥英、异喹胍、4′-羟基甲苯磺丁脲、4′-羟基美芬妥英、4′-羟基异喹胍、1′-羟基咪达唑仑(Sigma公司);咪达唑仑(批号:171270-201402,含量>98%,中国食品药品检定研究院);三重四极杆串联质谱仪(QTRAP型,美国Applied Biosystem公司);高效液相色谱系统(Agilent 1100,美国Agilent公司);紫外分光光度计〔Unico uv-2100,尤尼柯(上海)仪器有限公司〕。
1.2 方法
1.2.1 给药方案 24只Wistar大鼠,随机分成3组,每组8只。对照组和比索洛尔给药组分别灌胃给予生理盐水和富马酸比索洛尔0.90 mg/kg,连续给药7 d。苯巴比妥诱导组于其他两组给药的第5天开始腹腔注射苯巴比妥钠75 mg/kg,连续给药3 d。
1.2.2 肝微粒体的制备 拉颈椎处死动物后迅速取出肝脏,放置于冰冷的0.25 mol/L蔗糖溶液(pH7.4)中,剪碎,洗至无血色;取2 g加1.0 ml蔗糖溶液,用组织匀浆机在冰浴中制成匀浆;4℃下首先20 000 r/min离心20 min,然后取上清液于100 000 r/min离心60 min,所得沉淀在0.1 mmol/L Tris-HCl缓冲液(pH7.4)中悬浮均匀,-80℃保存。依据文献方法进行蛋白浓度测定〔6〕。
1.2.3 CYP450含量测定 用Tris-HCl缓冲液将肝微粒体样品蛋白稀释至0.3~0.5 mg/ml,依据文献方法〔7〕,将少量Na2S2O4加入样品池后,再通CO气体30 s,并分别记录450 nm和490 nm的吸光度。CYP450 (nmol/mg protein)=〔A (450-490)×1 000〕/(91×C)。A(450-490)为450 nm及490 nm的吸光度差,C为被测样品蛋白的浓度(mg/ml)。采用双样本分析,计算平均值。
1.2.4 CYP450酶各亚型活性测定 参照文献方法〔8~11〕,分别以非那西丁、甲苯磺丁脲、美芬妥英、异喹胍和咪达唑仑作为CYP1A2、CYP2C9、CYP2C19、CYP2D6和CYP3A4的底物,建立500 μl孵育体系,各成分终浓度如表1。孵育10 min,取样100 μl加入到 200 μl冰冷甲醇中以终止反应。分别建立定量测定对乙酰氨基酚、4′-羟基甲苯磺丁脲、4′-羟基美芬妥英、4′-羟基异喹胍和1′-羟基咪达唑仑的高效液相色谱串联质谱分析方法(样品处理过程及质谱、色谱条件略),通过计算不同代谢物的生成速度来评价CYP450酶各亚型的活性。分别以相应的各探针药物的代谢产物对乙酰氨基酚、4′-羟基甲苯磺丁脲及 4′-羟基美芬妥英、4′-羟基异喹胍和1′-羟基咪达唑仑的产率(单位:nmol·mg-1· min-1) 作为 CYP1A2、 CYP2C9 、CYP2C19、CYP2D6和CYP3A4 酶活性指标。

表1 CYP450酶各亚型活性测定反应体系
1.3 统计学方法 采用SPSS17.0软件进行ANOVA检验和t检验。
2 结 果
2.1 肝微粒体CYP450含量 与对照组〔(0.76±0.20)nmol/mg〕比较,比索洛尔组CYP450 含量〔(0.77±0.14)nmol/mg〕差异无统计学意义(P>0.05);苯巴比妥组〔(1.53±0.39)nmol/mg〕明显高于对照组(P<0.01)。
2.2 CYP450各亚型活性比较 比索洛尔组与对照组大鼠肝微粒体CYP1A2、CYP2C9、 CYP2C19、CYP2D6和CYP3A4 活性差异均无统计学意义(P>0.05)。说明比索洛尔对CYP1A2、CYP2C9、 CYP2C19、CYP2D6和CYP3A4 亚型活性没有抑制或诱导作用。见表2。
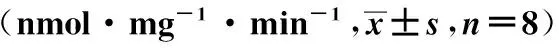
表2 CYP450酶各亚型活性
3 讨 论
联合用药时由于一种药物对CYP450酶特定亚型的诱导或抑制,从而影响经该CYP450酶亚型代谢的其他药物的代谢速度,导致DDI发生。近年来,心血管系统疾病已成为危害人类健康的常见病、多发病,由于老年人是心血管病的主要发病群体且常常合并其他疾病,心血管病人常常服用多种药物,因此抗心血管病药物与其他药物合用在老年人中更为常见。作为治疗心血管系统疾病的常用药,比索洛尔在临床上广泛应用,与其他药物联合用药的概率非常大。
有研究表明,3个CYP450酶亚型家族(CYP1、CYP2和CYP3)可参与95%的外源化合物的代谢〔12〕。本实验结果提示当比索洛尔与主要经CYP1A2、CYP2C9、CYP2C19、CYP2D6和CYP3A4代谢的药物合用时,具有临床意义的药物相互作用发生的可能性较小。比索洛尔口服给药后对CYP450酶各亚型的影响,目前文献报道甚少,Hefner等〔13〕表明比索洛尔对CYP2D6无临床意义的抑制作用,与本实验结果一致。本实验分别以非那西丁、甲苯磺丁脲、美芬妥英、异喹胍和咪达唑仑作为CYP1A2、CYP2C9、CYP2C19、CYP2D6和CYP3A4的特异性底物,通过测定相应的代谢产物对乙酰氨基酚、4′-羟基甲苯磺丁脲、4′-羟基美芬妥英、4′-羟基异喹胍和1′-羟基咪达唑仑的生成速度来评价CYP450酶各亚型的活性。该法具有肝微粒体制备容易、孵育条件易优化、重现性好等优点。但药物对 CYP450 酶的作用存在一定的种属差异性〔14〕。比索洛尔对人肝微粒体 CYP450 酶各亚型的作用,还有待于进一步研究考证。
1 Ong HT,Ong LM,Kow FP.Beta-blockers for heart failure:an evidence based review answering practical therapeutic questions 〔J〕.Med J Malaysia,2012;67(1):7-11.
2 皇甫丰田,唐龙骞,唐龙滨.比索洛尔的药理作用及临床应用 〔J〕.山东医药工业,2001;20(1):31-2.
3 王广基.药物代谢动力学〔M〕.北京:化学工业出版社,2005:40-1.
4 Cadieux RJ.Drug interactions in the elderly.How multiple drug use increases risk exponentially 〔J〕.Postgrad Med,1989;86(8):179-86.
5 Goldberg RM,Mabee J,Chan L,etal.Drug-drug and drug-disease interactions in the ED:analysis of a high-risk population 〔J〕.Am J Emerg Med,1996;14(5):447-50.
6 Lowry OH,Rosebrough NJ,Farr AL,etal.Protein measurement with the folin phenol reagent 〔J〕.J Biol Chem,1951;193(1):265-75.
7 Omura T,Sato R.The carbon monoxide-binding pigment of liver microsomes.I.Evidence for its hemoprotein nature 〔J〕.J Biol Chem,1964;239(7):2370-8.
8 Chen ZH,Zhang SX,Long N,etal.An improved substrate cocktail for assessing direct inhibition and time-dependent inhibition of multiple cytochrome P450s 〔J〕.Acta Pharmacol Sin,2016;37(5):708-18.
9 Chen A,Zhou X,Tang S,etal.Evaluation of the inhibition potential of plumbagin against cytochrome P450 using LC-MS/MS and cocktail approach 〔J〕.Sci Rep,2016;6:28482.
10 Li G,Huang K,Nikolic D,etal.High-throughput cytochrome P450 cocktail inhibition Assay for assessing drug-drug and drug-botanical interactions 〔J〕.Drug Metab Dispos,2015;43(11):1670-8.
11 Stewart NA,Buch SC,Conrads TP,etal.A UPLC-MS/MS assay of the “Pittsburgh cocktail”:six CYP probe-drug/metabolites from human plasma and urine using stable isotope dilution 〔J〕.Analyst,2011;136(3):605-12.
12 Lin JH.Pharmacokinetic and pharmacodynamic variability:a daunting challenge in drug therapy 〔J〕.Curr Drug Metab,2007;8(2):109-36.
13 Hefner G,Unterecker S,Shams ME,etal.Melperone but not bisoprolol or metoprolol is a clinically relevant inhibitor of CYP2D6:evidence from a therapeutic drug monitoring survey 〔J〕.J Neural Transm (Vienna),2015;122(11):1609-17.
14 Graham MJ,Lake BG.Induction of drug metabolism:species differences and toxicological relevance 〔J〕.Toxicology,2008;254(3):184-91.
〔2016-11-08修回〕
(编辑 曲 莉/滕欣航)
黑龙江省留学归国人员科学基金(LC2016039);佳木斯大学重点项目(Szj2008-015)
杨光远(1975-),男,主任医师,硕士生导师,主要从事心血管药理学研究。
刘明远(1973-),女,副教授,主要从事心血管药理学研究。
R969.2
A
1005-9202(2017)08-1836-02;
10.3969/j.issn.1005-9202.2017.08.006
1 佳木斯大学附属第一医院
