2,6-二苦氨基-3,5-二硝基吡嗪的合成与表征
2017-05-07刘季灯周新利王鹏程
刘季灯, 周新利, 王鹏程, 陆 明
(南京理工大学化工学院, 江苏 南京 210094)
1 引 言
耐热炸药分解温度较高,撞击感度适当,能量较高。近年来随着地下资源的不断开采和航天事业的高速发展,这些领域对耐热炸药的需求日益增大[1]。目前处于应用阶段的耐热炸药主要有1,3,5-三氨基-2,4,6-三硝基苯(TATB)、2,2′,4,4′,6,6′-六硝基茋(HNS)、2,6-二苦氨基-3,5-二硝基吡啶(PYX)等[2-3]。其中PYX耐热性能较为优异,具有良好的抗辐射和抗静电性能,是一种具有广阔前景的新型耐热炸药[4-5],然而PYX的爆轰性能并不理想(爆速7.48 km·s-1,爆压24.20 GPa)[6]。国外曾有报道[7]通过在PYX的分子上引入硝基等含能基团,改善爆轰性能,但其仅处于理论研究阶段; 国内曾有报道[8-9]通过合成亚微米级、纳米级PYX,间接地改善了其爆轰性能,但是制备成本较高不利于实际应用。因此,研制开发一类拥有类似PYX的热安定性、同时具有更高能量的含能材料,是目前合成新型耐热炸药的重要课题[7]。
基于此,本研究以PYX的合成路线为基础,设计合成了一种新含能化合物——2,6-二苦氨基-3,5-二硝基吡嗪,表征了其结构和热性能。探讨了溶剂与催化剂对缩合反应收率的影响,以及硝化反应因素对2,6-二苦氨基-3,5-二硝基吡嗪(BPNP)收率的影响,确定了最佳反应条件。用量子化学方法与Kamlet-Jacobs公式,预估了目标化合物的密度与爆轰性能。
2 实验部分
2.1 合成路线
BPNP的合成路线见Scheme 1。
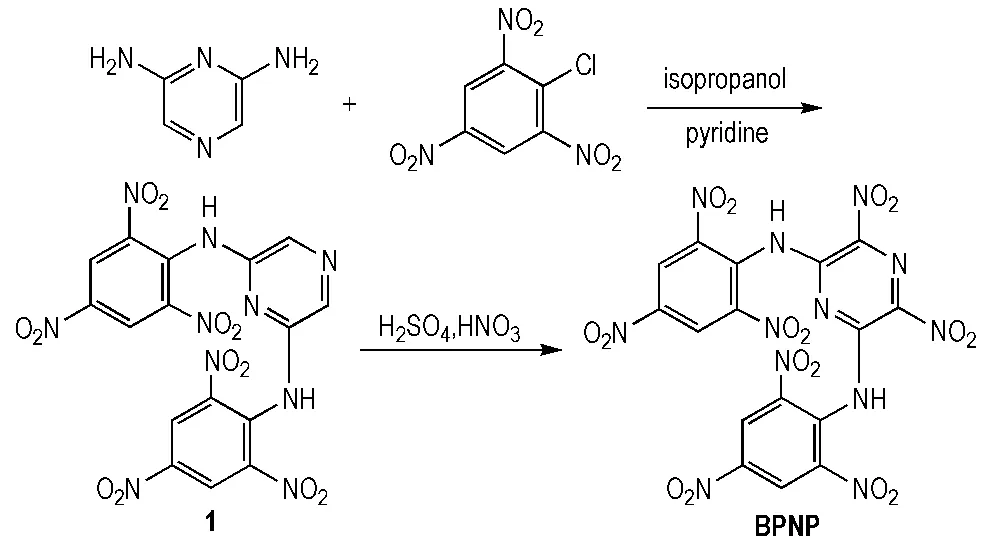
Scheme 1 Synthetic route of BPNP
2.2 试剂与仪器
试剂: 2,6-二氨基吡嗪(按文献[10-11]自制); 2,4,6-三硝基氯苯(参考文献[12-14]自制); 20%发烟硫酸、95%发烟硝酸(国药集团化学试剂有限公司); 其余试剂均为分析纯,使用前未经处理。
仪器: Avance Ⅲ 500MH核磁共振仪(德国Bruker 公司); Ultra AM TSQ quntium型高分辨质谱仪(美国Finnigan公司); Nicolet IS-10型傅里叶变换红外光谱仪(德国赛默飞世尔公司); SGWX-4熔点仪(上海测维光电仪器有限公司); TGA/SDTA851e热分析仪(瑞士METTLER TOLED公司); SDTQ600 DSC热分析仪(美国TA仪器公司); Vario EL Ⅲ型元素分析仪(德国Elementar公司)。
2.3 实验过程
2.3.1 2,6-二苦氨基吡嗪(1)的合成
将0.5 g(4.54 mmol) 2,6-二氨基吡嗪溶于20 mL异丙醇中,加入0.712 mL(9.09 mmol)吡啶和2.25 g(9.09 mmol)2,4,6-三硝基氯苯,加热至60 ℃,反应0.5 h后,升温至85 ℃,继续反应5 h。反应结束后,冷却,抽滤得灰色粉末状固体,再分别用甲醇10 mL、10%的稀盐酸溶液15 mL洗涤,最后用蒸馏水洗涤至水相成中性,真空干燥得 1.74 g(3.22 mmol)红棕色粉末化合物1,收率72%。1H NMR(DMSO-d6,500 MHz)δ: 10.37(s,2H,NH),8.83(s,4H,CH),8.15(s,2H,CH);13C NMR(DMSO-d6,126 MHz)δ: 146.02, 145.03, 142.62, 136.41, 130.34, 124.38; IR (KBr,ν/cm-1)3334,3082,1597,1476,1462,1295,1192,1154,1084,913,901,851,712,639,587; MS(ESI-),m/z: 530.88[M-1]-,483.88[M-HNO2]-; Anal.Calcd. for C16H8N10O12(%): C 36.09,H 1.50,N 26.32; Found C 35.73,H 1.26,N 26.54。
2.3.2 2,6-二苦氨基-3,5-二硝基吡嗪(BPNP)的合成
将95%发烟硝酸1.0 mL(21 mmol)和浓硫酸4.0 mL(67 mmol)加入到25 mL的三口烧瓶中,0 ℃下搅拌0.5 h后,缓慢加入0.5 g(0.93 mmol)化合物1,再缓慢升温至50 ℃反应3 h。反应结束后,冷却,将反应液倒入100 mL冰水中,抽滤并用6 mL丙酮洗涤,真空干燥得0.38 g(0.61 mmol)淡黄色固体2,收率66%,m.p.>300 ℃;1H NMR(DMSO-d6,500 MHz)δ: 8.83(s,4H,CH);13C NMR(DMSO-d6,126 MHz)δ: 146.25, 144.03, 140.62, 133.04, 128.57, 125.29; IR (KBr,ν/cm-1)3286,3081,1581,1535,1474,1427,1400,1341,1254,1093,938,922,904,852,837,826,775,719,597; MS(ESI-),m/z: 620.85[M-1]-,573.86[M-HNO2]-,481.82[M-H(NO2)3]-; Anal.Calcd. for C16H6N12O16(%): C 30.87,H 0.96,N 27.01; Found C 31.03,H 1.16,N 27.05。
3 计算方法
3.1 密度与生成热
采用Gaussian03数据包,运用密度泛函(DFT)理论下的B3LYP方法[15],选用基组6-31G++(d,p),对设计的分子结构进行结构构型优化,并确保振动分析无虚频; 体积的计算使用Monte-Carlo统计方法[16],并利用Kamlet-Jacobs方程[16]计算其性能数据。所有计算收敛参数均采用程序内定值[16-18]。
2,6-苦氨基-3,5-二硝基吡嗪的分子结构优化,如图1所示。
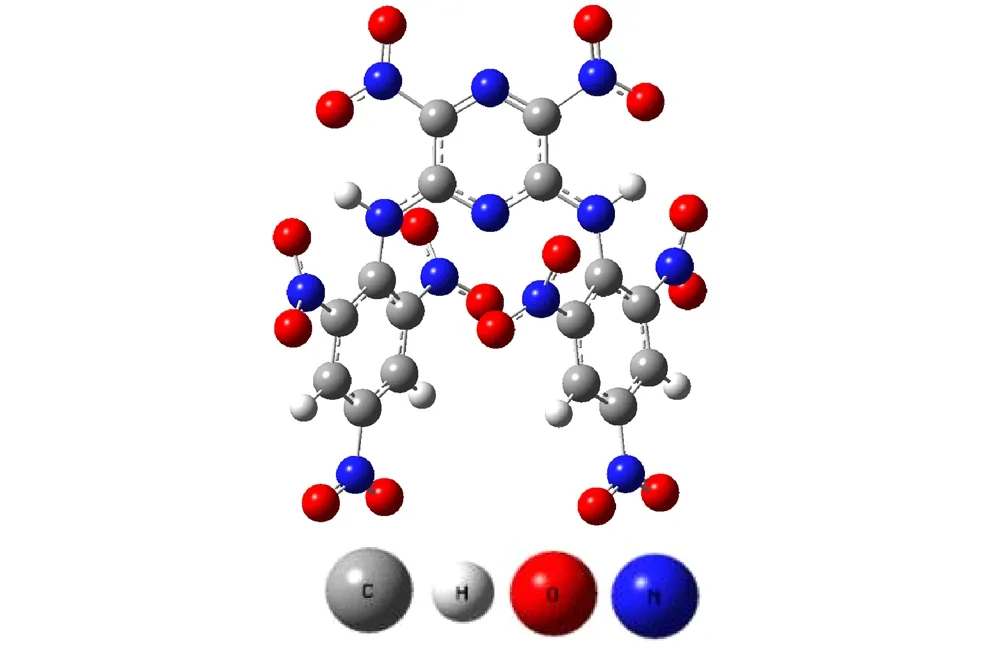
图1 BPNP的结构优化图
Fig.1 The optimized structure of TBPNP
采用设计等键反应法[19]计算生成热。等键方程设计如下:
R(NO2)n+nCH4→RHn+nCH3NO2
计算生成热为112.88 kJ·mol-1,并结合Monte-Carlo统计方法以及参考Politzer的晶体密度校正公式[20],计算BPNP密度为1.82 g·cm-3。
3.2 爆轰性能
利用Kamlet-Jacobs方程(式(1),式(2))[16],预估BPNP爆速为8.13 km·s-1,爆压为28.25 GPa:
(1)
(2)
根据Miroslav等[21]2010年报道的一种使用表面静电势描述分子对外界的敏感程度的方法,计算出BPNP在2.5 kg落锤,爆炸概率50%时的高度(H50)为83 cm。
4 结果与讨论
4.1 2,6-二苦氨基-3,5-二硝基吡嗪(BPNP)的表征
BPNP的质谱图如图2所示,从图2中可以看出[M-1]-=620.8是BPNP的分子离子峰; 同时结合离子碎片数据,可知M=573.8为BPNP失去一分子—HNO2的碎片峰[22],继续失去一分子—NO2得到M=527.8的碎片峰,而M=481.8为BPNP失去四分子—NO2的碎片峰,M=231.9为BPNP三个环裂开后其中吡嗪环部分的碎片峰。
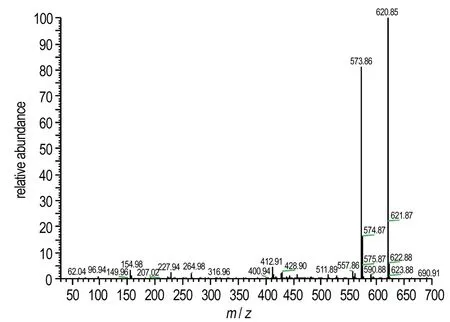
a. major ion peaks
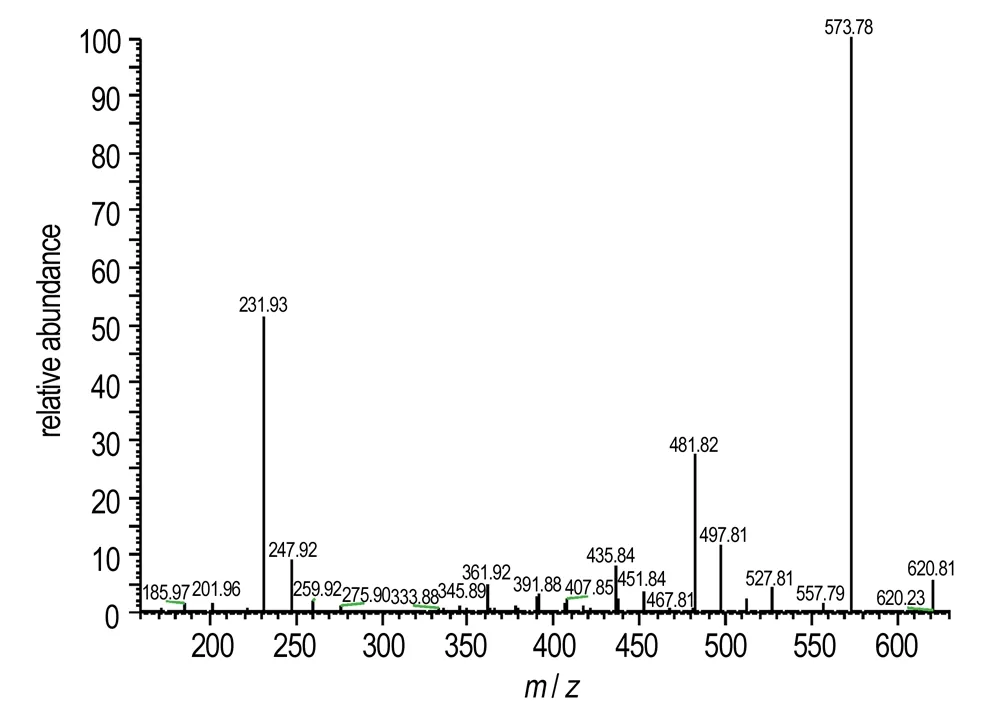
b. ion fragment peaks
图2 BPNP的质谱图谱
Fig.2 Mass spectrometer of BPNP
BPNP的1H NMR以及13C NMR的图谱如图3所示。1H NMR图谱表明,δ=8.83是苯环上的氢,而氨基上的氢是活泼氢,受浓度与酸碱度影响,化学位移很不稳定。13C NMR图谱中,δ: 125.29,128.59,144.03,146.25为苯环上的碳;δ: 133.04,140.61为吡嗪环上的碳。结合质谱数据,可以确认产物分子是2,6-二苦氨基-3,5-二硝基吡嗪。
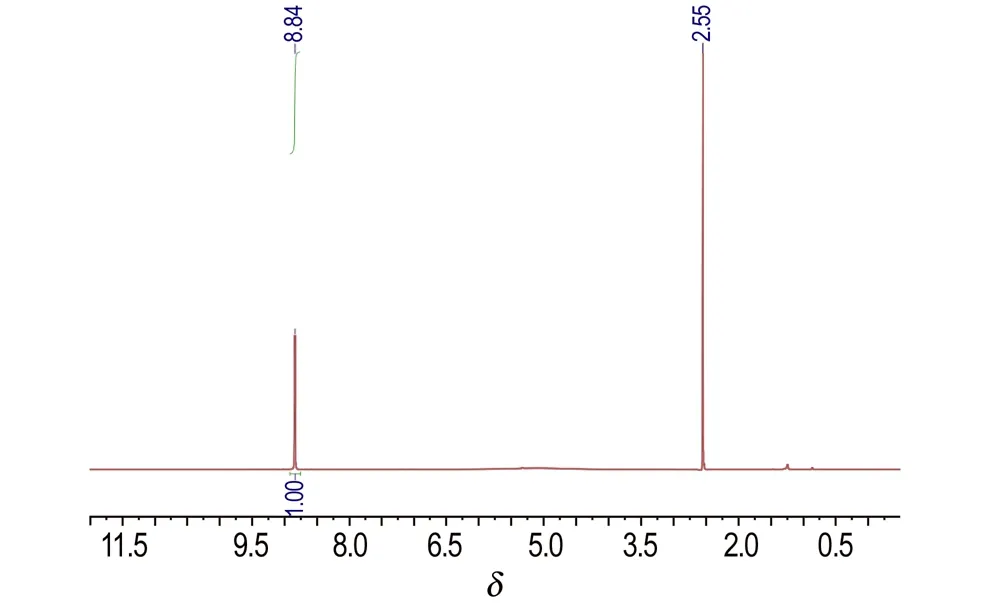
a. 1H NMR
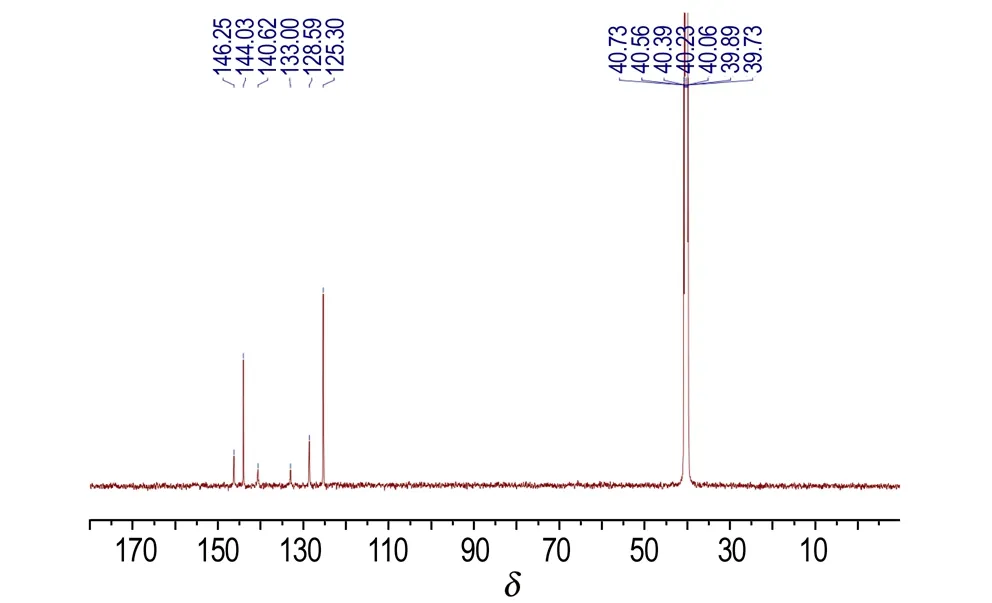
b. 13C NMR
图3 BPNP的1H NMR和13C NMR图谱
Fig.31H NMR and13C NMR spectrum of BPNP
4.2 2,6-二苦氨基吡嗪的缩合反应优化
4.2.1 溶剂对缩合反应的影响
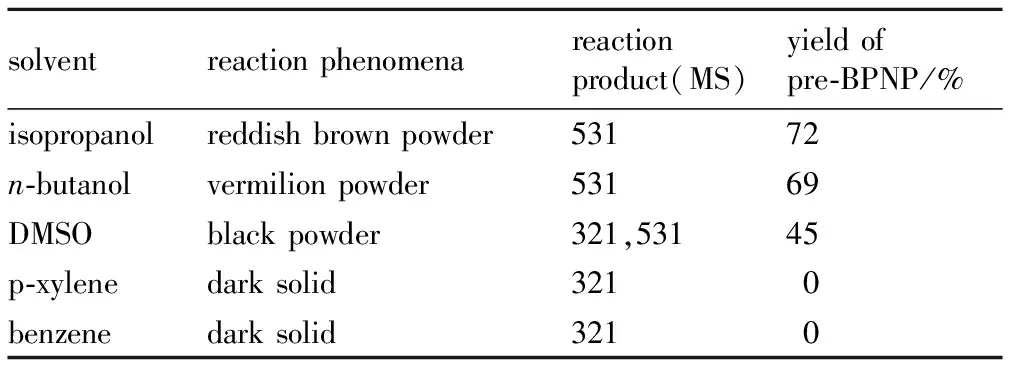
在反应温度85 ℃,反应时间为5 h的条件下,考察了不同溶剂对缩合反应的影响,结果见表1。由表1可知,缩合反应在极性较小的异丙醇、正丁醇中收率最高; 在强极性溶剂二甲亚砜中,产物大多为一取代物N-(2,4,6-三硝基苯基)-2,6-二氨基吡嗪(M=321),收率较低; 在非极性溶剂苯、对二甲苯中产物完全是一取代物。参考王乃兴[23-24]对2,6-二苦氨基吡啶的缩合反应研究,推测该反应历程见Scheme 2,其中C为Meisenheimer络合过渡态。结合反应历程判断缩合反应过程中溶剂的极性过大会不利于反应过渡态的形成; 同时该缩合反应是有机离子反应,非极性溶剂同样对反应不利。而具有适当极性的醇类,有利于过渡态的形成,使反应收率增加。同时相比于正丁醇,原料在异丙醇中的溶解性更好,有利于反应进行。因此,选用异丙醇做溶剂时收率最大。
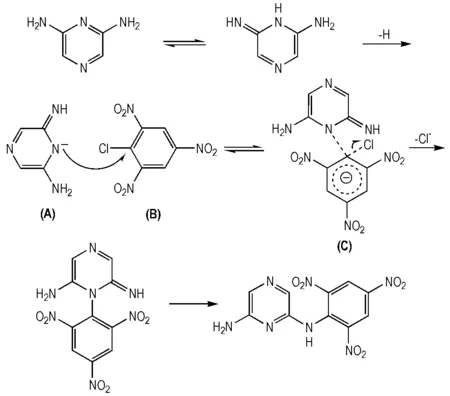
Scheme 2 Reaction mechanism of the condensation reaction
表1 不同溶剂对合成化合物1的影响
Table 1 Effect of different solvents on synsthesis of compound 1
solventreactionphenomenareactionproduct(MS)yieldofpre⁃BPNP/%isopropanolreddishbrownpowder53172n⁃butanolvermilionpowder53169DMSOblackpowder321,53145p⁃xylenedarksolid3210benzenedarksolid3210
4.2.2 催化剂对缩合反应的影响
在合成2,6-二苦氨基吡嗪的反应中,加入催化剂,能够有效吸收反应产生的氯化氢,促进反应平衡往产物方向移动,大幅提高反应速率。基于此,本研究在反应温度为85 ℃,反应时间为5 h,物料比n(催化剂)∶n(苦基氯)∶n(二氨基吡啶)=2∶2∶1的条件下,考察了不同催化剂对缩合反应的影响,结果见表2。由表2可知,反应体系中加入氟化钾后,会与苦基氯形成苦基氟,而吡嗪环上氨基没有吡啶环活泼,苦基氟无法与氨基吡嗪发生反应,导致收率下降; 而碳酸钾以及氢氧化镁会与酸反应生成水,导致苦基氯水解成苦味酸M=228,收率下降。反应体系加入三乙胺,可能由于三乙胺亲核性偏强,与2,6-二氨基吡嗪呈竞争关系,不利于反应进行,收率偏低。而吡啶的亲核性偏弱,利于过渡态的形成,且吸附氯化氢,更利于反应平衡往右移动,收率最高。因此,最佳的催化剂是吡啶。
表2 催化剂对合成化合物1的影响
Table 2 Effect of catalysts on synsthesis of compound 1

catalyticsystemreactionphenomenareactionproduct(MS)yieldofpre⁃BPNP/%KF,K2CO3darkmassivesolid228,53127Et3Nlightgreypowder53146pyridinedarkredpowder53172Mg(OH)2brownpowder228,53138
4.3 硝化反应条件优化
4.3.1 硝化体系对硝化反应收率的影响
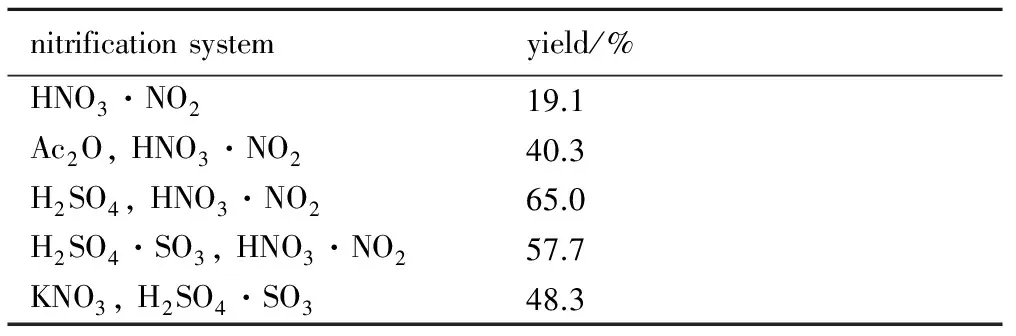
反应温度50 ℃,反应时间3 h,m(1)=0.5 g,V(HNO3)=1 mL,V(Ac2O)=4 mL,V(HNO3)=1 mL,V(H2SO4)=4 mL,V(HNO3)=1 mL,V(H2SO4·SO3)=4 mL,n(KNO3)∶n(1)=1∶1,V(H2SO4·SO3)=4 mL的条件下,考察了不同硝化体系对硝化反应收率的影响,结果见表3。
表3 不同硝化体系对硝化反应收率的影响
Table 3 Effect of different nitrification systems on the yield of nitrolysis reaction
nitrificationsystemyield/%HNO3·NO219.1Ac2O,HNO3·NO240.3H2SO4,HNO3·NO265.0H2SO4·SO3,HNO3·NO257.7KNO3,H2SO4·SO348.3
由表3可知,随着硝化体系硝化能力的上升,收率先增加后减少,这可能是因为吡嗪环上氮原子的电负性较强,环上电子云往氮原子附近偏移,导致α位硝化较苯和吡啶困难[25],较弱的硝化剂不能完全反应,收率不高; 但由于环上氨基的供电子作用,使得2,6-二苦氨基吡嗪比一般的二嗪类更易发生亲电取代反应[26],在硝化体系为浓硫酸、发烟硝酸时,收率最高。之后随着硝化体系硝化能力的提高,导致副产物增多,收率下降。因此,本研究采用浓硫酸、发烟硝酸为硝化体系,收率最高。
4.3.2 硫酸与硝酸体积比对硝化反应收率的影响
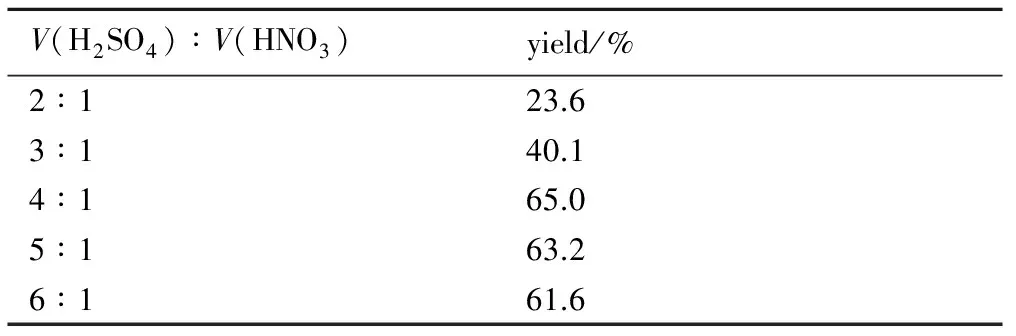
反应温度50 ℃,反应时间3 h ,料比n(1)∶n(HNO3)=1∶20的条件下,考察了硫酸与硝酸不同体积比对硝化反应收率的影响,结果见表4。
由表4可知,随着浓硫酸的增加,反应收率先增加后减少,在V(H2SO4)∶V(HNO3)=4∶1,硝化反应产率最高。分析可能因为硫酸体积过少,会导致体系中硝酰阳离子的浓度过低,硝化能力弱,反应收率低; 而硫酸的主要作用是吸水和形成硝酰阳离子,随着硫酸体积增大,收率无明显变化。因此,浓硫酸与发烟硝酸的最佳体积比是4∶1。
表4 硫酸与硝酸体积比对硝化反应收率的影响
Table 4 Effect of the volume ratio between H2SO4and HNO3on the yield of nitrolysis reaction
V(H2SO4)∶V(HNO3)yield/%2∶123.63∶140.14∶165.05∶163.26∶161.6
4.3.3 反应温度对硝化反应收率的影响
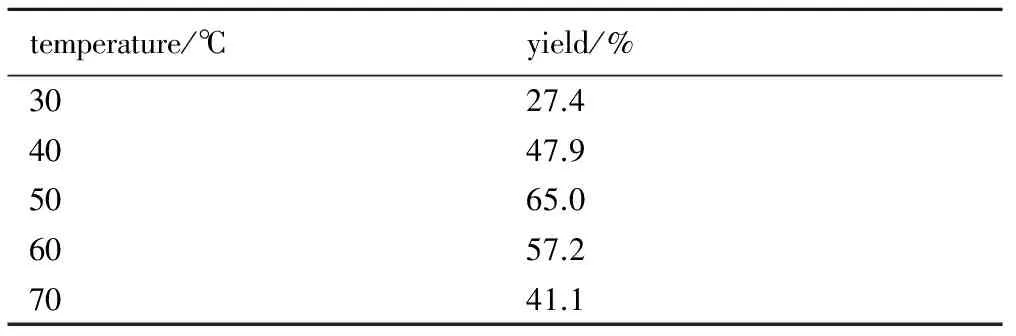
反应3 h,料比n(1)∶n(HNO3)=1∶20,V(H2SO4)∶V(HNO3)=4∶1下,考察了不同的反应温度对硝化收率的影响,结果见表5。由表5可知,随着反应温度的增加,反应收率先增加后减少,在温度为50 ℃时,反应收率最高,为65%。继续提高反应温度,收率降低,可能因为在硝化过程中,硝化温度越高,硝化能力越强,故在温度到达50 ℃前,收率成上升趋势; 而过高的温度下硝化体系硝化能力过强,导致氧化分解等副反应增多,收率降低[27]。因此,最佳反应温度为50 ℃。
表5 反应温度对硝化反应收率的影响
Table 5 Effect of the temperature on the yield of nitrolysis reaction
temperature/℃yield/%3027.44047.95065.06057.27041.1
4.3.4 反应时间对硝化反应收率的影响
反应温度50 ℃,料比n(1)∶n(HNO3)=1∶20,V(H2SO4)∶V(HNO3)=4∶1,考察了不同反应时间对硝化收率的影响,结果见表6。由表6可知,随着时间的增加,收率增加,3 h后反应趋于完全。延长反应时间,反应体系中水的增加导致硝化体系的硝化能力减弱,反应达到平衡,收率无明显变化。因此最佳反应时间为3 h。
表6 反应时间对硝化反应收率的影响
Table 6 Effect of reaction time on the yield of nitrolysis reaction
time/hyield/%131.4247.3365.0464.2563.8
4.4 BPNP的热稳定性研究
在氮气流速为30 mL·min-1,升温速率5 ℃·min-1,温度范围50~500 ℃,样品量为0.2300 mg条件下得到2,6-二苦氨基-3,5-二硝基吡嗪(BPNP)的TG-DSC曲线,结果见图4。DSC曲线表明,样品存在两个放热峰: 374.3,409.1 ℃。结合TG曲线所知,样品分两个阶段分解: 第一个阶段从354.0 ℃开始,当温度达到380.1 ℃,失重为46.2%; 第二阶段从380.1 ℃开始,当温度达到450 ℃时,失重为65.6%,之后随着温度提高,失重曲线趋于平缓。参考PYX的热分解历程,由于BPNP结构与之类似,导致其分两步分解: 第一步氨基和硝基断裂,生成芳香族多聚体; 第二步芳香族多聚体发生分解。BPNP的吡嗪环内氮原子与环内的碳原子成共轭体系,分子内—NO2与α—C上的—NH形成分子内或分子间氢键,以及BPNP的苦基与吡嗪环形成了共轭[28],得其具有较好的热稳定性。
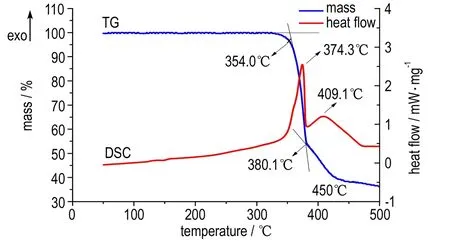
图4 BPNP的TG-DSC曲线
Fig.4 TG-DSC curves of BPNP
4.5 BPNP的性能分析
为了更好地分析BPNP的爆轰性能,本研究用相同方法计算了PYX和BPNP的密度、爆速、爆压和撞击感度,并列出了PYX和HNS的爆轰性能的文献实测值进行比对,结果见表7。由表7可知,PYX的计算值与文献值较为接近,表明该方法计算值有一定的参考价值; 而BPNP的密度、爆速与爆压,都高于HNS,略高于PYX的计算值和文献值; 撞击感度与PYX的计算值和文献值相当。这表明与PYX相比,BPNP具有更好的爆轰性能,是一种具有潜在应用前景的新型耐热含能材料。
表7 HNS、PYX与BPNP的性能对比
Table 7 Comparison of the properties of HNS, PYX and BPNP

compoundρ(crystal)/g·cm-3D/m·s-1p/GPaH50/cmHNS1.73[1]7019[1]20[1]-PYX1.75[4],1.777480[4],759024.20[4],26.0263[4],76BPNP1.82813028.2583
5 结 论
(1) 以2,6-二氨基吡嗪和2,4,6-三硝基氯苯为原料,经缩合、硝化两步反应,合成了一种新化合物2,6-二苦氨基-3,5-二硝基吡嗪(BPNP),总收率为47%,并用红外光谱、核磁共振、质谱对其结构进行表征。
(2) 研究了不同溶剂与催化剂对缩合反应的影响,确定了缩合反应溶剂为异丙醇,催化剂为吡啶,收率72%; 以浓硫酸发烟硫酸为硝化体系,确定了硝化反应的最优反应条件: 反应温度50 ℃,V(H2SO4)∶V(HNO3)=4∶1,反应时间为3 h,硝化反应收率为65%。
(3) 利用TG和DSC研究了2,6-二苦氨基-3,5-二硝基吡嗪的热性能,发现其从354.0 ℃开始分解,分解峰值为374.3 ℃,与PYX相当,具有较好的热安定性能。
(4) 预估了BPNP的物化和爆轰性能,其理论密度为1.82 g·cm-3,生成热为112.88 kJ·mol-1,爆速为8.13 km·s-1,爆压为28.25 GPa。
参考文献:
[1] Klapötke T M, Stierstorfer J, Weyrauther M, et al. Synthesis and investigation of 2,6-bis(picrylamino)-3,5-dinitro-pyredine (PYX) and its salts[J].ChemistryAEuropeanJournal, 2016, 22: 8619-8626.
[2] Agrawal J P. Some new high energy materials and their formulations for specialized applications[J].Propellants,Explosives,Pyrotechnics, 2015, 30(5): 316-328.
[3] 周建华, 于谦, 陈捷, 等. 耐热炸药TATB、 PYX和LLM-105的热安定性研究[J]. 化学研究与应用, 2014, 26(11): 1802-1803.
ZHOU Jian-hua, YU Qian, CHEN Jie, et al. Study on the thermal stability of heat-resistance explosives TATB, PYX and LLM-105[J].ChemicalResearchandApplication, 2014, 26 (11): 1802-1803.
[4] 陆明. 炸药的分子与配方设计[M]. 北京: 兵器工业出版社, 2004: 152-202.
LU Ming. Molecular and formulation design of explosives[M]. Beijing: Weapon Industry Press, 2004: 152-202.
[5] 邓明哲, 张川, 叶志虎, 等. 耐热炸药PYX制备工艺改进[J]. 应用化工, 2013, 42(5): 904-906.
DENG Ming-zhe, ZHANG Chuan, YE Zhi-hu, et al. Improvement on preparation of heat-resistant explosive PYX[J].AppliedChemicalIndustry, 2013, 42(5): 904-906.
[6] 王军, 黄靖伦, 廖龙渝, 等. 一种PYX制备新技术[J]. 含能材料, 2008, 16(4): 480.
WANG Jun, HUANG Jing-lun, LIAO Long-yu, et al. A new technology of PYX preparation[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2008, 16(4): 480.
[7] LIU Hui, WANG Fang, WANG Gui-xiang, et al. Theoretical investigations on structure, density, detonation properties, and sensitivity of the derivatives of PYX[J].JournalofComputationalChemistry, 2012, 33(1): 1790-1796.
[8] 王保国, 张景林, 陈亚芳. 超细PYX的制备和性能测试[J]. 含能材料, 2007, 15(3): 198-200.
WANG Bao-guo, Zhang Jin-ling, CHEN Ya-fang. Preparation and performance testing of ultra-fine PYX[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 2007, 15(3): 198-200.
[9] 刘兰, 王平, 曾贵玉, 等. 亚微米PYX的制备及性能[J]. 火炸药学报, 2009, 32(6): 44-48.
LIU Lan, WANG Ping, ZENG Gui-yu, et al. Preparation and proterties of submicron PYX[J].ChineseJournalofExplosives&Propellants, 2009, 32(6): 44-48.
[10] 赵晓峰, 刘祖亮.姚其正, 等. 2,6-二氨基-3,5-二硝基吡嗪-1-氧化物的合成[J]. 火炸药学报, 2012, 35(3): 15-18.
ZHAO Xiao-feng, LIU Zu-liang, YAO Qi-zheng, et al. 2,6-Diamino-3,5-dinitropyrazine-1-oxide Synthesis and Explosion Properties[J].ChineseJournalofExplosives&Propellants, 2012, 35(3): 15-18.
[11] 赵晓峰, 刘祖亮. 2,6-二氨基-3,5-二硝基吡嗪-1-氧化物合成及爆炸性质研究[J]. 高校化学工程学报, 2013, 27(2): 248-253.
ZHAO Xiao-feng, LIU Zu-liang. 2,6-Diamino-3,5-dinitropyrazine-1-oxide Synthesis and Explosion Properties[J].JournalofChemicalEngineeringofChineseUniversities, 2013, 27(2): 248-253.
[12] Smaili L, Refouvelet B, Xicluna A, et al. Phloroglucinol: novel synthesis and role of the magnesium cation on its binding with human serum albumin(HSA) using a biochromatographic approach based on Langmuir isotherms[J].JournalofPharmaceuticalandBiomedicalAnalysis, 2003, 32(1): 549-553.
[13] 陈天云, 吕春绪, 姜广涛. 2,4,6-三硝基氯苯的合成研究[J]. 火炸药学报, 1997, 20(2): 12-14.
CHEN Yun-tian, LÜ Chun-xu, JIANG Guang-tao. Synthetic study of 2,4,6-trinitro-chlorobenzene[J].ChineseJournalofExplosives&Propellants, 1997, 20(2): 12-14.
[14] 梁长玉. 3,5-二氨基多硝基吡啶及其衍生物的合成研究[D]. 南京: 南京理工大学, 2012.
LIANG Chang-yu. Synthesis of 3,5-diamino-multi-nitropyridine and its derivatives[D]. Nanjing: Nanjing University of Science and Technology, 2012.
[15] Lee Chengteh, Yang Wei-tao, Parr Robert G. Development of the Colle-Salvetti correlation-energy formula into a functional of the electron density[J].PhysicalReviewB, 1988, 37, 785-789.
[16] Kamlet M J, Jacobs S T. Chemistry of detonation. I. A simple method for calculating detonation properties of C, H, N, O explosives[J].JournalofChemicialPhysics, 1968, 48(1): 23-25.
[17] Lu T, Chen F, Multiwfn. A multifunctional wavefunction analyzer[J].JournalofComputationalChemistry, 2012, 33: 580-592.
[18] Frisch M J, Trucks G W, Schlegel H B, et al. Gaussian 03, Revision E.02. Gaussian Inc[C]∥Wallingford CT, 2003.
[19] Zhang Jian-ying, Du Hong-chen, Wang Fang, et al. DFT studies on a high energy density cage compound 4-trinitroethyl-2,6,8,10,12-pentanitrohezaazaisowurtzitane[J].JournalofPhysicalChemistry.A, 2011, 115(24): 6617-6621.
[20] Politzer P, Martinez J, Murray J S, et al. An electrostatic interaction correction for improved crystal density prediction[J].MolecularPhysics, 2009, 107(19): 2095-2101.
[22] 倪基华, 邓林, 陈鉴清. 硝基化合物的质谱研究[J]. 质谱学报, 1993, 14(3): 52-56.
NI Ji-hua, DENG Lin, CHEN Jian-qing. A study on the mass spectrometry of nitro & compounds[J].JournalofChineseMassSpectrometrySociety, 1993, 14(3): 52-56.
[23] 王乃兴, 李纪生. 2,6-二苦氨基-3,5-二硝基吡啶的新法合成探讨[J]. 含能材料, 1994, 2(3): 25-28.
WANG Nai-xing, LI Ji-sheng. A new method of synthesizing 2,6-bis(picrylamino)-3,5-dinitropyridine[J].ChineseJournalofEnergeticMaterials(HannengCailiao), 1994, 2(3): 25-28.
[24] 王乃兴. 2,6-二氨基吡啶的缩合反应研究[J]. 化学通报, 1993 (5): 32-34.
WANG Nai-xing. Study on the synthesis of 2,6-bis(picrylamino)-3,5-dinitropyridine[J].ChemistryBulletin, 1993 (5): 32-34.
[25] 甘雄. 吡啶、吡嗪和均三嗪耳朵量子化学理论研究[J]. 常州工学院学报, 2006, 19(3): 56-59.
GAN Xiong. A quantum chemistry study of pyridine, pyrazine and Triazine[J].JournalofChangzhouInstituteofTechnology. 2006, 19(3): 56-59.
[26] 刑其毅. 有机化学[M]. 北京: 高等教育出版社, 2005: 875-918.
XING Qi-yi. Organic chemistry[M]. Beijing: Higher Education Press, 2005: 875-918.
[27] 王鹏程. 芳烃的硝化反应及其理论研究[D]. 南京: 南京理工大学, 2013.
WANG Peng-cheng. Nitration of aromatics and its theoretical study[D]. Nanjing: Nanjing University of Science and Technology, 2013.
[28] 金朋刚, 常海, 陈智群, 等. PYX红外热行为研究[J].火炸药学报, 2006, 29(2): 69-72.
JIN Peng-gang, CHANG Hai, CHEN Zhi-qun, et al. Investigation on thermal behavior of PYX by infrared spectral analysis[J].ChineseJournalofExplosives&Propellants, 2006, 29(2): 69-72.
