激光消融活体猪甲状腺的实验研究
2017-04-20陈松旺,沈蛇凤,徐大华
激光消融活体猪甲状腺的实验研究
【作 者】陈松旺,沈蛇凤,徐大华
南京医科大学附属南京医院(南京市第一医院)超声科,南京市,210006
用3 W/1 800 J ND:YAG激光消融活体猪甲状腺,超声检查及造影观察消融的范围,探讨激光对活体猪甲状腺的消融效果。实验结果表明,用3 W/1 800 J激光消融活体猪甲状腺,消融效果明确,能形成较理想的消融灶。
激光;甲状腺;消融
【 Writers 】CHEN Songwang, SHEN Shefeng, XU Dahua
Department of Ultrasound, Nanjing Hospital Af fi liated to Nanjing Medical University (Nanjing First Hospital), Nanjing, 210006
【 Abstract 】To explore the ablation effect of porcine thyroid in vivo ablated with 3 W/1800 J ND:YAG laser,ultrasound examination and contrast-ultrasound were done to observe scope of ablation lesion. The experimental results showed that the ablation effect of porcine thyroid in vivo ablated with 3 W/1 800 J ND:YAG laser is definite, and ideal ablation lesion can be formed.
0 引言
近年来,激光热消融治疗甲状腺结节可见国外学者[1-6]及国内学者报道[9]。治疗病变包括良性甲状腺结节[1-2],高功能腺瘤[3],甲状腺乳头状癌[6],但国内外学者选用的激光功率及能量不同,分别为(1~7 ) W、(500~3 000) J不等。何种功率及能量能取得较好的消融效果,陈松旺等[10]通过离体猪甲状腺实验,得到了3 W/1 800 J激光组合能取得较好的消融效果的结论。本实验的目的是验证3 W/1 800 J激光在活体猪甲状腺的消融效果。
1 1 064 nm激光消融系统与实验方法
1.1 1 064 nm激光消融系统
激光仪由意大利百胜公司提供,型号为Echo Laser X4,功率(0~7)W,能量范围(500~1 800) J连续可调,产生波长为1 064 nm的Nd:YAG的近红外线激光。光纤为直径300 μm的石英光学纤维。彩超仪为百胜公司MyLab9.0,超声探头频率(6~18) MHz。
激光的光子被甲状腺组织的生色基团吸收后产生热能,其产生的热能与激光能量呈线性关系[7]。组织持续加热到高于某一温度一段时间后,蛋白质发生凝固变性,温度继续升高组织发生气化和炭化[9]。炭化可以显著增加组织热量吸收,从而减少组织穿透距离,并缩小坏死区域。过度高热还可能引起光导纤维本身的损坏[7]。
1.2 实验材料及步骤
活体猪6头,重量(25.98±3.71) kg,实验猪由南京医科大学动物实验中心提供。
(1)随机选择活猪6头,分别进行编号,并称重。
(2)实验前猪空腹12 h以上,实验前30 min,肌肉注射阿托品。氯胺酮与氯丙嗪1:1肌注麻醉,氯胺酮肌注5~6 mg/kg。
(3)麻醉成功后,将猪固定于操作台上。激光消融前,超声测量甲状腺大小,计算其体积。
(4)超声引导下21GPTC针穿刺沿猪甲状腺长轴进入甲状腺实质内,确认位置合适后,再通过PTC针置入激光光纤,将PTC针后退约10 mm,使激光光纤前端约10 mm直接接触甲状腺实质。
(5)激光发生器的功率设定为3 W,时间为600 s,启动激光发生器,开始激光消融。随着消融时间的增加,光纤周围甲状腺组织增强回声范围不断扩大,消融时间增加到一定程度,增强范围扩展缓慢,甚至无明显扩展。激光发生器的能量显示器数字到达设定数字时,立即停止激光消融。
(6)消融结束后,退出激光光纤及PTC针。
(7)实验猪7 d后行超声检查及造影检查。麻醉方法同上。超声检查消融灶的改变及大小。超声造影剂SonoVue(意大利Bracco公司产品)系25 mg冻干粉剂,由六磷酸酯包裹的六氟化硫(SF6)微泡组成,微泡平均直径2.5 μm。配置时加入5 mL注射用生理盐水(0.9%NaCl)振摇后形成微泡混悬液,混匀后抽取2.4 mL,经猪的耳静脉注入。注入后,即刻观察造影效果,甲状腺未消融区域可见造影剂充填,而消融区域为造影剂充盈缺损区。检测充盈缺损区的大小,此范围即为激光消融范围,用以评判消融效果。
(8)造影后,处死猪,解剖甲状腺,测量消融灶及其内部炭化区的范围,部分组织送病理及电镜。
1.3 病理学检查及统计学方法
肉眼观察消融灶的组织改变,将解剖的消融灶组织置于10%福尔马林溶液中固定,然后行病理切片、染色及显微镜下检查。进行电镜检查时,需用特殊的溶液固定后进行电镜观察。
采用SPSS 17.0统计软件包对数据进行分析处理,计量资料用均数±标准差(x±s)表示,组间比较用随机区组设计的方差分析,两两比较用t检验,以P<0.05为差异有统计学意义。
2 1 064 nm激光消融系统实验结果分析
2.1 正常猪甲状腺的超声图像
猪甲状腺位于猪的颈前6~8个气管环腹侧。纵切时其左右侧叶最大切面呈上下稍尖,中间厚实的长椭圆形,见图1。横切时,左右侧叶呈类三角形。实质回声类似人甲状腺回声,呈细密均匀分布的点状回声。
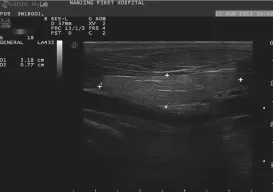
图1 纵切时活体猪甲状腺图像Fig.1 Image of porcine thyroid in vivo in longitudinal section
2.2 激光消融过程中的超声图像改变
激光消融开始后,激光光纤周围甲状腺组织回声不规则增强,见图2。随着消融的继续,回声增强范围快速扩展,当增强范围扩展到一定范围时,可见其扩展缓慢,甚至无明显扩展。

图2 消融开始后光纤周围甲状腺组织回声增强Fig.2 Hyperechogenicity in thyroid surrounding laser fi ber after ablation
2.3 消融灶的造影改变
造影剂注入猪的耳静脉后,随着时间增加,甲状腺实质内微泡回声进一步增强,增强时间约在注入后(10~20) s,其后增强回声不断减弱,直至造影剂完全消失。激光消融区域甲状腺组织由于组织坏死、炭化,其内无血流供应,造影过程中无造影剂充填,显示为明显的低回声区。用二维超声及造影超声测量纵切及横切造影剂充盈缺损区的大小,计算其体积,结果见表1。
2.4 消融灶的径线、体积
激光消融7 d后,超声观测甲状腺,可见消融灶为形态椭圆形的混合回声区域,其中可见部分不规则的高回声区及低回声区,见图3。造影结束后,处死猪,解剖出甲状腺,测量甲状腺消融坏死区域的大小及空腔的大小, 计算其体积,见表2。统计结果表明:二维超声、造影超声及解剖后测量消融灶的各径线大小及体积无明显差异(P>0.05)。即二维超声及造影超声测量的消融灶大小与解剖后测量的消融灶大小及体积相一致。
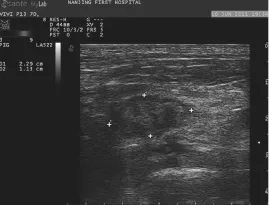
图3 消融7 d后,消融灶的二维图像Fig.3 Image of ablation after 7 days in two dimension
3 W/1800 J激光消融活体猪及离体猪甲状腺时,消融灶、空腔的各径线及体积测值及统计结果见表3。统计结果表明,活体猪甲状腺消融灶、空腔的体积明显小于离体猪甲状腺。

表1 消融灶的长径、宽径、厚径及体积Tab.1 Diameters in three direction and Volume of ablation
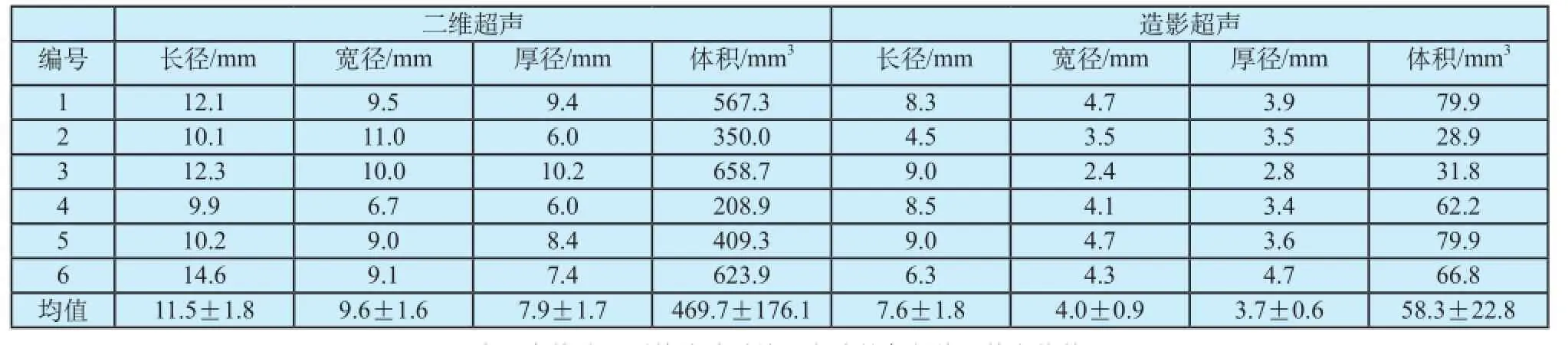
表2 消融灶及空腔的长径、宽径、厚径及体积Tab.2 Diameters in three direction and volume of ablation lesion and cavity
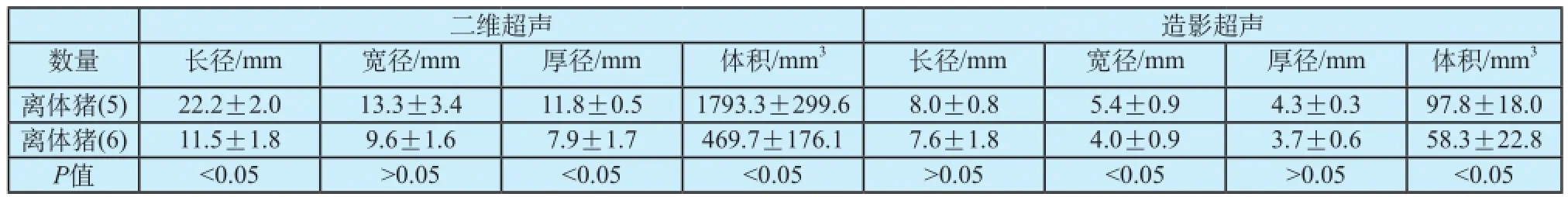
表3 离体猪及活体猪消融灶及空腔的各径线及体积均值Tab.3 Diameters in three direction and volume of ablation lesion and cavity in vitro and in vivo
2.5 消融区域组织的病理变化
(1)大体病理变化 活体猪甲状腺激光消融后,其剖面中心可见一空腔,空腔周围向外依次为炭化组织、坏死组织、移行区组织、正常组织。
(2)显微镜下病理变化 消融中心空腔内壁的炭化组织,无细胞形态。其外层甲状腺组织滤泡变性,部分滤泡腔内形成空泡。再外层甲状腺组织滤泡上皮未见明显异常。甲状腺小叶间动脉内膜增厚,动脉壁外膜变性,血管外组织呈灼伤后改变。
(3)电镜下病理变化 激光消融区域电镜检查:①坏死区 滤泡上皮细胞结构损毁,细胞器崩解,细胞核核膜破坏,染色质出现边集;②移行区 滤泡上皮细胞细胞膜显示尚清,细胞器肿胀,细胞核核膜部分中断,染色质出现边集;③远端区 滤泡上皮细胞细胞膜完整,细胞器显示清晰,细胞核核膜完整,核内染色质分布均匀。
3 讨论
3.1 3 W/1 800 J激光消融活体猪及离体猪甲状腺的病理改变及消融灶大小的比较
激光消融的功率与消融时间的乘积为消融的能量。离体猪实验表明[10],激光功率为3 W,消融时间为600 s,即激光消融能量为1 800 J时,达到较好消融效果。将离体实验的数据应用于活体猪甲状腺消融,得到了较好的消融效果。
3 W/1 800 J激光消融活体猪甲状腺的大体病理、显微镜下及电镜病理改变同离体猪甲状腺消融时的改变大体一致。
3 W/1 800 J消融时,活体猪甲状腺消融灶及空腔的大小明显小于离体猪甲状腺的大小。由于甲状腺的血供丰富,活体猪甲状腺消融时,不断循环的血流将局部消融时产生的热量部分带走,减少了激光热的效应,使得消融灶及空腔的大小减少。
3.2 超声造影及二维超声对消融灶的评估价值
超声造影是将微泡造影剂SonoVue经外周静脉注射后通过肺循环到达靶器官或靶组织,通过增加血流与周围组织间回声的差异,大大提高了对微细血管探测的敏感性和超声诊断的准确性。
活体猪甲状腺消融后1周的造影结果显示:激光消融区域甲状腺组织由于组织坏死,炭化及中央区空洞形成,其内无血流供应,造影过程中无造影剂充填,显示为明显的低回声区。
消融1周后,超声检查甲状腺,可见消融区域甲状腺回声明显不同于非消融区域甲状腺回声,据此可进行消融灶大小的测量及消融效果的评估。
活体猪的消融灶二维超声、造影超声及解剖后的测量结果统计学显示,三种方法测量消融灶大小的结果非常一致。因此,可用二维超声及造影超声评估消融效果。
3.3 影响甲状腺激光消融灶大小的因素
激光消融离体猪甲状腺,消融灶的大小与激光功率及能量有关。激光消融活体猪甲状腺,消融灶的大小还与活体猪甲状腺的血供有关。Pacella CM等[3]的临床应用结果显示结节体积缩小1 mL,冷结节需要(843~2 130) J的能量,高功能腺瘤需要(643~5 333) J的能量,其原因为高功能腺瘤血供丰富,随着血液的循环,将加热组织的热量带走,故需更高的能量。
3.4 激光消融的效果及安全性
实验结果显示,在超声的准确引导下,3 W/1 800 J激光消融活体猪甲状腺,能形成较理想的消融灶,并可避免周围组织的损伤,是一种安全性高的消融方法。
[1] Enrico P, Rinaldo G, Giancarlo B, et al. Treatment of benign cold thyroid nodules: A randomized clinical trial of percutaneous laser ablation versus levothyroxine therapy or follow-up[J]. Thyroid, 2007, 17(3): 229-235.
[2] Roberto V, Fabrizio R, Angelo B, et al. Percutaneous laser ablation of cold benign thyroid nodules: a 3-year follow-up study in 122 patients[J]. Thyroid, 2010, 20(11): 1253-1261.
[3] Pacella C M, Bizzarri G, Spiezia,et al.Thyroid tissue:US-guided percutaneous laser Thermal Ablation[J]. Radiology, 2004, 232(1): 272-280.
[4] Gerardo A, Mario R, Giovanni D C, et al. Clinical research:Low-energy interstitial laser photocoagulation for treatment of nonfunctioning thyroid nodules: therapeutic outcome in relation to pretreatment and treatment parameters[J]. Thyroid, 2006, 16(8):749-755.
[5] Helle D, Finn N B, Laszlo H. Effect of ultrasound-guided interstitial laser photocoagulation on benign solitary solid cold thyroid nodules: one versus three treatments[J]. Thyroid, 2006, 16(8): 763-768.
[6] Enrico P, Rinaldo G, Gharib H, et al. Ultrasound-guided laser ablation of incidental papillary thyroid microcarcinoma: a potential therapeutic approach in patients at surgical risk[J]. Thyroid, 2011, 21(6): 1-4.
[7] Hans-Joachim S, Frank E, Volkhard U F, et al. Basic principles of laser induced interstitial themotherapy in brain tumor[J]. Med Laser Appl, 2002, 17: 147-161.
[8] 杨继庆, 刘鲁伟, 文峻, 等. 激光生物组织热作用的影响因素[J].激光杂志, 2005, 26(5): 94.
[9] 刘 娟, 吴凤林, 隋洋, 等. 超声引导下经皮激光消融甲状腺良性实性结节[J]. 南方医科大学学报, 2013, 33(10): 1529-1532.
[10] 陈松旺, 徐大华, 顾建平. 基于超声引导的不同功率和能量的Nd:YAG激光消融效果的对比试验研究[J]. 中国医疗器械杂志, 2013, 37(1): 57-61.
Comparison of Ablation Lesions of Porcine Thyroid in Vivo Ablated with Laser
laser, thyroid, ablation
R318.51
A
10.3969/j.issn.1671-7104.2017.02.021
1671-7104(2017)02-0153-04
2016-08-29
陈松旺,E-mail: chensongwang@126.com
