对羟基苯甲酸分子印迹聚合物中模板分子的洗脱
2017-04-14刘小娟姜夏云吴锋景
刘小娟,姜夏云,吴锋景,陶 琦,李 伍
(湖南工程学院 化学化工学院,湘潭 411104)
对羟基苯甲酸分子印迹聚合物中模板分子的洗脱
刘小娟,姜夏云,吴锋景,陶 琦,李 伍
(湖南工程学院 化学化工学院,湘潭 411104)
以对羟基苯甲酸为模板分子,丙烯酰胺为功能单体,采用悬浮聚合法制备对羟基苯甲酸分子印迹聚合物,通过索氏提取和超声波/离心提取工艺洗脱模板分子,利用扫描电镜对洗脱后的印迹聚合物进行表征,并对洗脱后聚合物的吸附性能进行评价.实验结果表明,与索氏提取工艺相比,超声波/离心提取工艺在16.5 h内快速地洗脱印迹聚合物,洗脱后的印迹聚合物的形貌呈微球形状,粒径分布在0.5~6 μm之间,对模板分子具有良好的吸附性能.采取该方法可以快速检测环境中的对羟基苯甲酸.
对羟基苯甲酸;分子印迹聚合物;索氏提取;超声波/离心提取
对羟基苯甲酸 (4-Hydroxybenzoate,4-HB)是一种有机合成原料,主要应用于食品、化妆品、医药、农药和染料等领域,并且在防腐、杀菌等方面也有广泛的应用[1-3].对羟基苯甲酸属于酚酸类物质,具有致癌性,若处理不当排放到环境中,会带来严重的环境污染.目前检测微痕量对羟基苯甲酸的常用方法是液相色谱法[4-5],该法操作简便、重现性好,准确性高,但设备费用高、前处理复杂、分离慢,不适合广泛应用.因此建立快速检测对羟基苯甲酸的方法刻不容缓.
分子印迹技术是一项新兴的分子识别技术,源于1940年Pauling L[6]以抗原为模板合成抗体的设想.采用分子印迹技术制备的印迹聚合物(Molecularly Imprinted Polymer,MIP)[7]是模板分子与功能单体通过预聚作用,在交联剂和引发剂存在的情况下,采用加热或光照引发聚合形成的多聚物;当使用一定条件除去聚合物中的模板分子后,会留下与模板分子结构匹配的印迹孔穴,能选择性地吸附模板分子.因此,MIP在传感器[8]、固相萃取[9]、催化[10]等领域有着广阔的应用前景.然而,在制备MIP过程中模板分子的洗脱也相当关键,模板分子的去除直接影响到MIP的识别性能及应用,模板分子洗脱不完全会使MIP的分离能力下降,甚至发生模板分子渗漏而影响分子识别的准确性[11].为了在环境中快速吸附检测对羟基苯甲酸,本论文以对羟基苯甲酸为模板分子,丙烯酰胺为功能单体,乙二醇二甲基丙烯酸酯为交联剂,乙腈为溶剂,聚乙烯醇为分散剂,采用悬浮聚合法制备对羟基苯甲酸的分子印迹聚合物(4-HB-MIP).在模板分子洗脱工艺方面,对比索氏提取和超声波/离心洗脱模板分子的效果,以便找到高效快捷洗脱对羟基苯甲酸的方法,提高印迹聚合物的洗脱效率.
1 实验部分
1.1 试剂与仪器
对羟基苯甲酸,丙烯酰胺(AM),乙二醇二甲基丙烯酸酯(EGDMA),百灵威科技有限公司;偶氮二异丁腈(AIBN),聚乙烯醇,乙腈,甲醇,冰醋酸,西陇化工股份有限公司. 以上试剂均为分析纯,实验用水为超纯水.
上海元析UV-6000PC型紫外可见分光光度计;SU3500扫描电子显微镜(SEM);XOSHZ-A型往复式水浴恒温振荡器.
1.2 4-HB-MIP的制备
将1.0 mmol的4-HB和4.0 mmol AM 溶解在10 ml乙腈中,在4 ℃冰箱内过夜形成预聚合物,再加入20.0 mmol EGDMA配制成溶液A.将一定量的聚乙烯醇(1788 PVA)加到含有一定量蒸馏水的三口瓶中,加热至90 ℃溶解,待溶液冷却后加入少量的十二烷基磺酸钠,然后逐滴加入溶液A以及少量的AIBN,通氮气并超声,在60 ℃下搅拌反应24 h.待反应完成后,将制备的聚合物用蒸馏水洗涤去除残留的PVA,得到4-HB-MIP.而4-HB的非印迹聚合物(4-HB-Non-Molecucarly Imprinted Polymer,4-HB-NMIP)的制备方法同上,只是在制备过程中不加入模板分子.
1.3 4-HB-MIP的模板分子洗脱
1.3.1 索氏提取
准确称取1.5 g的4-HB-MIP于索式提取器中,用80 mL甲醇/醋酸(V/V,9∶1)混合溶液洗脱模板分子.设置放置索式提取器的恒温水浴锅的温度为85℃,每8 h从索氏提取管中取样一次,每次检测提取液中4-HB的含量,计算4-HB每次的提取率;按每8 h换液一次,直到提取液中4-HB的含量接近为0.而对应的4-HB-NMIP也按该方法进行洗脱.
1.3.2 超声波/离心提取
准确称取1.5 g 的4-HB-MIP于100 mL具塞锥形瓶中,加入50 mL甲醇/乙酸(9∶10,V/V)的混合溶液,在超声波作用下超声30 min,然后在4000 r/min的离心机中离心,取离心管上清液测试4-HB的含量.按每超声/离心一次更换洗脱液,计算4-HB每次的提取率,直到离心管上清液的4-HB的含量接近为0.而对应的4-HB-NMIP也按该方法进行洗脱.
1.4 MIP的形貌表征
将经过索氏提取和超声波/离心提取的4-HB-MIP分别取50 mg 放在对应的小烧杯中,加入1 mL乙醇后超声分散,各取微量置于清洁处理过的玻片上,干燥后喷金,然后用扫描电镜SEM对4-HB-MIP的表面形貌进行表征.
1.5 吸附性能评价
分别称取经过索氏提取和超声波/离心提取的4-HB-MIP和对应的4-HB-NMIP各50 mg,置于100 mL具塞锥形瓶中,加入0.5 mmol/L 4-HB的甲醇溶液.在20 ℃下,于往复式水浴恒温振荡器中震荡5 h后,取锥形瓶中的上清液稀释至合适的倍数,测试其中的4-HB的含量,根据吸附前后溶液中4-HB含量的变化计算聚合物的吸附量,对比两种洗脱工艺对模板分子的洗脱效果.
利用印迹聚合物吸附前后的浓度差值,可计算出4-HB-MIP和4-HB-NMIP的吸附量Q:
Q=(C0-C)V/W
其中Q为4-HB-MIP或4-HB-NMIP的吸附量(mmol/g);C0为4-HB的吸附前的浓度(mmol/L);C为达到吸附平衡后上层清液中4-HB的浓度(mmol/L);V为吸附溶液的体积(mL);W为印迹聚合物的重量(g).
2 结果与讨论
2.1 MIP洗脱模板分子的原理
分子印迹聚合物能够吸附模板分子在于印迹孔穴内固定排列的结合基团与模板分子间的相互作用,它主要是功能单体与模板分子复合作用产生的,形式有共价键、π-π键和氢键[12-14]等,不同结合类型的作用也是不一样的.其中,共价键只对专门的功能基团有专一的结合性,在制备MIP过程中以共价键结合的方法能产生专一性较好的MIP,但MIP快速结合模板分子不是很理想,而以氢键作用制备的MIP,是当前应用最多和最方便的方法.因为氢键作用在很多物质中存在,对比共价键作用,以氢键作用结合的MIP更容易洗脱.氢键存在于MIP外表面或内表面时,模板分子容易被洗脱下来;但位于MIP内部时,模板分子被网状聚合物包裹,洗脱难度较大,易造成MIP使用过程模板渗漏,影响MIP的吸附性能[11].因此,常采用极性较高的溶剂反复洗脱模板分子,常用的溶剂有水、乙腈、氯仿和乙腈/乙酸等.
在4-HB-MIP制备的过程中,模板分子4-HB与功能单体AM之间以氢键预聚合作用的(图1).因此,4-HB与聚合物4-HB-MIP之间的作用最终也是通过氢键形成的.文中选取甲醇/乙酸混合液作洗脱溶剂,其中甲醇极性较大,容易与MIP间形成较强的氢键,且添加一定量的乙酸可以增强溶剂的洗脱效果[15],因此选取体积比为9∶1的甲醇/乙酸的混合液作为洗脱液.
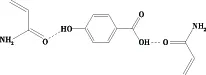
图1 4-HB与AM之间作用示意图
2.2 4-HB的标准曲线建立
精确称取13.8 mg(0. 1 mmol)的4-HB标准品于10 ml容量瓶中,用溶剂定容至刻度线,得到10 mmol/L的4-HB溶液.然后分别移取上述溶液0.5 ml、1 ml、2 ml、4 ml、6 ml和8 ml于相应的10 ml容量瓶中,用溶剂稀释至刻度线.以溶剂为空白,在254 nm处,测试紫外吸光度值Abs,绘制吸光度值随浓度C变化的标准曲线图.其中,在洗脱模板分子时,以甲醇/乙酸(V/V,9∶1)混合液作溶剂;在吸附性能评价时,以甲醇作溶剂.工作曲线如下:以甲醇/乙酸(V/V,9∶1)作溶剂:Abs=18.216C+0.01009,R2=0.99946;以甲醇作溶剂:Abs=13.933C+0.06546,R2=0.99992.
2.3 4-HB-MIP的洗脱曲线
利用索氏提取和超声波/离心提取工艺分别洗脱1.5 g的4-HB-MIP,并比较两种工艺对模板分子4-HB的洗脱效果(见图2和图3).索氏提取工艺对4-HB-MIP洗脱的影响如图2所示,在每8 h更换1次提取液的情况下,每次4-HB-MIP的模板分子提取率不同.洗脱三次(24 h)后的提取率为18.85%,在洗脱96 h后总的提取率才达到62.26%,洗脱144 h后总的提取率为90%以上,而要彻底洗脱完全则需要264 h.超声波/离心提取工艺对4-HB-MIP洗脱的影响如图3所示,按每次超声30 min后进行离心分离,洗脱两次(1 h)后提取率可以达到54.29%,随后每次提取率均低于10%.当提取时间在10 h后,4-HB-MIP的模板分子总的提取率为90.75%,在超声波/离心提取16 h后,模板分子4-HB提取率接近为零.从时间上考察4-HB-MIP的洗脱效果,索氏提取的时间是超声波/离心提取时间的16倍;溶剂消耗量来看,索氏提取的消耗高于超声波/离心提取工艺;而从洗脱次数考察,索氏提取的次数(33次)跟超声波/离心提取次数(34次)接近;所以,比较溶剂消耗,洗脱时间和次数,超声波/离心洗脱4-HB-MIP的工艺提取效率高于索氏提取洗脱工艺.
从图2和图3看到,随着洗脱时间的增加,均会出现初始洗脱提取率较高,然后缓慢降低的过程.由于制备的分子印迹聚合物中的某些模板分子可能暴露在微粒的表面,因此容易洗脱干净,提取率较高;而某些模板分子包裹在印迹聚合物的微粒内部,需要足够的传质推动力和传质时间来洗脱模板分子,洗脱4-HB-MIP较难,提取率较低.因此,采用超声波/离心提取工艺洗脱模板分子,可以在较短时间内彻底洗脱4-HB,反映了超声波/离心提取高效的特点.

图2 索氏提取工艺对4-HB-MIP洗脱的影响
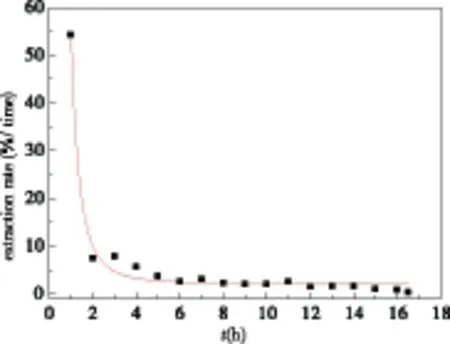
图3 超声波/离心提取工艺对4-HB-MIP洗脱的影响
2.4 SEM表征
利用扫描电镜分别表征索氏提取和超声波/离心提取工艺洗脱4-HB-MIP后的形貌,如图4和图5所示.从图中可知,经过两种工艺洗脱后的分子印迹聚合物的形貌基本未发生变化,均呈微球形状,粒径分布在0.5~6 μm之间,说明两种洗脱工艺不会破坏印迹聚合物的结构.

图4 索氏提取后的4-HB-MIP

图5 超声波/离心提取后的4-HB-MIP
2.5 吸附性能评价
利用经过索氏提取和超声波/离心提取洗脱的4-HB-MIP和4-HB-NMIP分别吸附0.5 mmol/L 4-HB的甲醇溶液,考察两种洗脱工艺对印迹聚合物吸附模板分子4-HB的效果,如表1所示.

表1 4-HB-MIP/4-HB-NMIP 的吸附效果
从表1可知,无论采取索氏提取,还是超声波/离心提取洗脱4-HB-MIP,只要印迹聚合物中模板分子洗脱较彻底,0.5 mmol/L 4-HB的甲醇溶液对这两种聚合物的吸附效果基本上是接近的.同样,4-HB-NMIP吸附4-HB的效果也基本类似.因此,采取超声波/离心提取洗脱4-HB-MIP是一种较为高效快捷洗脱对羟基苯甲酸的方法,可以提高检测环境中对羟基苯甲酸的效率.
3 结论
(1)对索氏提取和超声波/离心提取洗脱工艺比较,超声波/离心提取工艺的效率优于索氏提取,能在16.5 h内快速高效地洗脱4-HB-MIP,而索氏提取工艺则需264 h 完成洗脱.
(2)经两种提取工艺洗脱后的4-HB-MIP,印迹聚合物的形貌基本未发生变化,均呈微球形状,粒径分布在0.5~6 μm之间.
(3)对比索氏提取和超声波/离心洗脱工艺,4-HB-MIP或者4-HB-NMIP对0.5 mmol/L 4-HB的甲醇溶液的吸附效果基本接近.但是采取超声波/离心提取洗脱4-HB-MIP是一种较为高效快捷洗脱模板分子的方法,可以快速检测环境中的对羟基苯甲酸.
[1] 朱 莉,许超艳,李晶晶,等.生物合成对羟基苯甲酸的研究进展[J].生物工程学报, 2015, 31(3):328-337.
[2] 严 兵,章亚峰,梁子军,等.对羟基苯甲酸在有机合成中的应用[J].精细化工原料及中间体,2010(12):42-44.
[3] 张庭廷,何 梅,吴安平,等.对羟基苯甲酸对铜绿微囊藻的化感效应以及对鲤鱼的毒性作用[J].环境科学学报,2008,28(9):1887-1893.
[4] 王作君,韦 平,贾 辉,等.HPLC法同时测定千里光中对羟基苯甲酸和邻羟基苯甲酸的总含量及对羟基苯乙酸的含量[J].中国药师,2014(5):767-769.
[5] 闫 妍,刘永明,朱晓琼.HPLC法同时测定对羟基苯甲酸酯类及对羟基苯甲酸含量[J].中国药物评价,2014(2):82-85.
[6] Pauling L. A Theory of the Structure and Process of Formation of Antibodies[J]. Journal of the American Chemical Society, 1940, 62(10): 2643-2657.
[7] 小宫山真,竹内俊文,务川高志,等.分子印迹学:从基础到应用[M].吴世康,汪鹏飞,译.北京:科学出版社,2006.
[8] 魏小平,谭艳季,李建平.磁性粒子表面自组装辛可宁分子印迹电致化学发光传感器[J].分析化学,2015,43(3):424-428.
[9] 韦寿莲,刘 玲,黎京华,等.双分子印迹聚合物微球选择固相萃取环境和食品样品中壬基酚和双酚A[J].分析化学,2015,43(1):105-109.
[10]张连明,李建平,潘宏程.基于门控制电催化效应的分子印迹传感器[J].分析化学,2012,40(7):1025-1030.
[11]唐仕荣,刘全德,刘 辉,等.氯霉素分子印迹聚合物中模板分子的洗脱方法[J].徐州工程学院学报(自然科学版),2011,26(3):68-71.
[12]Wulff G. Selective Binding to Polymers Via Covalent Bonds. The Construction of Chiral Cavities as Specific Receptor Sites [J]. Pure & Applied Chemistry, 1982, 54(11):2093-2102.
[13]Zhou J, Xiwen H E, Zhao J, et al. A Study of Binding Action and Selectivity of Trimethoprim Molecular Template Polymer[J]. Chemical Research in Chinese Universities, 1999(2):204-208.
)[14]Zhang T, Liu F, Chen W, et al. Influence of Intramolecular Hydrogen Bond of Templates on Molecular Recognition of Molecularly Imprinted Polymers[J]. Analytica Chimica Acta, 2001, 450(1-2):53-61.
[15]Ellwanger A, Berggren C, Bayoudh S, et al. Evaluation of Methods Aimed at Complete Removal of Template from Molecularly Imprinted Polymers[J]. Analyst, 2001, 126(6):784-92.
Removal of Template Molecules from Molecularly Imprinted Polymer ofp-hydroxybenzoic Acid
LIU Xiao-juan, JIANG Xia-yun, WU Feng-jing,TAO Qi,LI Wu,
(School of Chemistry and Chemical Engineering, Hunan Institute of Engineering, Xiangtan 411104, China)
Molecularly imprinted polymer (MIP) for recognition ofp-hydroxybenzoic acid is synthesized by suspension polymerization. Acrylamide is used as functional monomer. The extraction of the template from MIP and adsorptive capacity to template are explored by comparative study. The ultrasonic/centrifugation extraction procedure for removing the template is completed in 16.5 h, as compared with the soxhlet extraction process in 264 h. The morphology of the extracted MIP is characterized by scanning electron microscopy, which shows that the MIP are microspheres and the diameters are between 0.5~6 μm. The MIP have higher adsorptive capacity than the non-molecularly imprinted polymer. In contrast with soxhlet extraction, the ultrasonic / centrifugation extraction procedure is more effective at rapid removal of template from molecularly imprinted polymer.
p-hydroxybenzoic acid; molecularly imprinted polymer; soxhlet extraction; ultrasonic / centrifugation extraction
2016-08-26
湖南省教育厅科研项目(16C0394);湖南工程学院校级青年项目(09001001);湖南工程学院大学生研究性学习和创新性实验计划项目.
刘小娟(1981-),女,硕士,工程师,研究方向:功能材料,E-mail:liuxiaojuan0923@163.com.
吴锋景(1978-),男,博士,工程师,研究方向:功能材料,E-mail:wfj2013@aliyun.com.
TB34
A
1671-119X(2017)01-0072-04
