羧甲基壳聚糖/ES纤维水刺医用敷料的制备和性能
2017-04-10邓惠文高颖俊靳向煜
邓惠文, 高颖俊, 靳向煜
(东华大学 纺织学院, 上海 201620)
壳聚糖(CTS)为甲壳素脱乙酰化产物,是至今发现的唯一天然碱性多糖,具有生物相容性和生物可降解性,可用于止血、防腐和促进伤口愈合[1].CTS能激活机体系统、介导机体系统的系列生物学效应,提高吞噬细胞的系统功能,还具有抑菌性[2],在生物医用敷料中有着广泛的应用.但由于CTS的水溶性差,只溶于酸或酸性溶液,产品呈微酸性,对人体有一定的刺激,在临床医学的应用受到极大限制.CTS羧甲基化产物,即羧甲基壳聚糖(CMC)既保留了CTS的优良性能,也极大改善了其水溶性、抗菌性、可降解性[3].CMC纤维接触去离子水后能迅速形成三维网状结构的水凝胶体,具有良好的保湿性能,符合湿润环境愈合理论[4],能为愈合时间较长的慢性伤口提供更有效和更快速的治疗,其应用于新型医用敷料已在医学界得到极大的认可[5].
水刺非织造工艺流程短、成本低,其产品质地柔软,吸湿、透湿性好,并且有一定强力,被广泛应用于医疗卫生领域.壳聚糖纤维卷曲度小、刚度较大[6],成网过程中会降低针齿对纤维的握持能力,影响纤维之间的缠结,难以成网[7-8],且壳聚糖纤维经羧甲基化改性后存在力学性能下降、纤维黏结成块等问题.为保持敷料的结构和力学性能,在原料中混入一定量的聚烯烃系双组分热熔黏结(ES)纤维[9].ES纤维具有化学稳定性和独特的皮芯结构,在壳聚糖羧甲基改性反应中不会被改性试剂所腐蚀,并且热熔点较低的纤维皮层能发生熔融黏结,而芯层保持纤维状态存在于材料中,可作为骨架维持织物空间结构,改善材料手感.
1 试样制备
1.1 原材料
CTS纤维,由山东华兴海慈新材料有限公司提供,1.68 dtex×38 mm,脱乙酰度为80.6%,卷曲度为2.5%;ES纤维,浙江新维狮合纤股份有限公司,2 dtex×50 mm,卷曲度为12.3%;氯乙酸钠,分析纯,上海麦克林生化科技有限公司;无水乙醇,分析纯,鸿盛精细化工;NaOH,分析纯,平湖化工试剂厂.
1.2 制备工艺
采用CTS纤维和双组分皮芯结构的ES纤维为原料,制备成质量配比为30/70, 50/50, 70/30, 100/0,面密度为110 g/m2的CTS/ES水刺医用敷料,再经过羧甲基化改性成为CMC/ES水刺医用敷料.
1.2.1非织造水刺工艺
CTS纤维和ES纤维混合后经平行铺网成网,使用FleissnerY500-2型平网式水刺机水刺缠结加固,包括两个缠结机制-预湿水刺系统和主水刺系统.为了改善非织造材料正反面毛羽和更有效的缠结,本文采用预湿水刺1道和正反面各2道主水刺的加固方式.由于水刺工艺中水刺压力的大小对纤维之间的缠结效果影响较大,影响到非织造材料的结构与性能,故控制为统一参数以便于分析羧甲基化改性和纤维原料对材料的影响.
1.2.2羧甲基化改性
羧甲基改性反应仅发生在CTS纤维,主要反应分为两步,碱化反应和醚化反应.首先通过在NaOH中发生碱化反应,CTS纤维发生溶胀并产生大量活化中心;然后再通过与一氯乙酸的醚化反应引入—CH2COOH完成改性反应.具体改性方法如下:将6 g CTS/ES水刺医用敷料置入800 mL烧杯中,加入质量分数为30%的NaOH水溶液200 g,搅拌使敷料完全浸入NaOH溶液中,室温下放置48 h碱化;取出材料置入800 mL烧杯中,加入无水乙醇200 g做为反应试剂,震荡条件下加入氯乙酸钠29.2 g作为反应试剂,室温下反应6 h后将试样取出;用乙醇溶液充分洗涤试样至中性,挤压试样去除多余液体,平铺于通风处自然风干,即得到CMC/ES水刺医用敷料[10-11].
1.2.3热风加固处理
本文使用的ES纤维是以聚乙烯为皮层和聚丙烯为芯层的双组分纤维,皮层材料熔点低且柔软性好,芯层材料则熔点高且强度高.经热风加固处理后,纤维芯层仍保留纤维状态,纤维皮层部分开始熔融黏结,并且纤维具有较好的耐化学性,这些特殊的性能使得ES纤维能成为CMC/ES水刺医用敷料的骨架.
ES纤维的差示扫描量热(DSC)测试曲线如图1所示.由图1可知,ES纤维皮层熔点为131.94 ℃,
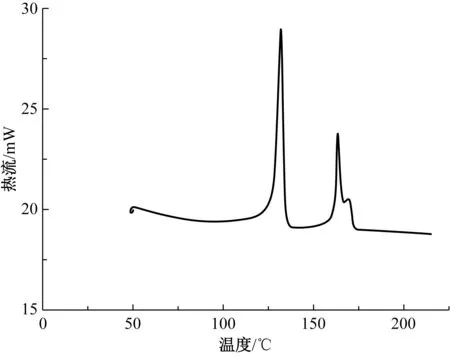
图1 ES纤维的DSC曲线Fig.1 DSC curve of ES fiber
芯层熔点为163.89 ℃.为达到ES纤维黏合目的,并尽量避免CMC纤维因过度受热而损伤,对敷料进行低温短时间(135 ℃,5~7 min)的热风穿透处理,使ES纤维皮层材料一定程度上熔融和黏结.
本文所用非织造材料工艺规格如表1所示.

表1 不同规格的水刺医用敷料
注:“+”为改性处理,“-”为未改性处理
2 测试方法
采用Nicolet Nexus 670型红外光谱仪对改性前后的壳聚糖医用敷料的分子结构进行表征,验证壳聚糖的羧甲基取代完成与否.采用日立TM-1000型台式扫描电子显微镜(SEM)对羧甲基改性前后的壳聚糖纤维和壳聚糖/ES医用敷料的表观形态.使用CFP-1100-AI型孔径及分布测试仪对改性前后的壳聚糖/ES医用敷料进行孔径分析,以更具体地了解样品的结构变化.
面密度和厚度是医用敷料十分重要的性能指标之一,与敷料很多性能关系密切,如敷料的透气性、透湿性等性能.面密度测试参照GB/T 24218.1—2009《纺织品 非织造布试验方法:第1部分单位面积质量》,使用FA2004A型电子天平,进行测试.厚度测试参照GB/T 24218.2—2009《纺织品 非织造布试验方法 第2部分:厚度的测定》,使用YG141N型织物厚度仪进行测定.
在创面愈合过程中,新型医用敷料不仅要提供适宜伤口愈合的湿润环境,还需要具备一定的透气性能,能够使氧气进入创面并及时排出皮肤代谢的二氧化碳,促进伤口的愈合的同时能防止细菌在无氧环境下的繁殖. 纤维之间的孔隙是气体通过的主要通道,材料的原料种类、面密度、厚度以及结构都影响试样的透气性能.透气性测试参照GB/T 5453—1997《纺织品,织物透气性的测定》测定,使用YG461N型数字式透气量仪测量透气性,通过测定流量孔径两面的压差,得到敷料的透气性.
液体吸收性参照YY/T 0471.1—2004《接触性创面敷料试验方法——第1部分:液体吸收性》中3.2的方法配制试验液(用磷酸盐缓冲液模拟人体体液pH) 进行测试.
3 结果分析
3.1 红外光谱表征
羧甲基改性前后壳聚糖/ES水刺敷料的红外光谱图如图2所示.

图2 羧甲基改性前后壳聚糖/ES水刺敷料的红外光谱图Fig.2 IR spectra of CTS/ES spunlanced wound dressing before and after carboxymethy/modification
由图2可知,羧甲基改性前后的医用敷料红外曲线分别在3 373和3 380 cm-1存在—OH吸收峰,在 2 921和2917 cm-1处存在—CH2—吸收峰,在1 068和1 071 cm-1处存在—C—O—C—的特征吸收峰.
由于图2中(b)曲线是试样发生羧甲基改性反应后的红外光谱图,明显存在(a)曲线中没有的吸收峰. 由图2(b)曲线可知,羧甲基改性后的医用敷料在1 590和1 411 cm-1处存在较强的吸收峰,分别为—COO—的非对称伸缩振动吸收峰和对称伸缩振动吸收峰,这一结果说明壳聚糖已经发生了羧甲基取代反应.
3.2 形态表征与孔径分析
CTS纤维和CMC纤维的SEM图如图3所示.

(a) CTS纤维(×3 000)

(b) CMC纤维(×2 500)
Fig.3SEMimagesofchitosanandcarboxymethylchitosanfibers
由图3(a)可知,壳聚糖纤维由湿法纺丝制备成形,纵向表面不完整,呈条形沟槽状,同时表面还存在不均匀的细微孔状裂痕.这些裂痕和细微的孔洞在纤维接触液体时形成毛细血管效应,使液体能储存在这些孔洞里,增加纤维吸湿性和保湿性[12].CMC纤维(如图3(b)所示)保持基本形态,但纤维直径增加约14.2%,表面变粗糙出现裂纹并且有突起颗粒物,这种粗糙表面的纤维有利于提高材料的舒适度.
水刺医用敷料试样SEM图如图4所示.

(a) CTS/ES水刺医用敷料

(b) CMC/ES水刺医用敷料

(c) 浸润后的CMC/ES水刺医用敷料
Fig.4SEMimageofsamples
由图4(a)可知,水刺医用敷料中存在清晰的水刺孔洞,壳聚糖纤维与ES纤维分布均匀,并且较好地相互抱和与缠结.对比图4(a)中不同纤维混比的敷料,壳聚糖纤维在外力作用下发生了弯曲和挤压,而ES纤维强度高于壳聚糖纤维,不易受外力作用影响,经梳理和水刺加固作用后仍能保持原有的纤维状态,为敷料结构提供一定的支撑.由图4(b)可知,羧甲基改性后敷料仍能保持非织造材料的形态结构,相对于未改性的敷料,羧甲基改性后的敷料中纤维之间缠结更紧密,部分ES纤维之间因热风处理发生了黏结,ES纤维表面较光滑未被刻蚀,表明ES纤维在羧甲基改性反应中未参加反应.将CMC/ES水刺医用敷料在去离子水中完全浸润后,羧甲基壳聚糖纤维失去纤维形态,形成了均匀的水凝胶体,将其烘干并使用SEM观察得到图4(c),水凝胶体的覆盖面积随羧甲基聚糖纤维含量增加而增加,ES纤维由于未发生改性作用在去离子水湿润后未产生改变,并且纤维间产生一定黏合,为羧甲基壳聚糖纤维在水溶液中形成的水凝胶体系的三维空间结构提供更坚固的骨架支撑.
为了进一步探究敷料因原料混比差异和羧甲基改性处理的结构变化,对试样1~8进行了材料孔径分析,材料孔径直径的最大值、最小值和平均值在羧甲基改性前后随纤维混比的变化如图5所示.

图5 孔径随混比的关系变化曲线Fig.5 Pore size varying with the blending ratio
对于未经羧甲基改性的CTS/ES水刺医用敷料试样1~4,平均孔径随ES纤维含量的增加呈上升趋势.这可能是由于壳聚糖纤维线密度小于ES纤维,一方面相同面密度的材料中壳聚糖纤维数量多于ES纤维,另一方面壳聚糖纤维直径小于ES纤维,故壳聚糖纤维之间形成的孔隙小于ES纤维形成的孔隙.经羧甲基改性后的水刺医用敷料试样5~8的平均孔径也有随ES纤维含量增加而呈上升的趋势.
对比羧甲基改性前后的CTS/ES水刺医用敷料,由图5可知,羧甲基改性后的试样5~8的平均孔径、最大孔径和最小孔径都小于未改性的试样1~4.这可能是因为羧甲改性后的壳聚糖纤维直径膨胀,而且纤维表面有未去除干净的反应残余物,导致纤维之间形成的孔隙减小.
3.3 面密度与厚度
在制备过程中将CTS/ES水刺医用敷料的面密度控制在(110±5) g/m2内,不同混比的CTS/ES水刺医用敷料于羧甲基改性前后的面密度对比图如图6所示.
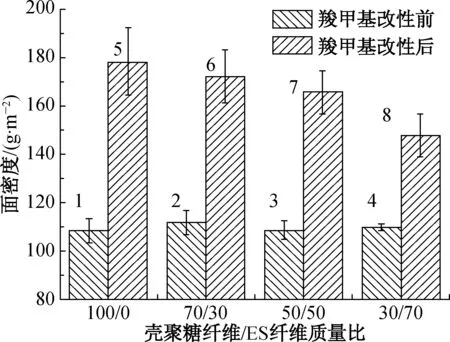
图6 混比对面密度的影响
Fig.6Surfacedensityvaryingwiththeblendingratio
由图6可知,同纤维混比的试样经羧甲基改性后,其面密度增加36.6%以上,随着壳聚糖纤维含量增加,面密度增加比率也随之上升.
对试样厚度进行测试结果如图7所示.由图7可知,同纤维混比的试样经羧甲基改性后,其厚度增加16.1%以上.这是由于羧甲基改性反应发生在壳聚糖纤维上,反应后纤维直径膨胀,纤维之间孔隙变窄,反应残留物不易洗涤和清除,附着在纤维表面,造成敷料的面密度和厚度增加.

图7 混比对厚度的影响
Fig.7Thicknessvaryingwithblendingtheratio
3.4 透气性
对试样进行透气性测试结果如图8所示. 对比试样2、 3、 4,随着材料中ES纤维含量增加,透气量增加.这是由于ES纤维直径比壳聚糖纤维直径大,纤维与纤维之间缠结形成的孔隙大.结合图5的孔径对比得到证实,而且ES纤维为皮芯结构,纤维为规整圆柱状且表面平滑,故纤维之间接触面积小,留出了较多空间可供气体通过.试样1透气量高于试样2,其原因可能是纯壳聚糖纤维卷曲度小,纤维之间难以缠结抱合,形成的非织造材料孔隙大.

图8 混比对透气性能的影响Fig.8 Permeability varying with the blending ratio
由图8可知,同种纤维混比的敷料,羧甲基改性之后透气量下降了约10%~40%.这是由于改性后敷料面密度增加,羧甲基壳聚糖纤维表面被腐蚀而变得粗糙,纤维之间的摩擦增加,纤维横向膨胀直径增大,纤维缠结更紧密,形成的孔隙更狭窄,随之透气性下降.
3.5 液体吸收性能
经过预调湿过的尺寸为10 cm×10 cm壳聚糖试样置于烧杯内,加入磷酸缓冲盐溶液(模拟人体体液pH值)500 mL,浸泡一定时间后称其质量,得到吸湿率.
吸湿率计算式为
Rma=(m-m0)/m0×100%
(1)
式中:Rma为吸湿率;m为吸湿脱水后材料的质量(g);m0为预调湿后材料的质量(g).
各试样试验结果对比如图9所示.
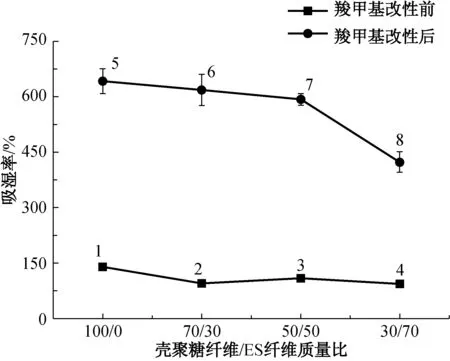
图9 混比对液体吸收性能的影响Fig.9 Absorbency varying with the blending ratio
由图9可知,对比壳聚糖/ES水刺非织造材料试样1~4,随着试样中ES纤维含量增加,吸湿率变化不是很明显,但仍能看出存在下降趋势.这是由于壳聚糖纤维的分子结构中存在大量的—OH、 —NH2等亲水性基团,分子内及分子间有大量氢键,而且纤维表面有微孔和裂痕,增加了纤维的吸湿性和液体吸收能力[12],而ES纤维的分子结构并未存在此类亲水基团,吸湿性较差,因此随着ES纤维含量的增加则导致材料的吸湿率降低.
相对于未改性的水刺非织造材料1~4,经羧甲基改性的试样5~8吸湿率提升了300%~500%,显著增加了敷料的吸湿性,并且随着壳聚糖纤维含量的增加,羧甲基改性后的医用敷料吸湿率增加.原因主要在于羧甲基改性仅发生在壳聚糖纤维上,羧甲基的取代增加了纤维的亲水集团,纤维吸湿性增加;壳聚糖纤维在改性过程中经碱化和醚化反应后,大分子的氢键被打开,分子链遭到打乱和重排,纤维的结晶区遭到破坏,有利于液体进入纤维内部;此外,改性后的纤维表面裂痕增加,毛细血管效应也进一步增加了纤维的吸湿性.
CMC水刺医用敷料在用去离子水润湿前(左)和润湿后形成凝胶(右)的数码照如图10(a)所示. 羧甲基改性后壳聚糖纤维的结晶区被破坏,非结晶区空间增加,液体能顺利渗入扩散至纤维内部,纤维发生高度膨胀并且形成一种三维网状结构的水凝胶状态,这种结构使得敷料能更好地锁住水分,极大增强其吸湿和保湿作用.对比传统的黏胶敷料或者棉质纱布,CMC/ES水刺医用敷料在接触水溶液后形成的三维网状结构,不仅能够极大增加医用敷料吸收伤口渗出液的能力,并且能为伤口提供湿润环境促进伤口愈合.在试样5上滴加适量去离子水后的显微镜图如图10(b)所示.其中,用虚线区分湿润纤维和未湿润纤维,虚线右侧纤维经去离子水湿润后开始逐渐溶胀甚至失去纤维原有形态形成透明的水凝胶,并且沿纤维分布逐渐向左扩散,虚线左侧为未湿润的材料结构图,纤维仍然保持原有形态.

(a) CMC/ES水刺医用敷料形成凝胶前后数码照

(b) CMC/ES水刺医用敷料水凝胶显微镜图
Fig.10ImageofCMC/ESspunlacedwounddressing
4 结 论
(1) 本文对制备的CTS/ES水刺医用敷料进行羧甲基改性,成功制备了一种CMC/ES水刺医用敷料,并使用红外光谱进行羧甲基表征鉴定.
(2) 经羧甲基改性后的CMC纤维仍保持纤维原有形态,纤维表面裂纹增加,直径膨胀14.2%,CMC纤维接触去离子水后迅速形成水凝胶体,ES纤维则不参与羧甲基改性反应.
(3) CTS/ES水刺医用敷料经羧甲基改性后,面密度增加36.6%以上,厚度增加16.6%以上,吸湿率增加,最高可提升500%以上.其中,CTS纤维含量越高,经羧甲基改性后的CMC/ES水刺医用敷料面密度和厚度越大.敷料的吸湿率随CMC纤维含量增加而增加,在去离子水中浸润后形成以ES纤维作为三维骨架的复合水凝胶体系,液体吸收能力得到了极大提升.
(4) 经羧甲基改性后的CMC/ES水刺医用敷料的平均孔径、最大孔径和最小孔径均下降. CTS/ES和CMC/ES水刺医用敷料的孔径均随ES纤维含量的增加而增大. 相较CTS/ES水刺医用敷料,羧甲基改性后的CMC/ES水刺医用敷料的透气性下降,但两者的透气性均随ES纤维含量增加而上升.
[1] JAYAKUMAR R, PRABAHARAN M, REIS R L, et al. Graft copolymerized chitosan—present status and applications[J]. Carbohydrate Polymers, 2005, 62(2):142-158.
[2] CAO W L, CHENG M Y, AO Q, et al. Physical, mechanical and degradation properties, and schwann cell affinity of cross-linked chitosan films[J].Journal of Biomaterials Science Polymer Edition, 2005, 16(6):791-807.
[3] WANG G, LU G, AO Q, et al. Preparation of cross-linked carboxymethyl chitosan for repairing sciatic nerve injury in rats[J]. Biotechnology Letters, 2010, 32(1):59-66.
[4] WELLER C, SUSSMAN G. Wound dressings update[J]. Journal of Pharmacy Practice and Research, 2006, 36(4):318-324.
[5] THOMAS S. A guide to dressing selection.[J]. Journal of Wound Care, 1997, 6(10):479-482.
[6] 王夕雯,靳向煜,柯勤飞.壳聚糖纤维性能的测试与分析[J].产业用纺织品,2011, 29(11):15-19.
[7] 徐小萍,张寅江,靳向煜,等.壳聚糖/黏胶水刺非织造布的制备及相关性能[J].纺织学报,2013,34(6):51-57.
[8] 王红,斯坚.ES纤维的发展及在非织造布领域的应用[J].非织造布,2008,16(2):37-38.
[9] 刘万顺.水溶性壳聚糖基纤维止血愈创材料及其制备方法和应用:101049513[P].2007-10-10.
[10] 秦益民.羧甲基甲壳胺纤维及制备方法和应用:1715465[P]. 2006-01-04.
[11] 钱清.甲壳质纤维的制备及应用[J].合成技术及应用,2001,16(3):29-32.
[12] 吴杰,吴海波,靳向煜.壳聚糖/黏胶水刺医用敷料的制备及其性能[J].东华大学学报(自然科学版),2014,40(3):276-281.
