腹腔镜下保留脾脏的胰体尾切除术的临床研究
2017-03-30金上博刘益民闫耀生郭智华
金上博,刘益民,闫耀生,郭智华
(宝鸡市人民医院,陕西 宝鸡,721000)
腹腔镜下保留脾脏的胰体尾切除术的临床研究
金上博,刘益民,闫耀生,郭智华
(宝鸡市人民医院,陕西 宝鸡,721000)
目的:探讨腹腔镜下保留脾脏的胰体尾切除术的临床价值。方法:回顾分析2014年11月至2016年4月为3例胰腺体尾部肿瘤患者行腹腔镜下保留脾脏的胰体尾切除术的临床资料。结果:3例均成功施行腹腔镜下保留脾血管的保脾手术,无中转开腹,其中1例术中撕裂脾静脉,腹腔镜下缝合脾静脉撕裂处,成功止血,72 h后恢复进食。1例患者因囊性肿瘤巨大,术中囊液外溢,造成术后胰腺切除区形成直径3 cm包裹性积液,术后2周自行吸收。术后病理均回报为胰腺粘液性囊腺瘤。出院后随访3~12个月,未见远期并发症及复发病例。结论:腹腔镜下保留脾脏的胰体尾切除术目前已成为治疗胰体尾良性肿瘤安全、可行的新选择,因其创伤小、康复快,已成为治疗胰体尾良性肿瘤的常规手术,目前也可在基层医院开展,但此术式仍需严格遵守循序渐进的推行原则。
胰腺肿瘤;保留脾脏的胰体尾切除术;腹腔镜检查
随着影像学技术的发展,越来越多的胰腺体尾部占位在临床上被发现,同时随着腹腔镜技术的发展,胰腺体尾部的腹腔镜外科治疗也逐渐成为热点[1],被越来越多的肝胆胰诊疗中心所关注,甚至在一些基层医院也陆续开展。过去的胰腺体尾部良性肿瘤常联合切除脾脏,但由于脾脏的功能日益被重视,能否最后保留脾脏成为腹腔镜胰体尾切除术中各学者更感兴趣的部分[2],2014年11月至2016年4月我科行腹腔镜下保留脾脏的胰体尾切除术3例,均采用保留脾血管的保脾手术(Kimura术式),患者术后均恢复良好,现报道如下。
1 资料与方法
1.1 临床资料 选取2014年11月至2016年4月我科行腹腔镜下保留脾脏的胰体尾切除术3例,1例患者女性,61岁,因胰腺体尾部巨大囊性占位导致持续性上腹痛住院,上腹部CT及增强 CT检查提示胰腺体尾部囊性占位,约11.8 cm大,多考虑胰腺囊腺瘤(图1);1例患者女性,42岁,无明显临床症状,体检发现胰腺尾部囊肿5.2 cm,增强CT考虑胰腺囊肿;1例患者女性,54岁,无明显临床症状,体检发现胰腺尾部囊肿4.8 cm,增强CT考虑胰腺囊腺瘤。3例患者血常规及肿瘤系列正常,其余各实验室检查未见明显异常。
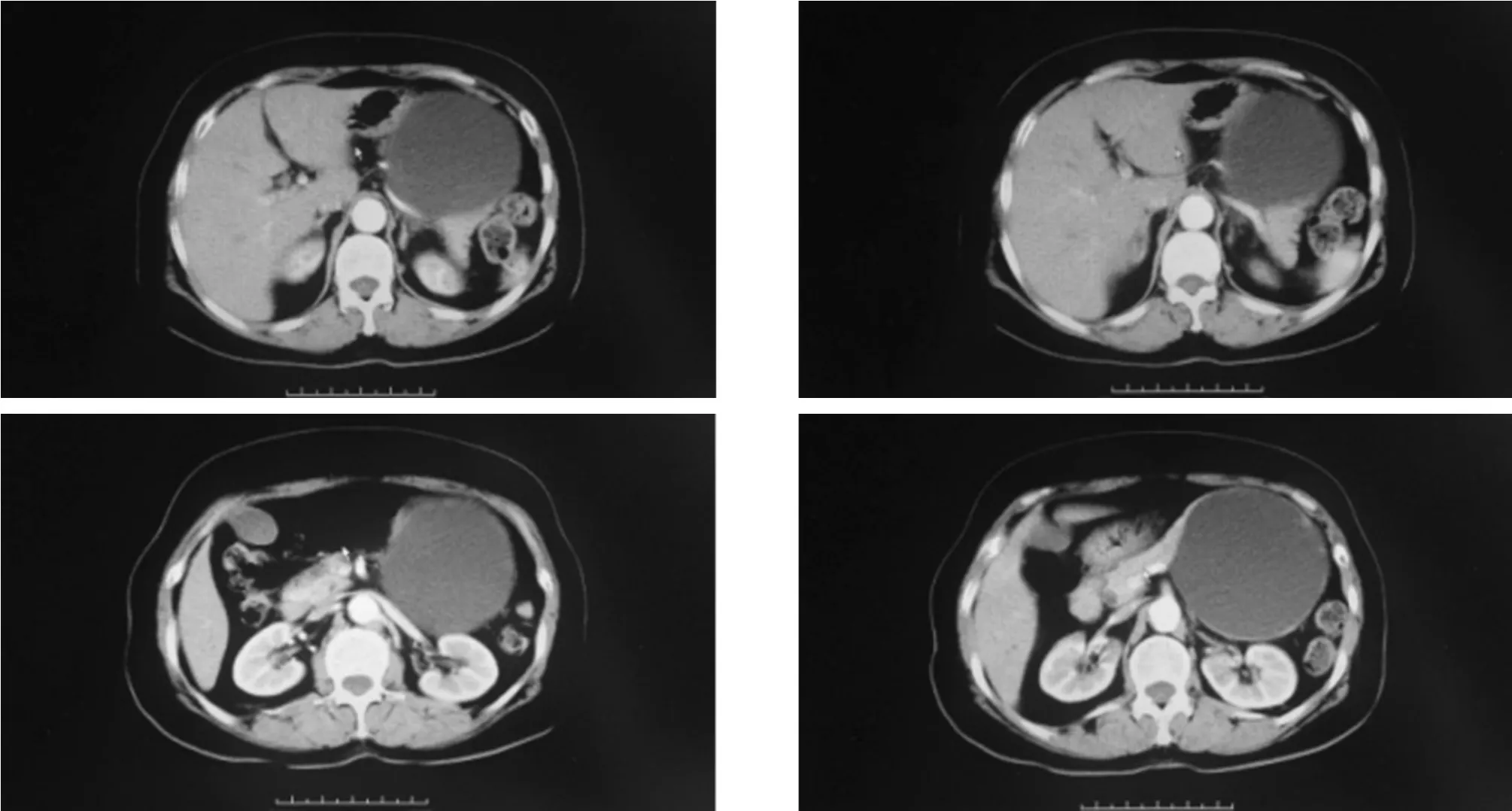
图1 一例巨大胰腺体尾部肿瘤术前影像学资料
1.2 术前准备及手术设备 术前常规检查血常规、血型、生化、输血前四项、凝血系列、肿瘤系列、胸片、心电图、肝胆胰脾B超、上腹部CT及增强CT,术前禁饮食,置胃管、尿管,肠道准备,术前半小时应用抗生素。
1.3 手术方法 手术用品包括常规腹腔镜手术设备、腹腔镜配套用光源、气腹装置、奥林巴斯超声刀、强生一次性直线切割闭合器、合成夹、血管缝线等。均采用气管插管全身麻醉。患者取平卧位,采用五孔法施术,脐上10 mm作观察孔,分别于左、右锁骨中线肋缘下8 cm处穿刺10 mm Trocar作主操作孔,左右腋前线肋缘下2 cm处穿刺5 mm Trocar作副操作孔。探查腹腔,用超声刀离断胃结肠韧带,于胃后方找到胰腺,进一步明确胰腺体尾部肿瘤位置,必要时腹腔镜下B超定位肿瘤位置,于肿瘤胰腺近端距离至少2 cm作预切线,在预切线处胰腺下方分离胰腺与后腹膜可见胰腺系膜,找到并解剖出胰腺正后方的脾静脉及胰腺后上方的脾动脉。用超声刀仔细分离胰腺后方与脾脏动静脉间的间隙,做一隧道,如遇胰后与脾静脉交通的小静脉仔细分离后可用Hem-o-lok夹闭后离断,隧道贯通后用红尿管顺所做隧道将胰腺悬吊,胰腺近端用强生一次性直线切割闭合器横断胰腺,向脾脏方面牵拉胰腺远端,用超声刀将胰腺远端自脾脏动静脉上及胰腺系膜区游离,胰腺后面的与脾静脉交通的小静脉及脾动脉发出的胰腺供血动脉通过Hem-o-lok夹闭后离断,向左游离,直至脾门处,注意勿撕破脾脏包膜,胰腺体尾部及肿瘤组织完整切除,胰腺断面放置腹腔引流管。
1.4 术后处理 术后继续禁饮食,持续性胃肠减压,预防感染,抑酸、抑酶、支持对症治疗,术后第3天复查血尿淀粉酶及腹腔引流管淀粉酶正常后可进低脂流食,逐渐过渡至正常饮食。
1.5 术后随访 通过电话及门诊随访方式,随访3~12个月,3例患者无远期并发症发生,复查均未见肿瘤复发。
2 结果
3例患者中1例61岁女性患者CT示胰体尾肿瘤11.8 cm,手术时间220 min,术中出血量210 ml,术中因肿瘤较大,剥离胰体尾过程中囊肿破溃,术后形成3 cm大的包裹性积液,保守治疗2周后积液消失。1例42岁女性患者胰体尾肿瘤5.2 cm,术中游离胰体尾过程中脾静脉破损,腹腔镜下修补脾静脉破损处止血,手术成功,术后无并发症发生,72 h后恢复进食。1例54岁女性患者,胰体尾肿瘤直径4.8 cm,术中无特殊情况。3例患者术中均未输血,术后常规抗感染,抑酸、抑酶、支持、对症治疗。术后第1天下地活动,术后第3天复查血尿淀粉酶,腹腔引流液淀粉酶正常后进低脂流食,逐渐过渡至正常饮食,均未发生严重并发症。形成腹腔包裹性积液患者术后住院治疗2周后积液消失,治愈出院,另2例患者术后1周治愈出院。3例患者病理均为胰腺粘液性囊腺瘤。3例患者术后随访3~12个月,均未见远期并发症发生,亦未见胰腺囊肿复发。
3 讨论
随着腹腔镜外科广泛应用于外科各个领域,腹腔镜下胰体尾切除术得到了广大外科学者的重视,在大的肝胆胰诊疗中心,已成为治疗胰腺体尾部良性肿瘤、低度恶性肿瘤的标准化治疗[3],甚至有一些医疗中心,对于部分胰腺体尾部恶性肿瘤亦采用腹腔镜胰体尾切除术治疗[4]。目前腹腔镜下保留脾脏的胰体尾切除术常分为Kimura法与Warshaw法两种,Kimura法保留了脾脏的动静脉,Warshaw法保留脾脏,但切断了脾脏的动静脉,依靠脾胃韧带间交通支保证脾脏血供,因为Warshaw法常需保证脾胃韧带间有足够的交通支提供脾脏血供,临床上常不够可靠。Warshaw法术后脾梗塞及区域性门脉高压的发生率明显高于Kimura手术[5],更多的学者在保留脾脏时即使手术难度有所增加,也更加愿意选择较保险的 Kimura法[6],腹腔镜下保留脾脏的Kimura法切除胰体尾手术目前被基本认可的适应证为[7]:(1)具有一定复发性而不能单纯摘除的胰体尾部良性肿瘤;(2)交界性及低度恶性的胰体尾部肿瘤,未侵犯或转移到其他组织,无重要血管侵犯者。由于恶性病灶常侵犯脾血管或脾门,并引起局部无菌性炎症及区域性门脉高压,技术层面也很难施行保脾手术。而胰体尾部良性或低度恶性的病灶是施行保脾手术的最佳适应证[8]。国内展翰翔教授所著的《腹腔镜保留脾脏胰体尾切除术:手术策略与技巧》建议腔镜技术熟练,并具备相应开放保留脾脏胰体尾切除手术经验的团队可施行此术式。因我们所在的基层医院积累了一定的开腹手术病例,因此我们选择合适病例,并循序渐进开展此术式[9]。
3.1 分离胰体尾的技巧 直线切割闭合器横断胰腺后,远端胰体尾自脾脏动静脉上的剥离是Kimura法的关键点与困难点。脾动脉发出的胰腺体尾部的供血动脉常因与脾动脉有一定间隙而更容易离断。脾静脉常走行于胰腺背面深部,约34%的脾静脉甚至出现在胰体尾背面被胰体尾组织包裹[10],切除胰体尾后观察会发现脾静脉所在的压迹。并且胰腺体尾部背面会出现类似于肝短静脉的与脾静脉交通的短静脉,给保留脾静脉切除胰腺体尾部造成了一定困扰,这就要求我们术中应仔细轻柔的找到相应的解剖层次,在 Gerota筋膜浅层分离胰腺体尾部背侧。对于脾静脉在胰腺体尾部形成压迹的病例,我们常需要分离出脾静脉并用血管吊带悬吊牵拉,保证一定的张力,便于分离胰体尾部。胰腺体尾部背侧发出到脾静脉的短小静脉均需用Hem-o-lok夹闭后离断,切不可抱有侥幸心理,超声刀离断常会导致术后不可控制的出血,总而言之,术中应保证对手术的控制,需要中转开腹时绝不可犹豫,及早中转开腹,以保证手术顺利,安全完成。
3.2 术中出血的处理 术中出血是腹腔镜手术失败的一大诱因,对于腹腔镜保留脾脏的胰体尾切除术,在脾脏的血管上进行相应操作,术中出现出血的风险较其他操作更大,一旦术中发生脾脏血管出血,常较为汹涌,术野明显受到干扰。腹腔镜操作不够熟练的外科医生可能会慌张的用纱布压迫并中转开腹。实际上对于多数术中出血是可在腹腔镜下精准操作控制的,发生脾脏动脉术中出血,我们用吸引器压迫出血处近端脾动脉,同时轻轻间断吸引出血,以保证视野清晰,但又不至于吸取腹腔内CO2气体造成腹腔内空间消失,这时我们用5-0小针血管线精准缝合出血点,可达到良好的止血效果。脾脏静脉的出血,我们可通过相同的方法用吸引器压迫脾静脉出血处远端,并轻轻间断吸引出血保证视野清晰,用血管线缝合脾静脉破损处。本组3例患者中1例发生术中脾静脉破损大出血,我们即通过这种方法从容缝合脾静脉破损处,顺利止血(图2)。以上两种方法如果还不能达到止血目的,可用吸引器吸引显露视野的同时用两把无损伤钳夹闭出血点两端,从容缝合出血点。最后还是要强调,当发生可能危及患者生命的大出血时应及时选择Warshaw法、联合脾脏切除的胰体尾切除术,甚至中转开腹。
3.3 预防术后胰瘘 有报道称目前腹腔镜下胰腺体尾部切除术后胰瘘的发生率为5%~12%[11]。胰瘘虽然无任何方法可彻底杜绝,但有研究证明通过强生一次性直线切割闭合器离断胰腺组胰瘘的发生率要低于手工离断缝合胰腺断端组(9.7%vs.13.2%)[12]。对于直线切割闭合器离断胰腺后,胰腺近端断面是否需要再缝合加固目前仍有两种观点,一种认为需要用Prolene线加固缝合,不仅可达到止血目的,同时还可达到预防胰瘘发生的目的[13];另一种观点认为强生的一次性直线切割闭合器三层钉已可达到充分防止胰瘘的目的,再次用血管线加固缝合胰腺断端会画蛇添足,不但延长了手术时间,而且因为胰腺颈体部顺血管线针眼会有小的胰管胰液漏出,且血管线加固会影响胰腺断端血供,增加术后胰瘘的发生率。胰腺断面如果有出血常可通过双极电凝达到止血目的[14]。有学者认为应用直线切割闭合器离断胰腺时缓慢持续性逐渐闭合胰腺预切定线处亦可降低术后胰瘘的发生率[15]。我们更认可后一种观点,本组3例患者均通过强生一次性直线切割闭合器离断胰腺,胰腺断端未再加固处理,术后均未发生胰瘘(图3)。
我们的初步研究表明腹腔镜下保留脾脏的胰体尾切除术是安全、可行的,患者创伤小,术后康复快,已得患者及术者的认可,不但目前已在大的肝胆胰医疗中心广泛开展,在基层医院也如雨后春笋般开展起来。在笔者看来,腹腔镜外科仅是传统手工外科到机器人外科全面发展的过渡阶段,随着达芬奇机器人技术、远程精准医疗的进一步推广,此手术会得到更进一步的应用与发展。
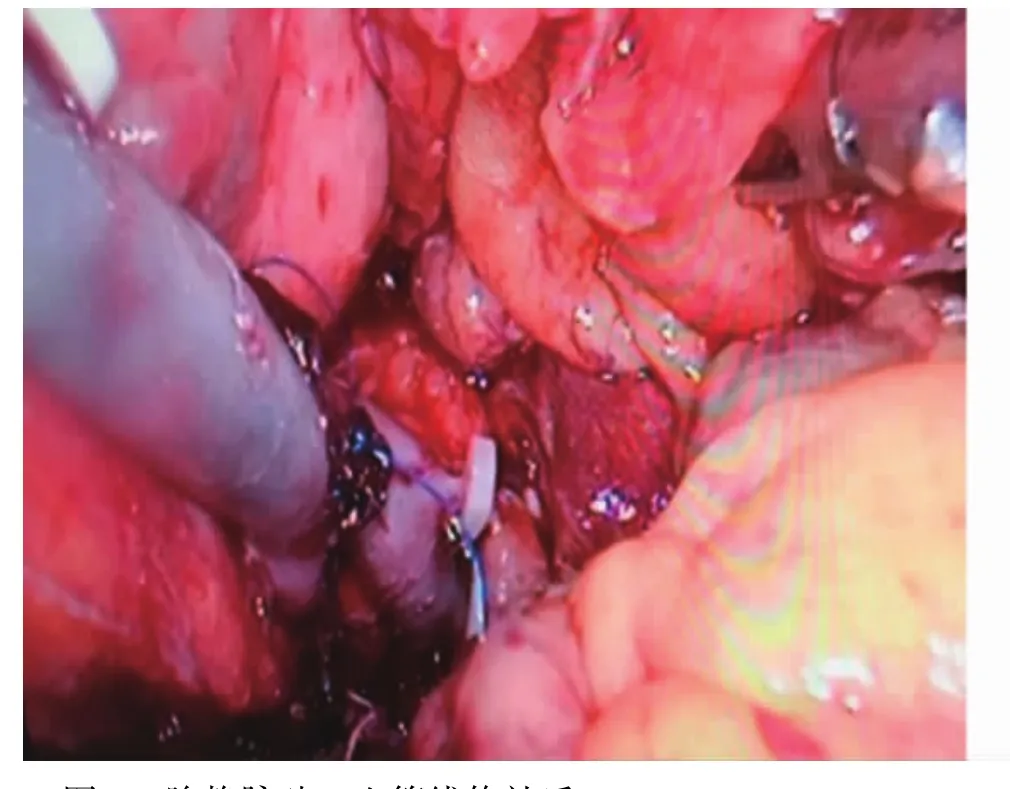
图2 脾静脉破口血管线修补后
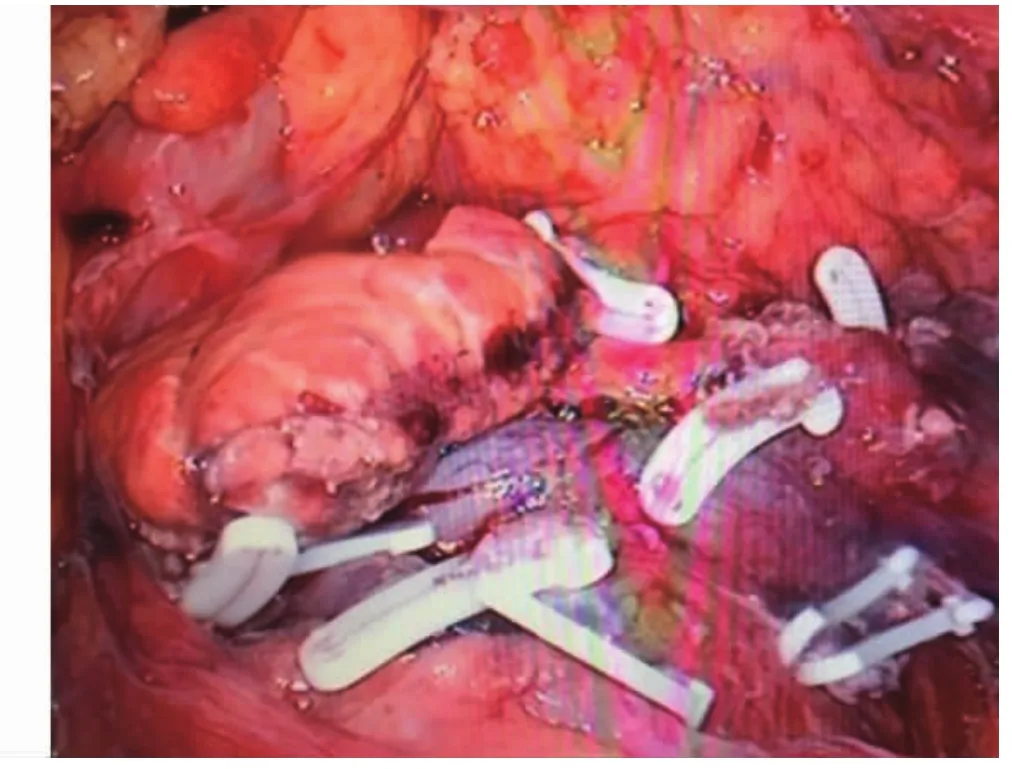
图3 胰腺断面未再加固缝合
[1] 洪德飞,彭淑牖.腹腔镜肝胆胰脾外科手术操作与技巧[M].北京:人民卫生出版社,2008:132-138.
[2] Abu Hilal M,Jain G,Kasasbeh F,et al.Laparoscopic distal pancreatectomy:critical analysis of preliminary experience from a tertiary referral centre[J].Surg Endosc,2009,23(12):2743-2747.
[3] Abu Hilal M,Hamdan M,Di Fabio F,et al.Laparoscopic versus open distal pancreatectomy:a clinical and cost-effectiveness study[J].Surg Endosc,2012,26(6):1670-1674.
[4] Cuschieri A,Jakimowicz JJ,van Spreeuwel J.Laparoscopic distal 70%pancreatectomy and splenectomy for chronic pancreatitis[J].Ann Surg,1996,223(3):280-285.
[5] Warshaw AL.Distal pancreatectomy with preservation of the spleen[J].J Hepatobiliary Pancreat Sci,2010,17(6):808-812.
[6] Kimura W,Yano M,Sugawara S,et al.Spleen-preserving distal pancreatectomy with conservation of the splenic artery and vein: techniques and its significance[J].J Hepatobiliary Pancreat Sci,2010,17(6):813-823.
[7] Kooby DA,Gillespie T,Bentrem D,et al.Left-sided pancreatectomy:a multicenter comparison of laparoscopic and open approaches[J].Ann Surg,2008,248(3):438-446.
[8] Jean-Philippe Adam,Alexandre Jacquin,Christophe Laurent,et al.Laparoscopic spleen-preserving distal pancreatectomy:splenic vessel preservation compared with the Warshaw technique[J].JAMA Surg,2013,148(3):246-252.
[9] 展翰翔,王磊,胡三元.腹腔镜保留脾脏胰体尾切除术:手术策略与技巧[J].腹腔镜外科杂志,2016,21(1):1-3.
[10] Kneuertz PJ,Patel SH,Chu CK,et al.Laparoscopic distal pancreatectomy:trends and lessons learned through an 11-year experience[J].J Am Coll Surg,2012,215(2):167-176.
[11] Jusoh AC,Ammori BJ.Laparoscopic versus open distal pancreatectomy:a systematic review of comparative studies[J].Surg Endosc,2012,26(4):904-913.
[12] Baker MS,Bentrem DJ,Ujiki MB,et al.A prospective single institution comparison of peri-operative outcomes for laparoscopic and open distal pancreatectomy[J].Surgery,2009,146(4):635-643.
[13] Bassi C,Dervenis C,Butturini G,et al.Postoperative pancreatic fistula:an international study group(ISGPF)definition[J].Surgery,2005,138(1):8-13.
[14] Jayaraman S,Gonen M,Brennan MF,et al.Laparoscopic distal pancreatectomy:evolution of a technique at a single institution[J].J Am Coll Surg,2010,211(4):503-509.
[15] Matsushima H,Kuroki T,Adachi T,et al.Laparoscopic spleen-preserving distal pancreatectomy with and without splenic vessel preservation:the role of the Warshaw procedure[J].Pancreatology,2014,14(6):530-535.
Clinical study of laparoscopic spleen-preserving distal pancreatectomy
JIN Shang-bo,LIU Yi-min,YAN Yao-sheng,et al.Department of Hepatobiliary Surgery,Baoji People's Hospital,Baoji 721000,China
Objective:To investigate the clinical value of laparoscopic spleen-preserving distal pancreatectomy.Methods:A retrospective analysis was made on the clinical data of 3 patients who suffered from tumor in body and tail of pancreas and underwent laparoscopic spleen-preserving distal pancreatectomy from Nov.2014 to Apr.2016.Results:All 3 cases were successfully performed laparoscopic spleen-preserving distal pancreatectomy with conservation of the splenic artery and vein,and no case was converted to laparotomy.The splenic vein was torn in 1 case,laparoscopic suturing was used for the splenic vein sutures,and bleeding was successfully stopped.The patient ate liquid food at 72 h after operation.1 patient suffered from large cystic tumor,the cystic fluid overflowed during the operation,postoperative encapsulated effusion with diameter of 3 cm formed at pancreatic resection area.The encapsulated effusion was absorbed in 2 weeks after operation.Postoperative pathological examination all revealed the diagnosis of pancreatic mucinous cystadenoma.No long-term complications or recurrence were found during the follow-up of 3 to 12 months.Conclusions:Laparoscopic spleenpreserving distal pancreatectomy has become a safe and feasible choice of the treatment of benign tumor at body and tail of the pancreas,because of its mini-trauma,rapid recovery,in many large medical centers laparoscopic spleen-preserving distal pancreatectomy has become the general treatment of benign tumor at pancreatic body and tail.At present,laparoscopic spleen-preserving distal pancreatectomy can be carried out in primary hospital.However,surgeons who perform this operation should strictly abide by the principle of gradual implementation.
Pancreatic neoplasms;Laparoscopy;Spleen-preserving distal pancreatectomy;Laparoscopy
R736.7
A
1009-6612(2017)02-0115-04
10.13499/j.cnki.fqjwkzz.2017.02.115
2016-05-15)
(英文编辑:杨庆芸)
1通讯作者:郭智华,E-mail:jinshangbo@163.com
金上博(1983—)男,回族,陕西省宝鸡市人民医院普通外科(肝胆)主治医师,主要从事肝胆胰方面的研究。
