HPLC-DAD波长转换法同时测定糖肾清毒颗粒中7种活性成分的含量Δ
2017-03-29石征蓉杨秀青谷江华袁强华成都中医药大学药学院成都60075成都中医药大学附属医院成都6007
石征蓉,杨秀青,谷江华,袁强华,宋 英#(.成都中医药大学药学院,成都 60075;.成都中医药大学附属医院,成都 6007)
HPLC-DAD波长转换法同时测定糖肾清毒颗粒中7种活性成分的含量Δ
石征蓉1*,杨秀青1,谷江华1,袁强华2,宋 英2#(1.成都中医药大学药学院,成都 610075;2.成都中医药大学附属医院,成都 610072)
目的:建立同时测定糖肾清毒颗粒中7种活性成分含量的方法。方法:采用高效液相色谱法。色谱柱为岛津Inert Sustain C18,流动相为乙腈-0.1%磷酸溶液(梯度洗脱),流速为1.0 mL/min,检测波长为327 nm(绿原酸和咖啡酸)、280 nm(黄芩苷)、228 nm(牛蒡苷)、276 nm(汉黄芩苷、黄芩素和汉黄芩素),柱温为35℃,进样量为10 μL。结果:绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素和汉黄芩素检测质量浓度线性范围分别为4.830~154.6 μg/mL(r=0.999 8)、0.750~24.1 μg/mL(r=0.999 7)、22.859~731.5 μg/mL(r=0.999 7)、8.491~271.7 μg/mL(r=0.999 3)、2.471~79.0 μg/mL(r=0.999 6)、6.656~213.0 μg/mL(r=0.999 4)、2.756~88.2 μg/mL(r=0.999 8);精密性、稳定性、重复性的RSD<2.0%;加样回收率分别为96.86%~100.82%(RSD=1.46%,n=6)、98.79%~101.09%(RSD=0.93%,n=6)、97.57%~101.51%(RSD=1.37%,n=6)、97.76%~99.63%(RSD=0.77%,n=6)、97.99%~100.12%(RSD=0.76%,n=6)、96.54%~101.07%(RSD=1.87%,n=6)、96.60%~99.59%(RSD=1.14%,n=6)。结论:该方法操作简便,精密度、稳定性、重复性好,可用于糖肾清毒颗粒中7种活性成分含量的同时测定。
高效液相色谱法;糖肾清毒颗粒;黄芩;黄酮类;牛蒡苷;含量测定
近年来,糖尿病微血管病变导致的糖尿病肾病(Diabetic nephrothy,DN)发病人群逐年扩大,成为攻克糖尿病的难题[1]。中医认为,内生热毒损伤肾络是此病发生发展的主要病机[2-3],采用清热解毒类药物配伍组方可有效防治DN[4]。糖肾清毒颗粒为成都中医药大学附属医院在研的中药六类新药,由黄芩、牛蒡子、蒲公英和豨莶草组合而成,具有清热解毒、活血通络之功效,主治DN热毒证。药效研究表明,黄芩中的黄酮类成分能减少蛋白尿,增加尿肌酐排泄量,其作用机制可能与提高肾脏的抗氧化功能有关[5];蒲公英和豨莶草中的有机酸类成分具有抗炎、抗病毒、抗菌、抗过氧化损伤等作用[6-7];牛蒡子主要含木脂素类成分牛蒡苷,对DN患者具有改善临床症状、减少尿蛋白及微量白蛋白的作用[8],上述3类成分为本方治疗DN的药效物质基础。成分定量研究方面,有文献报道同时测定该制剂中的黄酮类和有机酸类含量[9]。本试验采用高效液相色谱(HPLC)-DAD波长切换法首次对方中的绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素和汉黄芩素同时进行定量分析,并进行方法学验证,以期为糖肾清毒颗粒的质量控制提供一种合理可行的方法。
1 材料
1.1 仪器
1260型HPLC仪,包括四元泵、DAD检测器、在线脱气装置、OpenlAB工作站(美国Agilent公司);BP211D型十万分之一电子分析天平(瑞士Mettler-Toledo公司);AS20500BD型超声清洁仪(天津奥特赛恩斯仪器有限公司,功率:250 W,频率:50 kHz);CXP-500A型高速多功能粉碎机(上海市晟喜制药机械有限公司)。
1.2 药品与试剂
糖肾清毒颗粒(成都中医药大学附属医院自制,批号:20160513、20160515、20160519,规格:30 g/袋);黄芩苷对照品(批号:110715-201318,纯度:93.3%)、汉黄芩苷对照品(批号:112002-201501,纯度:98.8%)、黄芩素对照品(批号:111595-201306,纯度:97.8%)、汉黄芩素对照品(批号:111514-200403,纯度:98.4%)、绿原酸对照品(批号:110753-201313,纯度:96.6%)、咖啡酸对照品(批号:110885-200102,纯度:100%)、牛蒡苷对照品(批号:110819-201007,纯度:95.4%)均购自中国食品药品检定研究院;乙腈、甲醇为色谱纯,磷酸为分析纯,水为蒸馏水。
1.3 饮片
黄芩(批号:1408018)、蒲公英(批号:1407093)、牛蒡子(批号:1408046)、豨莶草(批号:1208022)均购自四川新荷花中药饮片股份有限公司。
2 方法与结果
2.1 色谱条件
色谱柱:Inert Sustain C18(250 mm×4.6 mm,5 μm);流动相:乙腈(A)-0.1%磷酸溶液(B),梯度洗脱(洗脱程序见表1);流速:1.0 mL/min;检测波长:327 nm(0~38 min,绿原酸和咖啡酸)、280 nm(38~48 min,黄芩苷)、228 nm(48~56 min,牛蒡苷)、276 nm(56~80 min,汉黄芩苷、黄芩素和汉黄芩素);柱温:35℃;进样量:10 μL。
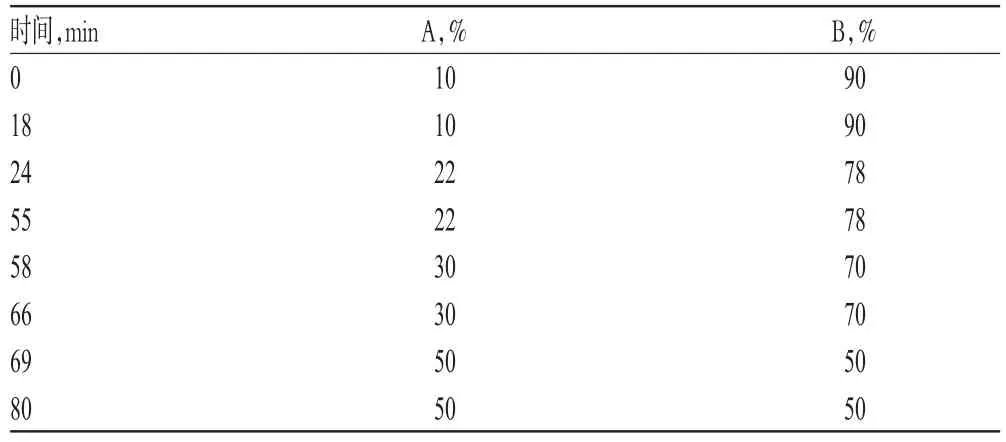
表1 梯度洗脱程序Tab 1 Gradient elution program
2.2 溶液的制备
2.2.1 混合对照品溶液 精密称取绿原酸对照品4.79 mg、咖啡酸对照品2.50 mg、黄芩苷对照品9.81 mg、牛蒡苷对照品7.12 mg、汉黄芩苷对照品2.00 mg、黄芩素对照品6.44 mg、汉黄芩素对照品5.64 mg,分别置于10 mL量瓶中,加50%甲醇溶液溶解并定容,制成单一对照品贮备液;分别精密吸取黄芩苷对照品贮备液2 mL,另外6种对照品溶液各1 mL,置于同一10 mL量瓶中,加50%甲醇溶液定容,摇匀,制成绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素、汉黄芩素质量浓度分别为0.047 9、0.025 0、0.196 0、0.071 2、0.020 0、0.064 4、0.056 4 mg/mL的混合对照品溶液。
2.2.2 供试品溶液 精密称取样品0.6 g,置于100 mL量瓶中,加50%甲醇溶液定容,超声处理30 min,冷却,加50%甲醇溶液定容,摇匀,滤过,取续滤液,即得。
2.2.3 阴性对照溶液 按糖肾清毒颗粒处方和工艺分别制备缺黄芩、牛蒡子、蒲公英的单一阴性样品,并按“2.2.2”项下方法制成单一阴性对照溶液。
2.2.4 空白对照溶液 以流动相作为空白对照溶液。
2.2.5 药材样品溶液 取蒲公英、豨莶草饮片各适量,分别按2015年版《中国药典》(一部)供试品溶液制备方法制成单一药材样品溶液[10]。
2.3 系统适用性试验与专属性试验
取“2.2”项下混合对照品溶液、供试品溶液、阴性对照溶液、药材样品溶液各适量,按“2.1”项下色谱条件进样测定,记录色谱,详见图1。结果,理论板数以绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素、汉黄芩素峰计均>3 000;分离度>1.5,各成分互不干扰。缺黄芩、牛蒡子的阴性对照色谱图在相应位置上无干扰,因此本方法对黄芩苷、牛蒡苷、黄芩素和汉黄芩素专属性良好;缺蒲公英的阴性对照色谱图在相应位置上出现了色谱峰,为作进一步分析本试验参考相关文献[11]测定处方的药材成分;蒲公英和豨莶草药材均含有绿原酸与咖啡酸,牛蒡子药材含有绿原酸,因此绿原酸和咖啡酸不具有专属性。
2.4 线性关系考察与检测限、定量限考察
精密称取各待测对照品适量,加甲醇制成绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素和汉黄芩素质量浓度分别为154.56、24.00、731.47、271.69、79.04、212.99、88.19 μg/mL的混合对照品贮备液,倍比稀释,制成系列混合对照品溶液。精密量取上述系列混合对照品溶液各10 μL,按“2.1”项下色谱条件进样测定,记录峰面积。以待测成分质量浓度(x,μg/mL)为横坐标、峰面积(y)为纵坐标进行线性回归,得绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素和汉黄芩素回归方程与线性范围,详见表2。取上述系列混合对照品溶液,倍比稀释,按“2.1”项下色谱条件进样测定,当信噪比为10∶1时,得定量限;当信噪比为3∶1时,得检测限,详见表2。
2.5 精密度试验

图1 高效液相色谱图Fig 1 HPLC chromatograms

表2 回归方程、线性范围、检测限与定量限Tab 2 Regression equation,linear range,limits and quantification of detection
2.5.1 日内精密度 取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件一日内连续进样测定6次,记录峰面积。结果,绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素和汉黄芩素峰面积的RSD分别为0.82%、1.77%、0.91%、0.97%、0.75%、1.14%、0.45%(n=6),表明日内精密度良好。
2.5.2 日间精密度 取“2.2.1”项下混合对照品溶液适量,按“2.1”项下色谱条件分别于第1、3、7日连续进样测定6次,记录峰面积。结果,绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素和汉黄芩素峰面积的RSD分别为0.90%、1.50%、1.10%、0.79%、0.95%、1.30%、0.82%(n=6),表明仪器日间精密度良好。
2.6 稳定性试验
取“2.2.2”项下供试品溶液(批号:20160513)适量,分别于室温下放置0、3、6、12、18、24 h时按“2.1”项下色谱条件进样测定,记录峰面积。结果,绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素和汉黄芩素峰面积的RSD分别为0.88%、1.70%、1.23%、0.89%、0.43%、1.10%、1.54%(n=6),表明供试品溶液在室温放置24 h内基本稳定。
2.7 重复性试验
精密称取同一批样品(批号:20160513)适量,按“2.2.2”项下方法制备供试品溶液,共6份,再按“2.1”项下色谱条件进样测定,记录峰面积并计算含量。结果,绿原酸、咖啡酸、黄芩苷、牛蒡苷、汉黄芩苷、黄芩素和汉黄芩素的平均含量分别为0.84、0.13、35.07、16.52、、9.41、3.66、1.18 mg/g,RSD分别为0.80%、1.90%、0.64%、1.20%、0.29%、0.71%、0.92%(n=6),表明本方法重复性良好。
2.8 加样回收率试验
取已知含量样品(批号:20160513)适量,共6份,每份0.4 g,分别加入一定质量的待测成分对照品,按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算加样回收率,结果见表3。
2.9 样品含量测定
取3批样品各适量,分别按“2.2.2”项下方法制备供试品溶液,再按“2.1”项下色谱条件进样测定,记录峰面积并计算样品含量,结果见表4。
3 讨论
3.1 检测指标的选择
中医治疗疾病强调用药的系统性和整体性,复方疗效的发挥是方中多种成分协同作用的结果,仅用某一个成分或一类成分作为评价指标无法全面反映该制剂的质量优劣,所以有必要建立多指标成分的含量测定方法。2015年版《中国药典》通过测定黄芩苷的含量,对黄芩药材及相关制剂进行质量控制,而现代研究表明,黄芩药材中其他黄酮类成分(汉黄芩苷、黄芩素、汉黄芩素等)同样具有黄芩的部分药理活性。在制剂工艺中,黄酮类成分可能受温度、pH等影响相互转化,黄芩苷降解为其苷元黄芩素。另外,阚红玉等[12]检测发现,黄芩药材中黄酮类成分因产地不同含量差异巨大,这进一步说明了单一用黄芩苷作为药材及其制剂的质量控制指标具有片面性。牛蒡苷属于木脂素类化合物,是牛蒡子治疗DN的主要活性成分[13]。蒲公英和豨莶草均含有绿原酸和咖啡酸,是本方清热解毒的有效成分,通过测量有机酸的含量有助于制剂整体质量控制。综上所述,7种成分均与本方主治功能相符,因此笔者选取它们作为质量控制指标。由于绿原酸和咖啡酸没有专属性,本课题在质量标准研究时,采用药材对照方法确定制剂中是否含蒲公英和豨莶草。
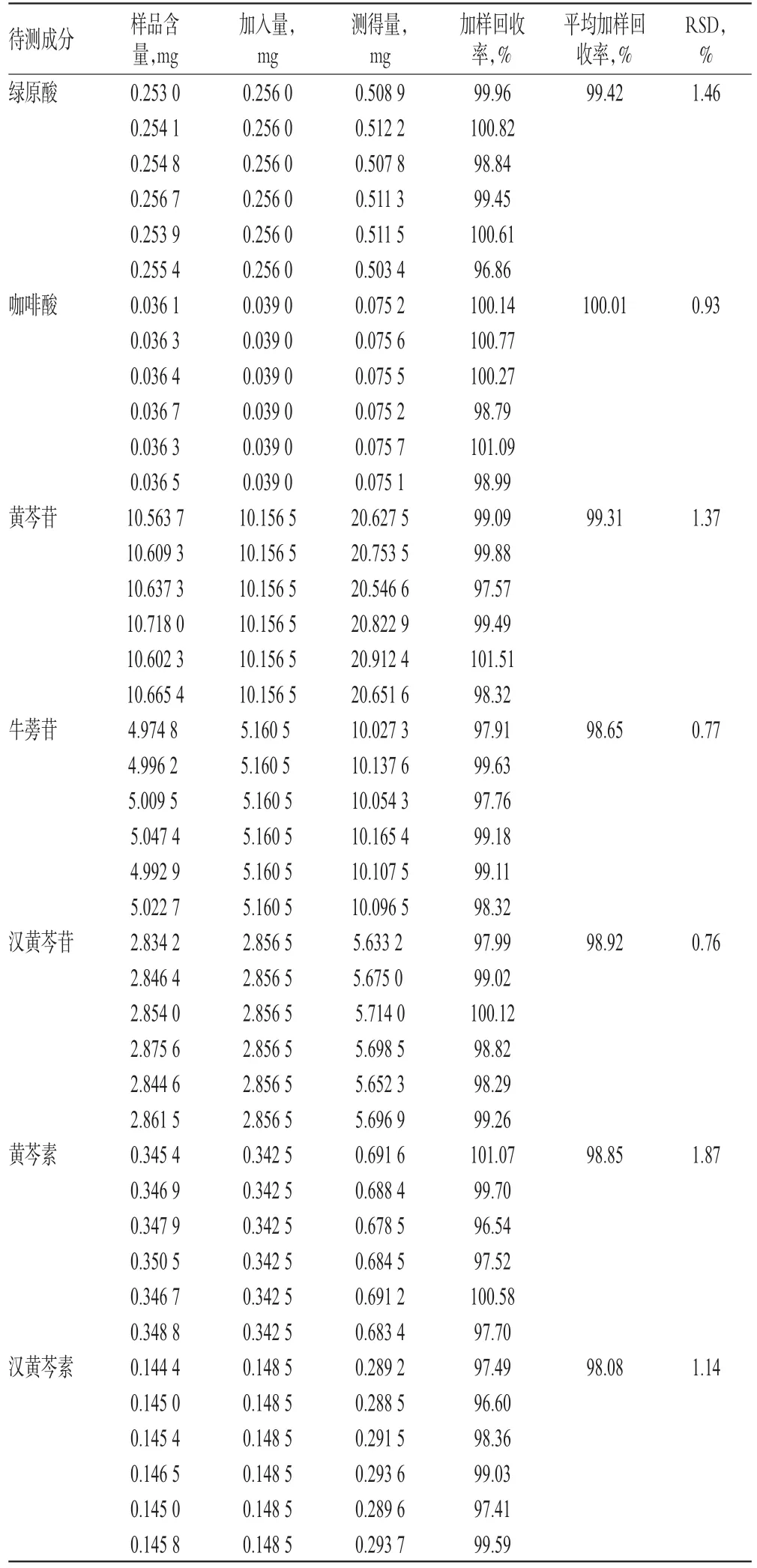
表3 加样回收率试验结果(n=6)Tab 3 Results of recovery test(n=6)
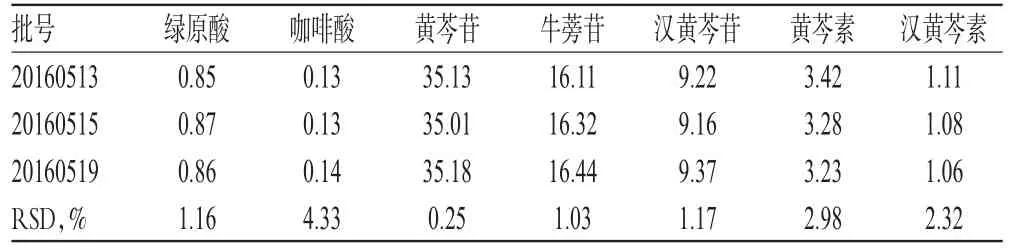
表4 样品含量测定结果(n=3,mg/g)Tab 4 Results of contents determination of samples(n=3,mg/g)
3.2 样品制备方法的选择
制备样品时,笔者分别以甲醇、75%甲醇溶液和50%甲醇溶液为提取溶剂,按“2.2.2”项下方法制备供试品溶液,结果50%甲醇溶液提取效率高,色谱峰对称性好,故选择50%甲醇溶液作为提取溶剂;以50%甲醇溶液作为提取溶剂,分别考察超声时间20、30、40 min对7种活性成分的提取效果,结果发现超声30 min和超声40 min成分含量差异不大,超声20 min成分却未提取完全,因此选择超声30 min为提取时间。
3.3 色谱条件的选择
笔者分别考察了25、30、35、40℃的柱温对7种活性成分分离度的影响,结果发现柱温越高,黄芩苷和牛蒡苷的分离度越好,但考虑到温度过高,影响绿原酸的含量,因此最终选定35℃的柱温。考察流动相时,本试验前期对不同比例的甲醇-水、乙腈-水和乙腈-磷酸溶液流动相系统进行考察,结果发现在流动相中加入一定比例的磷酸有助于提高待测成分峰与杂质峰之间的分离度;笔者还对磷酸的用量进行了考察,结果表明,当流动相的pH在2.0~2.5时,待测成分牛蒡苷含量最高,这与0.1%磷酸溶液的pH相符,因此选择乙腈-0.1%磷酸溶液组成的流动相系统进行梯度洗脱。选择检测波长时,采用DAD检测器在200~400 nm范围内对供试品溶液进行了全波长扫描,结果显示绿原酸和咖啡酸在327 nm、黄芩苷在280 nm、牛蒡苷在228 nm和汉黄芩苷、汉黄芩素、黄芩素在276 nm波长处紫外吸收较优,同时各待测成分互不干扰,因此选择波长切换法测定7个待测成分,且各成分响应信号稳定。
综上所述,本方法操作简便,精密度、稳定性、重复性好,可用于糖肾清毒颗粒中7种活性成分含量的同时测定。
[1] 谢席胜,艾娜,王宝福,等.糖尿病肾病流行病学研究进展[J].中国中西医结合肾病杂志,2013,14(10):937-940.
[2] 生生,李敬林,依秋霞,等.毒损肾络致糖尿病肾病的发病机制浅析[J].辽宁中医杂志,2015,42(5):957-960.
[3] 柴可夫,沈祥峰.通络法在糖尿病肾病治疗中的运用[J].中华中医药学刊,2007,25(8):1553-1555.
[4] 仝小林,周强,赵林华,等.糖尿病肾病的中医辨治经验[J].中华中医药杂志,2014,29(1):144-147.
[5] 郑勇凤,王佳婧,傅超美,等.黄芩的化学成分与药理作用研究进展[J].中成药,2016,33(1):141-144.
[6] 谢沈阳,杨晓源,丁章贵,等.蒲公英的化学成分及其药理作用[J].天然产物研究与开发,2012,24(Suppl):141-151.
[7] 滕天立,徐世芳,陈峰阳,等.中药豨莶草的化学成分及其药理作用研究进展[J].中国现代应用药学,2015,32(2):250-260.
[8] 张磊,李蓬秋,张学军,等.牛蒡子粉治疗糖尿病肾病的临床研究[J].四川医学,2011,32(5):656-658.
[9] 车坷科,杨帆,邓开英.HPLC法测定养阴合剂中黄芩苷的含量[J].中国药房,2016,27(24):3410-3412.
[10] 国家药典委员会.中华人民共和国药典:二部[S].2015年版.北京:中国医药科技出版社,2015:352-353、368.
[11] 袁强华,宋英,朱璐璐,等.感甦合剂的质量控制[J].中国医院药学杂志,2013,33(2):111-114.
[12] 阚红玉,宋殿荣,王跃飞,等.HPLC法同时测定黄芩中5种黄酮类成分的含量[J].中国药房,2010,21(11):1016-1019.
[13] 祁佳,张宇锋,朱建,等.牛蒡子治疗糖尿病肾病的系统评价[J].河北医药,2016,38(1):34-38.
Simultaneous Determination of 7 Active Constituents in Tangshen Qingdu Granule by HPLC-DAD
SHI Zhengrong1,YANG Xiuqing1,GU Jianghua1,YUAN Qianghua2,SONG Ying2(1.School of Pharmacy,Chengdu University of Traditional Chinese Medicine,Chengdu 610075,China;2.The Affiliated Hospital of Chengdu University of Traditional Chinese Medicine,Chengdu 610072,China)
OBJECTIVE:To establish a method for the simultaneous determination of 7 active constituents in Tangshen qingdu granule.METHODS:HPLC was performed on the column of SHIMADZU Inert Sustain C18with mobile phase of acetonitrile-0.1%phosphoric acid at a flow rate of 1.0 mL/min,detection wavelength was 327 nm for chlorogenic acid and caffeic acid,280 nm for baicalin,228 nm for arctiin and 276 nm for wogonoside,baicalein and wogonin,column temperature was 35℃,and injection volume was 10 μL.RESULTS:The linear range was 4.830-154.6 μg/mL for chlorogenic acid and(r=0.999 8),0.750-24.1 μg/mL for caffeic acid(r=0.999 7),22.859-731.5 μg/mL for baicalin(r=0.999 7),8.491-271.7 μg/mL for arctiin(r=0.999 3),2.471-79.0 μg/mL for wogonoside(r=0.999 6),6.656-213.0 μg/mL for baicalein(r=0.999 4)and 2.756-88.2 μg/mL for wogonin(r=0.999 8);RSDs of precision,stability and reproducibility tests were lower than 2.0%,recoveries were 96.86%-100.82%(RSD=1.46%,n=6),98.79%-101.09%(RSD=0.93%,n=6),97.57%-101.51%(RSD=1.37%,n=6),97.76%-99.63%(RSD=0.77%,n=6),97.99%-100.12%(RSD=0.76%,n=6),96.54%-101.07%(RSD=1.87%,n=6)and 96.60%-99.59%(RSD=1.14%,n=6).CONCLUSIONS:The method is simple with good precision,stability and reproducibilty,and can be used for the simultaneous determination of 7 active constituents in Tangshen qingdu granule.
HPLC;Tangshen qingdu granule;Baicalin;Flavonid;Arctiin;Content determination
R927.2
A
1001-0408(2017)06-0816-05
2016-08-23
2016-09-26)
(编辑:张 静)
四川省科技计划项目(No.2014SZ0140)
*硕士研究生。研究方向:中药新制剂、新工艺和新技术。E-mail:501560079@qq.com
#通信作者:教授,硕士生导师。研究方向:中药新制剂、新工艺和新技术。电话:028-87783251。E-mail:songying624@163.com
DOI10.6039/j.issn.1001-0408.2017.06.26
