人参皂苷对波动性高血糖大鼠肾脏Nrf2及NQO1表达的影响*
2017-03-29王丹黄琦
王 丹 黄 琦
1 浙江中医药大学 浙江 杭州 310053
2 浙江省中医院 浙江 杭州 310006
人参皂苷对波动性高血糖大鼠肾脏Nrf2及NQO1表达的影响*
王 丹1黄 琦2#
1 浙江中医药大学 浙江 杭州 310053
2 浙江省中医院 浙江 杭州 310006
目的:探讨人参皂苷对波动性高血糖大鼠肾脏转录因子NF-E2相关因子2(NF-E2-related factor2,Nr f2)及醌氧化还原酶1(quinone oxidoreductase l,NQO1)表达的影响及其机制。方法:将48只雄性SD大鼠随机分成正常对照组(NC组,n=8)和糖尿病模型组(n=40)。高脂饲料喂养糖尿病模型组大鼠2周后用小剂量链脲佐菌素(STZ)诱导建立糖尿病大鼠模型,之后随机分为稳定高糖组(SH组,n=8)和波动性高糖组(FH组,n=32),FH组错时注射葡萄糖、胰岛素制备血糖波动大鼠模型。2周后,将FH组随机分为4组,分别是低剂量组(LG组),中剂量组(MG组),高剂量组(HG组)及波动性高糖组(BG组),予人参皂苷低中高剂量(14、28、56mg/(kg·d))干预相对应的模型组8周。实验结束后切取肾脏组织,用western blot和RTPCR(Real-time Polymerase Chain Reaction)检测Nr f2和NQO1蛋白及mRNA表达。结果:与NC组相比,SH组Nr f2和NQO1的蛋白及mRNA的表达明显增加(P<0.05),与SH组相比,BG组Nr f2和NQO1的蛋白及mRNA的表达明显增加(P<0.05),与BG组相比,人参皂苷治疗组Nr f2和NQO1的蛋白及mRNA的表达明显增加(P<0.05)。结论:人参皂苷能够进一步促进波动性高糖状态下Nr f2及NQO1蛋白及mRNA表达,通过增加NQO1的含量,提高机体的抗氧化应激能力,保护波动性高血糖所致的肾脏损伤。
人参皂苷 波动性高血糖 转录因子NF-E2相关因子2 醌氧化还原酶1 氧化应激 大鼠
糖尿病肾脏病变是糖尿病患者常见的慢性微血管并发症,近年来研究发现,血糖波动与糖尿病血管并发症有着密切的关系[1],可能在糖尿病肾病中发挥了一定的作用。在生理状态下,机体内的神经内分泌系统可以正常调节空腹血糖及餐后血糖,使其维持在正常水平,而糖尿病患者由于胰岛素的缺乏或者分泌不足,血糖往往波动较大,与稳定性高血糖相比,波动性高血糖对糖尿病患者肾脏的危害性更大[2],但其导致的糖尿病肾病的发生机制尚不明确,但氧化应激似乎在肾脏损伤过程中起着重要作用。人参皂苷作为人参的提取物,可抗氧化及清除机体内自由基[3]。因此,它可能在治疗糖尿病肾病中起到一定作用。
转录因子NF-E2相关因子2(Nr f2)是一种核转录因子,它通过与应答元件(ARE)结合,激活下游各种细胞保护基因的转录,包括血红素加氧酶-1(HO-1),NQO1醌氧化还原酶1(NQO1),从而在细胞内发挥其抗氧化应激损伤作用[4]。研究表明,在糖尿病肾病的发病过程中,ARE/Nr f2通路的活性会增加[5]。因此,通过上调ARE/Nr f2信号通路,提高其下游抗氧化应激因子的表达,可能作为治疗糖尿病肾病的一种方法。本实验用人参皂苷对波动性高血糖所致肾脏损伤的大鼠进行干预,观察肾脏组织中Nr f2和NQO1的蛋白及基因的表达,旨在探讨人参皂苷对波动性高血糖所致的肾脏损伤的治疗作用及其保护机制,从而为人参皂苷的临床治疗提供依据。
1 材料与方法
1.1 主要试剂与仪器:人参皂苷粉末(浙江省中医院自制,制剂批准号:201308190);超短效胰岛素诺和锐(丹麦诺和锐);链尿佐菌素(Sigma公司);自制高脂饲料:蔗糖10%、蛋黄10%、猪油10%、胆固醇0.5%、基础饲料69.5%;NQO1和Nr f2引物(Takara公司);兔抗NQO1多克隆抗体和兔抗Nr f2多克隆抗体(CST公司);RT-PCR反应试剂盒(TaKaRa公司);Trizol裂解液(Invit rogen公司);血糖试纸及血糖仪(德国罗氏);Step one plus PCR仪(美国生物应用系统公司)。
1.2 动物分组及模型制备:6~8周龄SD雄性大鼠48只,体质量160~180g,由上海西普尔必凯实验动物有限公司提供[SCXK(沪)2008-0016],饲养于浙江中医药大学动物实验研究中心[SYXK(浙)2008-0115]。48只SD大鼠随机分为正常对照组(NC组)、稳定性高糖组(SH组)、波动性高糖组(BG组)、人参皂苷低剂量组(LG组)、人参皂苷中剂量组(MG组)、人参皂苷高剂量组(HG组),每组8只。除正常对照组使用正常饲料喂养外,其余各组均使用高脂饲料喂养2周后禁食不禁水16小时,用小剂量STZ 35mg/kg腹腔注射诱导建立糖尿病大鼠模型,造模1周后,禁食不禁水16h,测空腹血糖15~20mmol/L为模型制作成功。NC组给予腹腔注射生理盐水0.375g/(kg·d)体质量作为对照,SH组定时给予腹腔注射250g/L葡萄糖溶液0.375g/(kg·d)。BG组、LG组、MG组、HG组予腹腔注射250g/L葡萄糖溶液0.375g/(kg·d),错时30min后给予腹腔注射超短效胰岛素类似物诺和锐,造成一天中血糖值大幅度波动模型,使其血糖值在高血糖和低血糖间反复漂移,注射后30min测血糖,制作波动性高血糖模型,连续6周,血糖波动幅度>1SD为有效波动。LG组、MG组、HG组分别予人参皂苷(14、56mg/kg/d)灌胃,BG组予等量生理盐水灌胃8周作对照,每日2次。
1.3 标本采集:每周用血糖仪测尾尖血血糖,称其体质量,并计算水和食物的摄入量。至实验结束,大鼠禁食12小时,切取肾脏组织,放入液氮罐中保存,用于western blot及RT-PCR检测。
1.4 western blot检测NQO1和Nr f2蛋白表达水平:从液氮罐中取出肾脏组织,放入液氮预冷过的研钵中,加入蛋白酶抑制剂+裂解液(1∶100)适量,研磨至液体澄清;吸取全部液体放入离心管中,12000rpm,4℃,离心15min,提取细胞总蛋白;采用考马斯亮蓝法测定蛋白浓度;吸取蛋白样品,以60V电压电泳,当条带跑至分离胶和浓缩胶分界面时改为90V电泳,时间2~4h;PVDF转膜(250MA,2.5h);将PVDE膜浸于封闭液中,4℃封闭过夜;取出膜,与一抗接触,室温旋转孵育2~3h,用TBST冲洗3次,同样的方法二抗室温孵育1~2h后,TBST洗3次;加入ECL试剂,将PVDF膜放在Chemi Doc XRS上采集图像。以β-actin表达水平作为内参,目标蛋白与内参蛋白灰度值的对比表示蛋白的表达量。
1.5 RT-PCR检测NQO1和Nr f2mRNA表达:由基因库查的所需mRNA的核苷酸序列,PrimerPremier计算机软件辅助引物设计,引物由TakaRa公司设计并合成。, Nr f2上下游引物分别为:5’-TGTAGTGCGAGGAAGAGGTATGA-3′和5’-GGAGGGAAAGGAGAGGAAGG-3′,NQO1上下游引物分别为:5’-ATTGTGCTTGTGAGGGTGTTTC-3′和5’-CCCTTCCTGTCTTTTCTTCTCTCT-3′。从液氮中取出肾脏组织冰上迅速研碎后,用Trizol法提取总RNA;吸取1μl抽提的RNA在Nanodropl000上进行RNA浓度测定,用1%琼脂糖凝胶进行电泳,检测RNA的完整性;取RNA按照逆转录体系逆转录为cDNA;取cDNA 2μl及Nr f2和NQO1上下游引物各0.4μl,SYBRPremix Ex TaqTM(2×)10μl,Rox Reference Dye II(50×)0.4μl,灭菌双蒸水6.8μl(扩增条件为:95℃、5min,94℃、1min,57℃、1min,72℃、1min,32个循环后,72℃8min。2%琼脂糖凝胶中进行电泳,然后置于Bio-Rad Gel凝胶图像分析系统进行吸光度扫描分析,以GAPDH作为内参照,用目的基因的吸光度与GAPDH吸光度的比值分析目的基因的相对表达水平。)
1.6 统计学分析:采用SPSS17.0统计软件,多样本均数的两两比较采用单因素方差分析,如果方差齐采用LSD,方差不齐采用Tamhane'sT2。以P<0.05差异有显著性。
2 结果
2.1 人参皂苷对Nr f2和NQO1蛋白的表达:Western blot结果显示,与NC组相比,SH组NQO1和Nr f2蛋白表达增高(P<0.05);与SH组相比,BG组NQO1和Nr f2蛋白表达均明显增高(P<0.05);与BG组相比,LG、MG、HG组NQO1和Nr f2蛋白表达均明显增高(P<0.05),且随着人参皂苷浓度的增加,低、中、高剂量组NQO1及Nr f2蛋白表达明显增加(P<0.05)。(图1~2)
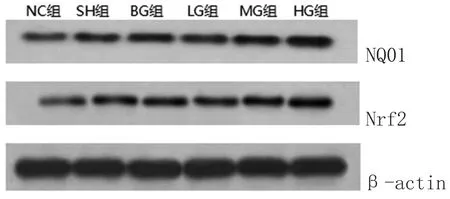
图1 各组大鼠肾脏Nr f2及NQO1蛋白的表达
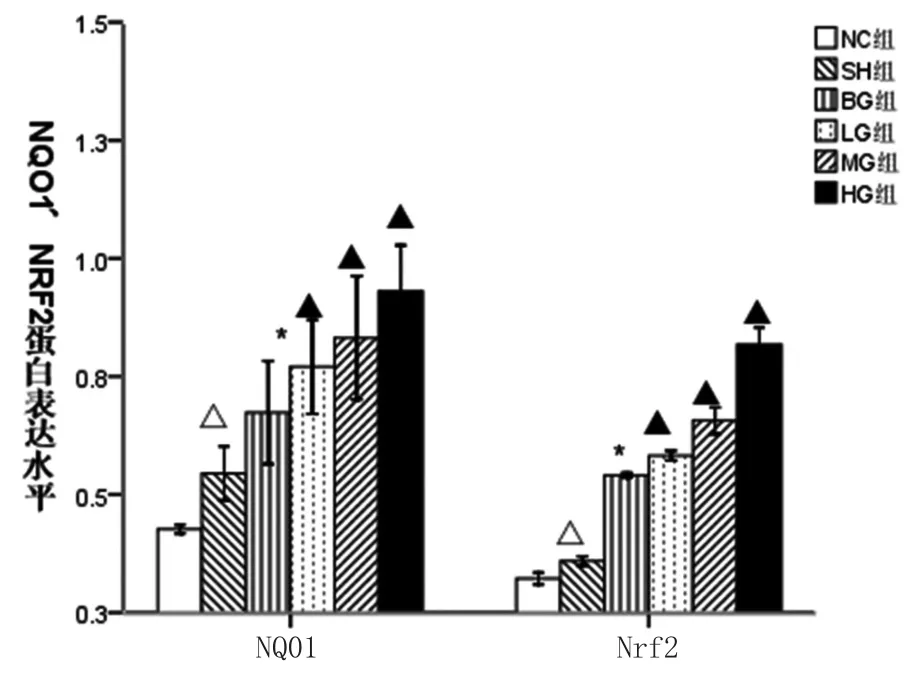
图2 各组大鼠肾脏Nr f2及NQO1蛋白的表达量
2.2 人参皂苷对NQO1和Nr f2 mRNA的表达:RT-PCR结果显示,与NC组相比,SH组NQO1和Nr f2 mRNA表达增高(P<0.05);与SH组相比,BG组NQO1和Nr f2 mRNA表达均明显增高(P<0.05);与BG组相比,LG、MG、HG组NQO1和Nr f2 mRNA表达均明显增高(P<0.05),且随着人参皂苷浓度的增加,低、中、高剂量组NQO1及Nr f2 mRNA表达明显增加(P<0.05)。见图3。
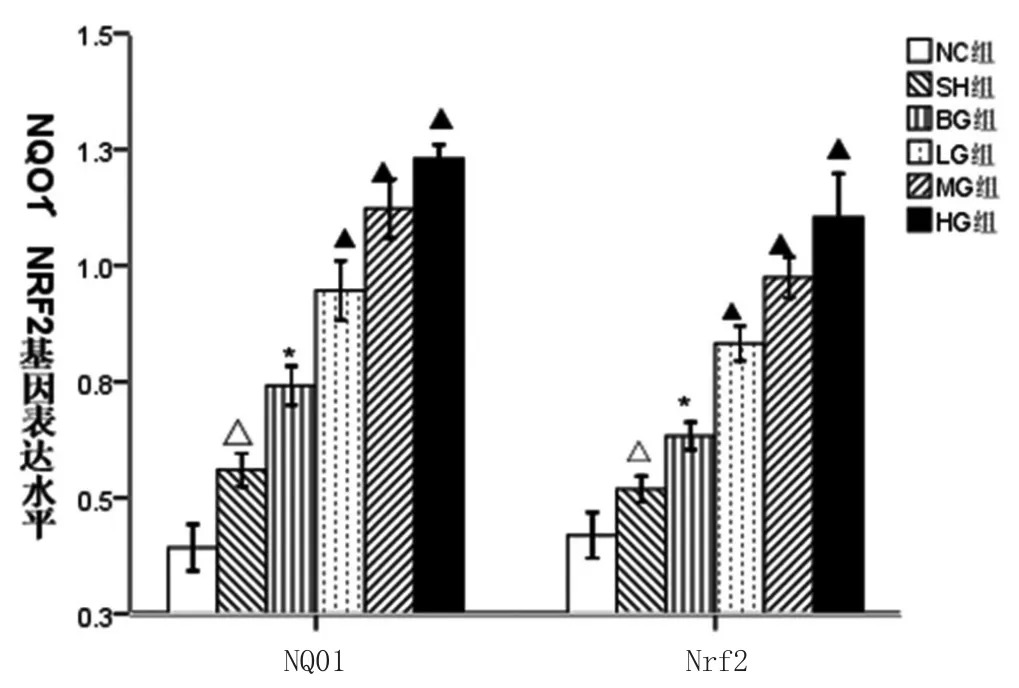
图3 各组大鼠肾脏NQO1及Nr f2基因的表达
3 讨论
本实验研究发现,SH组及BG组Nr f2和NQO1蛋白及mRNA表达明显高于NC组,但BG组Nr f2和NQO1蛋白及mRNA表达明显高于SH组,说明在生理状态下,其表达量较低,但在引起氧化应激的因素诱导下如高血糖可诱导其显著表达。虽然血糖升高刺激Nr f2和NQO1蛋白及mRNA表达增加,但其并不能对抗氧化应激对波动性高血糖大鼠肾脏的损伤。较稳定性高血糖,波动性高血糖的慢性并发症的发病率更高,而且出现的时间越早,慢性并发症越高,这与氧化应激对机体的损伤的增加有着密切的关系。
人参素有“百草之王”“神草”等称号,《神农本草经》把人参列为上品,味甘,微寒,“主补五脏、安精神、止惊悸、除邪气、明目、开心益智、久服轻身延年”功效。人参作为补虚中药的第一要药,治疗“消渴”早有记载。《伤寒论》第222条记载,“渴欲饮水,口干舌燥者,白虎加人参汤主之”。糖尿病属“消渴”范畴,其病机主要在于阴精亏虚,燥热偏胜,故以清热润燥、养阴生津为治疗大法。现代医学研究表明,人参皂苷是其主要活性成分,具有抗氧化、清除自由基、抑制肿瘤细胞增殖、提高免疫力、降血糖等作用[6-8]。在该实验中,人参皂苷有效上调了大鼠肾脏内Nr f2和NQO1的表达。Nr f2被认为在细胞内发挥重要的抗氧化应激作用,当受到外界氧化刺激时,Nr f2从Keap-1中解离,通过与ARE结合,并参与下游II相代谢酶基因和抗氧化基因的转录,促进NQO1的表达[9]。Nr f2的激活可以诱导NQO1的表达,抗氧化蛋白含量增加,提高了机体的抗氧化反应能力。
综上所述,NQO1是细胞内的一种保护性还原酶,可减少外界物质对细胞的氧化损伤,本文研究显示人参皂苷可通过上调Nr f2和NQO1基因和蛋白的表达,减缓波动性高糖所致氧化应激对肾脏功能的损害,其机制可能是通过激动Nr f2/ARE信号通路启动该抗氧化蛋白的转录和表达,在临床上,现有的治疗及研究很难从根源上彻底逆转胰岛β细胞功能的障碍和凋亡,而作为传统中药人参的提取物,人参皂苷发挥了其自身优势,为应用于糖尿病肾脏病变的临床治疗提供了实验室依据。
[1]Monnier L,Colet te C,Mas E,et al.Regulation of oxidative st ress by glycaemic cont rol:evidence for an independent inhibitory ef fect of insulin therapy[J]. Diabetologia,2010,53(3):562-571.
[2]Ge QM,Dong Y,Zhang HM,et al.Ef fects of intermittent high glucose on oxidative st ress in endothel ial cel ls[J].Acta Diabetologica,2010,47(1):97-103.
[3]杨秋娅,李晓宇,刘皋林.人参皂苷Rb1的药理作用研究进展[J].中国药学杂志,2013,48(15):1233-1237.
[4]Park JS,Jung JS,Jeong YH,et al.Antioxidant mechanism of isof lavone metabol ites in hydrogen peroxidestimulated rat primary ast rocytes:critical role of hemeoxygenase-1 and NQO1 expression[J].Neurochem, 2011,119(5):909-919.
[5]Uruno A,Yagishita Y,Yamamoto M.The Keap1-Nr f2 system and diabetes mel l itus[J].Archives of Biochemistry and Biophysics,2015,566(1):76-84.
[6]孟凡丽,苏晓田,郑毅男.人参皂苷Rb3对糖尿病模型小鼠的降血糖和抗氧化作用[J].华南农业大学学报,2013,34 (4):553-557.
[7]谢海龙,都晓伟,王立娟.中药皂苷类成分防治糖尿病的药理研究进展[J].中医药学报,2006,34(6):45-47.
[8]张娟,杨汝春,俞东容,等.人参皂苷Rg1对尿蛋白诱导的肾小管上皮细胞凋亡的影响[J].浙江中医杂志,2013,48(7):484-486.
[9]Park JS,Jung JS,Jeong YH,et al.Antioxidant mechanism of isof lavone metabol ites in hydrogen peroxidestimulated rat primary ast rocytes:critical role of hemeoxygenase-1 and NQO1 expression[J].Neurochem, 2011,119(5):909-919.
2016-07-06
浙江省中医药科技计划项目人参皂苷通过Nr f2/ARE信号通路干预波动性高糖致内皮细胞凋亡的作用机制研究,编号:2014ZA045
# 通讯作者:黄 琦,E-mail:hq871201@163.com
