类硫锂二次电池中锂离子浓度变化及锂枝晶生长研究
2017-03-28张洪涛张泽森
张洪涛, 张泽森
(1.湖北工业大学纳米电子技术与微系统实验室,武汉,430068; 2.湖北工业大学电气与电子工程学院,武汉,430068;3.武汉楚能电子有限公司,武汉,430068)
1 前言
硫锂电池的能量密度达到2600Wh/kg, 与其它锂二次电池相比,如磷酸铁锂-碳电池、钛酸锂-碳电池和聚合物-碳电池,在能量密度和功率密度方面具有明显的优势,是下一代锂二次电池,可以广泛用于电动汽车和储能领域。然而,尽管采用硫与碳混合烧制成复合正极,可以大大提升其电池寿命[1],但锂金属作为负极,其产生锂枝晶导致正负极短路引起的安全性一直是人们关心的问题。到目前为止,尚未见到对这一问题的深入讨论。磷酸铁锂-石墨二次电池中作为负极活性材料,石墨所嵌入的锂离子的含量超过了它所承受的范围,多余的锂离子就会和负极中穿梭而来的电子结合,在碳负极表面上开始沉积(deposition)。而对于要形成锂枝晶,一个必要的条件就是,负极的表面是不平整的(roughness),锂沉积在隔膜和负极的接触部位,生长的方向是沿着从负极→隔膜的走向,因此反应发生的位置是在负极与电解液的界面上[2]。同理,Yamaki 等人认为在负极表面SEI膜下应力分布不均产生锂枝晶生长[3,4]。本文以其锂离子与金属锂原子于电解液中离子化与原子化的相互转换的微观电化学机理讨论这个问题。感谢锂离子电池的发明者,这个问题的解决,可以带活一大批类硫锂二次电池,从而可能抛弃现有磷酸铁锂(或三元锂材料)-碳二次电池电池、铅酸蓄二次电池等制备工艺产生的环境污染并改善能源结构、提升能源效率,推动电动汽车和清洁能源技术的发展。
2 硫锂电池中锂金属生长条件
在类锂硫电池循环过程中发生的电化学反应是氧化-还原反应。电池释放能量,是放电过程,失去一个电子,使金属锂原子氧化为锂离子,从金属片上剥落,进入非水电解液,迁移到正极周围,嵌入活性材料的晶格中。充电过程中外部电源施加电能量给电池,正极发生还原反应,处于正极材料结构空位上的锂离子得到电子,还原为锂原子,进入非水电解液,迁移到锂金属负极周围,在上面生长形成锂金属。负极端化学反应如下:
Li++ e-= Li
类硫-锂二次电池以硫和锂分别构成二次电池的正负极。以1.0 M LiPF6/(PC+DMC)(1∶1)电解液混合聚碳酸酯等的非水电解液,隔膜为Celgard构成电池。在循环动力学的电化学条件下,考察其锂离子与锂原子在氧化还原反应中的相互转化过程中锂离子浓度的变化,由此推断锂枝晶的生长条件。
设计电压窗口在3.5V~0.3V,充放电电流0.3mA/cm2。可以看到第一次循环容量放电比容量为760mAh/g,充电比容量为740mAh/g,库伦效率在97.4%。在10个循环后容量衰减,放电容量为90mAh/g,充电容量70mAh/g。电池进入电极碎裂粉化状态,电池不能工作。锂离子还原电位在2.06V,实测其容量衰减曲线为渐变小。这里要考查每一次循环过程电解液中锂离子浓度的变化。显然,随着容量减小,嵌入正极材料中的锂离子浓度降低,使溶液中的锂离子浓度逐渐增加,这部分锂离子使溶液过饱和。
经过计算,在10次循环以内,每次循环电解液中锂离子比上次循环平均浓度上升0.35%;在11~30次,浓度平均上升0.87%;在30次以后上升的平均浓度达到2.4%,并不断增长,这样,在电解液中夺取电子还原为锂原子,可产生结晶状态。锂离子电池出现热扩散风险骤然增加。如图1 所示。这一结果意味着每一次循环过程正极材料嵌入锂离子的浓度(这里暂定义为正极固体中锂离子嵌入量用浓度表示)在逐步下降,而电解液中的锂离子浓度在逐步增加,达到临界过饱和,这会提供锂原子结晶为固体枝晶的条件。
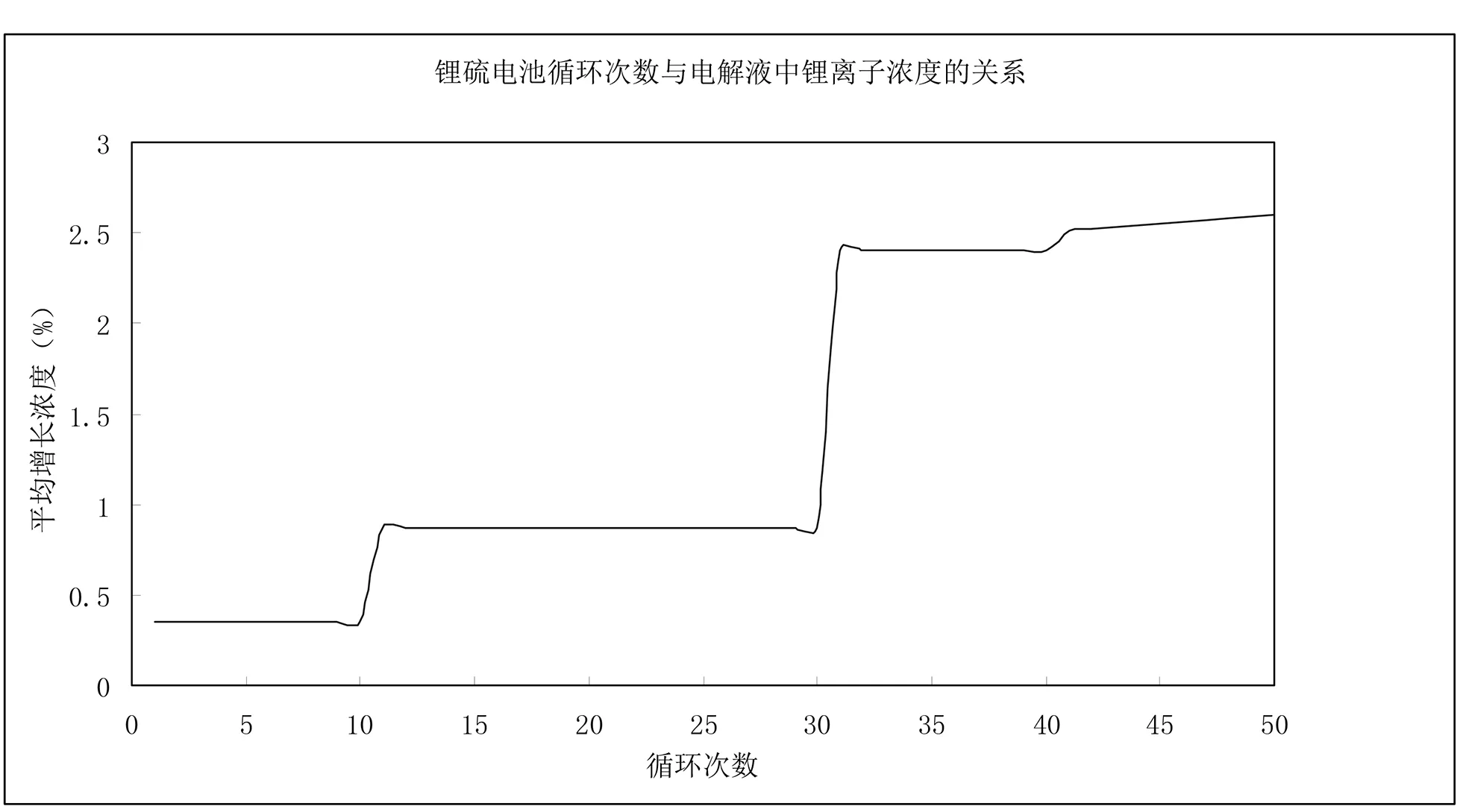
图1 类锂硫电池循环次数与电解液中锂离子浓度的关系
这一阶段每一次循环正极材料嵌入锂离子浓度将会降低,溶液中转化为锂原子的量在不断增加,出现锂枝晶的生长[5]。
锂原子浸出模型,它指锂离子在电化学环境下锂离子还原成锂原子的过程中在一定的浓度下可以生长为金属晶体的能力[1-13]。这个过程取决于电池中电化学环境体系、氧化还原电位以及过饱和浓度。
其实这类电池中一般情况下都会产生锂离子还原为锂原子和原子氧化为离子的动态的平衡变化。放电过程发生氧化作用,金属锂变成锂离子进入溶液,在电场作用下,锂离子迁移到正极,嵌入到正极材料的晶格中;而充电过程发生还原作用,锂离子脱出晶格到电解液中,并在外界电场作用下,迁移到负极周围,得到电子成为锂原子;在金属键的作用下成为金属晶体的一部分。在理想的电池电化学体系中,这是一个平衡过程,金属自我的嵌合力,使之保持脱锂原子的量等于嵌入金属锂中的锂原子的量,不破坏脱掉金属又补充到锂片层的机制。
然而由于电池中绝大部分电极材料的容量随循环周期而衰减,导致锂离子浓度在循环过程中电池电解液中不断积累,产生过饱和,锂原子浸出量多于前一循环周期氧化锂原子的量。在电池稳定的环境中,锂片表面具有一定的粗糙度,锂原子过度浸出,故而锂原子在这些凸点产生显著的金属晶体生长现象。这一现象体现为枝晶生长[3]。这一生长现象可能产生过长的针状体,刺穿隔膜,导致电池正负电极短路,这应该是锂金属-碳二次电池发生燃烧的潜在原因。
电极容量衰减过程可细分为三个状态,快速衰减,中速衰减和慢速衰减。显然,对于与锂片作为对电极构成二次电池的正极材料,像碳或者石墨烯这样的正极,容量衰减很快,产生枝晶的可能性大大增加;而中速衰减和慢速衰减,则不会快速产生枝晶的生长,这可能是聚合物锂电池可以较长时间不破坏的原因。
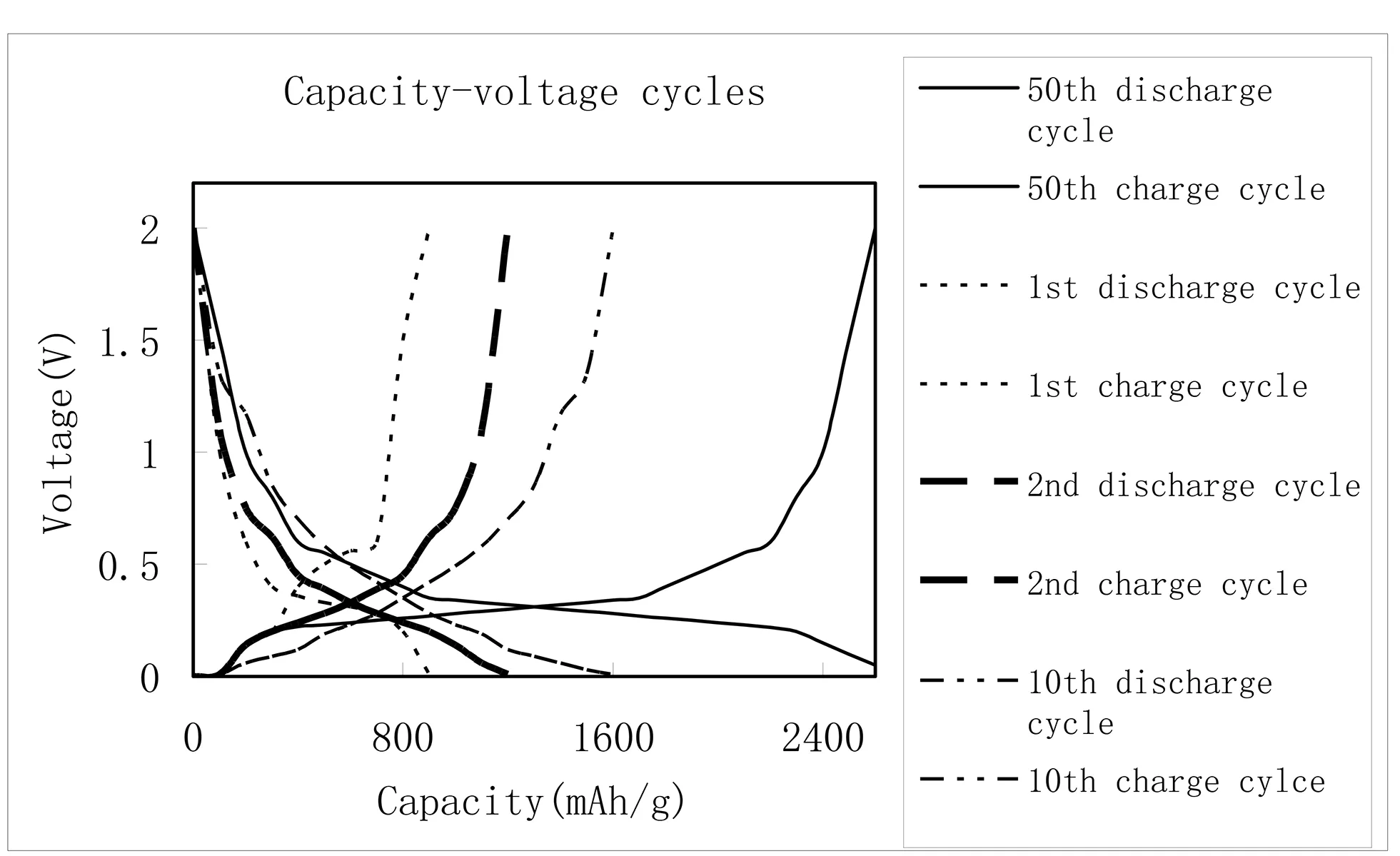
图2 纳米碳化硅薄膜-锂电池的循环特性图
同样是这种浓度的锂卤化物盐电解液,换一种电极,这种电极属于碳化硅薄膜电极。设计同样的窗口电压和电流,循环10次。首次放电容量达到900mAh/g,充电容量890mAh/g。第5次循环容量达到1200mAh/g。这个现象说明在这一阶段,每次循环都会有新的锂原子被氧化为锂离子进入电解液,相反过程不会产生结晶。从第六次循环开始直到第10次循环结束,其容量保持在1200mAh/g。如图2所示。由于每一次充放电过程锂离子浓度都在平衡范围,产生锂结晶为枝晶的前提不存在。
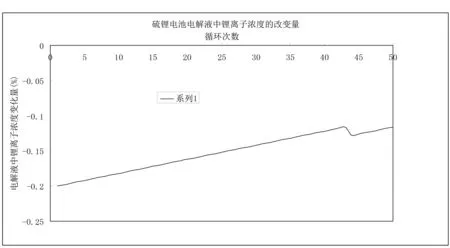
图3 类锂硫电池循环周期与锂离子浓度增量变化
由图3见,随着循环周期的增加,电池电解液中锂离子浓度呈现欠饱和状态。这意味着每一次循环都必须从锂片上剥离锂原子进入溶液,经电化学反应增加锂离子浓度,以满足正极材料不断增加的锂离子嵌入量需要。在达到平衡时,这一嵌入过程可以维持锂离子浓度的饱和或欠饱和状态。
3 实验及其锂枝晶生长模型
在电池电化学过程中,一般情况下发生锂离子慢过饱和、快过饱和、饱和以及不饱和等四种情况。所谓慢过饱和状态,是指锂离子充放电循环一定次数后随着容量损失,正极材料嵌入锂离子的浓度缓慢下降,留存在电池中的锂离子浓度逐渐增加,这样在达到一定的浓度临界值,会产生锂原子浸出效应,促进金属锂原子在锂金属片上的生长。这种情况轻易不能够生长金属锂枝晶。若环境是扰动的,可能会在金属锂片表面生长金属颗粒;若环境相对平静,有可能在金属锂表面生长锂枝晶。这是一个长期的缓慢发生的过程,这也正好说明了,一般这种电池在工作三年到五年后有的电池发生燃烧的原因。
快过饱和状态是指,随着循环周期的增加,正极材料很快地产生容量衰减,在电池体系中很快产生过高浓度的锂离子,高过临界值后,析出锂原子,溶液中锂以离子和原子状态共存,升高锂原子浓度,可能产生晶体金属的生长,形成锂枝晶。
饱和情况是指随着嵌脱锂反应的进行,电池在电化学循环过程中电解液溶液中锂离子浓度达到饱和状态,随着循环过程的进行,保持电解液中锂离子浓度饱和状态不变,这种情况产生锂离子浸出锂原子的量与锂原子氧化量是平衡的,不会产生锂枝晶的生长。
欠饱和状态是指,随着循环周期的增加,正极材料嵌入锂离子浓度增大,电解液中锂离子浓度在这一阶段处于不饱和状态,锂离子浸出为锂原子的量小于锂金属原子氧化为锂离子的量,因此,浸出的锂原子生长为枝晶的可能性很小。
4 类锂硫电池的前景
硫锂电池存在正极循环周期短的缺陷,但这一缺陷正在不断改进,如国内很多单位通过十几年的努力,已经初见成效,如国内中科院大连化物所、南京工业大学团队、复旦大学、南开大学、北京理工大学、防化院等[6-13];国外如加拿大滑铁卢大学、美国能源部橡树岭国家实验室、日本国家能源研究所等都做出了杰出的工作。现在的问题是与硫共存的硫碳架构中的碳是否有燃烧的可能性?这个问题希望国内的研究机构能够进一步回答。如果这个问题搞清楚,并明确答案,那么,未来硫锂电池的发展就会得到重大应用。
那么类硫锂电池的正极材料就会都得到大力的开发,将会使锂二次电池产生重大的实质性的发展。
5 结论
探讨锂硫二次电池体系中锂离子析出效应,并进一步分析锂枝晶的生长机理,推测有四种状态决定锂离子浓度析出成为原子的状态,即慢饱和、快饱和、饱和以及欠饱和等四种情况。这四种状态的前两种将有可能导致锂原子从溶液中析出,有可能产生枝晶生长。而后两种情况产生锂离子析出为锂原子的可能性很小,其生长为枝晶的可能性更小。
[1] Liang X, Hart C, Pang Q, Garsuch A, Weiss T,and Nazar L F.A Highly Efficient Polysulphide Mediator for Lithium Sulfur Batteries. Nature Communications,2015,6,5682.
[2] Cohen Y S, air Cohen A Y, Aurbach D. Micromorphological Studies of Lithium Electrodes in Alkyl Carbonate Solutions Using in Situ Atomic Force Microscopy.J.phys.chem. b,2000,104 (51) :12282-12291.
[3] Yamaki J,Tobishima S,Hayashi K,Saito K,Nemoto Y. A consideration of the morphology of electrochemically deposited lithium in an organic electrolyte. Journal of Power Sources,1998,74 (2) : 219-227.
[4] Zhang Y,Qian J,Xu W,Russell SM,Chen X. Dendrite-free lithium deposition with self-aligned nanorod structure.Nano Letters,2014,14(12):6889-96.
[5] Lu Y Y,yuan Z,and Lynden A.Archer.Stable lithium electrodeposition in liquid and nanoporous solid electrolytes. Nature. Vol.13,p961-969,DOI:10.1038/NMAT404,2014.10.
[6] 黄震雷,应皆荣,孙莞柠,姜长印,万春荣.锂离子电池含硫无机电极材料研究进展.稀有金属材料与工程.2010年1期:182-188.
[7] 赖超,李国春,叶世海,高学平*.高容量硫/碳复合正极材料.化学进展.2011,23 (0203):527-532.
[8] 梁宵,温兆银,刘宇.高性能锂硫电池材料研究进展. 化学进展.2011,23(0203): 520-526.
[9] 王维坤,余仲宝,苑克国,王安邦,杨裕生. 高比能锂硫电池关键材料的研究.化学进展.2011,23(0203): 540-547.
[10] 万文博,蒲薇华,艾德生.锂硫电池最新研究进展.化学进展.2013,25(11): 1830-1841.
[11] 苗力孝,王安邦等.含单质硫正极复合材料.化学进展.2013,25(11):1867-1875.
[12] 周兰,余爱水.锂硫电池硫碳复合正极材料研究现状及展望.电化学.2015,21(3):211-220.
[13] 刘颖佳,刘万生.中科院大连化物所锂硫电池工程技术取得新进展.[DB/OL]. http://news.sciencenet.cn/htmlnews/2015/9/326166.shtm,2015.