2016年高考反应热考查方式透析
2017-03-28陕西马亚楼
陕西 马亚楼
2016年高考反应热考查方式透析

能源问题是社会热点问题,是高考必考知识,其中与反应热有关的判断与计算是高考考查的重点,也是难点。现就2016年高考试题中反应热的有关题型分类例析如下:
题型一:反应热化学方程式的书写与正误判断
例1 (2016四川)工业上常用磷精矿[Ca5(PO4)3F]和硫酸反应制备磷酸。已知25℃,101 kPa时:
则Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式是___________。
解析:本题主要考查了反应热化学方程式的书写。由题给已知25℃,101 kPa时两反应分别编号①②,根据盖斯定律:①×5-②得Ca5(PO4)3F和硫酸反应生成磷酸的热化学方程式,ΔH=-418 kJ/mol。
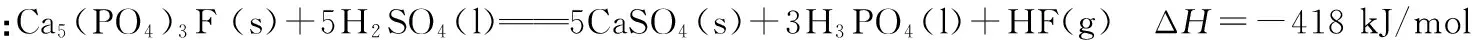
评注:本题考查了热化学方程式的书写,题目难度中等,注意掌握热化学方程式的书写原则,明确热化学方程式的叠加是解这类试题的关键。
题型二:反应中能量的判断
例2 (2016天津)氢气可用于制备H2O2。已知:
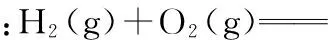
答案:<
题型三:已知热量求反应热
例3 (2016海南)油酸甘油酯(相对分子质量884)在体内代谢时可发生如下反应:
已知燃烧1 kg该化合物释放出热量3.8×104kJ,油酸甘油酯的燃烧热ΔH为
( )
A.3.8×104kJ·mol-1___________B. -3.8×104kJ·mol-1
C.3.4×104kJ·mol-1___________D. -3.4×104kJ·mol-1
解析:本题主要考查了由热量来计算反应热。燃烧热指的是燃烧1 mol可燃物生成稳定的氧化物所放出的热量。燃烧1 kg油酸甘油酯释放出热量3.8×104kJ,则 1 kg 该化合物的物质的量为1 000 g÷884 g/mol,则油酸甘油酯的燃烧热ΔH=-3.8×104kJ÷(1 000 g÷884 g/mol)=-3.4×104kJ·mol-1,故选D。
答案:D
评注:这类试题解题的关键是理解燃烧热的含义和燃烧物质的物质的量,利用公式q=Q÷n。
题型四:利用盖斯定律计算
例4 (2016新课标Ⅲ)已知下列反应:
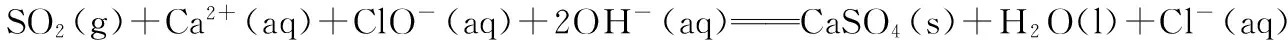
解析:将已知反应依次编号①②③,则根据盖斯定律可知①+②-③即得目标反应,即ΔH=ΔH1+ΔH2-ΔH3。
答案:ΔH1+ΔH2-ΔH3
题型五:已知燃烧热,计算反应热
例5 (2016浙江)催化还原CO2是解决温室效应及能源问题的重要手段之一,研究表明,在Cu/ZnO催化剂存在下,CO2和H2可发生两个平行反应,分别生成CH3OH和CO,反应的热化学方程式如下:
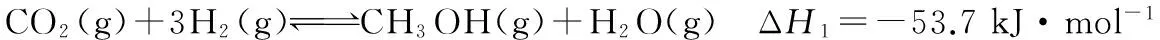

已知:①CO和H2的标准燃烧热分别为-283.0 kJ·mol-1和-285.8 kJ·mol-1
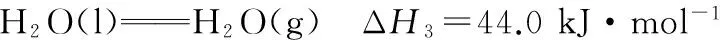
反应Ⅱ的ΔH2=___________ kJ·mol-1。
