黑豆蛋白的分级提取及黑豆花色苷的成分鉴定
2017-03-27祝振洲李书艺何静仁
江 甜,何 毅,祝振洲,李书艺,何静仁
(武汉轻工大学食品科学与工程学院,湖北 武汉 430023)
黑豆蛋白的分级提取及黑豆花色苷的成分鉴定
江 甜,何 毅,祝振洲,李书艺,何静仁*
(武汉轻工大学食品科学与工程学院,湖北 武汉 430023)
以黑豆为原料,添加不同浓度(0、5、10、15、20、25 mmol/L)的不同二价阳离子(Ca2+、Mg2+和Zn2+)分级提取黑豆蛋白,经冷冻干燥后用凯氏定氮法测得蛋白质量浓度,并对所得蛋白级分(7S、11S)的纯度和得率进行分析。结果表明,黑豆提取过程中所加入二价阳离子的类型及浓度显著影响7S和11S球蛋白的得率和纯度。利用综合平衡法,最终选定添加10 mmol/L的Mg2+分级提取黑豆球蛋白,得到7S蛋白纯度和得率分别为(86.29±3.25)%和(2.90±0.14)%,11S蛋白纯度和得率分别为(87.42±3.30)%和(9.11±0.28)%。用乙醇法提取黑豆花色苷,测得黑豆中总花色苷含量为(0.58±0.03)mg/g,总酚含量为(2.22±0.12)mg/g,对黑豆花色苷进行高效液相色谱-串联质谱分析,其组成成分为飞燕草色素-3-O-葡萄糖苷、矢车菊色素-3-O-葡萄糖苷、牵牛花色素-3-O-葡萄糖苷和锦葵花色素-3-O-葡萄糖苷。
黑豆;分级提取;7S球蛋白;11S球蛋白;花色苷
黑豆是豆科大豆属植物大豆的黑色种子。又名乌豆、橹豆、马料豆[1]。《本草纲目拾遗》中记载,长期食用黑豆可以强身健体、滋养肌肤、美容乌发,具有延缓衰老的功效[2]。黑豆含有丰富的蛋白质、维生素、脂肪、微量元素等营养成分[3],同时还含有黑豆多糖[4]、黑豆色素[5]和异黄酮[6]等多种生物活性物质。
研究表明,黑豆中蛋白质含量达到36%~40%,与普通大豆相比,其蛋白质含量较高,一直是人类食谱的重要组成部分,主要分为2S、7S、11S和15S四个组成部分[7-9]。在制备过程中,由于2S球蛋白组分的分子质量比较小,而且极易分散于水溶液中,在超速离心条件下也很难将其回收;而研究表明15S球蛋白是11S球蛋白的一种二聚体,它是一种大分子质量的蛋白组分,在离心时又很难溶于溶液而残留于豆渣中,不易被提取出来[10-11]。研究发现,黑豆蛋白具有较好的凝胶性和乳化性[12],还有吸油、保水、成膜等许多功能特性[13],其在肉制品、人造食品和调味制品等方面得到广泛应用[14-15]。除蛋白质以外,黑豆皮富含的花青素也具有重要功效,它是很好的抗氧化剂来源,能清除体内自由基[4,16],尤其是在胃的酸性环境中,抗氧化效果好,有养颜美容、增加肠胃蠕动的功效[17-18],因近年来合成色素使用受到限制,黑豆作为一种新型天然色素源也得到了重视[18]。
我国黑豆资源丰富,且在日常食用中消耗量不断增大,急需开发利用其价值。已有多位学者对黑豆的基本营养成分进行了比较分析[2-3,19],但对于黑豆主成分蛋白的分级和花色苷成分的鉴定研究较少。本实验旨在研究黑豆蛋白的分级提取和利用高效液相色谱-串联质谱(high performance liquid chromatography-tandem mass spectrometry,HPLC-MS/MS)法对黑豆花色苷的成分进行鉴定分析,为黑豆蛋白的高效提取及其开发利用提供理论依据,并且为黑豆花色苷的分离鉴定提供文献参考,使黑豆资源得到高效利用。
1 材料与方法
1.1 材料与试剂
黑小豆(江苏省建湖县) 江苏几百粒食品股份有限公司。
石油醚、NaOH、盐酸、乙醇、ZnCl2、MgCl2、CaCl2国药集团化学试剂有限公司;MD44-3.5透析袋(截留分子质量3 500 g/mol) 美国Viskase公司;没食子酸 美国Sigma公司;Folin-酚 上海荔达生物科技有限公司;所有试剂均为分析纯。
1.2 仪器与设备
FW-100粉粹机 北京市永光明医疗仪器有限公司;SB-5200DTN超声波清洗机 宁波新芝生物科技股份有限公司;STARTER 3100 pH计 奥豪斯仪器(上海)有限公司;AL204电子天平 梅特勒-拖利多仪器有限公司;Sorvall RC6 plus高速冷冻离心机、Evolution 220紫外-可见光分光光度计、Accela-LTQ XL HPLC-MS/MS联用仪 美国Thermo Fisher公司;ALPHA 2-4 LD plus冷冻干燥机 德国Christ公司;UDK159全自动凯氏定氮仪意大利Velp公司;R-3旋转蒸发仪 瑞士Büchi公司。
1.3 方法
1.3.1 黑豆蛋白的分析
1.3.1.1 黑豆球蛋白的提取及分级分离
黑豆粉碎后过80 目筛,用石油醚脱脂,得脱脂黑豆粉。豆粉以1∶15(g/mL)的比例加水后,用1 mol/L NaOH溶液调pH值至7.0,并在25 ℃条件下超声辅助提取1 h。所得分散相在4 000×g条件下离心20 min后弃去豆渣。所得上清液经G4砂芯漏斗抽滤后得到黑豆蛋白提取液。在25 ℃条件下,向蛋白提取液中加入3 mmol/L的Na2SO3溶液,再分别加入0~25 mmol/L的MgCl2、CaCl2、ZnCl2,用1 mol/L的盐酸调节pH值到5.8~6.0,搅拌10 min,在4 000×g条件下离心20 min,得到的沉淀为11S球蛋白。用1 mol/L的盐酸调节上清液pH值至4.2~4.5,再搅拌10 min。在4 000×g条件下离心20 min,弃去上清液,所得沉淀为7S球蛋白[20-21]。用截留分子质量为3 500 g/mol的透析袋透析除去其中的小分子物质。经过冷冻干燥后得到11S球蛋白与7S球蛋白样品。
1.3.1.2 黑豆球蛋白纯度的测定
参考GB 5009.5—2010《食品中蛋白质的测定》[22],采用凯氏定氮法测定。蛋白质含量即为蛋白纯度。
1.3.1.3 黑豆球蛋白得率的测定
根据各级分蛋白的质量、脱脂豆粉质量,按公式(1)计算各蛋白组分的得率。
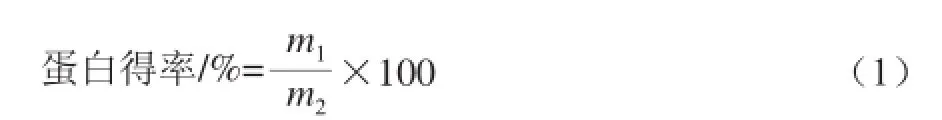
式中:m1为各级分蛋白质量/g;m2为脱脂豆粉质量/g。
1.3.2 花色苷的分析
1.3.2.1 花色苷的提取
取脱脂黑豆粉5.00 g按1∶20(g/mL)比例加入80%乙醇-盐酸溶液(pH 3),在温度为40 ℃、功率为240 W条件下超声辅助提取30 min,4 000 r/min离心20 min,经分离得到含有花色苷的上清液。重复1 次,合并上清液,于37 ℃条件下减压浓缩除去乙醇,定容到50 mL,备用。
1.3.2.2 总花色苷含量测定
采用pH示差法测定黑豆花色苷含量[23]。1 mL样品分别用pH 1.0缓冲液和pH 4.5缓冲液稀释,在最大吸收波长Amax和波长700 nm处测定吸光度。总花色苷含量按矢车菊素-3-O-葡萄糖苷计,按公式(2)计算总花色苷含量:
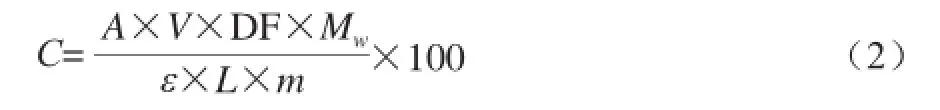
式中:C为总花色苷含量/(mg/g);A=(Amax-A700nm)pH1.0-(Amax-A700nm)pH4.5;V为提取液体积/mL;DF为稀释倍数;Mw为重均分子质量/(g/mol),Mw=449.2 g/mol;L为光程/cm;ε为摩尔消光系数/(L/(mol·cm)),以矢车菊素葡萄糖苷计,ε=26 900 L/(mol·cm);m为样品质量/g。
1.3.2.3 总酚含量测定
采用Folin-酚法测定黑豆花色苷总酚含量[24]。准确吸取1 mL于10 mL棕色容量瓶中,加5.0 mL蒸馏水,再加0.5 mL Folin-酚试剂,摇匀1 min后再加入1.5 mL质量分数20% Na2CO3溶液,用蒸馏水稀释至刻度,室温避光反应2 h后于波长760 nm处测定吸光度。以没食子酸为标准品绘制标准曲线,总酚含量以没食子酸含量计,单位为mg/g。得出标准曲线回归方程为Y=11.3X+0.019 2(R2=0.998 7)。
1.3.2.4 花色苷的纯化
浓缩的上清液加入乙酸乙酯萃取3 次,去除黑豆的弱极性杂质。选用已处理的AB-8大孔吸附树脂对黑豆花色苷进行动态吸附-解吸[25],上样液质量浓度为0.058 mg/mL,上柱流速为3~4 BV/h,吸附饱和后,用蒸馏水洗涤,去除花色苷中的蛋白质、糖类、有机酸等杂质,再用体积分数70%乙醇溶液1~2 BV/h流速进行解吸,洗脱得到的溶液于37 ℃条件下减压浓缩除去乙醇,得到纯化的花色苷,备用。
1.3.2.5 HPLC条件
色谱柱:T h e r m o F i s h e r反相C18色谱柱(100 mm×2.1 mm,1.9 μm);流动相:A相为0.3%甲酸溶液,B相为甲酸-乙腈-水(0.3∶30∶69.7,V/V)溶液;线性梯度洗脱:0~30 min,A相从70%降至10%;保持2 min;32~35 min A相从10%升至70%;保持3 min;流速1 mL/min;柱温25 ℃:进样量10 μL;检测波长526 nm;二极管阵列检测器。
1.3.2.6 MS条件
电喷雾离子源;正离子扫描;质量扫描范围m/z 100~2 000;N2流速20 L/min;毛细管电压26 V;毛细管温度270 ℃。
2 结果与分析
2.1 蛋白纯度及蛋白得率的分析
在pH值为7条件下,添加不同浓度(0、5、10、15、20、25 mmol/L)的不同二价阳离子(Ca2+、Mg2+、Zn2+),其对所得组分的7S与11S球蛋白纯度的影响如图1所示。
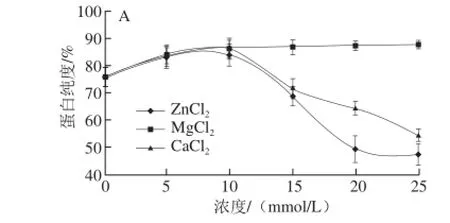
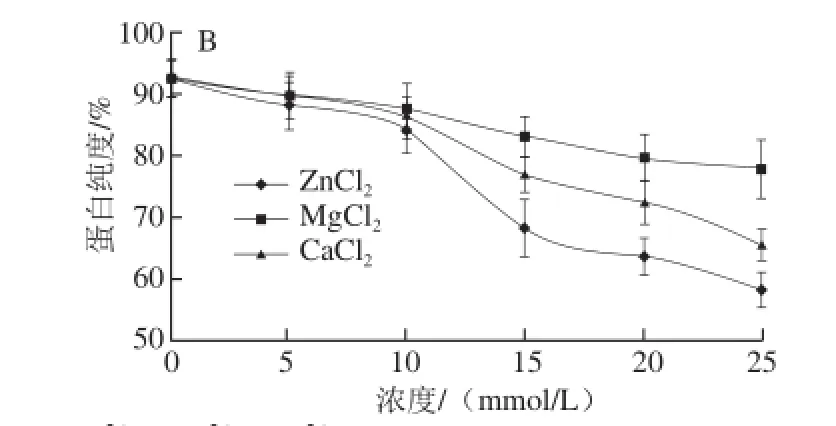
图1 Zn2+、Mg2+、Ca2+浓度对7S球蛋白(A)和11S球蛋白(B)纯度的影响Fig.1 Inf l uence of Zn2+, Mg2+and Ca2+concentrations on the purity of 7S globulin (A) and 11S globulin (B)
根据双因素试验的方差分析可知,在pH值为7条件下,所加入的二价阳离子的类型及浓度显著影响黑豆中7S与11S球蛋白级分纯度。在本实验添加的3 种二价阳离子(Zn2+、Mg2+和Ca2+)中,添加Zn2+得到的7S与11S球蛋白级分的纯度最低,而添加Mg2+得到的7S与11S球蛋白级分的纯度明显高于添加Zn2+和Ca2+的情况,尤其是在较高的离子浓度条件下(大于10 mmol/L),说明Mg2+与7S或11S球蛋白结合的特异性远高于Zn2+和Ca2+。在0~25 mmol/L的离子浓度内,随着Mg2+浓度的升高,提取的7S球蛋白级分的纯度逐渐增加至87.5%,而在添加Zn2+和Ca2+的条件下,随着浓度的升高,7S球蛋白级分的纯度先增加后降低且在10 mmol/L时纯度最大;而11S球蛋白级分的纯度则随Zn2+、Mg2+和Ca2+浓度的增加均逐渐下降。
在pH值为7条件下,添加不同浓度(0、5、10、15、20、25 mmol/L)的不同二价阳离子(Ca2+、Mg2+、Zn2+),其对所得组分的7S与11S球蛋白得率的影响见图2。

图2 Zn2+、Mg2+、Ca2+浓度对7S球蛋白(A)和11S球蛋白(B)得率的影响Fig.2 Inf l uence of Zn2+, Mg2+and Ca2+concentrations on the yield of 7S globulin (A) and 11S globulin (B)
根据双因素试验的方差分析可知,在pH值为7条件下,所加入的二价阳离子的类型及浓度显著影响黑豆中7S与11S球蛋白级分的得率。在本实验添加的3 种二价阳离子(Zn2+、Mg2+和Ca2+)中,添加Mg2+得到的7S球蛋白得率明显高于添加Ca2+和Zn2+的情况,而对于11S球蛋白,添加Zn2+所得的得率最高,说明Mg2+对7S球蛋白的结合能力高于其他2 种离子,而Zn2+对11S球蛋白的结合能力高于其他2 种离子。在0~25 mmol/L的离子浓度范围内,随Zn2+、Mg2+和Ca2+浓度的升高,7S球蛋白级分的得率逐渐降低,而11S球蛋白级分的得率则逐渐增加。
实验结果表明,不同浓度(0、5、10、15、20、25 mmol/L)的不同二价阳离子(Ca2+、Mg2+和Zn2+)对黑豆蛋白中7S球蛋白与11S球蛋白得率和纯度的影响各不相同,可能是由于不同二价阳离子与蛋白的结合方式和结合强度存在差异。最终,利用综合平衡法,选定添加10 mmol/L的Mg2+提取黑豆球蛋白,所得的7S与11S球蛋白的得率和纯度均较高。此条件下得到的7S球蛋白纯度和得率分别为(86.29±3.25)%和(2.90±0.14)%,11S球蛋白纯度和得率分别为(87.42±3.30)%和(9.11±0.28)%。Wu Shaowen等[26]研究表明,2 组分的纯度均达到(90±0.9)%,然而两组分的得率分别只达到(1.7±0.05)%与(3.6±0.03)%[21]。Deak等[27]研究表明,制得7S与11S组分的纯度分别为(67±0.4)%及(94±0.2)%,得率分别为(4.5±0.09)%与(4.7±0.2)%[21]。与之相比,本研究的提取方法得到的7S的纯度略低于文献[26]却显著高于文献[27]的方法所得结果,7S球蛋白的得率高于文献[26]而低于文献[27]的研究结果,11S球蛋白的纯度略低于文献[26]和文献[27]而得率显著高于文献[26-27]的研究结果。
2.2 花色苷的分析
2.2.1 总花色苷和总酚成分含量测定
经测定,黑豆中总花色苷含量为(0.58±0.03)mg/g,总酚含量为(2.22±0.12)mg/g。
2.2.2 花色苷结构分析
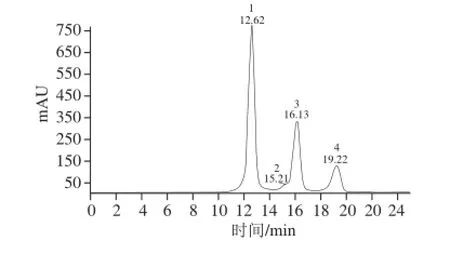
图3 黑豆花色苷提取物的HPLC图Fig.3 HPLC chromatograms of black soybean anthocyanin extract
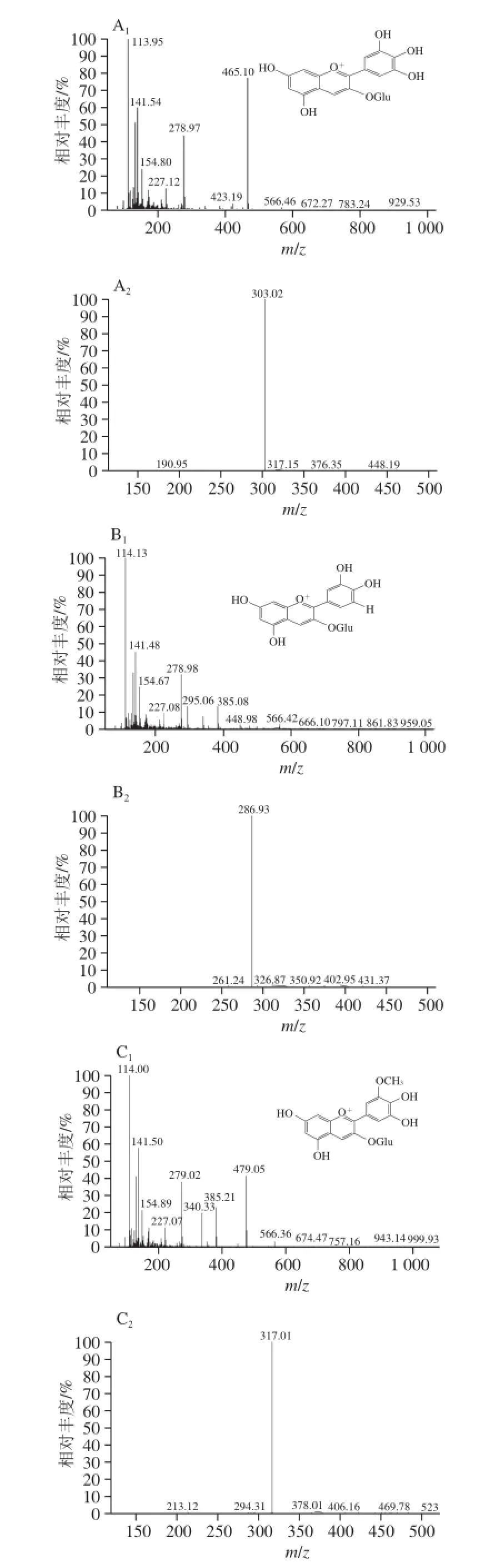

图4 黑豆花色苷各峰的一级和二级质谱图Fig.4 ESI+-mass spectra of black soybean anthocyanins
由图3和图4A可知,其分子离子[M+H]+为m/z 465.10,碎片离子为m/z 303.02,是由分子离子丢失了一个质量数为162葡萄糖的中性碎片而得。因此,峰1可能为飞燕草色素-3-O-葡萄糖苷。由图4B可知,其分子离子[M+H]+为m/z 448.98,碎片离子为m/z 286.93,是由分子离子丢失了一个质量数为162葡萄糖的中性碎片而得。因此,峰2可能为矢车菊色素-3-O-葡萄糖苷。由图4C可知,其分子离子[M+H]+为m/z 479.05,碎片离子为m/z 317.01,是由分子离子丢失了一个质量数为162葡萄糖的中性碎片而得。因此,峰3可能为牵牛花色素-3-O-葡萄糖苷[28-30]。由图4D可知,其分子离子[M+H]+为m/z 493.09,碎片离子为m/z 331.02,是由分子离子丢失了一个质量数为162葡萄糖的中性碎片而得。因此,峰4可能为锦葵花色素-3-O-葡萄糖苷。该结论和Kim等[30]的研究结果大致相同,均发现飞燕草色素-3-O-葡萄糖苷、矢车菊色素-3-O-葡萄糖苷和牵牛花色素-3-O-葡萄糖苷,而其研究未发现锦葵花色素-3-O-葡萄糖苷。
3 结 论
黑豆提取过程中所加入的二价阳离子的类型及浓度显著影响7S和11S球蛋白的得率和纯度,而且影响结果各不相同。在0~25 mmol/L的离子浓度内,随着Mg2+浓度的升高,提取的7S球蛋白级分的纯度逐渐增加至87.5%,而随着Zn2+和Ca2+浓度的升高,7S球蛋白级分的纯度先增加后降低且在10 mmol/L时纯度最大;随Zn2+、Mg2+和Ca2+浓度的增加,11S球蛋白级分的纯度逐渐下降,7S球蛋白级分的得率逐渐降低,而11S球蛋白级分的得率则逐渐增加。添加10 mmol/L的Mg2+提取黑豆球蛋白最优,得到7S球蛋白纯度和得率分别为(86.29±3.25)%和(2.90±0.14)%,11S球蛋白纯度和得率分别为(87.42±3.30)%和(9.11±0.28)%。
黑豆中总花色苷含量为(0.58±0.03)mg/g,总酚含量为(2.22±0.12)mg/g。HPLC-MS/MS分析得出黑豆花色苷主要包括4 种成分,分别为飞燕草色素-3-O-葡萄糖苷、矢车菊色素-3-O-葡萄糖苷和牵牛花色素-3-O-葡萄糖苷和锦葵花色素-3-O-葡萄糖苷。
[1] 王晶, 马文君, 陈勇, 等. 超声辅助提取黑豆蛋白及其功能性质的研究[J]. 食品工业科技, 2014, 35(21): 86-90. DOI:10.13386/ j.issn1002-0306.2014.21.009.
[2] 郭婕, 刘中华, 袁淑培, 等. 黑豆中大豆异黄酮微波提取工艺的优化[J]. 食品工业科技, 2015, 36(5): 255-257. DOI:10.13386/ j.issn1002-0306.2015.05.045.
[3] 陈颖, 徐巍. 黑豆主要营养成分分析[J]. 安徽农业科学, 2008, 36(34): 14928-14929. DOI:10.3969/j.issn.0517-6611.2008.34.050.
[4] 龙盛京, 马文力. 黑豆色素及多糖对全血化学发光和活性氧的抑制作用[J]. 食品科学, 1999, 20(9): 9-12. DOI:10.3321/ j.issn:1002-6630.1999.09.002.
[5] 王玉丽, 任海伟, 李志忠, 等. 用清除DPPH自由基法评价药黑豆色素的抗氧化能力[J]. 食品工业科技, 2009, 30(8): 102-105. DOI:10.13386/j.issn1002-0306.2009.08.096.
[6] 豆亚静, 张晓龙, 常丽新, 等. 响应面优化超声波法提取黑豆异黄酮的工艺研究[J]. 食品工业科技, 2013, 34(5): 259-263. DOI:10.13386/ j.issn1002-0306.2013.05.021.
[7] 周凯琳, 陶莎, 薛文通. 黑豆蛋白及其抗氧化肽研究进展[J]. 食品工业, 2015, 36(5): 204-207.
[8] 陈学玲. 大豆11S、7S球蛋白的功能特性及其与淀粉相互作用研究[D].武汉: 华中农业大学, 2005. DOI:10.7666/d.y806540.
[9] 毕爽, 马文君, 李杨, 等. 脉冲电场-超声波作用对黑豆球蛋白功能性质的影响[J]. 食品科学, 2016, 37(9): 7-12. DOI:10.7506/spkx1002-6630-201609002.
[10] 周瑞宝, 周兵. 大豆7S和11S球蛋白的结构和功能性质[J]. 中国粮油学报, 1998, 13(6): 39-42. DOI:10.3321/j.issn:1003-0174.1998.06.011.
[11] WOLF W J, NELSEN T C. Partial purification and characterization of the 15S globulin of soysoybeans, a dimer of glycinin[J]. Journal of Agricultural and Food Chemistry, 1996, 44(3): 785-791. DOI:10.1021/ jf940493p.
[12] 陶玲玲, 杨春华, 石彦国, 等. 提取条件对大豆7S和11S球蛋白凝胶性的影响[J]. 大豆科技, 2010(6): 20-23. DOI:10.3969/ j.issn.1674-3547.2010.06.008.
[13] 胡超, 黄丽华, 李文哲. 大豆球蛋白11S/7S比值对大豆蛋白功能性的影响[J]. 中国粮油学报, 2004, 19(1): 40-42. DOI:10.3321/ j.issn:1003-0174.2004.01.011.
[14] 陈海敏, 华欲飞. 品种差异对大豆蛋白质功能性的影响[J]. 中国油脂, 2000, 25(6): 178-180. DOI:10.3321/j.issn:1003-7969.2000.06.054.
[15] 陆恒. 黑豆蛋白质的营养价值优势及利用对策[J]. 现代商贸工业, 2003(2): 40-42. DOI:10.3969/j.issn.1672-3198.2003.02.023.
[16] 曹春艳, 赵永华, 赵莹莹. 黑豆皮色素提取工艺的研究[J]. 粮食与饲料工业, 2012(9): 22-24.
[17] 李桂兰, 凌文华, 高永清. 黑豆中花色苷水解工艺和定量研究[J].食品科学, 2010, 31(12): 1-5.
[18] 方军军, 李冬梅. 黑豆红色素理化性质及提取工艺的研究[J]. 民营科技, 2013(3): 74-75. DOI:10.3969/j.issn.1673-4033.2013.03.072.
[19] 丛建民. 黑豆的营养成分分析研究[J]. 食品工业科技, 2008, 19(4): 262-264.
[20] 郑二丽, 杨晓泉, 吴娜娜. 不同的二价阳离子(Ca2+、Mg2+、Zn2+)对大豆蛋白分级效果的影响[J]. 食品工业科技, 2012, 33(5): 108-112. DOI:10.13386/j.issn1002-0306.2012.05.079.
[21] 刘翀. 大豆蛋白分级分离机理的研究[D]. 广州: 华南理工大学, 2009.
[22] 卫生部. 食品中蛋白质的测定: GB 5009.5-2010[S]. 北京: 中国标准出版社, 2010: 1-7.
[23] LEE J, DURST R W, WROLSTAD R E. Determination of total monomeric anthocyanin pigment content of fruit juices, beverages, natural colorants, and wines by the pH differential method: collaborative study[J]. Journal of AOAC International, 2005, 88(5): 1269-1278.
[24] DENG G F, LIN X, XU X R, et al. Antioxidant capacities and total phenolic contents of 56 vegetables[J]. Journal of Functional Foods, 2013, 5(1): 260-266. DOI:10.1016/j.jff.2012.10.015.
[25] 刘岱琳, 董晋泉, 王媚, 等. YWD-01大孔吸附树脂分离纯化黑豆红色素的研究[J]. 食品科学, 2007, 28(3): 85-88. DOI:10.3321/ j.issn:1002-6630.2007.03.017.
[26] WU S, MURPHY P A, JOHNSON L A, et al. Simplified process for soybean glycinin and β-conglycinin fractionation[J]. Journal of Agricultural and Food Chemistry, 2000, 48(7): 2702-2708. DOI:10.1021/jf990785w.
[27] DEAK N A, MURPHY P A, JOHNSON L A. Fractionating soybean storage proteins using Ca2+, and NaHSO3[J]. Journal of Food Science, 2006, 71(7): C413-C424. DOI:10.1111/j.1750-3841.2006.00132.x.
[28] JIN H L, KANG N S, SHIN S O, et al. Characterisation of anthocyanins in the black soybean (Glycine max L.) by HPLCDAD-ESI/MS analysis[J]. Food Chemistry, 2009, 112(1): 226-231. DOI:10.1016/j.foodchem.2008.05.056.
[29] ASTADI I R, ASTUTI M, SANTOSO U, et al. In vitro antioxidant activity of anthocyanins of black soybean seed coat in human low density lipoprotein (LDL)[J]. Food Chemistry, 2009, 112(3): 659-663. DOI:10.1016/j.foodchem.2008.06.034.
[30] KIM E H, LEE O K, KIM J K, et al. Isoflavones and anthocyanins analysis in soybean (Glycine max (L.) Merill) from three different planting locations in Korea[J]. Field Crops Research, 2014, 156(2): 76-83. DOI:10.1016/j.fcr.2013.10.020.
Fractional Extraction of Protein and Characterization of Anthocyanins from Black Soybean Seeds
JIANG Tian, HE Yi, ZHU Zhenzhou, LI Shuyi, HE Jingren*
(College of Food Science and Engineering, Wuhan Polytechnic University, Wuhan 430023, China)
Crude protein extract from black soybean seeds was fractionated by addition of different concentrations (0, 5, 10, 15, 20 and 25 mmol/L) of divalent cations (Ca2+, Mg2+and Zn2+). After the precipitated protein fractions (7S globulin and 11S globulin) were freeze dried, total nitrogen was determined by the Kjeldahl method and the yield and purity of the two fractions were measured. The results revealed that the type and concentration of divalent cations significantly affected the yield and purity of 7S and 11S globulin. Based on comprehensive consideration of yield and purity, 10 mmol/L of Mg2+was selected to extract black soybean globulin. The purity and yield of the obtained 7S protein were (86.29 ± 3.25)% and (2.90 ± 0.14)%, respectively, while the purity and yield of the obtained 11S protein were (87.42 ± 3.30)% and (9.11 ± 0.28)%, respectively. Anthocyanins from black soybean seeds were extracted with ethanol. It turned out that the content of anthocyanins was (0.58 ± 0.03) mg/g and total phenol was (2.22 ± 0.12) mg/g. By high performance liquid chromatography tandem-mass spectrometry (HPLC-MS/MS) analysis, the isolated anthocyanins were characterized as delphinidin-3-O-glucoside, cyanidin 3-O-glucoside, petunidin 3-O-glucoside and mallow-3-O-glucoside, respectively.
black soybean; fractional extraction; 7S globulin; 11S globulin; anthocyanin
10.7506/spkx1002-6630-201704035
TS201.1
A
1002-6630(2017)04-0217-06
江甜, 何毅, 祝振洲, 等. 黑豆蛋白的分级提取及黑豆花色苷的成分鉴定[J]. 食品科学, 2017, 38(4): 217-222.
DOI:10.7506/spkx1002-6630-201704035. http://www.spkx.net.cn
JIANG Tian, HE Yi, ZHU Zhenzhou, et al. Fractional extraction of protein and characterization of anthocyanins from black soybean seeds[J]. Food Science, 2017, 38(4): 217-222. (in Chinese with English abstract) DOI:10.7506/spkx1002-6630-201704035. http://www.spkx.net.cn
2016-06-01
国家自然科学基金面上项目(31371727);国家国际科技合作专项(2014DFG32310);湖北省科技支撑计划项目(2015BHE015);湖北省自然科学基金项目(2014CFB891)
江甜(1992—),女,硕士研究生,研究方向为农产品加工化学与食品营养。E-mail:13476183768@163.com
*通信作者:何静仁(1974—),男,教授,博士,研究方向为膳食功效物质基础与分子营养。E-mail:jingren.he@whpu.edu.cn
