SLS人体单次斑贴试验阳性对照物基准模型的建立
2017-03-24
SLS人体单次斑贴试验阳性对照物基准模型的建立
杨丽洁1胡蔚毅1马亚峰2袁 超1
目的:建立十二烷基磺酸钠(SLS)人体单次斑贴试验阳性基准模型。方法:60名健康受试者使用0.01%、0.05%、0.10%、0.50%和1.00%SLS进行第一阶段皮肤单次斑贴试验,确定阳性对照物的初步合适浓度区间。然后再选取60名健康受试者根据第一阶段合适浓度范围设计浓度进行第二阶段试验,进一步确定合适浓度。结果:第一阶段的试验提示,阳性基准物的浓度在0.01%~0.05%之间,第二阶段确定0.02%SLS的1级皮肤反应人数≤5例,2级皮肤反应人数<2例,该反应率与标准中的阳性结果最为接近。结论:建议以0.02%SLS作为人体单次斑贴试验的阳性对照物基准模型。
皮肤斑贴试验;刺激反应;基准模型;十二烷基磺酸钠
我国化妆品产业已经呈现出消费市场不断扩大、产品更新换代不断加快、新型化妆品不断涌现、新原料不断开发的新趋势。化妆品产业的这种发展趋势必然会增加化妆品不良反应发生的可能性。国际上通常采用人体重复激发斑贴试验(Human Repeated Insult Patch Test,HRIPT)来评价化妆品对皮肤潜在的致敏性[1];而皮肤刺激性评价方法上,目前在国家药品食品监督管理局的监管下,按照《化妆品卫生规范》(2007版)对化妆品进行单次皮肤斑贴试验,以此来检测化妆品对人体皮肤潜在不良反应。据上海市皮肤病医院2008年统计的“3497件特殊用途化妆品人体单次皮肤斑贴试验结果分析”认为[2]:斑贴试验进行的季节、受试者性别对其结果有一定影响,如冬季化妆品斑贴试验阳性率高于夏季,男性对化妆品阳性率高于女性。
如何在斑贴试验的方法学上规避混杂因素对其试验结果的影响,这是化妆品监测管理中的重要环节之一。在很多研究中,十二烷基磺酸钠(Sodium Lauryl Sulphate,SLS)常常被应用为皮肤刺激物模型,以SLS作为阳性对照物进行相应的判断[3,4]。因此,我们设想在化妆品监测管理中,如加上合适浓度的SLS作为阳性判读的依据,是否能够将之前所提及的混杂因素进行规避,这是我们此次的研究目的。
1 材料与方法
1.1 研究对象试验分为两个阶段进行:阶段一,SLS阳性反应浓度的初步确定。按照《化妆品卫生规范》(2007版)中“人体皮肤斑贴试验”的受试者选择要求,60名健康自愿受试者分两次进行试验。阶段二,SLS阳性反应浓度的进一步确定,再次选择60名健康自愿受试者分为两次进行试验。120名受试者基本信息见表1。试验前,每位受试者签署知情同意书。受试者试验期间,避免背部试验部位的洗浴或搔抓,并停用任何药物。整个试验过程和方法经过上海市皮肤病医院伦理委员会审核和通过。为了避免季节因素对试验结果的影响,选择同一季节(九月份)进行试验。
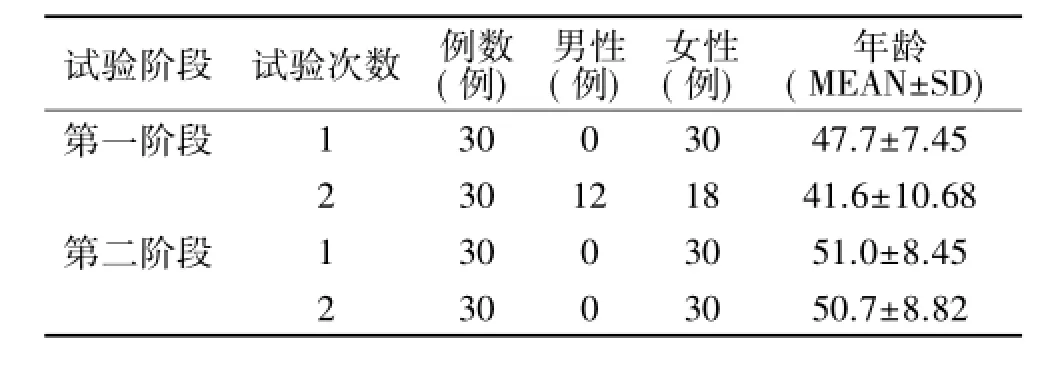
表1 试验不同阶段的受试者性别和年龄分布
1.2 材料与方法
1.2.1 材料斑试器:上海市卫生材料厂出品。其直径为8 mm。可调微量移液器:上海求精生化试剂及仪器公司生产。其可调范围为10~50μL。SLS:希格玛公司出品。为试验用分析纯浓度99%。
1.2.2 方法根据《化妆品卫生规范》(2007版)中人体皮肤斑贴试验的基本原则和方法,对不同浓度的SLS进行检测,阶段一中试验用SLS浓度为0.01%、0.05%、0.10%、0.50%和1.00%;阶段二中试验用SLS浓度为0.01%、0.02%、0.03%和0.04%。试验过程:将试验物和空白对照、蒸馏水对照贴覆于受试者背部24 h。在去除受试物斑试器后0.5 h、24 h及48 h对皮肤反应进行评价,并记录评价结果。所有皮肤反应均有受过专业培训的两位皮肤科医师按照统一标准判读。评判标准使用《化妆品卫生规范》(2007版)中的“皮肤不良反应分级标准”。该试验在经过中华人民共和国国家药品食品监督管理局认定的人体安全性和功效性检验机构及国家计量认证单位认证的实验室内进行,符合良好非创伤性检测试验条件。
1.2.3 统计学方法应用SPSS医学统计软件包进行分析。计数资料采用卡方检验,其显著性水平为0.05。
2 结果
2.1 第一阶段的结果
2.1.1 不同浓度SLS反应人数情况1%SLS在第一阶段的两次试验中,均引起了100%反应率;而0.01%和0.05%SLS反应率相对较低,见表2。对照《化妆品卫生规范》(2007版)中“结果解释”部分:30例受试者中出现1级皮肤不良反应人数多于5例(反应率为16.7%),判定受试物对人体有皮肤不良反应。与16.7%的反应率相比,0.10%、0.50%和1.00%的SLS反应率较高(P<0.05)。可以初步推断,阳性对照物的合适浓度区间范围在0.01%~0.05%之间,需要进一步分层探索其合适浓度。
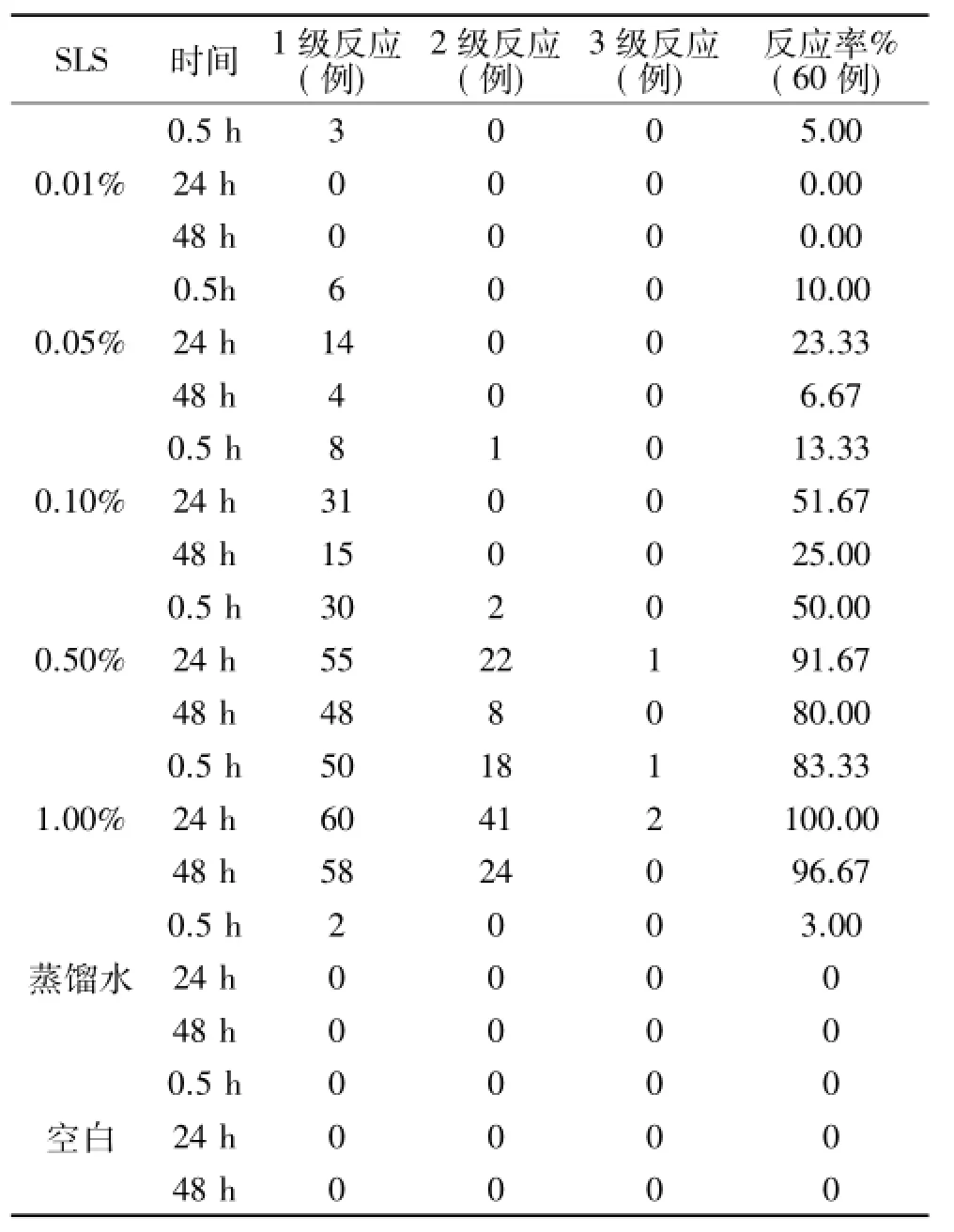
表2 第一阶段中不同浓度SLS反应人数情况
2.1.2 不同性别的反应率比较男性对SLS反应率在0.05%和0.10%之间显著高于女性(P<0.05),而在0.01%、0.50%及1%时和女性没有显著性差异(P>0.05)。此结果与2008年统计的“3497件特殊用途化妆品人体单次皮肤斑贴试验结果分析”中一致,说明对于低浓度的刺激物而言,男性的阳性反应率高于女性(图1)。
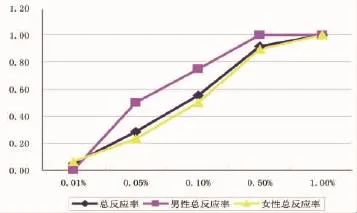
图1 阶段一中不同性别反应率比较
2.2 第二阶段的结果根据阶段一的结果,将SLS的试验浓度调整为0.01%、0.02%、0.03%及0.04%,再次进行人体皮肤斑贴试验。
2.2.1 不同浓度SLS反应人数情况两个批次的试验中,0.02%SLS反应率低于“1级皮肤不良反应人数5例”(反应率为16.7%)的标准,且无显著性统计学差异(P>0.05);0.03%SLS的反应率高于16.7%,也无显著性差异(P>0.05);而0.01%或0.04%SLS均显著低于或高于该标准(P<0.05),见表3。
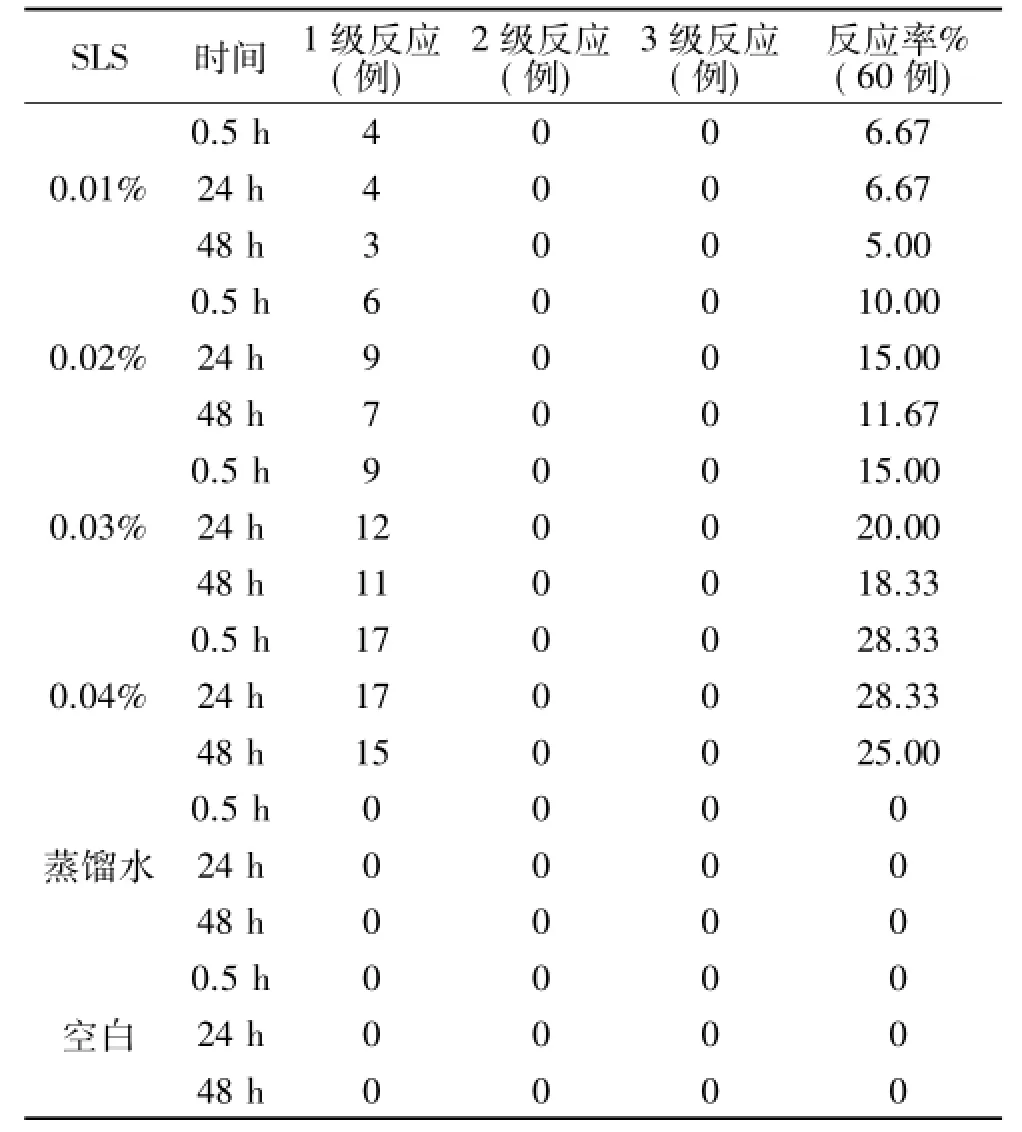
表3 第二阶段中不同浓度SLS反应人数情况
2.2.2 与卫生规范标准的比较按照《2007版化妆品卫生规范》中“结果解释”的标准,比较这四种不同浓度SLS的1级反应和2级反应人数,认为:两次试验中,0.02%SLS的1级皮肤反应人数≤5例,且2级皮肤反应人数<2人。见图2,3。
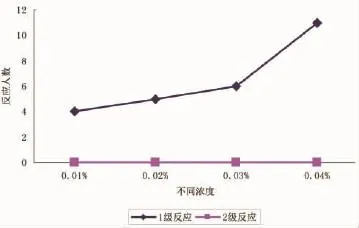
图2 第一批1级和2级皮肤反应人数
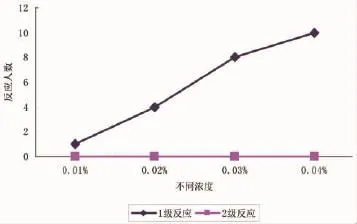
图3 第二批1级和2级皮肤反应人数
3 讨论
早在九十年代早期,Basketter等人就提倡使用人体4 h斑贴试验来替代动物试验辨别皮肤急性刺激反应[5,6]。但因为化妆品终产品很少产生急性刺激反应,且大多产品需要驻留在皮肤表面,所以该方法应用的并不多。在1996年,由欧洲化妆品-洗涤产品-香精协会(COLIPA)的特别小组制定了一项指南,通过该指南明确了化妆品终产品对人体皮肤潜在不良反应的检测规定:该指南中有明确的单次/多次开放型斑贴试验和单次/多次封闭性或半封闭性斑贴试验方法与操作步骤[7]。国内在2007年颁布的《化妆品卫生规范》中明确规定了人体皮肤斑贴试验的原则和方法,并且作为一种行业规范在全国的各大化妆品行政许可检验机构进行实施和评价。
对于人体皮肤斑贴试验的结果解释,一直在化妆品安全性评价中有着一定的争议。虽然在规范中定义了受试者选择和排除的相关标准,但是在实施过程中,我们发现:受试者皮肤屏障功能对检测结果及化妆品判定有重要影响,而影响皮肤屏障功能的因素有很多:如人种、性别、年龄、药物、环境温度、湿度等[8]。在国外,如泰国卫生行政许可检验斑贴试验中,就是使用2.5%SDS(Sodium Dodecyl Sulfate)作为阳性对照物,将待测化妆品终产物与阳性对照物进行比对,来判定产品的安全性[9]。刺激性皮炎发生原因很多,但最重要的是刺激物渗透到角质层,并影响到角质层相关结构,从而出现刺激反应。在既往很多研究中,应用SLS斑贴试验来评估患者是否容易产生刺激性皮炎,这就是一种对皮肤屏障功能评价手段。Gloor M等用1%SLS在手臂屈侧进行皮肤斑贴试验,并应用多普勒血流仪测定其红斑改变情况,研究发现红斑可一直持续到试验后7~9天[10]。该结果和我们研究一致,在参与1%SLS斑贴60人中,100%出现了反应,说明该浓度是可以引起明显刺激反应。
在对阳性基准物模型探索中,我们逐步降低SLS浓度,期望能够得到一个符合卫生规范标准的合适浓度。试验第一阶段中,通过五种不同浓度SLS比较,分析出阳性对照物的合适浓度区间范围在0.01%~0.05%之间;在第二阶段中,将0.01%~0.05%进行分层,发现0.02%SLS反应情况最接近“1级皮肤不良反应人数5例”的标准。在人体皮肤斑贴试验的操作中,将0.02%SLS作为阳性对照基准物,如化妆品终产品反应大于0.02%SLS的反应,认为可能对皮肤存在潜在刺激反应可能;相反,如化妆品终产品反应小于或等于0.02%SLS的反应,认为产品是安全的。
当然,本次研究只是在寻找阳性对照物基准模型中的一个初步摸索,正式使用该标准还需要在实际工作中不断总结和提炼,最好能在多个不同试验室进行比对工作,以获得更多数据支持。另外,在我们的研究中,仅仅将SLS定义为一个刺激物模型,如出现SLS变态反应,则需要对结果进行科学分析。同时,该方法只有在评价刺激反应时,可以规避混杂因素对斑贴试验结果的影响,而对变态反应的评价时,就需要应用其他类型斑贴试验进行证实。
[1]McNamee PM,Api AM,Basketter DA,et al.A review of critical factors in the conduct and interpretation of the human repeat insult patch test[J].Regul Toxicol Pharmacol,2008,52(1):24-34.
[2]秦鸥,王学民.3497件特殊用途化妆品人体单次皮肤斑贴试验结果分析[J].中国卫生监督杂志,2009,16(1):57-60.
[3]Mehling A,Chkarnat C,Degwert J,et al.Interlaboratory studies with a proposed patch test design to evaluate the irritation potential of surfactants[J].Contact Dermatitis,2010,62(3):157-164.
[4]Jungersted JM,H gh JK,Hellegren LI,et al.Effects of topical corticosteroid and tacrolimus on ceramides and irritancy to sodium lauryl sulphate in healthy skin[J].Acta Derm Venereol,2011,91(3):290-294.
[5]Basketter DA,York M,McFadden JP,et al.Determination of skin irritation potential in the human 4-h patch test[J].Contact Dermatitis,2004,51(1):1-4.
[6]Robinson MK,McFadden JP,Basketter DA.Validity and ethics of the human 4-h patch test as an alternative method to assess acute skin irritation potential[J].Contact Dermatitis,2001,45(1):1-12.
[7]Walker AP,Basketter DA,Baverel M,et al.Test guidelines for the assessment of skin tolerance of potentially irritant cosmetic ingredients in man.european cosmetic,toiletry and perfumery association[J].Food Chem Toxicol,1997,35(10-11):1099-106.
[8]刘玮.皮肤屏障功能解析[J].中国皮肤性病学杂志,2008,12(22):758-761.
[9]Wattanakrai P,Suwanachote S,Kulkollakarn S,et al.The study of human skin irritation of a novel herbal skin care product and ingredients by human single closed patch testing[J].J Med Assoc Thai,2007,90(6):1116-1122.
[10]Gloor M,Senger B,Langenauer M,et al.On the course of the irritation reaction after irritant reaction after irritation with Sodium Lauryl Sulphate[J].Skin Res Technol,2004,10(3):144-148.
(收稿:2016-07-28修回:2016-10-08)
Establishment of positive control for benchmark in human single patch test
YANGLijie1,HUWeiyi1,MAYafeng2,YUANChao1.
1.ResearchLaboratoryofcosmeticsandskin,ShanghaiDermatologyHospital,Shanghai200443,China;2.DepartmentofDermatology,theAffiliatedHospitalofXuzhouMedicalUniversity,Xuzhou210002,China Correspondingauthor:YUANChao,E-mail:dermayuan@163.com
Objective:To establish the positive control for benchmark model of human asingle patch test.Methods:In the first stage,sixty healthy subjects were tested by different concentrations(0.01%、0.05%、0.10%、0.50%and 1.00%)of sodium lauryl sulphate(SLS)in single patch test in order to determine the proper concentration.In the second stage,the results obtained from the first stage of the experiment was used to determine the test concentration in 60 study subjects.Results:The positive benchmark concentration was between 0.01%-0.05%in the first study stage.When the concentration of SLS was 0.02%,there was less than 5 subjects in level 1 skin reaction and less than 2 subjects in level 2 skin reaction,which was most close to the positive standard according to the Cosmetics Health Standards 2007.Conclusion:0.02%SLS is applicable as a positive control for benchmark in human single patch test.
Skin Patch Test;irritative reaction;benchmark model;sodium lauryl sulphate
1上海市皮肤病医院,皮肤与化妆品研究室,上海,200443 2徐州医科大学附属医院皮肤科,江苏徐州,221002
袁超,E-mail:dermayuan@163.com
