2015年我院102例药物不良发应报告分析
2017-03-18杨欢汪洋
杨欢+汪洋

[摘要]目的 分析我院上报的不良反应报告的发生情况,指导临床合理用药及预防不良反应的发生。方法 回顾性分析研究我院2015年上报的102例药品不良反应报告,分析不良反应发生的影响因素与表现形式。结果 102例药品不良反應中,以10岁以下及21~30岁年龄组的患者发生率最高,抗菌药物引起的不良反应最多,导致的损害主要为皮肤及其附件,给药途径以注射给药为主,不良反应的类型主要为一般。结论 临床应用药物过程中,应充分了解药物的不良反应,选择合适的给药途径,并密切关注患者情况,保障合理用药。
[关键词]药物不良反应;分析;影响因素
[中图分类号] R392.8 [文献标识码] A [文章编号] 1674-4721(2017)01(b)-0153-04
药品不良反应(adverse drug reaction,ADR)是指合格的药品在正常剂量及用法下预防、诊断、治疗疾病或调节生理机能时,因药物本身的作用或药物间相互作用而产生的与用药目的无关的有害反应,主要表现为躯体及心理副反应、毒性反应、过敏性或特异性反应等。近年来,由于大量新药的上市,药物种类、剂型的逐步增多,以及合并用药的现象不可避免,药品在发挥着治疗效果治疗疾病的同时,药物不良反应的发生率也有所增加,对患者机体也产生不同程度的损害[1]。ADR是药品固有特性所引起的,任何药品都有可能引起不良反应。为更好地合理用药及预防不良反应的发生,现分析我院收集ADR报告,探讨其发生原因、发病类型、药物种类及影响因素等,现报道如下。
1资料与方法
1.1一般资料
依据国家卫生计生委药物不良反应监测中心评价标准,本研究选用2015年1~12月本院药械科收集并上报至国家不良反应监测中心的102例符合要求的ADR报告,对报告中患者的性别于年龄无特殊要求。
1.2方法
采用回顾性方法分析102例ADR报告中的内容,包括患者的年龄、药品种类、给药途径、不良反应累及的器官或系统及主要表现等。
2结果
2.1患者年龄分布情况
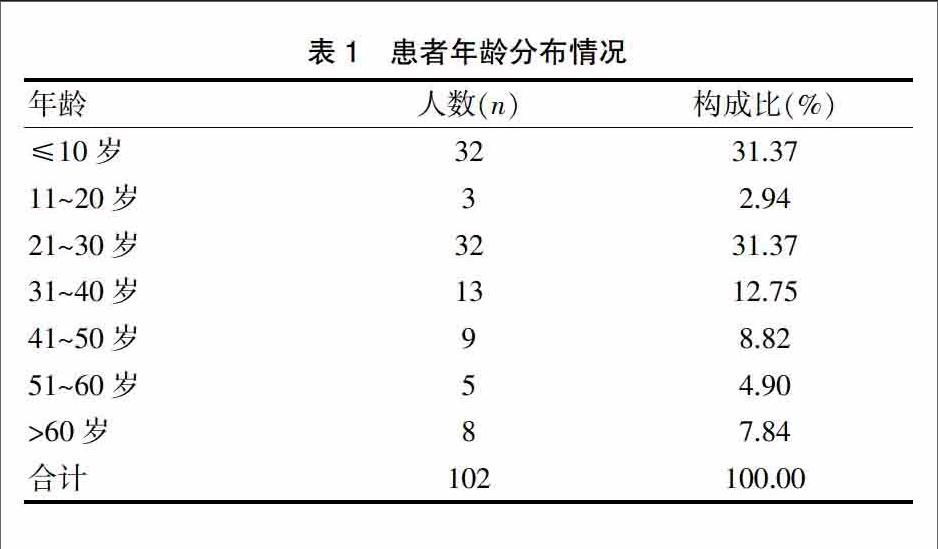
102例ADR报告中,最小年龄1个月,最大年龄90岁;≤10岁、21~30岁年龄段发生例数比例最高,均为32例,占31.37%;11~20岁年龄段发生例数比例最低,仅有3例,占2.94%。见表1。
2.2 ADR药物种类和例数
导致不良反应的药物共涉及43种,其中所占比例最高的药物为抗菌药物,抗菌药物中以大环内酯类引起的不良反应发生率最高。见表2。
2.3 ADR损害类型及其临床表现
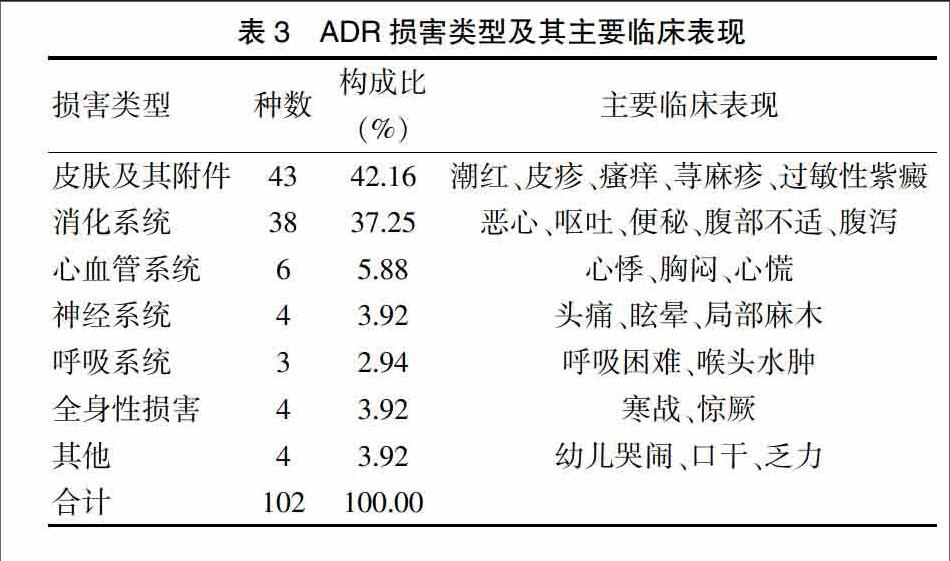
不良反应导致的损害主要累及皮肤及其附件,占42.16%,其次为消化系统,占37.25%。见表3。
2.4 ADR与给药途径的关系
ADR易发生于静脉注射给药,占78.43%。见表4。
2.5 ADR报告类型分析
102例ADR报告中,有83例报告类型为一般,占81.37%。见表5。
3讨论
3.1 ADR与患者年龄
本次研究结果显示,2015年度我院上报的ADR报告中,≤10岁及21~30岁年龄组的患者发生率最高,均为31.37%;其次为31~40岁年龄组,发生率为12.75%,主要原因是我院收治的患者主要为儿童与生育期妇女。儿童由于受到年龄和体质的限制而成为一类特殊的用药群体,其整个身体状况正处于生长发育的阶段,各系统器官功能不健全,肝脏对药物的解毒作用与肾脏对药物的排泄能力低下,肝酶系统发育尚未完全,以及自身免疫系统尚未完善,易致过敏等原因,易产生ADR[2]。而21~40岁的生育期妇女主要来我院进行妇科疾病治疗、围生期保健、自然生产或剖宫分娩以及实施无痛人流术,因此人数相对较多。女性在生理期、妊娠期及哺乳期用药时,需要格外重视所用药品的药理作用与不良反应,警惕药品的特殊影响,避免严重不良反应的发生。
3.2 ADR与药物种类
抗菌药物在使用过程中引起的ADR最多,占全部药物不良反应报告的54.90%,与相关文献报道一致[3]。通过对ADR报告的分析可知,很多患者尤其是幼儿,使用抗菌药物的病因大部分是呼吸道感染,而呼吸道感染性疾病多数以病毒感染为主。抗菌药物在临床上的使用多依据患者的临床表现采用经验疗法,导致抗菌药物的使用无原则,造成抗菌药物的滥用现象。此外,由于细菌耐药性的提高,抗菌药物的使用剂量也随之增加,使用指征也逐渐放宽,药物的其他药理作用也被忽视,从而使ADR发生的概率增加,因此,在临床使用抗菌药物时,应按照患者的适应证、药敏试验结果,合理选择药物的种类与剂量,保障患者的用药安全[4]。
3.3 ADR与损害类型及临床表现
ADR涉及人体的多个组织器官,包括肠胃系统、呼吸系统、神经系统等,影响着患者的健康。在本次分析ADR损害类型中,主要以皮肤及其附件损害为主,所占比例为42.16%,与相关文献报道一致[5];其次为消化系统损害,所占比例为37.25%。皮肤及其附件损害临床表现主要为潮红、皮疹、瘙痒、荨麻疹、过敏性紫癜;消化系统损害临床表现主要为恶心、呕吐、便秘、腹部不适、腹泻。皮肤为人体最大的器官,富含大量的免疫效应细胞[6],极易产生变态反应,且反应表现较为直观,较容易被患者及临床医务人员发现和诊断,因此此类变态反应上报数量较多,且经及时处理后一般恢复良好。一些潜在的不易被发现的药物不良反应存在较高的漏报率,阻碍了患者的治疗进程,因此在发生此类不良反应的同时,应注意其他器官和系统是否出现了不良反应,包括神经系统、呼吸系统、心血管系统等部位,尤其对肝肾功能不全的患者应进行重点监测。医护人员应加大药物不良反应的监测力度,积极收集不良反应信息,综合分析不良反应发生的原因,做出正确的处理。
3.4 ADR与给药途径
在给药途径的统计分析中,以注射给药引发的药物不良反应最多,占全部药物不良反应的78.43%,其次为口服给药,占15.69%,显著高于其他给药途径引发的ADR,与相关文献报道是一致的[7],可能是因为注射与口服给药是临床最常见的给药方式。采用注射方式给药时,药物将会直接进入体内血液循环,与患者内环境接触,药物中的各种成分因素,包括微粒、渗透压、pH、内毒素等,可直接引起不良反应的发生[8]。此外,注射给药通常是在医院中进行的,医护人员在密切监测患者用药后的表现时,能及时观察到不良反应的发生;而采用口服给药等其他给药方式时,不良反应难以被医护人员监测发现。另外由于部分患者对不良反应的上报积极性与意识不强,导致以其他方式给药时,药物不良反应的上报数量较少[9]。在进行临床用药时,如果采用口服给药的方式能够达到治疗效果,尽量不要采用注射给药的方式。在必须使用注射给药前,必须详细了解患者的药物过敏史,从而保证安全用药,减少不良反应的发生率。在注射给药过程中一旦发生不良反应,必须立即停药,医护人员应做好相应的处理工作[10]。
3.5 ADR的报告类型
102例不良反应的报告中,类型为一般的所占比例最大为81.37%,其次为新的、一般为17.65%和严重为0.98%。出现严重的不良反应的患者因“子宫平滑肌瘤”入院,术中为预防细菌感染,静脉滴注克林霉素磷酸酯注射液后,静脉注射丙泊酚注射液、注射用维库溴铵、枸橼酸芬太尼注射液与咪达唑仑注射液行麻醉诱导。后患者出现全身皮疹、眼睑水肿、喉头水肿及喉头痉挛过敏症状,血氧饱和度下降至65%,危及生命。经抢救后患者体征恢复正常无其他不适。其中怀疑药品为克林霉素磷酸酯注射液、丙泊酚注射液、注射用维库溴铵。
克林霉素会产生多种不良反应,由于机体对某些致敏物质发生变态反应,导致小动脉、小静脉及毛细血管的通透性和脆性增加,产生皮肤、黏膜及某些器官出血,同时也会伴有荨麻疹、血管神经性水肿等其他过敏症状;与阿片类镇痛药合用,克林霉素的神经肌肉阻滞作用与阿片类药物的中枢抑制作用累加而可能导致呼吸抑制或麻痹[11];克林霉素在某些情况下还会产生急性喉水肿,导致急性喉阻塞,引起呼吸困难。丙泊酚注射液使用时可能会引起短暂性呼吸暂停[12];注射用维库溴铵,因其神经肌肉阻滞作用[13],导致呼吸功能不全或缺氧、支气管痉挛及皮肤改变。可能因为患者的个体差异性,以及在三种可疑药物与其他两种药物联用的情况下不良反应的累加,严重不良反应的发生概率也会增大。
“用药安全”一直是当今社会尤为关注的话题,其目的是在合理用药的前提下保证疾病的成功治愈,同时又不会产生不良后果增加患者的痛苦,保证患者的生活质量。ADR不可避免,但是可以采取相应措施减少其发生率。临床医生在疾病治疗过程中谨慎选择使用药物,应明确了解药物的药理学特性及药物与机体、药物与药物之间的相互作用;与患者增加沟通,详细询问患者过敏史;对易产生不良反应及不良反应不易被观察到的药物,应在使用时密切监测患者的状态。一旦发现有不良反应能做到及时处理,减少伤害的发生。我院为妇幼保健专科医院,儿童及妇女患者尤其是围产期患者占大多数。儿童处于集体发育阶段,生理结构具有独特性,肝、肾等重要器官功能发育不完善,对药物的代谢与排泄能力低,与成人用药特点存在较大差异[14]。妊娠期妇女的身体状况处于一种特殊阶段,用药安全直接影响下一代的身心健康。大多数药物可以通过胎盘进入胎儿体内,胎儿的生长和发育过程比较复杂,器官和功能尚不健全,不能将体内蓄积的药物完全清除。同时药物对胎儿的影响尚不明确,妊娠期间用药不当会对孕妇及胎儿产生不良后果[15],因此儿童及围生期妇女用药安全要格外重视,合理用药,减少不良反应的发生,保证患者的身心健康。
[参考文献]
[1]李韵梅.药物不良反应545例分析[J].当代医学,2013,19(6):54-55.
[2]佟德恩.儿童抗菌药物导致不良反应的现状及影响因素分析[J].药物研究,2012,(2):27-28.
[3]朱发伟,王金明.浙江台州市椒江区726例药品不良反应报告分析[J].中国药房,2011,22(2):171-173.
[4]俞剑叶.我院80例药品不良反应报告分析[J].中国乡村医药,2015,11(22):37-38.
[5]张娟,熊永山,王登峰.武汉市2010年5252例药品不良反应报告分析[J]中国药房,2012,23(2):153-156.
[6]楼方舟,王宏林.皮肤免疫系统功能性研究进展[J].生命科学,2016,28(2):268-274.
[7]周勇,田月洁,黄传海,等.1388例严重药品不良反应报告分析[J].药物警戒,2008,5(4):225-230.
[8]段立鸣.静脉滴注给药常见不良反应及预防措施分析[J].医学美学美容旬刊,2014,(3):383-384.
[9]韩伟,刘瑞丽.药物不良反应原因分析及解决方法[J].医药论坛杂志,2009,30(2):77-79.
[10]廖燕玲,刘承统,陈治宇.2011-2013年312例医院抗感染类药物不良反应分析[J].现代药物与临床,2014,19(3):303-305.
[11]张子啸.克林霉素的不良反应[J].自我保健,2010,(6):59.
[12]包天秀,梁小女,張建友,等.地佐辛复合丙泊酚用于宫腔镜手术的效果[J].临床麻醉学杂志,2011,27(12):1202-1203.
[13]程璠,潘志强,刘庆,等.维库溴铵静脉泵注与单次静脉注射麻醉效果比较[J].临床合理用药杂志,2014,7(31):70-71.
[14]朱良.2008~2010年我院儿科用药不良反应监测分析[J].海峡药学,2011,23(11):243-244.
[15]明蕾.围产期临床用药的现存问题与评价[J].世界临床药物,2014,35(1):50-53.
(收稿日期:2016-11-18 本文编辑:顾雪菲)
