顶空气相色谱法测定奥扎格雷钠中残留溶剂
2017-03-07明宝钢张琳琳
明宝钢,张琳琳
顶空气相色谱法测定奥扎格雷钠中残留溶剂
明宝钢,张琳琳
目的 建立奥扎格雷钠中甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷残留量的测定方法。方法 采用DB-5毛细管色谱柱(30 m×0.532 mm,1.0 μm),载气为氮气,柱温采取程序升温,初始温度40 ℃,保持4 min,然后以25 ℃/min的速率升至150 ℃,保持4 min;顶空进样,进样口温度200 ℃;氢火焰离子化检测器(FID),检测器温度220 ℃。结果 甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷的线性范围分别为0.26~0.39、0.41~0.62、0.41~0.62、0.071~0.047、4.75~7.12 μg/mL,平均回收率(n=9)分别为101.3%、98.2%、95.4%、95.8%、95.4%。结论 该方法简便,灵敏度高,重复性好,结果准确,适合奥扎格雷钠中有机溶剂残留量的测定。
奥扎格雷钠;气相色谱法;顶空进样;残留溶剂
0 引言
奥扎格雷钠(Sodium ozagrel)为血栓素A2(TXA2)合成酶抑制剂,具有抗血小板凝聚和扩张血管的作用。依据本品的合成工艺路线,在合成过程中可能使用的有机试剂为甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷。根据中国药典2010年版二部附录ⅤE的要求[1],参考相关文献[2-9],本文采用气相色谱顶空进样法对上述溶剂的残留情况进行了测定。所建方法专属性强,重复性好,结果可靠,可用于奥扎格雷钠中甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷的残留量测定。
1 材料
气相色谱仪(日本岛津公司 GC-2010);顶空自动进样器(日本岛津公司 AOC-5000);高纯氮(纯度>99.9%);电子分析天平(瑞士sartorius公司,CP225D)。奥扎格雷钠原料来自A企业,批号:201201、201202、201203。甲醇为色谱纯,水为纯化水,其他试剂均为分析纯。
2 方法与结果
2.1 溶液的制备
2.1.1 对照品储备液的制备 精密称取甲醇、无水乙醇、乙醚、二氯甲烷和三氯甲烷各约0.3、0.5、0.5、0.06、0.006 g,置 100 mL 量瓶中,加少量二甲基甲酰胺使溶解后,加水稀释至刻度,摇匀,即得对照品储备液。
2.1.2 对照品溶液的制备 精密量取1、2、5、10、15、20、30 mL,分别置100 mL量瓶中,加水溶液稀释至刻度,摇匀,精密量取上述溶液各 5 mL,分别置20 mL顶空瓶中密封,即得对照品溶液①、②、③、④、⑤、⑥、⑦。
2.1.3 供试品溶液的制备 精密称取供试品约0.5 g,置 20 mL 顶空瓶中,精密加入水溶液5 mL使溶解,密封,即得。
2.1.4 空白溶液的制备 精密量取水5 mL,置 20 mL顶空瓶中,密封,即得。
2.2 色谱条件 采用DB-5 毛细管色谱柱(30 m×0.053 mm,1.0 μm);FID 检测器;载气为氮气,流速为 1.0 mL/min,采取程序升温,初始温度 4 ℃,保持4 min,然后以25 ℃/min的速率升至200 ℃,保持4 min;进样口温度 200 ℃;检测器温度220 ℃;顶空瓶平衡温度为60 ℃,平衡时间为30 min,定量环温度为60 ℃。按上述条件,取空白溶液、对照品溶液、供试品溶液进样,记录色谱图,见图1。在空白溶液色谱中,甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷主峰的保留时间处没有干扰峰出现;对照品溶液④色谱中各主峰的理论塔板数均不低于8 000,分离度均>1.5。
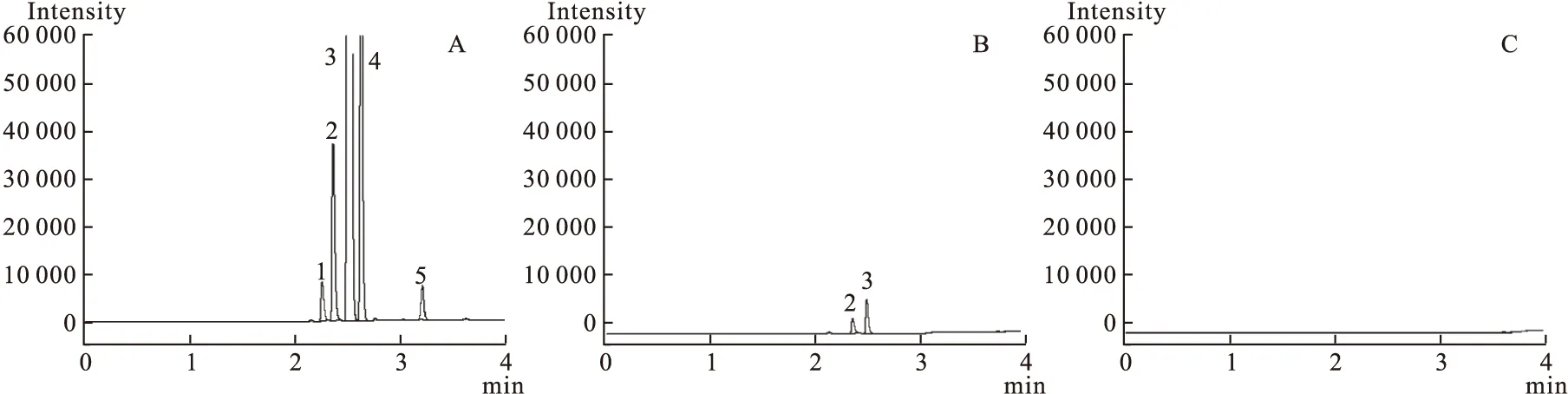
图1 奥扎格雷钠色谱图
2.3 线性关系考察 取“2.1.2”项下的系列对照品溶液,进样。以峰面积为纵坐标、对照品溶液浓度为横坐标,绘制标准曲线,计算得甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷的回归方程见表1。
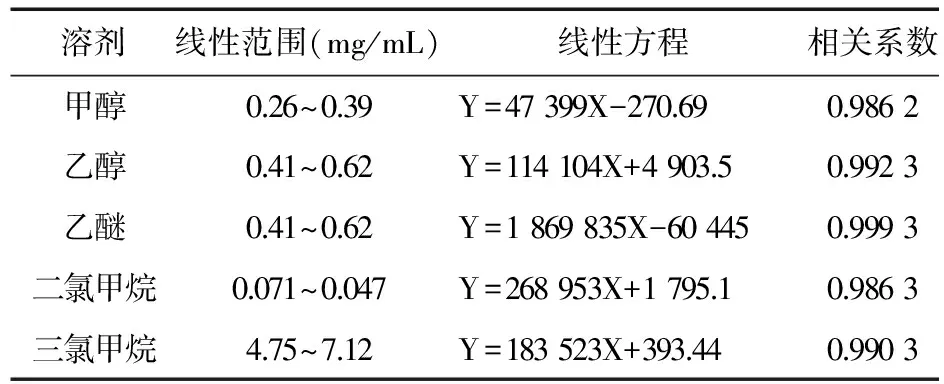
表1 线性方程与线性范围
2.4 重复性试验 按照“2.1.3”项下方法平行制备 6 份供试品溶液,顶空进样,结果表明,该方法重复性良好,具体结果见表2。

表2 重复性试验结果(%)
注:—为未检出
2.5 检测限与定量限测定 将对照品溶液④逐步稀释,精密量取5 mL,置20 mL顶空瓶中,密封,顶空进样,记录色谱图,所得图谱计算甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷色谱峰信噪比,测得甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷的检出限分别为2.5、2、10、60、120 ng/mL (信噪比为3∶1),定量限分别为6、4、50、120、240 ng/mL (信噪比为10∶1),结果见表3。
2.6 回收率试验 精密称取甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷适量,照对照品溶液④的配制方法,分别配制相当于其80%、100%、120%的溶液各3份,置100 mL量瓶中。精密称取供试品约0.5 g,共9 份,分别置20 mL 顶空瓶中,分别精密加入上述低、中、高3 个浓度的对照品溶液5 mL,密封,摇匀,按上述气相色谱条件测定,记录色谱图。计算得甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷的平均回收率(n=9)分别为101.3%、98.2%、95.4%、95.8%和95.4%;RSD分别为1.4%、1.4%、1.5%、3.4%和1.4%,结果见表4。
2.7 样品残留溶剂测定 按照“2.4”项下方法制备供试品溶液,顶空进样,结果3批样品均未检出甲醇、二氯甲烷和三氯甲烷,三批样品中乙醇和乙醚分别为0.05%和0.001%。
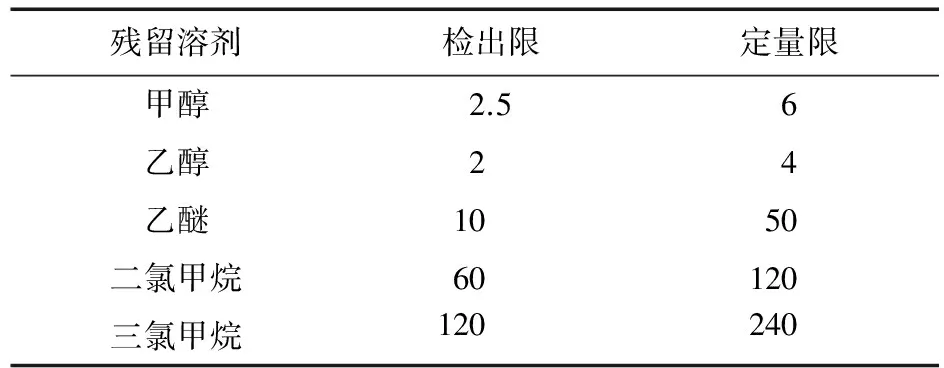
表3 检出限及定量限试验结果(μg/mL)
3 讨论
3.1 实验中对顶空温度及平衡时间进行了筛选,顶空温度分别考察了50、60、70 ℃;平衡时间考察了15、30、45 min。试验结果显示,顶空温度60 ℃,平衡时间30 min,顶空瓶中气液两相中的甲醇、乙醇、乙醚、二氯甲烷和三氯甲烷可充分平衡,峰面积适宜,故选择顶空温度60 ℃,平衡时间30 min。
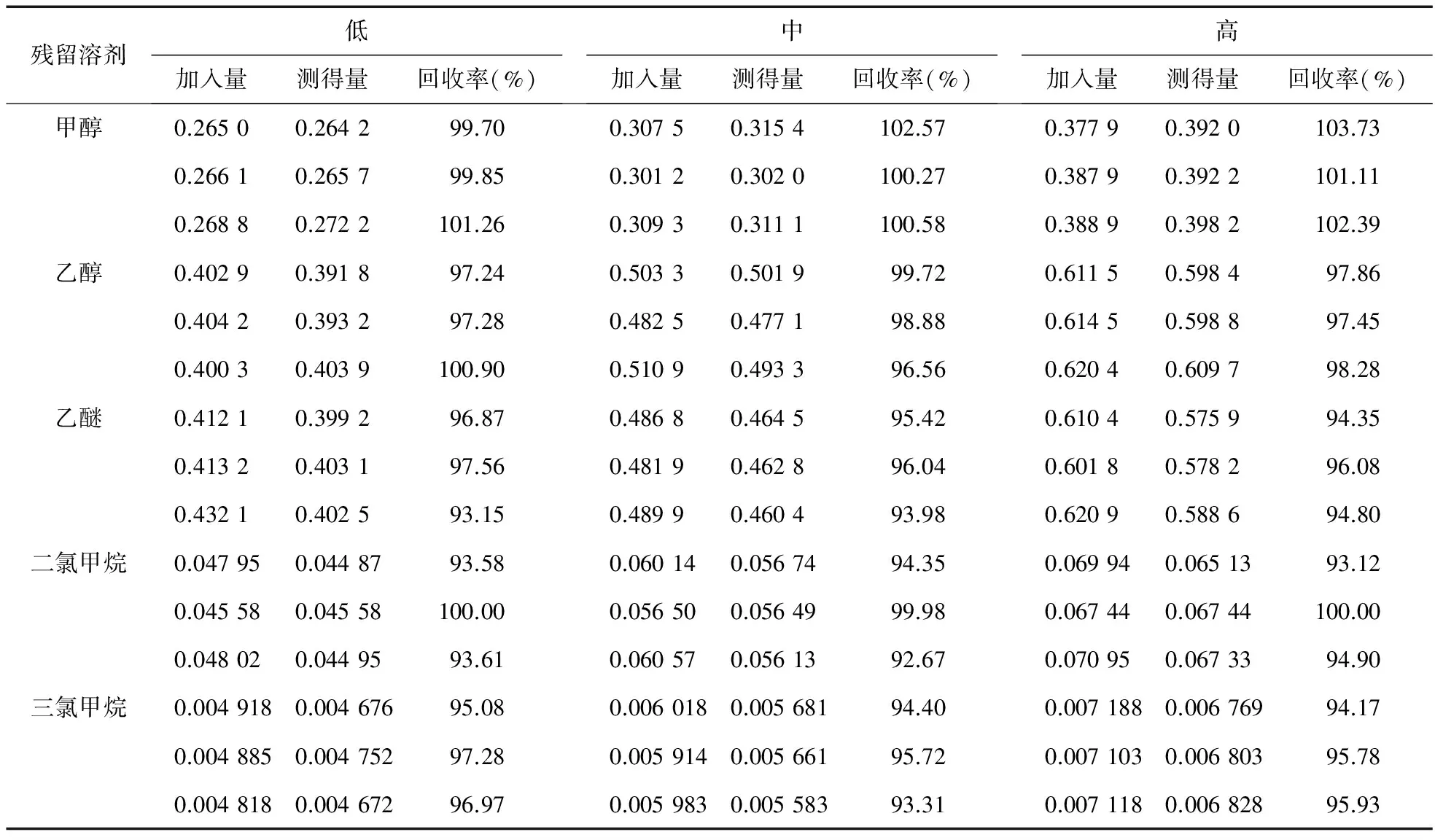
表4 回收率试验结果(mg/L)
注:乙醇测得量=[(检出量-称样量)×0.05%];乙醚测得量=[(检出量-称样量)×0.001%]
3.2 生产工艺中还涉及二甲基甲酰胺和四氯化碳等有机溶剂。试验中发现以水为溶剂时,顶空温度提高至100 ℃,或以水-二甲亚砜(9∶1)为溶剂,顶空温度提高至120 ℃,二甲基甲酰胺均无法采用顶空法进行测定;四氯化碳采用FID检测器响应值过低,对照品溶液的响应值刚刚达到检出限,故上述两种残留溶剂不适宜采用该方法同时测定。
3.3 该方法线性良好,回收率在92%~103%之间,重复性良好,结果表明,本文所建立的检测方法简便、准确、有效,能够满足实际样品检测的需要。
[1]卫生部药典委员会.中华人民共和国药典(二部)[S].北京:化学工业出版社,2010:31.
[2]张艳红,吕昭云,张颖,等.顶空毛细管气相色谱法测定羟戊基苯甲酸钾中的残留溶剂[J].药物分析杂志,2009,29(9):1565.
[3]程奇蕾,张德瑞,李慧义.盐酸西替利嗪中残留溶剂检查方法的研究[J].药物分析杂志,2008,28(8):1355.
[4]李心泓,杨直,胡晓炜.毛细管顶空进样法测定硫辛酸中有机溶剂残留量[J].中国新药杂志,2007,16(7):554-555.
[5]胡慧廉,丁乃立,吴莲珍.顶空气相色谱法测定左乙拉西坦中有机溶剂残留量[J].中国新药杂志,2007,16(22):1882-1884.
[6]洪志玲,胡猛慎.氢溴酸西酞普兰原料药中10种残留溶剂的检查方法研究[J].中国药房,2012,23(45):4303.
[7]陈汝红,杨春巧,张轶华.顶空气相色谱法检测苄星青霉素原料药中的5种残留溶剂[J].中国药房,2012,23(45):4287.
[8]吴朝华,王秀梅,顾宝明.顶空毛细管气相色谱法测定盐酸丁卡因原料药中的残留溶剂[J].药物分析杂志,2011,31(6):1188.
[9]崇小萌,胡昌勤.利用中等极性气相色谱系统分析药物残留溶剂[J].药物分析杂志,2014,34(11):2048.
·安全用药·
Headspace GC determination for residual solutions in sodium ozagrel
MING Bao-gang,ZHANG Lin-lin
(Department of Pharmacy,Shengjing Hospital of China Medical University,Shenyang 110004,China)
Objective To establish a headspace GC method for the determination of residual solution in sodium ozagrel.Methods DB-5 column (30 m×0.532 mm,1.0 μm) was adopted,with nitrogen as a carrier gas and FID as a detector.The initial temperature was kept at 40 ℃ for 4 min,and the temperature was raised to 150 ℃ at the rate of 25 ℃/min.The injecting port temperature was 200 ℃,and the detector temperature was 220 ℃.Results The calibration curve of methanol,ether,acetone and carbon dichloride showed a good linearity within the ranges of 0.26~0.39,0.41~0.62,0.41~0.62,0.071~0.047 and 4.75~7.12 μg/mL.The average recovery rates (n=9) were 101.3%,98.2%,95.4%,95.8% and 95.4%,respectively.Conclusion The method is simple,sensitive,reproducible and accurate for the determination of residual solution in sodium ozagrel.
Sodium ozagrel;GC;Headspace sampling;Residual solvent
2016-03-04
中国医科大学附属盛京医院药学部,沈阳 110004
10.14053/j.cnki.ppcr.201702024
