芬顿氧化-混凝深度处理二级出水试验研究
2017-03-06冯素敏宋振扬边永欢邵立荣靳薛凯
冯素敏,王 浩,宋振扬,边永欢,邵立荣,靳薛凯
(1. 河北科技大学环境科学与工程学院,河北石家庄 050018; 2. 河北省污染防治生物技术实验室,河北石家庄 050018; 3.河北科技大学建筑工程学院,河北石家庄 050018)
芬顿氧化-混凝深度处理二级出水试验研究
冯素敏1,2,王 浩3,宋振扬3,边永欢1,2,邵立荣1,2,靳薛凯3
(1. 河北科技大学环境科学与工程学院,河北石家庄 050018; 2. 河北省污染防治生物技术实验室,河北石家庄 050018; 3.河北科技大学建筑工程学院,河北石家庄 050018)
为了解决污水处理厂二级出水中有机物、总磷(TP)等污染物的超标问题,采用芬顿氧化-混凝工艺对污水进行深度处理,通过正交试验和单因素试验探讨了该工艺对污水的处理效果。研究表明:在芬顿氧化反应时间为40 min,初始pH值为6.0,FeSO4·7H2O和H2O2投加量(质量浓度)分别为600 mg/L和850 mg/L,且混凝反应pH值为8.0,阴离子聚丙烯酰胺(APAM)投加量(质量浓度)为3.0 mg/L的最优反应条件下,出水化学需氧量(COD)、色度和TP的去除率分别为97.5%,96.7%和99.2%,且均达到《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A标准。该工艺作为污水深度处理技术,可广泛应用于城镇污水处理厂对难降解污染物的深度处理。
水污染防治工程;芬顿氧化;混凝;二级出水;深度处理
随着城市化进程地不断发展,环境问题越来越受到人们的关注,而城镇污水处理厂作为污水处理的一个重要设施,国家对其出水指标提出了更高的排放要求[1]。目前,城镇污水处理厂多采用生物法作为污水的二级处理工艺,但对于富含难降解有机物且色度和总磷(TP)均偏高的污水,经处理后仍难达到《城镇污水处理厂污染物排放标准》(GB 18918—2002;以下简称“污水厂排放标准”)一级A标准。而高级氧化技术作为城镇污水的深度处理工艺越来越被广泛采用,并且该技术现已成为处理难降解有机物的研究热点[2]。高级氧化技术是利用芬顿试剂在水中使Fe2+催化H2O2生成·OH自由基,由此获得较强的氧化能力,可降解污水中的污染物[3],生成的Fe3+发生混凝沉淀作用去除有机物和磷酸盐[4-5],因此,在此过程中芬顿试剂同时具有强氧化和混凝2种作用[6],并且不会产生二次污染[7]。
本试验以降低出水中的化学需氧量(COD)、色度和TP为主要目的,采用“芬顿氧化-混凝”方法深度处理某城镇污水处理厂二级出水,使其达到“污水厂排放标准”一级A标准。
1 材料与方法
1.1 试验用水
选取华北地区某城镇污水处理厂二级生化出水,根据《水和废水监测分析方法》[8]检测水样的水质指标,其结果与相应的“污水厂排放标准”一级A标准值列于表1。
由于该污水处理厂所处地区已经形成了以纺织、食品工业为主导,机械、造纸、建材、化工等行业为支柱的工业体系,因此该污水处理厂的进水为工业废水和生活污水的混合水,且工业废水所占比例较高,造成了二级出水的COD和TP偏高,难以达到排放标准。
表1 水样水质指标检测结果与相应排放标准值
Tab.1 Results of the water quality index in wastewater and the discharge standard

检测指标测试水样GB18918—2002一级A标准pH值7.0^8.06.0^9.0ρ(COD)/(mg·L-1)267.050.0ρ(NH3-N)/(mg·L-1)4.25.0ρ(TP)/(mg·L-1)7.30.5色度/倍150.030.0
1.2 药剂和仪器
1)药剂:阴离子聚丙烯酰胺(APAM,工业级),质量分数为30%的过氧化氢(H2O2,分析纯),硫酸亚铁(FeSO4·7H2O,分析纯),浓硫酸(H2SO4,分析纯),氢氧化钠(NaOH,分析纯)。
2)仪器:PHB-2型便携式酸度计(杭州奥立龙仪器有限公司提供),FA2204B电子天平(上海仪电科学仪器股份有限公司提供),COD消解仪(汕头市环海工程总公司提供),78-1型磁力搅拌器(金坛市鑫鑫实验仪器有限公司提供),MY3000-6A-2六联混凝试验搅拌仪(潜江市梅宇仪器有限公司提供),WFJ722E型可见分光光度计(上海光谱仪器有限公司提供)。
1.3 试验方法
采用正交试验和单因素试验考察不同初始pH值、H2O2投加量、FeSO4·7H2O投加量和反应时间对芬顿氧化处理效果的影响。具体操作步骤:取污水水样250 mL,用H2SO4调节pH值,向溶液中加入一定量的FeSO4·7H2O和H2O2,在磁力搅拌器上混合搅拌反应一定时间后,用NaOH调节水样pH值到8.0~8.5,静置30 min后取上清液检测。
采用单因素试验考察不同初始pH值和APAM投加量对混凝处理效果的影响。具体操作步骤:取芬顿氧化后的污水250 mL,用NaOH调节pH值后,加入一定量的APAM,在六联混凝试验搅拌仪上以50 r/min搅拌5 min,静置30 min后取上清液检测。
2 结果与讨论
2.1 芬顿氧化正交试验
为了初步确定芬顿氧化处理污水的最佳工艺条件,以污水初始反应pH值(A)、H2O2投加量(B)、FeSO4·7H2O投加量(C)和反应时间(D)为变量,设计了四因素三水平的正交试验,其因素水平见表2,试验结果见表3。
经过对表3正交试验结果极差分析,得出4个因素对处理效果影响大小的顺序:反应时间>初始反应pH值>FeSO4·7H2O投加量>H2O2投加量。初步确定最佳反应条件为A3B2C3D3,即初始pH值为6.0,H2O2投加量(质量浓度,下同)为1 000 mg/L,FeSO4·7H2O投加量(质量浓度,下同)为600 mg/L和反应时间为60 min。
由芬顿氧化后出水的水质检测结果可知,NH3-N的去除率很低,约为4%,但该污水处理厂的二级生化出水中NH3-N的质量浓度(下同)为4.2 mg/L,已达到一级A排放标准(<5 mg/L),故在接下来的试验中不再考虑NH3-N的去除效果。

表2 正交试验因素水平表
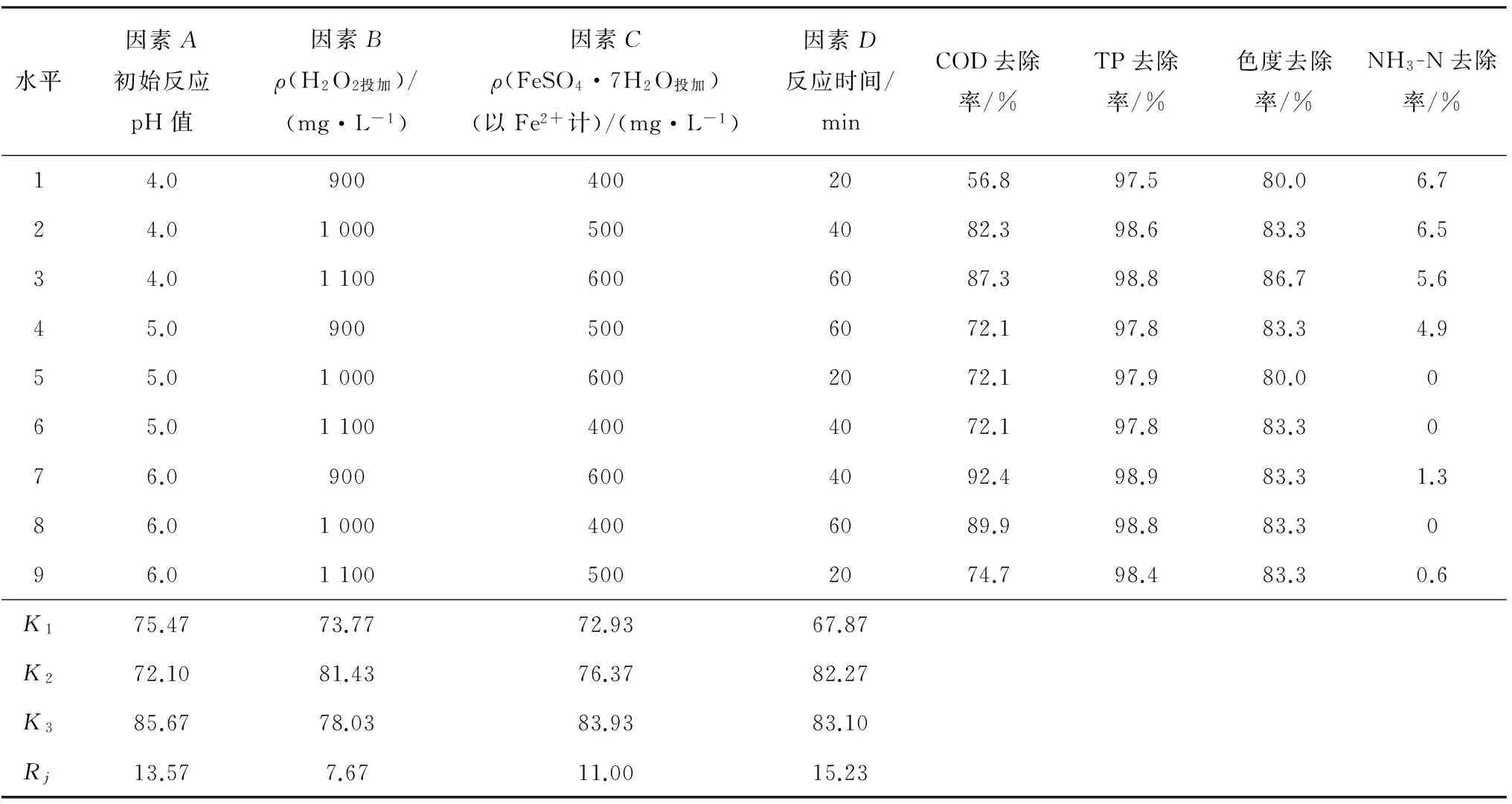
表3 正交试验结果表
注:根据COD的去除率进行试验结果分析。
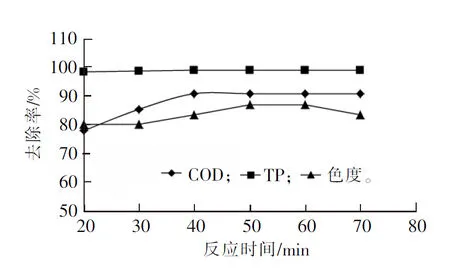
图1 反应时间对污水处理效果的影响
Fig.1 Influence of reaction time on wastewater treatment efficiency
2.2 芬顿氧化单因素试验
2.2.1 最佳反应时间的确定
根据正交试验的结果,控制初始反应pH值为6.0,H2O2投加量为1 000 mg/L,FeSO4·7H2O投加量为600 mg/L,考察反应时间分别为20,30,40,50,60和70 min时对污水去除效果的影响,试验结果见图1。
由图1可见:1)反应时间小于40 min时,COD的去除率随时间的延长而呈线性增长关系,当时间超过40 min后,趋于稳定,且在40 min时,COD去除率达到最大值90.6%,此时出水COD的质量浓度为25.3 mg/L;2)色度的去除率随时间的延长呈现先增长后降低的变化规律,在50 min时达到最大值(86.7%),但在反应时间为40 min时,出水色度达到25倍,去除率为83.3%,达到一级A排放标准;3)TP的去除效果较为明显,且随着处理时间的延长基本保持稳定,平均去除率为98.5%,出水平均值为0.1 mg/L(质量浓度,下同),这是由于Fe2+与H2O2发生反应生成Fe3+,Fe3+既与磷酸盐反应生成难溶性的盐,又发生强烈的水解反应,并在水解时发生聚合反应生成铁的络合物,通过中和、吸附架桥和卷扫等作用,使磷酸盐发生絮凝沉淀,从而将磷去除[9-11]。综合考虑确定最佳反应时间为40 min。
2.2.2 最佳初始反应pH值的确定
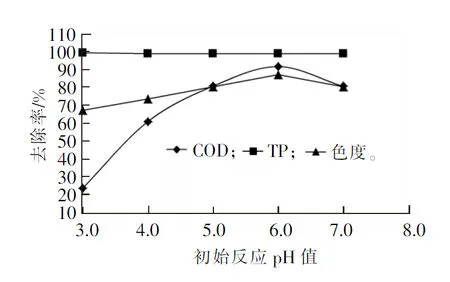
图2 初始反应pH值对污水处理效果的影响
Fig.2 Influence of initial reaction pH on wastewater treatment efficiency
根据正交试验的结果及单因素试验确定的最佳反应时间,控制反应时间为40 min,H2O2投加量为1 000 mg/L,FeSO4·7H2O投加量为600 mg/L,考察初始反应pH值为3.0,4.0,5.0,6.0和7.0时对污水处理效果的影响,试验结果见图2。
由图2可见: 1)pH值对于芬顿氧化处理效果影响显著,随pH值的增加,COD去除率呈先上升后下降的变化规律,当pH值为6.0时,COD的去除率最高,为91.2%,此时出水COD的质量浓度为23.6 mg/L。这是由于pH值很低时,H2O2稳定性高,不利于·OH的生成,同时污水中H+消耗了大量的·OH[12-13],影响了芬顿试剂氧化有机物的效果;当pH值过高时,Fe2+和Fe3+以氢氧化物的形式存在,不仅影响了Fe2+的催化能力,还抑制了·OH的生成,从而导致COD的去除率下降[14]; 2)色度的去除率随pH值的增加同样呈现先增长后降低的变化规律,在pH值为6.0时去除率达到最大值,为86.7%,出水色度为20倍;3)TP的去除率同样保持基本稳定,平均去除率为98.6%,出水TP的平均质量浓度为0.1 mg/L。综合考虑确定最佳初始反应pH值为6.0。
2.2.3 最佳FeSO4·7H2O投加量的确定
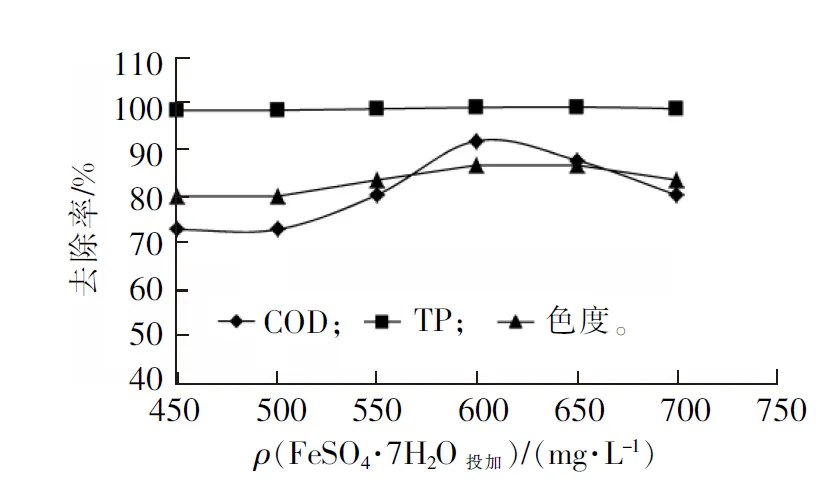
图3 FeSO4·7H2O投加量对污水处理效果的影响
Fig.3 Influence of the dose of FeSO4·7H2O on wastewater treatment efficiency
根据正交试验的结果及单因素试验确定的最佳反应时间和初始反应pH值,控制反应时间为40 min、初始反应pH值为6.0以及H2O2投加量为1 000 mg/L,考察FeSO4·7H2O投加量为450,500,550,600,650和700 mg/L时对污水处理效果的影响,试验结果见图3。
由图3可见: 1)COD去除率首先随FeSO4·7H2O投加量的增加呈现上升趋势,在投加量为600 mg/L时,去除率达到最大值(91.7%),此时出水COD的质量浓度为22.3 mg/L;随着投加量的继续增加,COD去除率下降。这是由于当Fe2+浓度较低时,产生的·OH也较少,且速率低,催化反应慢,抑制了有机物的降解过程;而Fe2+浓度过高时,Fe2+与H2O2发生反应生成Fe3+,既消耗了H2O2,又会产生大量的Fe3+,增加了出水的色度[15]; 2)色度随FeSO4·7H2O投加量的增加变化较平缓,同样在投加量为600 mg/L时,色度去除率最大(86.7%),出水色度为20倍; 3)TP的去除率随着FeSO4·7H2O投加量的增加依然保持稳定,平均去除率为98.6%,出水TP的平均质量浓度为0.1 mg/L。综合考虑确定FeSO4·7H2O最佳投加量为600 mg/L。
2.2.4 最佳H2O2投加量的确定
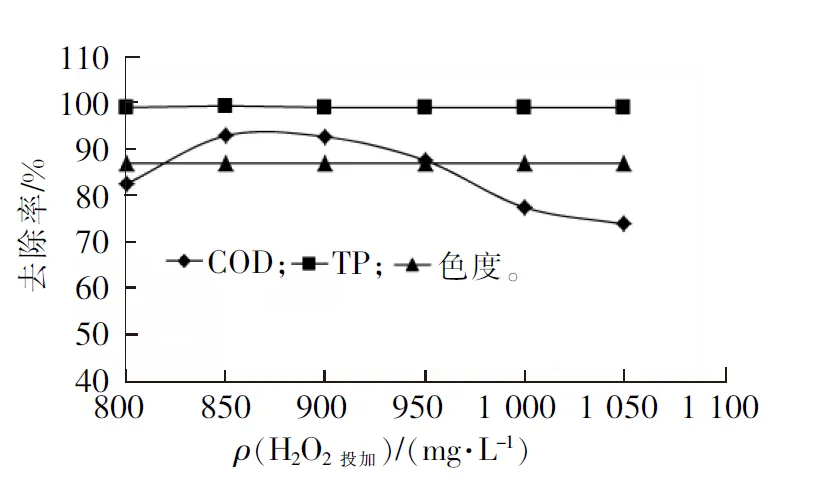
图4 H2O2投加量对污水处理效果的影响
Fig.4 Influence of the dose of H2O2on wastewater treatment efficiency
根据正交试验的结果及单因素试验确定的最佳反应时间、初始反应pH值和FeSO4·7H2O投加量,控制反应时间为40 min,初始反应pH值为6.0以及FeSO4·7H2O投加量为600 mg/L,考察H2O2投加量为800,850,900,950,1 000和1 050 mg/L时对污水处理效果的影响,试验结果见图4。
由图4可见:1)在H2O2投加量增加的初期,有利于COD的去除,当H2O2投加量为850 mg/L时,COD去除率达到最大值92.7%,其出水质量浓度为19.7 mg/L;而继续增加H2O2的投加量,COD去除率转而降低,这是由于初期H2O2投加量少,产生的·OH较少,只能使难降解的有机物结构被分解成小分子结构的物质,无法进一步矿化[16],随着H2O2投加量的增加,产生的·OH也随之增加,则氧化有机物能力增强;但由于H2O2是·OH的清除剂,并且会造成H2O2的无效分解导致氧化效果降低[19],同时多余的H2O2会干扰COD的测定,在酸性条件下,Cr6+会被多余的H2O2还原成Cr3+,影响测定结果[20]。因此,当废水中H2O2含量较高时,COD去除率降低[17-18]。2)H2O2投加量对于色度和TP均无明显影响,色度和TP的平均去除率分别维持在86.7%和98.7%,其出水色度和TP质量浓度分别为20倍和0.09 mg/L。综合考虑确定最佳H2O2投加量为850 mg/L。
2.3 混凝单因素试验
该废水经芬顿氧化后,COD虽得到去除,但出水仍呈黄绿色浑浊状,这是因为其中含有亚铁离子、胶态氢氧化铁和未被氧化的有机物,因此为了得到更好的出水水质,对芬顿氧化后的出水需进一步混凝处理。
由于H2O2和Fe2+反应生成Fe3+,而Fe3+和APAM是常用的混凝药剂。因此投加APAM可以强化芬顿氧化处理污水的效果。本组试验考察混凝阶段的最佳反应pH值和APAM投加量对芬顿氧化后出水的处理效果。
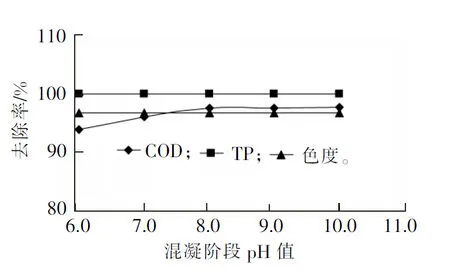
图5 反应pH值对污水处理效果的影响
Fig.5 Influence of reaction pH on wastewater treatment efficiency
2.3.1 混凝阶段最佳pH值的确定
取最佳反应条件下经芬顿氧化处理后的出水,调节水样的pH值从6.0依次增大至10.0,投加3.0 mg/L(质量浓度,下同)的APAM进行混凝试验,试验结果如图5所示。
由图5可见: 1)随着pH值的增加,COD的去除率趋于稳定,在pH值为8.0时,去除率为97.5%,出水COD的质量浓度为6.8 mg/L,此后去除率增加缓慢; 2)TP的去除率始终保持在99.0%,出水TP的质量浓度为0.07 mg/L,而色度的去除率较芬顿氧化后有较大提高,其去除率始终为96.7%,并且出水色度达到了5倍,远远高于一级A排放标准。综合考虑确定混凝阶段最佳反应pH值为8.0。
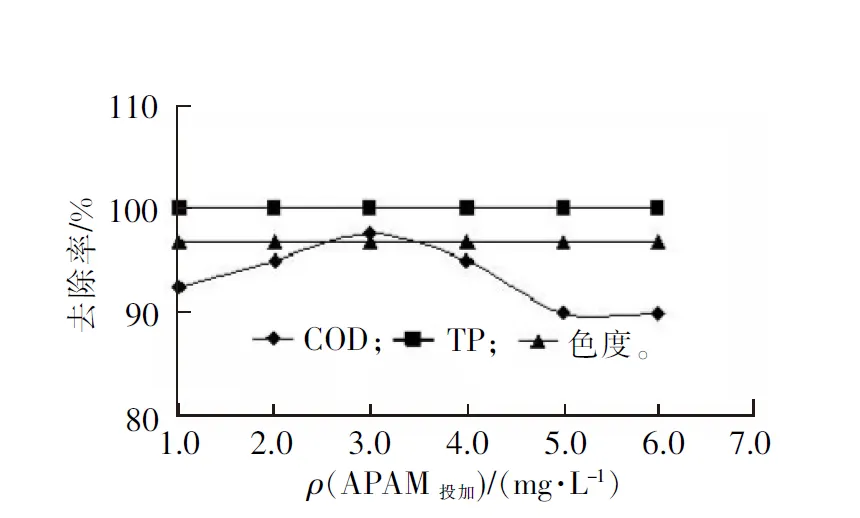
图6 APAM投加量对污水处理效果的影响
Fig.6 Influence of the dose of APAM on wastewater treatment efficiency
2.3.2 混凝阶段最佳APAM投加量的确定
根据混凝阶段单因素试验控制最佳反应pH值为8.0,考察APAM投加量为1.0,2.0,3.0,4.0,5.0和6.0 mg/L时对该污水去除效果的影响,试验结果见图6。
由图6可见: 1)COD去除率随APAM投加量的增加呈先增加、后降低的变化规律,当投加量为3.0 mg/L时,COD的去除率最高,其值为97.5%;APAM投加量的增加引起的COD去除率的变化规律说明,当APAM投加量小于3.0 mg/L时,絮凝体沉淀速度随其投加量增加而加快,废水上清液愈加清澈;当助凝剂APAM的投加量达到3.0 mg/L时,出水COD的质量浓度降至6.8 mg/L,这时COD去除率最大;当APAM的投加量超过3.0 mg/L时,COD的去除率降低,这是因为当APAM投加过量时,胶体被大量高分子链包围,使得没有过多的部位去吸附其他的分子链,即达到了饱和状态[21];2)色度和TP的去除率分别稳定保持在96.7%和99.2%,色度和TP质量浓度分别为5倍和0.06 mg/L。综合考虑确定混凝阶段的最佳APAM投加量为3.0 mg/L。
3 结 论
本研究采用芬顿氧化-混凝工艺对某城镇污水处理厂二级出水进行深度处理,通过正交试验得出芬顿氧化中各影响因素对处理效果的贡献排序(反应时间>初始反应pH值>FeSO4·7H2O投加量>H2O2投加量),在此基础上,又通过单因素试验得到该工艺的最佳反应条件:反应时间为40 min,芬顿氧化初始反应pH值为6.0,FeSO4·7H2O投加量为600 mg/L,H2O2投加量为850 mg/L,混凝反应pH值为8.0,APAM投加量为3.0 mg/L,其中混凝反应进水为芬顿氧化出水。在该条件下,污水中的COD、色度和TP的去除率分别为97.5%,96.7%和99.2%,出水各项指标均达到《城镇污水处理厂污染物排放标准》(GB 18918-2002)一级A标准。
目前由于工业化水平的提高,致使污水中难降解物质的成分越来越复杂,从而给污水处理工作增加了难度,而芬顿氧化-混凝工艺对于含有难降解物质的污水具有处理效果好、运行稳定、操作灵活方便等优点,因此可广泛应用于城镇污水处理厂对难降解污染物的深度处理。
/References:
[1] 吴琪,江乐勇,宋乾武,等.BCM城市污水深度处理技术[J].水处理技术,2013,39(3):103-106. WU Qi, JIANG Leyong, SONG Qianwu, et al. BCM urban sewage advanced treatment technology[J]. Technology of Water Treatment, 2013, 39(3): 103-106.
[2] 张志宏.废水处理中的常用高级氧化技术[J].安徽化工,2012,38(3):1-4. ZHANG Zhihong. Advanced oxidation processes frequently-used in wastewater treatment[J]. Anhui Chemical Industry, 2012, 38(3): 1-4.
[3] 李再兴,刘焕,刘艳芳,等.ClO2催化氧化处理土霉素废水处理站二级出水[J].河北科技大学学报,2013,34(4):365-369. LI Zaixing, LIU Huan, LIU Yanfang, et al. Treatment of secondary effluent of oxytetracycline wastewater treatment plant by chlorine dioxide catalytic oxidation[J]. Journal of Hebei University of Science and Technology, 2013, 34(4): 365-369.
[4] 王维,费庆志,孙承林,等.混凝-芬顿氧化处理油田含油污水[J].现代化工,2015(10):105-109. WANG Wei, FEI Qingzhi, SUN Chenglin, et al. Treatment of oilfield sewage by combination of coagulation and Fenton oxidation[J]. Modern Chemical Industry, 2015(10): 105-109.
[5] 何玉洁,陈卫,郑晓英,等.芬顿氧化PAM助凝法预处理高浓度烟草香料废水试验[J].河海大学学报(自然科学版),2012,40(5):525-529. HE Yujie, CHEN Wei, ZHENG Xiaoying, et al. Pretreatment experiment of high-concentration aromatic tobacco flavor wastewater with Fenton reagent and PAM coagulation[J]. Journal of Hohai University(Natural Sciences), 2012, 40(5): 525-529.
[6] 江传春,肖蓉蓉,杨平.高级氧化技术在水处理中的研究进展[J].水处理技术,2011,37(7):12-16. JIANG Chuanchun, XIAO Rongrong, YANG Ping. Research process of advanced oxidation processes in wastewater treatment[J]. Technology of Water Treatment, 2011, 37(7): 12-16.
[7] 白敏菂,冷宏,张启岳,等.高级氧化技术研究现状及其发展趋势[J].科技导报,2011,29(35):74-79. BAI Mindi, LENG Hong, ZHANG Qiyue, et al. Application, experimentation and development tendency of advanced oxidation processes[J]. Science & Technology Review, 2011, 29(35): 74-79.
[8] 国家环境保护总局,《水和废水监测分析方法》编委会.水和废水监测分析方法[M].3版.北京:中国环境科学出版社,1989.
[9] 刘宁,陈小光,崔彦召,等.化学除磷工艺研究进展[J].化工进展,2012,31(7):1597-1603. LIU Ning, CHEN Xiaoguang, CUI Yanzhao, et al. Research progress of chemical dephosphorization process[J]. Chemical Industry and Engineering Progress, 2012, 31(7): 1597-1603.
[10]徐丰果,罗建中,凌定勋.废水化学除磷现状与进展[J].工业水处理,2003,23(5):18-20. XU Fengguo, LUO Jianzhong, LING Dingxun. Present and prospects of the removal of phosphorus from wastewater chemically[J]. Industrial Water Treatment, 2003, 23(5): 18-20.
[11]徐国想,阮复昌.铁系和铝系无机絮凝剂的性能分析[J].重庆环境科学,2001,23(3):52-55. XU Guoxiang, RUAN Fuchang. Performance analysis of iron-based and al-based inorganic flocculants[J]. Chongqing Environment Science, 2001, 23(3): 52-55.
[12]KANG Y W, HWANG K Y. Effects of reaction conditions on the oxidation efficiency in the Fenton process[J]. Water Research, 2000, 34(10): 2786-2790.
[13]YANG Deng. Physical and oxidative removal of organics during Fenton treatment of mature municipal landfill leachate[J]. Journal of Hazardous Materials, 2007, 146(1/2): 334-340.
[14]杨亚男,陈晓轩,刘春,等.Fenton氧化深度处理制药废水的研究[J].河北科技大学学报,2015,36(6): 639-643. YANG Yanan, CHEN Xiaoxuan, LIU Chun, et al. Advanced treatment of pharmaceutical wastewater by Fenton reagent oxidation process[J]. Journal of Hebei University of Science and Technology, 2015, 36(6): 639-643.
[15]李明玉,唐启红,张顺利.无机高分子混凝剂聚合铁研究开发进展[J].工业水处理,2000,20(6):1-4. LI Mingyu, TANG Qihong, ZHANG Shunli. The research and development of inorganic polymer coagulant polyferric sulfate[J]. Industrial Water Treatment, 2000, 20(6): 1-4.
[16]YANG Deng, ENGLEHARDT J D. Treatment of landfill leachate by the Fenton process[J]. Water Research, 2006, 40(20): 3683-3694.
[17]LIU Huanhuan, CHEN Quanyuan, YANG Yu, et al. Influence of Fenton’s reagent doses on the degradation and mineralization of H-acid[J]. Journal of Hazardous Materials, 2013, 263(2): 593-599.
[18]SINGH S K, TANG W Z, TACHIEV G. Fenton treatment of landfill leachate under different COD loading factors[J]. Waste Management, 2013, 33(10): 2116-2122.
[19]杨丽云,李怡帆,孙剑辉.Fenton氧化法深度处理草浆造纸废水的研究[J].工业水处理,2010,30(11): 59-62. YANG Liyun, LI Yifan, SUN Jianhui. Study on the advanced treatment of pulp and papermaking wastewater by Fenton oxidation[J]. Industrial Water Treatment, 2010, 30(11): 59-62.
[20]陆茵,汪诚文.Fenton氧化深度处理柠檬酸生产废水[J].给水排水,2010,36(sup1):236-240. LU Yin, WANG Chengwen. Fenton oxidation of citric acid production wastewater for advanced treatment[J]. Water & Wastewater Engineering, 2010, 36(sup1): 236-240.
[21]李亚峰,杨严,王建.PAC和PAM复合混凝剂处理垃圾渗滤液的试验研究[J].工业安全与环保,2011,37(10):9-11. LI Yafeng, YANG Yan, WANG Jian. Treatment of landfill leachate by composite coagulant of polyaluminum chloride and polyacrylamide[J]. Industrial Safety and Environmental Protection, 2011, 37(10): 9-11.
Experimental study on advanced treatment of secondary effluent by Fenton oxidation-coagulation
FENG Sumin1,2, WANG Hao3, SONG Zhenyang3, BIAN Yonghuan1,2, SHAO Lirong1,2, JIN Xuekai3
(1.School of Environmental Science and Engineering, Hebei University of Science and Technology, Shijiazhuang, Hebei 050018, China; 2.Pollution Prevention Biotechnology Laboratory of Hebei Province, Shijiazhuang, Hebei 050018, China; 3.School of Civil Engineering, Hebei University of Science and Technology, Shijiazhuang, Hebei 050018, China)
In order to solve the problem of having excessive organics, total phosphorus(TP) and other pollutants in secondary effluent from municipal wastewater treatment plant, Fenton oxidation-coagulation unit is adopted to treat the wastewater. The treatment efficiency of the treatment process is discussed through the orthogonal experiments and the single factor experiments. It shows that the removal efficiency of COD, colority and TP are 97.5%, 96.7% and 99.2% respectively under the optimal reaction conditions that the Fenton oxidation reaction time is 40 min, initial pH value is 6.0, the dosage of FeSO4·7H2O and H2O2are 600 mg/L and 850 mg/L respectively,the coagulation reacting pH value is 8.0 and the dosage of APAM is 3.0 mg/L. The water quality can meet the first A level discharge standard of theDischargeStandardofPollutantsforMunicipalWastewaterTreatmentPlant(GB 18918—2002).The process, as the advanced treatment technology of wastewater, can be widely used in the advanced treatment of refractory pollutants in the municipal wastewater treatment plant.
water pollution control engineering; Fenton oxidation; coagulation; secondary effluent; advanced treatment
1008-1542(2017)01-0094-07
10.7535/hbkd.2017yx01015
2016-07-05;
2016-09-27;责任编辑:王海云
河北省科学研究计划项目(12276708D);河北省高校重点学科建设项目;河北科技大学博士科研启动基金
冯素敏(1962—),女,河北晋州人, 副教授, 主要从事水处理理论与技术方面的研究。
E-mail:fengsumin2003@sina.com
X703
A
冯素敏,王 浩,宋振扬,等.芬顿氧化-混凝深度处理二级出水试验研究[J].河北科技大学学报,2017,38(1):94-100. FENG Sumin,WANG Hao,SONG Zhenyang,et al.Experimental study on advanced treatment of secondary effluent by Fenton oxidation-coagulation[J].Journal of Hebei University of Science and Technology,2017,38(1):94-100.
