阿托伐他汀在非酒精性脂肪肝治疗中的应用价值
2017-03-03王东旭赵艳梅蔺晶晶王云莫乐君
王东旭 赵艳梅 蔺晶晶 王云 莫乐君
·论著·
阿托伐他汀在非酒精性脂肪肝治疗中的应用价值
王东旭 赵艳梅 蔺晶晶 王云 莫乐君
目的探究阿托伐他汀在非酒精性脂肪肝(NAFLD)治疗中的应用价值。方法88例NAFLD患者,按照住院号的奇偶数分为观察组和对照组,各44例。对照组给予甘草酸二铵肠溶胶囊治疗,观察组患者在对照组基础上加用阿托伐他汀治疗,比较两组患者临床症状评分、肝功能、代谢情况、不良反应、脂肪肝的程度评分情况。结果与治疗前比较,两组患者治疗后临床症状明显改善(P<0.05)。治疗后,观察组疲乏(0.46±0.35)分,肝区不适(0.67±0.35)分,腹胀(1.35±0.68)分,纳差恶心(0.59±0.55)分,明显低于对照组的(0.92±0.53)、(1.01±0.67)、(1.73±0.72)、(0.93±0.65)分(P<0.05)。与治疗前比较,两组治疗后丙氨酸氨基转移酶(ALT)、天门冬氨酸氨基转移酶(AST)、谷氨酰转移酶(GGT)、总胆红素(TB)、脂肪肝程度评分下降显著(P<0.05);两组ALT、AST、GGT、TB比较差异无统计学意义(P>0.05);观察组脂肪肝程度评分(1.16±0.38)分,明显低于对照组的(1.31±0.24)分,差异有统计学意义(P<0.05)。两组组治疗后血糖(GLU)、总胆固醇(TG)、甘油三酯(TC)、高密度脂蛋白胆固醇(HDL-C)、低密度脂蛋白胆固醇(LDL-C)改善程度明显优于治疗前,差异有统计学意义(P<0.05);且观察组患者治疗后GLU、TG、TC、HDL-C、LDL-C改善明显优于对照组,差异有统计学意义(P<0.05)。两组患者均无明显不良反应。结论阿托伐他汀治疗非酒精性脂肪肝的临床疗效显著,不良反应少,值得临床推广与应用。
阿托伐他汀;非酒精性脂肪肝;应用价值
NAFLD指除酒精和其他明确的损肝因素所致的,以弥漫性肝细胞大泡性脂肪变为主要特征的临床病理综合征。大多数患者非酒精性脂肪肝组织学表现为“单纯性脂肪肝”即脂肪肝无实质性炎症或纤维化。单纯性脂肪肝进展为肝硬化和肝功能不全风险非常低[1,2]。但有10%~30%的NAFLD患者存在或将来会发展为非酒精性脂肪性肝炎(NASH),这些患者肝脏均存在明显肝小叶炎症,甚至是纤维化,部分患者进展为肝硬化。目前随着人们生活水平日益提高,其饮食结构也发生了改变,主要以高糖、高脂、高热量饮食为主,加之工作压力大、缺乏运动,进而影响体内一系列代谢过程,促进NAFLD的形成。当前,这类病症逐年上升,对人们的身心健康构成较大的影响[3]。而阿托伐他汀为血脂调节药,可影响体内胆固醇的合成,对NAFLD有较好的治疗作用。本研究主要探讨阿托伐他汀对NAFLD的治疗价值。现将研究结果报告如下。
1 资料与方法
1.1 一般资料 选取2014年3月~2015年6月在本院消化内科住院的88例NAFLD患者,按照住院号的奇偶数分为对照组和观察组,各44例。观察组男36例,女8例;平均年龄(40.6±4.4)岁。对照组男25例,女19例;平均年龄(43.5±4.7)岁。两组患者性别、年龄、临床症状等一般资料比较,差异无统计学意义(P>0.05),具有可比性。所有患者均符合NAFLD的诊断标准[1]:①影像学或组织学检测出肝脏脂肪变性;②无饮酒史或饮酒量:女性<20 g/d,男性<30 g/d;③排除如病毒性肝炎、自身免疫性肝脏疾病以及代谢性、药物性或遗传性肝病在内的其他可导致脂肪肝的慢性肝病。所有患者入组前2个月未服用调脂药物及肝损害药物。所有患者均自愿参加,并签订知情同意书。本研究方案经玉林市第一人民医院伦理委员讨论通过。
1.2 治疗方法 两组患者均给予减重、运动、饮食干预等基础治疗;对照组患者给予甘草酸二铵肠溶胶囊(江苏正大天晴药业股份有限公司,国药准字H20040628,规格:50mg /片)口服,450mg/d,分3次服用。观察组患者在对照组治疗基础上加用阿托伐他汀(辉瑞制药有限公司,国药准字H20051407,规格:10mg/片 )治疗,10mg/d,晚餐顿服。疗程为8周。
1.3 观察指标及评价标准 主要观察两组治疗前后的临床症状评分、肝功能的变化、B超检测脂肪肝的程度评分、血糖和血脂代谢和不良反应情况。临床症状(疲乏、纳差恶心、肝区不适、腹胀)评分:0分:没有上述任何症状;1分:有轻微症状,但不影响日常工作生活;2分:日常工作生活轻微受限,稍劳累即可引起上述症状;3分:日常工作生活明显受限,休息时亦可出现上述症状。肝功能及代谢指标主要通过全自动生化分析仪检测ALT、AST、GGT、TB及GLU、TG、TC、HDL-C、LDL-C。肝脏B超检查脂肪肝的程度评分:0分:无脂肪肝;1分:轻度脂肪肝;2分:中度脂肪肝;3分:重度脂肪肝,其诊断标准参照中华医学会肝脏病学分会脂肪肝和酒精性肝病学组的诊断:①肝区近场回声弥漫性增强(强于肾脏和脾脏),远场回声逐渐衰减;②肝内管道结构显示不清;③肝脏轻至中度肿大,边缘角圆钝:④彩色多普勒血流显象提示肝内彩色血流信号减少或不易显示,但肝内血管走向正常;⑤肝右叶包膜及横膈回声显示不清或不完整。具备上述第1项及第2~4项中一项者为轻度脂肪肝;具备上述第1项及第2~4项中两项者为中度脂肪肝;具备上述第1项以及2~4项中两项和第5项者为重度脂肪肝。
1.4 统计学方法 采用SPSS22.0 统计学软件对数据进行统计分析。计量资料以均数± 标准差(±s)表示,采用t检验;计数资料以率(%)表示,采用χ2检验。P<0.05表示差异具有统计学意义。
2 结果
2.1 两组患者临床症状评分 与治疗前比较,两组患者治疗后其临床症状明显改善,差异有统计学意义(P<0.05)。治疗后,观察组疲乏(0.46±0.35)分,肝区不适(0.67±0.35)分,腹胀(1.35±0.68)分,纳差恶心(0.59±0.55)分,明显低于对照组的(0.92±0.53)、(1.01±0.67)、(1.73±0.72)、(0.93±0.65)分(P<0.05)。见表1。
2.2 两组患者肝功能及脂肪肝程度评分 与治疗前比较,两组治疗后ALT、AST、GGT、TB、脂肪肝程度评分下降显著,差异有统计学意义(P<0.05);两组ALT、AST、GGT、TB比较差异无统计学意义(P>0.05);观察组脂肪肝程度评分(1.16±0.38)分,明显低于对照组的(1.31±0.24)分,差异有统计学意义(P<0.05)。见表2。
2.3 两组患者代谢情况 两组治疗后GLU、TG、TC、HDL-C、LDL-C改善程度明显优于治疗前,差异有统计学意义(P<0.05);且观察组患者治疗后GLU、TG、TC、HDL-C、LDL-C改善明显优于对照组,差异有统计学意义(P<0.05)。见表3。
表1 两组患者临床症状评分比较(±s,分)

表1 两组患者临床症状评分比较(±s,分)
注:与治疗前比较,aP<0.05;与对照组治疗后比较,bP<0.05
组别 例数 时间 疲乏 肝区不适 腹胀 纳差恶心观察组 44 治疗前 2.34±0.76 1.96±0.85 2.26±0.70 1.34±0.68治疗后 0.46±0.35ab0.67±0.35ab1.35±0.68ab0.59±0.55ab对照组 44 治疗前 2.18±0.82 2.03±0.88 2.09±0.73 1.38±0.71治疗后 0.92±0.53a1.01±0.67a1.73±0.72a0.93±0.65a
表2 两组患者肝功能及脂肪肝程度评分比较(±s)
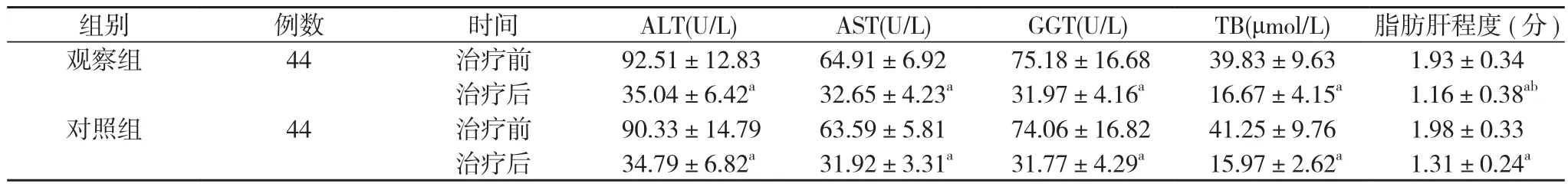
表2 两组患者肝功能及脂肪肝程度评分比较(±s)
注:与治疗前比较,aP<0.05;与对照组治疗后比较,bP<0.05
组别 例数 时间 ALT(U/L) AST(U/L) GGT(U/L) TB(μmol/L) 脂肪肝程度(分)观察组 44 治疗前 92.51±12.83 64.91±6.92 75.18±16.68 39.83±9.63 1.93±0.34治疗后 35.04±6.42a32.65±4.23a31.97±4.16a16.67±4.15a1.16±0.38ab对照组 44 治疗前 90.33±14.79 63.59±5.81 74.06±16.82 41.25±9.76 1.98±0.33治疗后 34.79±6.82a31.92±3.31a31.77±4.29a15.97±2.62a1.31±0.24a
表3 两组患者代谢情况比较(±s,mmol/L)
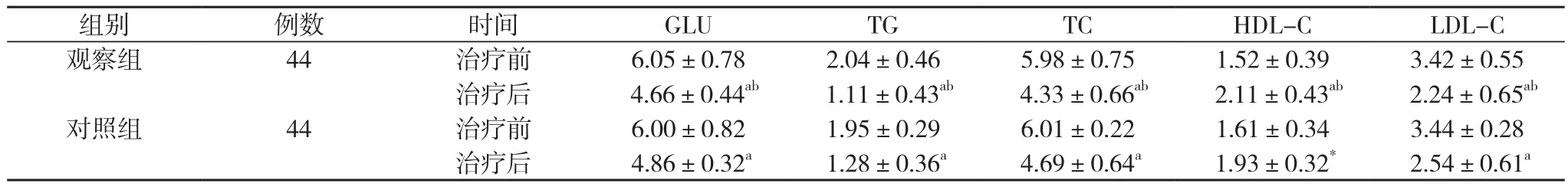
表3 两组患者代谢情况比较(±s,mmol/L)
注:与治疗前比较,aP<0.05;与对照组治疗后比较,bP<0.05
组别 例数 时间 GLU TG TC HDL-C LDL-C观察组 44 治疗前 6.05±0.78 2.04±0.46 5.98±0.75 1.52±0.39 3.42±0.55治疗后 4.66±0.44ab1.11±0.43ab4.33±0.66ab2.11±0.43ab2.24±0.65ab对照组 44 治疗前 6.00±0.82 1.95±0.29 6.01±0.22 1.61±0.34 3.44±0.28治疗后 4.86±0.32a1.28±0.36a4.69±0.64a1.93±0.32*2.54±0.61a
2.4 两组患者不良反应情况 治疗过程中,观察组有2例患者4周时出现ALT升高,但未超过正常上限值的2倍,未予特殊干预,继续观察,至该实验结束时复查患者转氨酶已明显下降;其余患者未有明显不良反应。
3 讨论
随着人们生活水平的提高,人们的饮食习惯也发生了巨大的改变。由饮食不良习惯诱发的慢性肝病也越来越多,以NAFLD最常见。该病确切的病因及发病机制目前尚未明确。临床研究显示,NAFLD与代谢紊乱综合征(如脂肪代谢紊乱、 胰岛素抵抗、 氧化应激等)密切相关[4]。另有研究发现约有20%的NAFLD患者其血TG水平和TC水平处于异常的状态[5]。NAFLD患者临床上常无自觉症状,部分患者可有明显乏力、肝区隐痛、消化不良、肝脾肿大等非特异性体征及症状。对于该病的治疗主要包括:一般治疗、药物治疗及外科手术治疗[6]。本文主要研究一般治疗及药物治疗,一般治疗即采用改变生活方式:饮食干预、减肥、增加运动量,药物方面主要采用护肝及调脂药物治疗。
甘草酸二铵是甘草酸二铵肠溶胶囊的主要成分,它是中药甘草有效成分的第三代提取物,对病毒性肝炎、 肝硬化、脂肪肝等各种因素导致的肝损害均有显著疗效。研究显示[7],甘草酸二铵在人体内可表现出类糖皮质激素样作用,能在不同程度上减轻肝细胞水肿或坏死,减少组胺的释放并抑制合成花生四烯酸、PGE等炎症介质,可显著改善肝损害患者肝功能,促进肝脏细胞生长。阿托伐他汀为他汀类强效降脂药物[8,9],属于3-羟基-3甲基戊二酰辅酶A还原酶抑制剂。其通过竞争性抑制胆固醇合成过程中的限速酶(HMG-CoA还原酶)活性,从而阻断内源性胆固醇合成,而上调细胞表面的低密度脂蛋白(LDL)受体,增加肝脏对LDL的摄取,加速血浆LDL的分解,降低TG、TC和LDL-C水平,进而防止脂质沉积。而且能升高HDL-C水平[10-14]。因此,其在降血脂稳定动脉粥样斑块以及消除肝脏脂质沉积,改善肝功能方面具有重要功能,除此之外,还可改善内皮细胞功能、促进免疫调节等,对肝细胞脂肪酸合成脂肪具有重要影响[15-18]。本研究中观察组患者通过甘草酸二胺与阿托伐他汀联合治疗,患者临床症状、代谢情况、脂肪肝的程度评分情况均得到明显改善,优于单用甘草酸二胺的对照组(P<0.05)。说明甘草酸二胺联合阿托伐他汀在NAFLD治疗中有很好的疗效。两组患者在肝功能评价指标比较差异无统计学意义(P>0.05)。说明标准剂量的阿托伐他汀不会引起肝功能损害,这与国内外的研究结果相一致[10,11]。
综上所述,阿托伐他汀类药物在NAFLD患者的治疗中安全、有效,值得临床推广使用。
[1]庞淑珍,吴爱华,蔡中起.非酒精性脂肪肝病研究进展.临床肝胆病杂志,2008,24(1):70-72.
[2]Farrell GC,Larter CZ.Nonalcoholic fatty liver disease:from steatosis to cirrhosis.Hepatology,2006,43(2 Suppl 1):S99-S112.
[3]Zhang T,Qin H,Wang T,et al.Global publication trends and research hotspots of nonalcoholic fatty liver disease:a bibliometric analysis and systematic review.Springer Plus,2015,4(1):1-9.
[4]Ahmed MH.Non-Alcoholic Fatty Liver Disease(NAFLD):new challenge for general practitioners and important burden for health authorities? Primary Care Diabetes,2010,4(3):129-137.
[5]曾正洪.阿托伐他汀钙治疗2型糖尿病血脂异常患者的临床疗效.医学临床研究,2013,15(11):2218-2219.
[6]林三仁.消化内科学高级教程.北京:人民卫生出版社,2011:361-365.
[7]董巍.甘草酸二铵在治疗急慢性肝炎中的临床疗效研究.中国医药指南,2011,9(29):239-240.
[8]曾民德.降血脂药物在脂肪肝治疗中的应用.中华肝脏病杂志,2012,8(2):116-117.
[9]张丽英.阿托伐他汀钙片治疗80例高脂血症的临床疗效分析.中国现代药物应用,2016,10(3):177-178.
[10]Foster T,Budoff MJ,Saab S,et al.Atorvastatin and antioxidants for the treatment of nonalcoholic fatty liver disease:the St Francis Heart Study randomized clinical trial.American Journal of Gastroenterology,2011,106(1):71-77.
[11]杨玲,王陶丽.阿托伐他汀治疗伴高脂血症的非酒精性脂肪肝临床观察.中国药师,2012,15(6):865-866.
[12]戴禄寿,戴益琛,江拥军,等.阿托伐他汀治疗非酒精性脂肪肝136例疗效分析.临床军医杂志,2010,38(5):774.
[13]丁海英.强肝胶囊联合阿托伐他汀治疗非酒精性脂肪肝50例.陕西中医,2013,34(5):529-530.
[14]盛雄,李洁萍,孙丹凤.阿托伐他汀钙联合硫普罗宁治疗非酒精性脂肪肝60例分析.中国现代医生,2013,51(27):77-79.
[15]李彦.阿托伐他汀治疗伴高脂血症的非酒精性脂肪肝临床分析.中国社区医师,2015(3):42-43.
[16]拜钱,王强.阿托伐他汀对非酒精性脂肪肝的疗效评价.中国基层医药,2016,23(8):1171-1174.
[17]曹蕾.阿托伐他汀对非酒精性脂肪肝的治疗研究.山东医学高等专科学校学报,2015,37(2):102-104.
[18]尤占永.阿托伐他汀联合硫普罗宁治疗非酒精性脂肪肝临床观察.医学理论与实践,2014(15):2016-2017.
Application value by atorvastatin in treatment of non-alcoholic fatty liver disease
WANG Dong-xu,ZHAO Yan-mei,LIN Jing-jing,et al.Department of Gastroenterology,Yulin City First People’s Hospital,Yulin 537000,China
ObjectiveTo investigate application value by atorvastatin in treatment of non-alcoholic fatty liver disease(NAFLD).MethodsA total of 88 NAFLD patients were divided by admission order into observation group and control group,with 44 cases in each group.The control group received diammonium glycyrrhizinate enteric-coated capsules for therapy,and the observation group also received additional atorvastatin for treatment.Comparison was made on clinical symptom score,liver function,metabolic status,adverse reactions and fatty liver degree score between the two groups.ResultsComparing with those before treatment,both groups had obviously improved clinical symptoms after treatment(P<0.05).After treatment,the observation group had fatigue score as(0.46±0.35) points,liver discomfort score as(0.67±0.35) points,abdominal distension score as(1.35±0.68) points,poor appetite and nausea score as(0.59±0.55) points,which were all much lower than(0.92±0.53),(1.01±0.67),(1.73±0.72) and(0.93±0.65) points in the control group(P<0.05).Comparing with those before treatment,both groups had obviously decreased alanine aminotransferase(ALT),aspartate aminotransferase(AST),glutamyltransferase(GGT),total bilirubin(TB) and fatty liver degree score(P<0.05).There was no statically significant difference of ALT,AST,GGT and TB between the two groups(P>0.05).The observation group had much lower fatty liver degree score as(1.16±0.38) points than(1.31±0.24) points in the control group,and the difference had statistical significance(P<0.05).Both groups had obviously better improvements of blood glucose(GLU),total cholesterol(TC),triglyceride(TG),high density lipoprotein cholesterol(HDL-C),and low density lipoprotein cholesterol(LDL-C) after treatment than those before treatment,and the difference had statistical significance(P<0.05).The observation group had all better improvements of GLU,TG,TC,HDL-C and LDL-C after treatment than the control group,and the difference had statistical significance(P<0.05).Both groups showedno obvious adverse reactions.ConclusionAtorvastatin provides precisely clinical effect in treating non-alcoholic fatty liver disease,with few adverse reactions.It is worth clinical promotion and application.
Atorvastatin; Non-alcoholic fatty liver disease; Application value
10.14164/j.cnki.cn11-5581/r.2017.01.001
2016-11-22]
537000 玉林市第一人民医院消化内科(王东旭赵艳梅 王云 莫乐君);北京王府中西医结合医院急诊科(蔺晶晶)
