中药白芷中欧前胡素、异欧前胡素体外经皮渗透特性的串联质谱研究
2017-02-21皮子凤孙云霞刘志强宋凤瑞胡秀丽韩红祥
张 琳,皮子凤,孙云霞,刘志强,宋凤瑞,胡秀丽,韩红祥
(1.吉林大学药学院,吉林 长春 130021;2.中国科学院长春应用化学研究所,长春质谱中心,吉林省中药化学与质谱重点实验室,吉林 长春 130022;3.吉林农业大学,吉林 长春 130118;4.吉林省现代中药及生物制药基地建设办公室,吉林 长春 130041)
中药白芷中欧前胡素、异欧前胡素体外经皮渗透特性的串联质谱研究
张 琳1,皮子凤2,孙云霞1,刘志强2,宋凤瑞2,胡秀丽1,韩红祥3,4
(1.吉林大学药学院,吉林 长春 130021;2.中国科学院长春应用化学研究所,长春质谱中心,吉林省中药化学与质谱重点实验室,吉林 长春 130022;3.吉林农业大学,吉林 长春 130118;4.吉林省现代中药及生物制药基地建设办公室,吉林 长春 130041)
欧前胡素和异欧前胡素属于6,7-呋喃香豆素类化合物,是中药白芷的主要药效成分。为了考察二者的经皮渗透特性,采用改进型的Franz扩散池,以大鼠离体皮肤作为渗透屏障,以高效液相色谱-串联质谱(HPLC-MS/MS)法测定白芷提取液的经皮渗透液中欧前胡素和异欧前胡素的含量,据此来考察白芷提取液中欧前胡素和异欧前胡素的经皮渗透特性。实验结果表明,欧前胡素和异欧前胡素在48 h内,单位面积的累积渗透量分别为116.11 μg/cm2和140.84 μg/cm2,累积渗透百分率分别为37.75%和71.86%。欧前胡素的稳态渗透速率为26.5 μg/h·cm2,其体外经皮渗透符合Higuchi方程。本研究阐明了欧前胡素的体外经皮渗透机制,可为白芷作为外用经皮给药制剂的发展提供实验依据和理论基础。
高效液相色谱-串联质谱(HPLC-MS/MS);白芷;欧前胡素;异欧前胡素;体外经皮渗透;Higuchi方程
中药白芷RadixAngelicaeDahuricae为伞形科植物白芷或杭白芷的干燥根,具有散风除湿、通窍止痛的功效,其有效成分主要是以欧前胡素和异欧前胡素为代表的香豆素类成分[1]。研究表明,欧前胡素和异欧前胡素均具有镇痛、抗炎、抗菌、平喘等作用[2-4],除此之外,异欧前胡素还具有明显的抗肿瘤作用[5]。白芷在外用制剂中有广泛的应用,如:白芷散敷贴用于治疗足跟痛[6];用于治疗痤疮等皮肤疾病的东风痤康凝胶剂处方中的主要成分含有白芷,主要起祛风除湿、利血脉、消肿生肌等作用[7];用于烧伤、烫伤的白芷烧伤酊,通过临床验证证明其具有抗感染、止血、收敛等疗效,能缩短病程[8];除此之外,白芷还具有美容功效,外用可以治疗黄褐斑、白癜风、痤疮等多种皮肤疾病[9]。因此,考察白芷提取液中欧前胡素和异欧前胡素的经皮渗透能力对于开发利用含白芷的经皮给药制剂具有重要意义。
目前,中药化学成分的分析方法主要有薄层色谱法(TLC)、气相色谱法(GC)和液相色谱法(LC)等,但由于中药存在成分复杂、分离困难、某些成分含量低等问题,传统的TLC、LC方法有时很难对其成分进行测定和分析。高效液相色谱-质谱联用技术(HPLC/MS)是近年来发展起来的一门综合性分析技术,它既具有液相色谱对复杂样品较强的分离能力,又具有质谱的高灵敏度、高选择性以及能够提供相对分子质量和丰富结构信息的特征,可弥补传统技术分析样品时的局限,已成为现代分析手段中必不可少的组成部分和药物研究中强有力的工具[10]。基于HPLC/MS技术发展起来的高效液相色谱-串联质谱技术(HPLC-MS/MS),其中的串联质谱技术的工作原理是根据待测化合物母离子质量数与碎片离子质量数,选择母离子-子离子对,允许符合要求的子离子进入碰撞室,碰撞结束后,只记录设定子离子信号,通过母粒子与子离子的两次选择,去除干扰离子,以此来降低化学背景,提高灵敏度[11]。近年来,串联质谱已成为一种成熟的技术,在许多领域特别是在中药学领域发挥了巨大作用。
目前,已有采用HPLC法测定白芷透皮渗透液中欧前胡素含量的研究[12-14],但还未见关于HPLC-MS/MS测定透皮渗透液中欧前胡素和异欧前胡素含量的报道。本研究拟采用HPLC-MS/MS 法测定白芷提取液的透皮渗透液中欧前胡素和异欧前胡素的含量,考察二者的体外经皮渗透特性,希望为含有白芷的经皮制剂的药效物质基础研究以及制剂质量标准的建立提供理论支撑和可行性依据。
1 实验部分
1.1 主要仪器
Xevo-TQ三重四极杆质谱仪:美国Waters公司产品,配备Acquity UPLC系统,Waters Masslynx V4.1数据工作站;Sanorius BS110S分析天平:北京赛多利斯有限公司产品;ZTY智能透皮吸收仪:巩义市予华仪器有限责任公司产品;KQ-500DE型医用数控超声波清洗器:昆山市超声仪器有限公司产品。
1.2 主要材料与试剂
白芷:购自长春市宏检大药房,经长春中医药大学王淑敏教授鉴定;欧前胡素对照品(批号:140602)、异欧前胡素对照品(批号:140327):纯度均为98%,上海融禾医药科技有限公司产品;甲醇(色谱纯):美国Thermo-Fisher公司产品。
1.3 实验动物
7只清洁级SD大鼠,雄性,其质量为(200±20) g,由吉林大学实验动物中心提供。
1.4 实验条件
1.4.1 色谱条件 色谱柱:Diamonsil C18柱(4.6 mm×250 mm,5 μm);流动相:甲醇-水溶液(80∶20,V/V);流速:0.8 mL/min;柱温:35 ℃。
1.4.2 质谱条件 电喷雾电离源,正离子模式(ESI+),多反应监测模式(MRM);毛细管电压4.0 kV;离子源温度150 ℃;脱溶剂气:N2,温度500 ℃,流速650 L/h;锥孔气流速50 L/h;碰撞气:氩气,压力0.15 Pa。欧前胡素和异欧前胡素的裂解电压、碰撞能量以及扫描离子片段列于表1。
1.5 白芷提取液的制备与测定
1.5.1 白芷提取液的制备 称量250 g白芷,粉碎成细粉,混合均匀,加入8倍质量浓度为80%(体积分数)的乙醇回流提取2次,每次2 h,过滤,合并滤液,减压浓缩至相对密度为1.0~1.2(50 ℃),即得白芷提取液。
1.5.2 白芷提取液中化学成分含量的测定
取1 mL制得的白芷提取液,于50 ℃烘箱中烘干,然后加入1 mL甲醇,超声溶解,过0.45 μm滤膜,即得待测液。以HPLC-MS/MS法测得白芷提取液中欧前胡素的含量为2.2 g/L,异欧前胡素的含量为0.98 g/L。
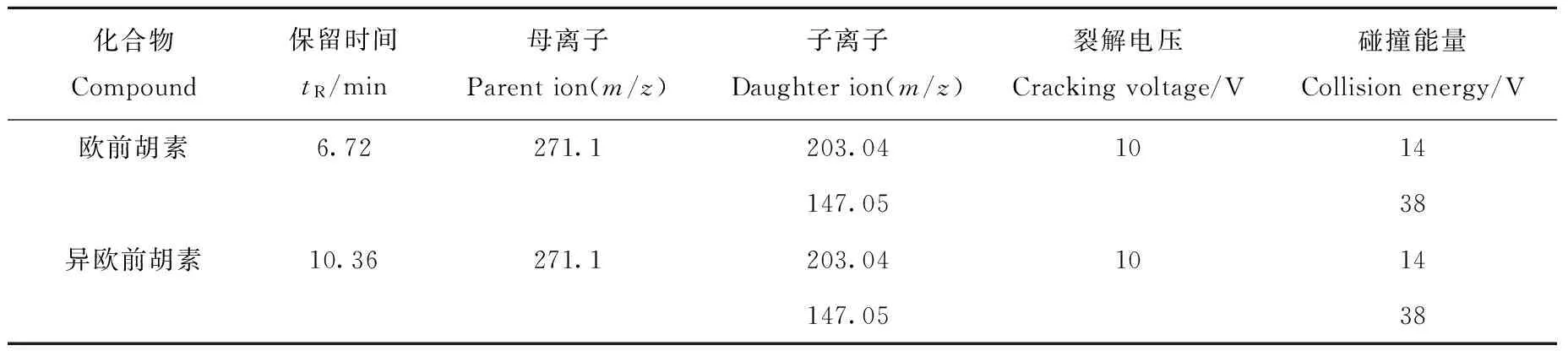
表1 欧前胡素和异欧前胡素的多反应监测条件Table 1 HPLC-MS/MS MRM conditions of imperatorin and isoimperatorin
1.6 透皮吸收实验
1.6.1 经皮吸收扩散装置 经皮吸收扩散装置由上下两室对合而成,上室为扩散室,下室为接受室,将皮肤固定于两室中间。在接受室的侧部连有一个取样管,供取样、补充接受液和排除气泡用,渗透面积为1.13 cm2,实验中以多功能电磁搅拌器维持接受室动态环境,实验温度维持(37.0±0.5) ℃。
1.6.2 离体鼠皮的制备 取(200±20) g的雄性大鼠,用脱毛膏脱毛,然后处死动物,分离腹部皮肤,小心剥离皮下脂肪,用生理盐水反复洗净,备用。
1.6.3 实验方法 将处理好的动物皮肤固定在渗透扩散装置的扩散室与接受室之间,在接受室中注入20.0 mL生理盐水,液面恰与皮肤内层接触且没有气泡。开动电磁搅拌器,保持恒温下恒速搅拌,取0.05 mL已制备的白芷提取液涂于皮肤上,用保鲜膜封口,分别在1、2、4、8、12、24 h取1.0 mL样品于小瓶中,每次取样后均立即补加相同体积的新鲜生理盐水,并排除接受室中的气泡,计算每次实验的单位面积累积渗透量(Q)。
1.6.4 透皮接收液的处理 将装有透皮接收液的小瓶于50 ℃烘箱烘干,加入1 mL甲醇超声溶解,经0.45 μm微孔滤膜过滤,然后采用HPLC-MS/MS法测定滤液中的欧前胡素、异欧前胡素的含量,按式(1)计算单位面积的累积渗透量Q(μg/cm2)。
Q=(CnV+Vr∑Cp)/A
(1)
式中,Cn为第n个取样点实际测得的药物浓度(g/L);∑Cp为该取样点前各点的药物测定浓度之和(g/L);V为接受液的体积(mL);Vr为取样体积(mL);A为渗透面积(cm2)。
2 结果与讨论
2.1 欧前胡素和异欧前胡素定性、定量信息的确定
将浓度为10 mg/L的欧前胡素、异欧前胡素标准溶液分别以直接进样的方式注入质谱仪中,在m/z50~300扫描范围内,以正离子模式对其进行一级质谱全扫描,以确定欧前胡素、异欧前胡素分子的[M+H]+峰;以分子离子峰为母离子,对离子源参数进行优化,使质谱仪的测定灵敏度达到最高;然后在一定的碰撞能量下对欧前胡素、异欧前胡素的子离子进行全扫描,以确定其主要的离子碎片,其二级质谱扫描图示于图1。由图1可见,欧前胡素、异欧前胡素均可产生m/z147.05和m/z203.04两个主要的碎片离子,结合样品空白基质的质谱图选取离子丰度最高、本底干扰最小的m/z271. 1→203.04为定量离子对,m/z271. 1→147. 05为定性离子对。
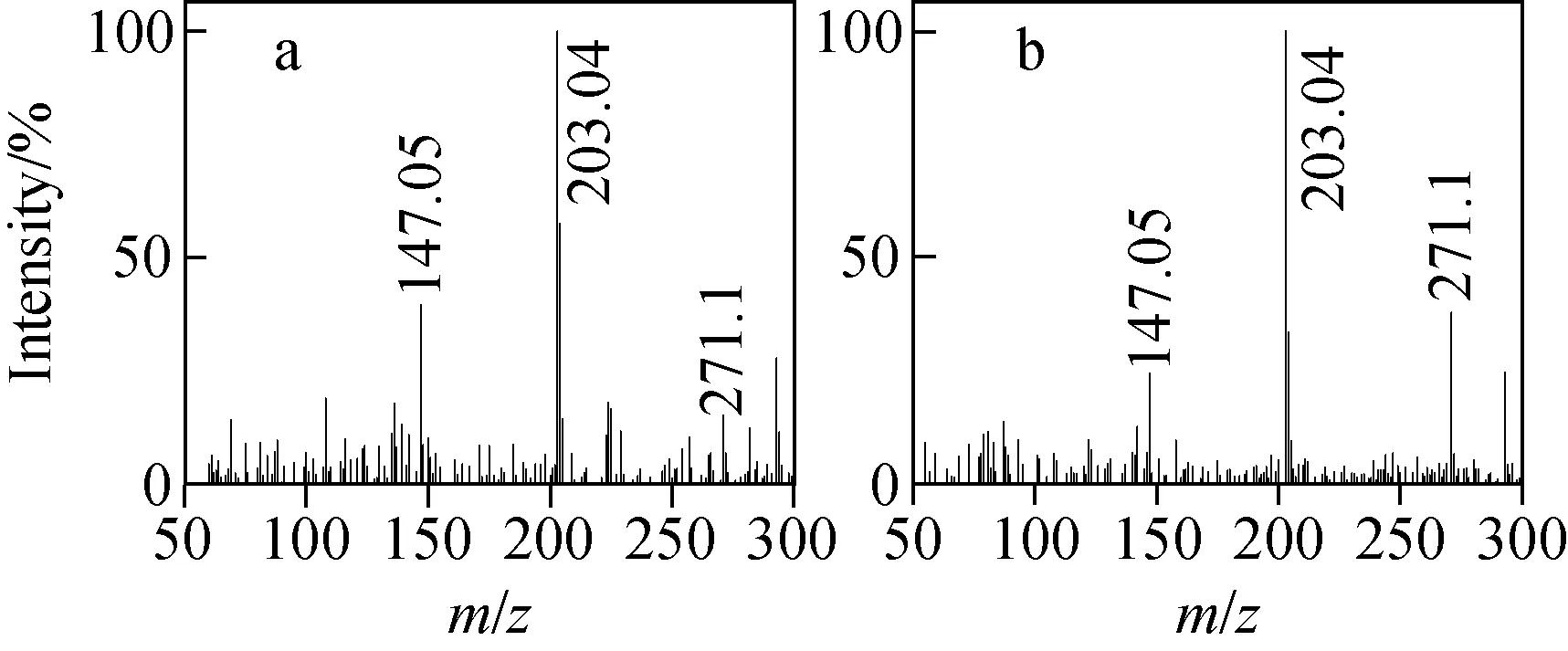
图1 欧前胡素(a)和异欧前胡素(b)准分子离子[M+H]+的子离子全扫描质谱图Fig.1 Full scan product ion spectra of imperatorin (a) and isoimperatorin (b) parent ion [M+H]+
2.2 方法学考察
2.2.1 专属性考察 分别取空白透皮接收液、欧前胡素对照液、异欧前胡素对照液、白芷提取液、白芷透皮接收液,按照1.4节条件进行测定。欧前胡素的保留时间约为6.72 min,异欧前胡素的保留时间约为10.36 min,空白透皮接收液中未检测到欧前胡素和异欧前胡素。各样品的HPLC-MS/MS色谱图示于图2。

注:a.空白透皮接收液;b.欧前胡素对照液;c.异欧前胡素对照液;d.白芷提取液;e.白芷透皮接收液图2 5种样品溶液的HPLC-MS/MS色谱图Fig.2 HPLC/MS/MS chromatograms of 5 samples
2.2.2 标准曲线的制备 将1 g/L的对照品储备液用甲醇逐级稀释,得到系列对照品溶液,其中欧前胡素的质量浓度分别为0.001、0.0025、0.01、0.05、0.1、0.2、1 mg/L;异欧前胡素的质量浓度分别0.001、0.002 5、0.01、0.02、0.05、0.1、1 mg/L。按照1.4节条件进行测定。分别以欧前胡素、异欧前胡素的峰面积(y)为纵坐标,欧前胡素、异欧前胡素的质量浓度(x)为横坐标,进行线性回归,得到线性方程;向空白透皮接收液中添加对照品,分别以10倍信噪比(S/N=10)和3倍信噪比(S/N=3)计算欧前胡素和异欧前胡素的方法定量限(LOQ)和方法检出限(LOD)。结果表明,欧前胡素和异欧前胡素在0.001~1 mg/L范围内呈现良好的线性关系,其线性方程、相关系数、检出限和定量限结果列于表2。

表2 HPLC-MS/MS方法的线性方程、相关系数、检出限和定量限Table 2 Linear equations, correlation coefficients (r2), limits of detection (LOD) and limits of quantitation (LOQ) of HPLC-MS/MS
2.2.3 精密度、稳定性、重复性和加样回收率的考察 通过对欧前胡素和异欧前胡素进行精密度、稳定性(24 h内)、重复性(日内重复性和日间重复性)实验,结果表明,欧前胡素和异欧前胡素的精密度、稳定性RSD值均小于2%,说明本方法精密度良好,且在24 h内供试品溶液保持稳定。
重复性实验结果显示,欧前胡素和异欧前胡素的日内重复性RSD值均小于2%,日间重复性RSD值均小于4% ,说明本方法的重复性良好。
欧前胡素和异欧前胡素的加样回收率实验结果分别列于表3、表4。

表3 欧前胡素的加样回收率(n=6)Table 3 Recoveries of imperatorin (n=6)

表4 异欧前胡素的加样回收率(n=6)Table 4 Recoveries of isoimperatorin (n=6)
2.2.4 基质效应的考察 配制高、中、低(20、40、80 g/L)3个浓度的欧前胡素和异欧前胡素标准样品各20 μL,置于小EP管中。分别以180 μL基质(空白透皮接收液)和甲醇作为溶剂稀释,涡旋混合均匀,制得加入基质组和未加基质组样品溶液,每个浓度各做3个样本。将加入基质的标准样品浓度与未加基质的标准样品浓度检测结果相比,如果比值为1,证明基质无影响,否则说明存在基质效应。实验结果显示,欧前胡素高、中、低组的基质效应分别为0.95±0.05、1.04±0.14、0.99±0.11;异欧前胡素高、中、低组的基质效应分别为1.07±0.08、1.04±0.10、1.05±0.05,比值都接近1,说明基质对欧前胡素和异欧前胡素检测的影响很小,不影响其准确测定。
2.3 透皮实验结果
分别以单位面积累积渗透量Q、累积渗透百分率Q%为纵坐标,以时间t为横坐标,绘制48 h内Q-t渗透动力学曲线,示于图3。

注:a.欧前胡素Q-t曲线;b.异欧前胡素Q-t曲线;c.欧前胡素Q%-t曲线;d.异欧前胡素Q%-t曲线 图3 欧前胡素和异欧前胡素的Q-t、Q%-t渗透动力学曲线(n=3)Fig.3 Q-t and Q%-t permeation kinetics curves of imperatorin and isoimperatorin (n=3)
由图3可知,欧前胡素在1 h后即开始经皮渗透,而异欧前胡素在12 h后才开始。在48 h处,欧前胡素的累积渗透百分率为37.75%,而异欧前胡素的累积渗透百分率为71.86%。该结果说明,异欧前胡素经皮渗透虽然开始的时间较晚,但其48 h的累积渗透百分率远远高于欧前胡素。
对欧前胡素的体外经皮渗透行为分别进行零级方程、一级方程和Higuchi方程拟合,其结果列于表5。
累积渗透量采用式(1)计算,稳态渗透速率为最优拟合方程的斜率,滞后时间为Q=0时计算得到的t值。经计算,欧前胡素的各体外渗透相关参数列于表6。

表5 欧前胡素的体外经皮渗透行为的拟合方程(n=3)Table 5 In vitro cumulative release fitting equation of imperatorin

表6 欧前胡素的体外渗透相关参数Table 6 Relative parameters of imperatorin in vitro
由表5中相关系数的大小可知,欧前胡素的体外经皮渗透行为更接近于Higuchi方程(r=0.982 3)。表6中体外渗透各相关参数反应了欧前胡素的经皮渗透特点,稳态渗透速率反应了欧前胡素的经皮渗透速度,滞后时间则表明欧前胡素在大鼠皮肤滞留的时间,说明其在0.233 5 h以后开始经皮渗透。
3 结论
本实验采用HPLC-MS/MS 法考察白芷提取液中欧前胡素和异欧前胡素的经皮渗透能力。结果表明,二者均具有经皮渗透的能力,欧前胡素的经皮渗透起始时间明显早于异欧前胡素,但在检测的48 h中,异欧前胡素的累积渗透百分率远远高于欧前胡素。欧前胡素和异欧前胡素的累积渗透量均随时间的延长而增加,两种成分的累积渗透量在48 h后仍未完全达到稳态,表明欧前胡素和异欧前胡素具有经皮给药释药缓慢的特点。欧前胡素的释药曲线经拟合后与Higuchi模型基本吻合,表明其释放主要遵循扩散控制机理,能以稳定速率释放。本实验可为后续将欧前胡素和异欧前胡素制成经皮给药制剂提供理论基础和可行性依据。
[1] 白洁,陆洋,杜守颖,等. 欧前胡素体外经皮渗透研究[J]. 中国中药杂志,2013,38(16):2 605.
BAI Jie, LU Yang, DU Shouying, et al. Study oninvitropenetration of imperatorin[J]. China Journal of Chinese Materia Medica, 2013, 38(16): 2 605(in Chinese).
[2] 连其深,胡晓,上官珠,等. 蛇床子素镇静作用的研究[J]. 中药新药与临床药理,2000,11(4):244.
LIAN Qishen, HU Xiao, SHANGGUAN Zhu, et al. Study on sedative effect of Osthole[J]. Traditional Chinese Drug Research and Clinical Pharmacology, 2000, 11(4): 244(in Chinese).
[3] 杨小花,胡晓. 欧前胡素与异欧前胡素的药理学研究进展[J]. 南昌大学学报:医学版,2012,52(3):95-100.
YANG Xiaohua, HU Xiao. Pharmacology research progress of imperatorin and isoimperatorin[J]. Journal of Nanchang University(Medical Science), 2012, 52(3): 95-100(in Chinese).
[4] NGWENDSON J N, BEDIR E, EFANGE S M, et al. Constituents ofPeucedanumzenkeriseeds and their antimicrobial effects[J]. Pharmazie, 2003, 58(8): 587-589.
[5] 王梦月,贾敏如,马逾英,等. 白芷中四种线型呋喃香豆素类成分药理作用研究[J]. 天然产物研究与开发,2010,22(3):485-489.
WANG Mengyue, JIA Minru, MA Yuying, et al. Pharm acological effect of four linear furocoum arins inRadixAngelicaeDahuricae[J]. Natural Product Research and Development, 2010, 22(3): 485-489(in Chinese).
[6] 贾小靖,杨月青. 白芷散敷贴治疗足跟痛56例临床观察[J]. 临床医药实践,2012,21(7):557-558.
JIA Xiaojing, YANG Yueqing. Heel pain 56 cases ofAngelicadahuricapowder sticking treatment clinical observation[J]. Proceeding of Clinical Medicine, 2012, 21(7): 557-558(in Chinese).
[7] 樊东升,曹学东,刘春泉. 东风痤康凝胶剂的质量控制[J]. 中国药物与临床,2014,14(7):909-910.
PAN Dongsheng, CAO Xuedong, LIU Chunquan. The quality control of Dongfeng Cuokang gel[J]. Chinese Remedies and Clinics, 2014, 14(7): 909-910(in Chinese).
[8] 王文凯,袁宏伟. 白芷烧伤酊的研制与应用[J]. 河南中医,2000,20(5):61.
WANG Wenkai, YUAN Hongwei. The development and application ofAngelicadahuricaburntincture[J]. Henan Traditional Chinese Medicine, 2000, 20(5): 61(in Chinese).
[9] 周典,张建华,李华,等. 白芷不同提取物对黑色素影响的比较研究[J]. 上海中医药大学学报,2007,21(5):72-75.
ZHOU Dian, ZHANG Jianhua, LI Hua, et al. Comparative study on effects of different extracts fromAngelicadahuricaon melanin[J]. Acta Universitatis Traditionis Medicalis Sinensis Pharmacologiaeque Shanghai, 2007, 21(5): 72-75(in Chinese).
[10]张莉,张丽萍,孙成春. 液-质联用技术在中药研究中的应用[J]. 解放军药学学报,2010,26(6):558.
ZHANG Li, ZHANG Liping, SUN Chengchun. Application of liquid-mass spectrometry in traditional Chinese medicine research[J]. Pharmaceutical Journal of Chinese People’s Liberation Army, 2010, 26(6): 558(in Chinese).
[11]陈晓水,侯宏卫,边照阳,等. 气相色谱-串联质谱(GC-MS/MS)的应用研究进展[J]. 质谱学报,2013,34(5): 308-320.
CHEN Xiaoshui, HOU Hongwei, BIAN Zhaoyang, et al. Research progress on application of GC-MS/MS[J]. Journal of Chinese Mass Spectrometry Society, 2013, 34(5): 308-320(in Chinese).
[12]刘聪敏,白洁,杜守颖,等. 止痛凝胶膏剂体外透皮行为研究[J]. 中国中药杂志,2013,38(16):2 609-2 613.
LIU Congmin, BAI Jie, DU Shouying, et al. Study on transdermal behavior ofZhitongcataplasm[J]. China Journal of Chinese Materia Medica, 2013, 38(16): 2 609-2 613(in Chinese).
[13]卢闻,贺浪冲. 白芷香豆素类有效部位体外透皮特性研究[J]. 中国药学杂志,2003,38(12):45-47.
LU Wen, HE Langchong. Study on the transdermal permeability of coumarins inRadixAngelicaDahuricainvitro[J]. China Pharmaceutical Journal, 2003, 38(12): 45-47(in Chinese).
[14]章烨雯,王琼,于竞新,等. 止痛微乳凝胶膏的制备及体外评价[J]. 北京中医药大学学报,2015,38(4):253-259,291.
ZHANG Yewen, WANG Qiong, YU Jingxin, et al. Preparation and in vitro evaluation of analgesic microemulsion cataplasm[J]. Journal of Beijing University of Traditional Chinese Medicine, 2015, 38(4): 253-259, 291(in Chinese).
In Vitro Percutaneous Permeability of Imperatorin and Isoimperatorin inRadixAngelicaeDahuricaeby Tandem Mass Spectrometry
ZHANG Lin1, PI Zi-feng2, SUN Yun-xia1, LIU Zhi-qiang2, SONG Feng-rui2, HU Xiu-li1, HAN Hong-xiang3,4
(1.SchoolofPharmaceuticalSciences,JilinUniversity,Changchun130021,China;2.NationalCenterforMassSpectrometryinChangchun,JilinProvinceKeyLaboratoryofChineseMedicineChemistryandMassSpectrometry,Changchun130022,China;3.JilinAgriculturalUniversity,Changchun130118,China; 4.JilinProvinceTraditionalChineseMedicineOffice,Changchun130041,China)
Imperatorin and isoimperatorin are 6,7-furocoumarin compounds, which are the major medicinal effective ingredients ofRadixAngelicaeDahuricae. Coumarin compounds are widely used in topical formulations because it has many properties, such as anti-bacterial, anti-inflammatory, antipyretic and analgesic effects. At present, the chemical components of traditional Chinese medicine are mainly analyzed by thin layer chromatography (TLC), gas chromatography (GC) and high performance liquid chromatography (HPLC). However, because there are some difficulties in Chinese medicine analysis, such as complex composition, difficulty in separation and low content, traditional methods (TLC, HPLC, etc.) were difficult to determine and analyze the composition sometimes. HPLC/MS is a comprehensive technique, it has become an important modern separation and analysis technique because of its high separation ability, high sensitivity, wide application range and strong specificity. Tandem mass spectrometry (MS/MS) has higher sensitivity and selectivity than unipolar mass spectrometry and can obtain more structural information. In this study, the in vitro percutaneous permeability of imperatorin and isoimperatorin inRadixAngelicaeDahuricaelextracting solution was evaluated by the modified Franz diffusion cell with isolated rat skin. The content of imperatorin and isoimperatorin was determined by high performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS). The chromatographic conditions were as follows: Dimonsil C18 column (250 mm×4.6 mm, 5 μm), the temperature of column is 35 ℃, mobile phase was methanol-water (80∶20,V/V) and flow rate was 0.8 mL/min. A tandem mass spectrometer coupled with positive electro-spray ionization (ESI) source was used for detection. The quantitative and qualitative analysis were performed on selective ion chromatograms acquired by a multiple reaction monitoring (MRM) mode of following transitions:m/z271.1→m/z203.04,m/z271.1→m/z147.05. The results showed that the limits of detection (LODs) of imperatorin and isoimperatorin were 0.01 and 1 μg/L, and the limits of quantification (LOQs) of imperatorin and isoimperatorin were 0.25 and 2 μg/L, respectively. Calibration curves were linear over the range of 0.001-1 mg/L for imperatorin and isoimperatorin. Both the inter-day and intra-day reproducibility (RSDs) were lower than 4%, the precision and stability of the method were lower than 2%, which indicated that the method has good precision, and the test solution could keep steady within 24 h. The mean recoveries of imperatorin and isoimperatorin were 98.09% and 100.60%. The cumulative permeation amounts of imperatorin and isoimperatorin were 116.11 μg/cm2and 210.06 μg/cm2and the percentage of cumulative permeation were 37.75% and 71.86%, respectively. The steady state permeation rate of imperatorin was 26.5 μg/h·cm2and its in vitro percutaneous permeabilities was conformed to Higuchi equation. This study clarified the percutaneous permeation mechanism of imperatorin in vitro and provided a theoretical basis for the development ofRadixAngelicaeDahuricaeas a topical transdermal preparation.
high performance liquid chromatography-tandem mass spectrometry (HPLC-MS/MS); imperatorin; isoimperatorin;RadixAngelicaeDahuricae; in vitro percutaneous permeability; Higuchi equation
2016-08-16;
2016-11-23
吉林省科技发展计划项目(20140311096YY)资助
张 琳(1991—),女(汉族),吉林四平人,硕士研究生,药学专业。E-mail: zhanglin14@mails.jlu.edu.cn
皮子凤(1978—),女(汉族),山西运城人,副研究员,从事中药活性成分筛选及代谢研究。E-mail: mslab21@ciac.ac.cn;韩红祥(1983—),男(汉族),吉林长岭人,助理研究员,从事中药有效成分的分析研究。E-mail: hanhongxiang@163.com
O657.63
A
1004-2997(2017)01-0037-08
10.7538/zpxb.2017.38.01.0037
