沙棘总黄酮-聚乙烯吡咯烷酮K30固体分散体的制备、表征及体外溶出研究
2017-02-18贺敬霞尹蓉莉杨军宣成都中医药大学药学院成都637重庆医科大学中医药学院重庆40006
田 茜,何 晨,贺敬霞,尹蓉莉#,杨军宣,张 礼(.成都中医药大学药学院,成都 637;.重庆医科大学中医药学院,重庆 40006)
沙棘总黄酮-聚乙烯吡咯烷酮K30固体分散体的制备、表征及体外溶出研究
田 茜1*,何 晨1,贺敬霞1,尹蓉莉1#,杨军宣2,张 礼1(1.成都中医药大学药学院,成都 611137;2.重庆医科大学中医药学院,重庆 400016)
目的:制备沙棘总黄酮(TFH)-聚乙烯吡咯烷酮K30(PVP K30)固体分散体,并对其进行表征及体外溶出研究。方法:采用溶剂法制备不同药载比(1∶1、1∶2、1∶3、1∶4、1∶5)的TFH-PVP K30固体分散体,以溶出参数Td为指标设计单因素试验筛选药载比,以体外溶出度为指标设计正交试验优选制备工艺中的超声时间、水浴温度和干燥时间,并进行验证。采用扫描电镜法(SEM)、差示扫描量热法(DSC)和傅里叶红外光谱法(FT-IR)对固体分散体进行表征。结果:药载比为1∶3时TFH-PVP K30固体分散体的Td最小;最优工艺为超声时间10 min、水浴温度60℃、干燥时间12 h。以此工艺制备的TFH-PVP K30固体分散体90 min的累积溶出度平均值为90.22%(RSD=1.74%,n=3)。SEM、DSC与FT-IR结果表明,TFH以无定形分散在PVP K30载体中,二者之间形成氢键。结论:成功制得TFH-PVP K30固体分散体,其体外溶出度明显提高。
沙棘总黄酮;聚乙烯吡咯烷酮K30;固体分散体;溶出度;正交试验;表征
沙棘(Hippophae rhamnoides L.)为胡颓子科植物沙棘的干燥成熟果实,其味酸、涩,性温[1],具有抗心肌缺血、抗心律失常、提高耐缺氧能力、降低血清胆固醇等药理功效[2],是药食同源的中药材之一,含有丰富的营养物质与生物活性成分。沙棘总黄酮(Total flavonoids of Hippophae rhamnoides,TFH)是沙棘的主要有效成分,能够有效治疗心脑血管疾病。但TFH极微溶于水,导致其体外溶出度低,影响口服生物利用度,限制了其临床应用[3]。固体分散(Solid dispersion,SD)技术是将难溶性药物以分子、无定形或微晶状态高度分散在载体材料中的新型制剂技术,可显著提高难溶性药物的体外溶出速率,进而改善其生物利用度[4-10]。本研究采用溶剂法制备TFH-聚乙烯吡咯烷酮K30(PVP K30)固体分散体,考察其体外溶出度,利用正交试验优化其制备工艺,并用多种分析方法表征药物在固体分散体中的存在状态,为开发TFH新剂型提供依据。
1 材料
1.1 仪器
ZRS-8G型智能溶出试验仪(天津天大天发科技有限公司);DGG-9240型电热恒温鼓风干燥箱(上海森信实验仪器有限司);UV-1102型紫外分光光度计(上海天美科学仪器有限公司);PerkinElmer DSC 4000型差示量热扫描(DSC)仪和Spectrum 100型傅里叶红外光谱(FTIR)仪(美国珀金埃尔默仪器有限公司);6390 LV型扫描电镜(SEM,日本电子公司)。
1.2 药品与试剂
芦丁对照品(中国食品药品检定研究院,批号:100080-201202,纯度:≥98%);TFH原料药[南京欣厚生物科技有限公司,纯度:≥85%(以芦丁计)];三氯化铝、氢氧化钠、磷酸二氢钾、PVP K30(成都市科龙化工试剂厂);其他试剂为分析纯,水为蒸馏水。
2 方法与结果
2.1 TFH-PVPK30固体分散体的制备
采用溶剂法制备TFH-PVP K30固体分散体。按1∶1、1∶2、1∶3、1∶4、1∶5的质量比称取TFH原料药与PVP K30载体适量,分别溶解于适量无水乙醇中,将原料药溶液缓慢加入载体溶液,充分搅拌,并超声5 min使混匀。置于50℃旋蒸除去大部分无水乙醇,转移至恒温水浴50℃中,继续加热并搅拌直至完全除去无水乙醇。将所得产物置于60℃下干燥12 h,然后转移至干燥器中平衡48 h,粉碎,过80目筛,即得TFH-PVP K30固体分散体,备用。
2.2 TFH-PVPK30物理混合物的制备
按照“2.1”项下同样比例称取TFH原料药和PVP K30载体,分别过80目筛,置于研钵混匀,即得TFHPVP K30物理混合物,置于干燥器中备用。
2.3 体外溶出度的测定
2.3.1 检测波长的选择 称取芦丁对照品、TFH原料药适量,用无水乙醇溶解,分别加入1%三氯化铝无水乙醇溶液1 mL,摇匀,无水乙醇定容,制备成一定质量浓度的溶液,放置20 min。以空白试剂为对照,在200~800 nm波长范围内进行扫描。结果显示,芦丁对照品溶液与TFH原料药供试品溶液均在430 nm波长处有最大吸收(排除末端吸收峰干扰);同法测得PVP K30在该波长处无吸收,对TFH测定无干扰。故选择430 nm为检测波长。
2.3.2 方法学考察 精密称取芦丁对照品适量,置于50 mL量瓶中,加无水乙醇制成108µg/mL的对照品溶液。分别精密量取上述对照品溶液1、1.5、2.5、3、3.5、4.5、5 mL,置于25 mL量瓶中,各加入1%三氯化铝无水乙醇溶液1 mL,摇匀,无水乙醇定容,放置20 min。以空白试剂为参比,在430 nm波长处测定吸光度(A)。以芦丁质量浓度(c)为横坐标、A为纵坐标,进行回归分析,得回归方程为A=0.035 3c+0.005 9(r=0.999 9)。结果表明,芦丁检测质量浓度的线性范围为4.32~21.6µg/mL。其余方法学考察结果均符合相关规定。
2.3.3 体外溶出度试验 按照2015年版《中国药典》(四部)0931溶出度测定第二法(桨法)[11],设定转速为75 r/min、温度为(37±0.5)℃、溶出介质为900 ml pH 7.4磷酸盐缓冲液(经脱气处理),依法操作。
2.4 单因素试验筛选药载比
取适量TFH原料药及含等量TFH的不同药载比(1∶1、1∶2、1∶3、1∶4、1∶5)的TFH-PVP K30固体分散体和1∶3的TFH-PVP K30物理混合物,以药物粉末接触溶出介质液面时开始计时,分别于5、10、15、30、45、60、90 min时取样5 mL,同时补加等温等量溶出介质。溶出液经0.45 μm微孔滤膜滤过后适当稀释,按“2.3.2”项下方法测定吸光度,计算累积溶出度,绘制溶出曲线。采用Origin 8.5软件将溶出度数据进行威布尔(Weibull)模型拟合得到相关系数(R2),并回归计算溶出参数Td[12]。溶出曲线见图1,溶出参数见表1。
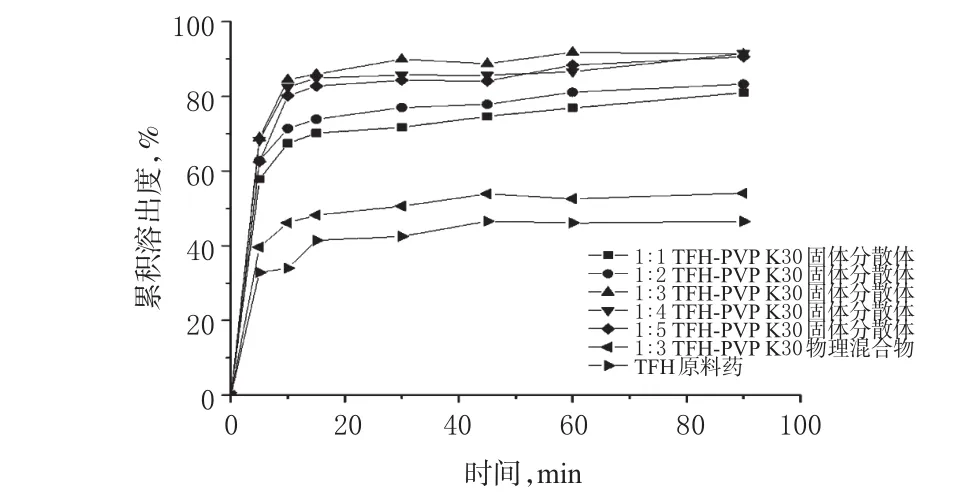
图1 7种样品的体外溶出曲线Fig 1 Dissolution curves in vitro of 7 samples
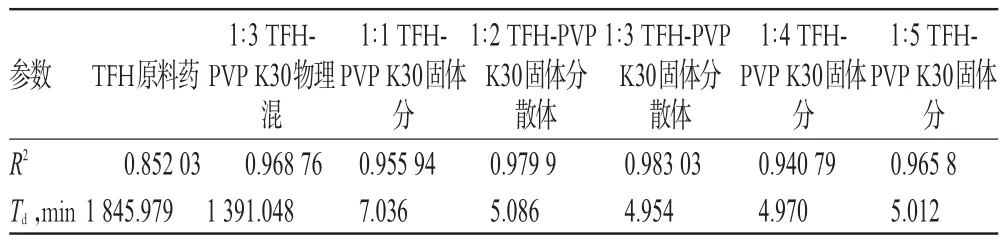
表1 7种样品的溶出参数Tab 1 Dissolution parameter of 7 sample
由图1可知,药物溶出度随着药载比的增加而增加,但药载比达到1∶3后,药物溶出度增加不明显。当TFH-PVP K30固体分散体的药载比为1∶3时,其体外溶出度显著高于TFH原料药及对应比例的TFH-PVP K30物理混合物(P<0.05)。同时由表1可知,1∶3 TFHPVP K30固体分散体的溶出曲线拟合优度最好,Td最小,提示溶出63.2%所需的时间最短。
2.5 正交试验优选制备工艺
2.5.1 正交试验设计 以1∶3为药载比制备TFH-PVP K30固体分散体,以累积溶出度(90 min)为指标,以超声时间(A,min)、水浴温度(B,℃)和干燥时间(C,h)为因素,按L9(34)正交表作3因素3水平设计试验,优选TFHPVP K30固体分散体的制备工艺。因素与水平见表2,正交试验设计与结果见表3。

表2 正交试验因素与水平Tab 2 Factors and levels of orthogonal test

表3 正交试验设计与结果Tab 3 Design and results of orthogonal test
2.5.2 结果分析 由表3可知,各因素对制备工艺的影响顺序为B>A>C。以极差最小的D为误差项进行方差分析,结果表明,A、B有显著影响(P<0.05或P<0.01),C没有显著影响(P>0.05)。为节约时间、降低成本,综合考虑,确定最优制备工艺为A2B2C1,即超声时间为10 min、水浴温度60℃、干燥时间为12 h。方差分析结果见表4。
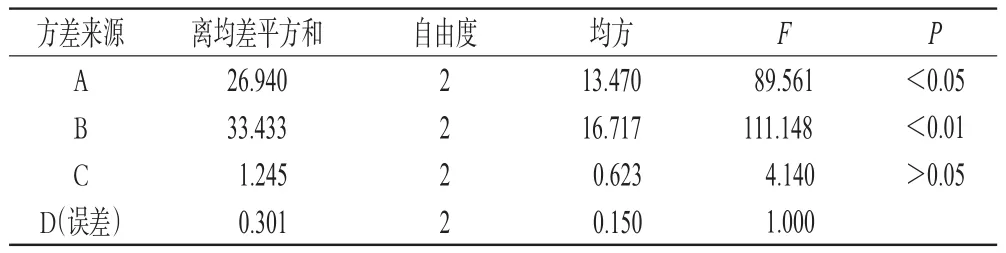
表4 方差分析结果Tab 4 Analysis result of variance
2.5.3 验证试验 按最优制备工艺重复3次制备TFHPVP K30固体分散体,测得其90 min的累积溶出度分别为88.47%、91.53%、90.67%,平均值为90.22%,RSD=1.74%(n=3),结果表明制备工艺合理可行、重现性好。
2.6 固体分散体的表征
2.6.1 SEM观察 采用SEM观察TFH原料药、PVP K30、TFH-PVP K30物理混合物(1∶3)与TFH-PVP K30固体分散体(1∶3)的表面和晶体结构,测试条件为真空镀金70 s、高压15.0 kV。观察样品的外观形貌并采集图像。结果显示,4个样品的表面结构完全不同:TFH原料药以大小不一的结晶形式存在;PVP K30为球形或类球形颗粒状;TFH-PVP K30物理混合物中仍可观察到TFH原料药和PVP K30的单独结构特征;而在TFH-PVP K30固体分散体中无明显晶体存在,表明TFH原料药以无定形均匀分散在PVP K30载体中,且TFH原料药晶体特征基本消失,提示已形成固体分散体。4种样品的SEM图见图2。

图2 4种样品的SEM图(×200)Fig 2 SEM images of 4 samples(×200)
2.6.2 DSC分析 采用DSC对TFH原料药、PVP K30、TFH-PVP K30物理混合物(1∶3)与TFH-PVP K30固体分散体(1∶3)进行分析,测试条件为铝坩埚,升温速率为10.00℃/min,升温范围为50~400℃,样品量约10 mg。结果显示,TFH原料药在316℃处出现明显熔融吸热峰;TFH-PVP K30物理混合物在316℃处出现与TFH原料药相应的吸热峰,提示TFH原料药与PVP K30载体之间未发生本质上的改变,TFH原料药的晶型未发生改变;而TFH-PVP K30固体分散体未出现TFH原料药的吸热峰,表明TFH原料药可能以无定形分散在PVP K30载体中,该结果与SEM观察结果的推测一致。4种样品的DSC图见图3。
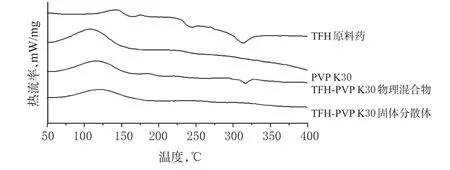
图3 4种样品的DSC图Fig 3 DSC spectrograms of 4 samples
2.6.3 FT-IR分析 采用KBr压片法进行FT-IR分析。取TFH原料药、PVP K30、TFH-PVP K30物理混合物(1∶3)与TFH-PVP K30固体分散体(1∶3),设分辨率为4 cm-1,扫描30次,4 000~400 cm-1全谱扫描。结果显示,TFH原料药含有O—H及C=O,图谱中分别在3 423 cm-1与1 656 cm-1呈伸缩振动;PVP K30在3 452 cm-1呈O—H伸缩振动峰,在1 662 cm-1呈C=O伸缩振动。通过FT-IR分析比较,TFH原料药与TFH-PVP K30物理混合物在3 423 cm-1与2 927 cm-1处均有强吸收峰,同时在1 656 cm-1与1 602 cm-1处也均有吸收峰。TFH-PVP K30物理混合物的O—H及C=O伸缩振动仍清晰可见,表明其IR结果为TFH原料药与PVP K30的简单叠加;而TFH-PVP K30固体分散体中出峰波数由3 423 cm-1降到3 417 cm-1,且吸收峰变宽变钝;吸收峰波数从2 927 cm-1增加到2 939 cm-1,吸收峰强度变强;但1 666 cm-1处有1个强吸收峰,1 602 cm-1处吸收峰消失。由此推断,TFH-PVP K30固体分散体中TFH原料药与PVP K30分子之间可能发生相互作用,形成氢键。4种样品的FTIR图见图4。
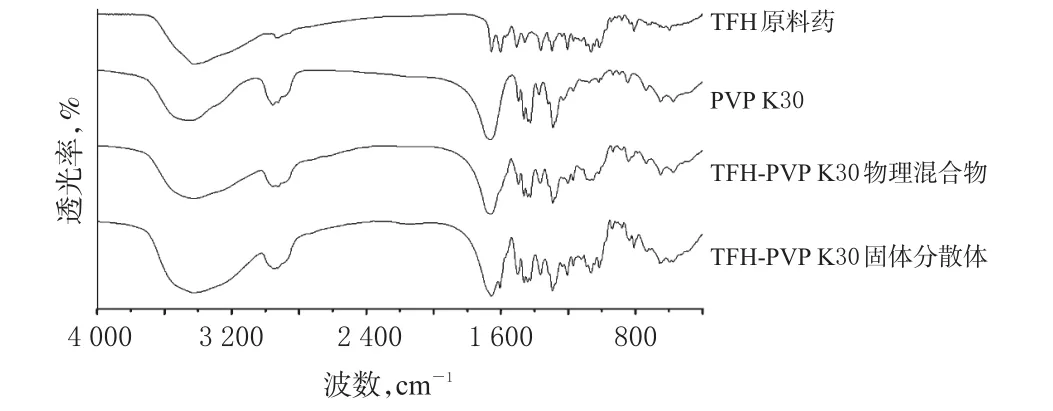
图4 4种样品的FT-IR图Fig 4 FT-IR spectrograms of 4 samples
3 讨论
本研究以PVP K30为载体制备固体分散体,但由于PVP K30的熔点较高,不宜用熔融法制备固体分散体,故采用溶剂法。在制备过程中,以药载比为1∶1制备固体分散体混匀时,出现乳白状现象;转移至减压旋转,溶液先澄清后又出现乳白状现象。而其他比例制备固体分散体时并未出现此现象。故推测当药物与载体比例相当时,药物可能不能充分高度均匀地分散在载体中,影响了其固体分散体的制备。
固体分散体显著改善药物溶出的机制包括:水溶性高分子材料能增加药物的表面润湿性、药物在固体分散体中以无定形态缔合,其提高或降低溶出率取决于载体的性质和药物在固体分散体中的分散状态[13-14]。通过SEM、DSC、FT-IR表征证实,以PVP K30为载体制备的TFH-PVP K30固体分散体,可有效阻止TFH原料药的结晶,使其以无定形状态存在,其体外溶出度显著提高。TFH-PVP K30固体分散体的体外溶出度增加的原因可能是因为PVP K30为非离子型高分子化合物,亦是一种良好的亲水性表面活性剂,使TFH原料药更易润湿,增加了TFH原料药在介质中的溶解;同时因其特殊结构(在溶液以网状结构出现),当TFH原料药与PVP K30按适当的比例制备成固体分散体时,二者之间发生相互作用(分子间氢键作用)[15],且在作用过程中载体PVP K30可有效阻止TFH原料药结晶使其以无定形状态存在,增加TFH原料药体外溶出速率,从而提高TFH的生物利用度,为后续制备渗透泵控释片奠定了基础。
[1] 国家药典委员会.中华人民共和国药典:一部[S].2015年版.北京:中国医药科技出版社,2015:184-185.
[2] 刘凤云.沙棘总黄酮的药理研究概况[J].中药材,2004,27(2):145-147.
[3] 王月茹,张莉,张建,等.沙棘总黄酮自微乳化制剂处方研究[J].陕西中医,2014,35(1):92-94.
[4] Newman A,Knipp G,Zografi G.Assessing the performance of amorphous solid dispersions[J].J Pharm Sci,2012,101(4):1355-1377.
[5] Hussain MD,Saxena V,Brausch JF,et al.Ibuprofen-phospholipid solid dispersions:improved dissolution and gastric tolerance[J].Int J Pharm,2012,422(1/2):290-294.
[6] 唐婷,严航,周江,等.莲心碱固体分散体的表征及体外溶出度的测定[J].中成药,2015,37(8):1853-1855.
[7] 赵俊霞,尹蓉莉,孙彩霞,等.广金钱草总黄酮-PVP-K30固体分散体的制备及体外特征[J].中成药,2014,36(10):2070-2074.
[8] Onoue S,Sato H,Ogawa K,et al.Improved dissolution and pharmacokinetic behavior of cyclosporine A using high-energy amorphous solid dispersion approach[J].Int J Pharm,2010,399(1):94-101.
[9] Hong SW,Lee BS,Park SJ,et al.Solid dispersion formulations of megestrol acetate with copovidone for enhanced dissolution and oral bioavailability[J].Arch Pharm Res,2011,34(1):127-135.
[10] 蒋艳荣,张振海,陆艳,等.丹参酮ⅡA二元载体固体分散体的研究[J].中国中药杂志,2012,37(10):1383-1387.
[11] 国家药典委员会.中华人民共和国药典:四部[S].2015年版.北京:中国医药科技出版社,2015:121-124.
[12] 周郁斌,袁中文,李海刚,等.用Origin软件计算药物溶出度Weibull分布参数[J].医药导报,2011,30(6):721-723.
[13] 乔井会,郭建鹏,马艳,等.阿托伐他汀钙泊洛沙姆188固体分散体的制备及表征[J].中国药房,2015,26(1):103-106.
[14] 李标.固体分散体在药剂学中的应用[J].中国药房,2009,20(10):790-792.
[15] 孙彩霞,尹蓉莉,赵俊霞,等.水蜈蚣总黄酮固体分散体的制备及其性质研究[J].中草药,2014,45(14):2018-2021.
(编辑:邹丽娟)
Preparation,Characterization and in vitro Dissolution Study of Total Flavonoids of Hippophae rhamnoides-PVP K30 Solid Dispersion
TIAN Qian1,HE Chen1,HE Jingxia1,YIN Rongli1,YANG Junxuan2,ZHANG Li1(1.School of Pharmacy,Chengdu University of TCM,Chengdu 611137,China;2.College of TCM,Chongqing Medical University,Chongqing 400016,China)
OBJECTIVE:To prepare total flavonoids of Hippophae rhamnoides(TFH)-PVP K30 solid dispersion,and to characterize and study its in vitro dissolution.METHODS:Solvent method was used to prepare TFH-PVP K30 solid dispersion with different drug-loading ratio of 1∶1,1∶2,1∶3,1∶4,1∶5;single factor test was designed to screen drug-loading ratio using dissolution parameter Tdas index;orthogonal test was designed to optimize ultrasonic time,temperature of water bath and drying time for preparation technology using in vitro dissolution rate as index,and then validated.SEM,DSC and FT-IR were used to characterize solid dispersion.RESULTS:Tdof TFH-PVP K30 solid dispersion was the lowest when drug-loading ratio was 1∶3.Optimal technology was ultrasonic time 10 min,temperature of water bath 60℃and drying time 12 h.90 min accumulative dissolution rate of prepared TFH-PVP K30 solid dispersion was 90.22%in average(RSD=1.74%,n=3).The results of SEM,DSC and FT-IR showed that the drug as amorphous form dispersed in the PVP K30,the formation of hydrogen bond of the both.CONCLUSIONS:TFH-PVP K30 solid dispersion is prepared successfully,and in vitro dissolution rate of it is improved significantly.
Total flavonoids of Hippophae rhamnoides;PVP K30;Solid dispersion;Dissolution rate;Orthogonal test;Characterization
R943
A
1001-0408(2017)01-0115-04
2016-07-05
2016-08-19)
*药师,硕士。研究方向:中药新制剂、新剂型、新技术。E-mail:cherryrz@sina.com
#通信作者:教授,博士生导师。研究方向:中药新制剂、新剂型、新技术。E-mail:yinronglili@163.com
DOI10.6039/j.issn.1001-0408.2017.01.30
