Mn-Zn复合氧化物的结构及其负载Ni脱硫催化剂的脱硫性能
2017-02-08王海彦关纵弛王钰佳刘冬梅杨占旭
康 蕾, 王海彦, 关纵弛, 王钰佳, 刘冬梅, 杨占旭
(1. 中国石油大学 化学工程学院, 山东 青岛 266580; 2. 辽宁石油化工大学 化学化工与环境学部, 辽宁 抚顺 113001)
Mn-Zn复合氧化物的结构及其负载Ni脱硫催化剂的脱硫性能
康 蕾1,2, 王海彦1,2, 关纵弛2, 王钰佳2, 刘冬梅2, 杨占旭2
(1. 中国石油大学 化学工程学院, 山东 青岛 266580; 2. 辽宁石油化工大学 化学化工与环境学部, 辽宁 抚顺 113001)
采用水热法合成了Mn-Zn复合氧化物,用等体积浸渍法制备了Mn-Zn复合氧化物负载Ni脱硫催化剂。采用XRD、FT-IR、N2吸附-脱附、XPS等手段表征Mn-Zn复合氧化物和相应Ni催化剂,并以正庚烷-噻吩为模型化合物,考察了所制备的脱硫催化剂的催化活性。结果表明,Mn-Zn形成复合氧化物后,Mn以+4价离子存在,并且进入ZnO的晶格内部,替代了Zn的格位,改变了ZnO的晶胞参数和粒子尺寸,比表面积、孔体积、孔径明显增大;负载金属Ni的Mn-Zn复合氧化物催化剂的脱硫催化活性比纯ZnO负载Ni催化剂的脱硫催化活性提高14%,并且具有良好的重复使用性能。
水热法; Mn; ZnO; S-Zorb; 脱硫
燃料油中的含硫化物对人类健康和环境造成严重的威胁,生产超低硫燃料油己经受到越来越多的关注[1-2]。ZnO是一种常用的吸附脱硫剂,由于其脱硫压力低、辛烷值损失小而备受关注[3-7],但在脱硫过程中存在失活快、剂耗高等问题。Zhang等[8-12]采用浸渍法将Ni元素负载于ZnO上制得脱硫剂。李芬等[13-14]向纳米ZnO中添加铈(Ce)、Fe等元素,李治俊等[15]用钕元素对ZnO脱硫剂进行改性,提高其脱硫性能。由于ZnO晶体的极性生长特征,过渡金属离子易于掺杂[16],而且掺杂后会引起ZnO晶体结构的变化[17],对ZnO脱硫性能有极为重要的影响。因此,笔者采用掺杂Mn改性ZnO,形成Mn-Zn复合氧化物,用于燃料油脱硫。Mn-Zn复合氧化物作为半导体材料以及在光催化方面应用广泛[18-19],但其在脱硫方面的应用报道较少,尤其是Mn-Zn复合氧化物在脱硫过程中的作用机理,以及Mn-Zn两组分之间的“协同”作用尚不明确。笔者表征了所制备的Mn-Zn复合氧化物的结构,考察了其脱硫性能及再生性能,并讨论了Mn-Zn之间的相互协同作用及其对脱硫性能和重复使用性能的影响。
1 实验部分
1.1 原料和试剂
硝酸镍(Ni(NO3)2·6H2O)、醋酸锌(Zn(AC)2·2H2O)、醋酸锰(Mn(AC)2·4H2O)、氢氧化钠(NaOH)、正庚烷(C7H16)、噻吩(C4H4S)、乙醇(C2H5OH),分析纯,国药集团化学试剂有限公司产品。
1.2 脱硫剂的制备
取一定量的Zn(AC)2·2H2O和Mn(AC)2·4H2O,按n(Mn)/n(Zn)为0、0.10、0.15、0.20、0.25配制成混合液。取混合溶液100 mL,加入10 mL乙醇,剧烈振荡,缓慢加入20 mL浓度为1 mol/L的NaOH溶液,置于高压水热釜中,120℃下反应24 h。得到的沉淀经过滤、洗涤,在120℃下烘干12 h,500℃下程序升温焙烧3 h,得到5种不同n(Mn)/n(Zn)的复合氧化物样品,记为M0Z、M0.1Z、M0.15Z、M0.2Z、M0.25Z。
采用等体积浸渍法将Ni(NO3)2分别负载到M0Z、M0.1Z、M0.15Z、M0.2Z、M0.25Z上,保持NiO的负载量占Mn-Zn复合氧化物总质量的5%,120℃下烘干12 h,500℃下程序升温焙烧3 h,制得脱硫催化剂NM0Z、NM0.1Z、NM0.15Z、NM0.2Z、NM0.25Z。
1.3 脱硫性能的评价
采用固定床反应器,以硫质量浓度为10 mg/L的噻吩正庚烷溶液作为模型汽油,制备的脱硫催化剂剂经压片后,筛取20~40 目的颗粒,装填量为10 mL。在350℃、0.6 MPa下还原3 h;然后在进料的体积空速为5 h-1、0.6 MPa、300℃的条件下进行加氢脱硫。采用华东分析仪器厂DL-2B微库仑测硫仪测定反应前后模拟油中的硫含量,计算其脱硫率。
使用后的脱硫催化剂在550℃、160 mL/min空气流量下焙烧5 h,进行再生。
1.4 脱硫催化剂的表征
采用日本理学D/max-RB X射线衍射仪测定样品的晶相结构,Cu-Kα辐射(λ=0.15406 nm),管电压40 kV,管电流100 mA,测角仪半径185 mm,光阑系统为DS=SS=1°,RS=0.15 mm。采用美国康塔公司Micromeritics ASAP-2010型吸附仪测量样品的N2吸附-脱附等温线,用BET法计算催化剂样品的比表面积,用BJH法计算孔容和孔径分布。采用美国Thermo VG公司ESCALAB250型X射线光电子能谱测定样品中Mn和Zn的价态,激发源A1Kα,以C1s(284.6 eV)为内标校正核电效应。
2 结果与讨论
2.1n(Mn)/n(Zn)对Mn-Zn复合氧化物晶体结构的影响
图1为不同n(Mn)/n(Zn)的M0Z、M0.1Z、M0.15Z、M0.2Z、M0.25Z 5个样品的XRD谱。将其与JCPDS标准卡对照, M0Z、M0.1Z、M0.15Z、M0.2Z 4个样品均在2θ为31.7、34.3、36.2、47.5、57.0、62.7、66.4、67.8、69.0处出现了明显的对应六方铅锌矿ZnO(100)、(002)、(101)、(102)、(110)、(103)、(200)、(112)、(201)晶面的特征衍射峰[20]。随着样品中n(Mn)/n(Zn)增加,ZnO特征衍射峰的位置没有发生变化,只是强度先增强后减弱。这是因为添加Mn后,ZnO与MnO形成了复合晶相,当n(Mn)/n(Zn)较小时,Mn的添加能有效提高ZnO的结晶度,使ZnO的特征衍射峰增强;但随着n(Mn)/n(Zn)的增加,复合氧化物微结构中的ZnO含量减少,导致ZnO微结构的ZnO特征衍射峰强度逐渐变小[18]。M0.1Z、M0.15Z样品除出现ZnO的特征衍射峰外,并没有其他物质的特征衍射峰,这可能是Mn离子高度分散在ZnO的表面或是进入了ZnO的晶格内部,无法检测到的缘故;M0.2Z样品在2θ=30.2和2θ=43.8处出现了ZnMnO3的特征峰[21],说明了Mn-Zn复合氧化物的存在;M0.25Z样品的ZnO的特征峰及2θ=43.8处出现的ZnMnO3的特征峰逐渐弱化,这可能是ZnO晶体中的各类缺陷,如O空位和Zn填隙原子等的相对密度有所增加,导致了晶体结构的变化[17]。为了进一步研究Mn与Zn结合形成的复合氧化物,对M0.2Z进行了XPS表征,结果示于图2。
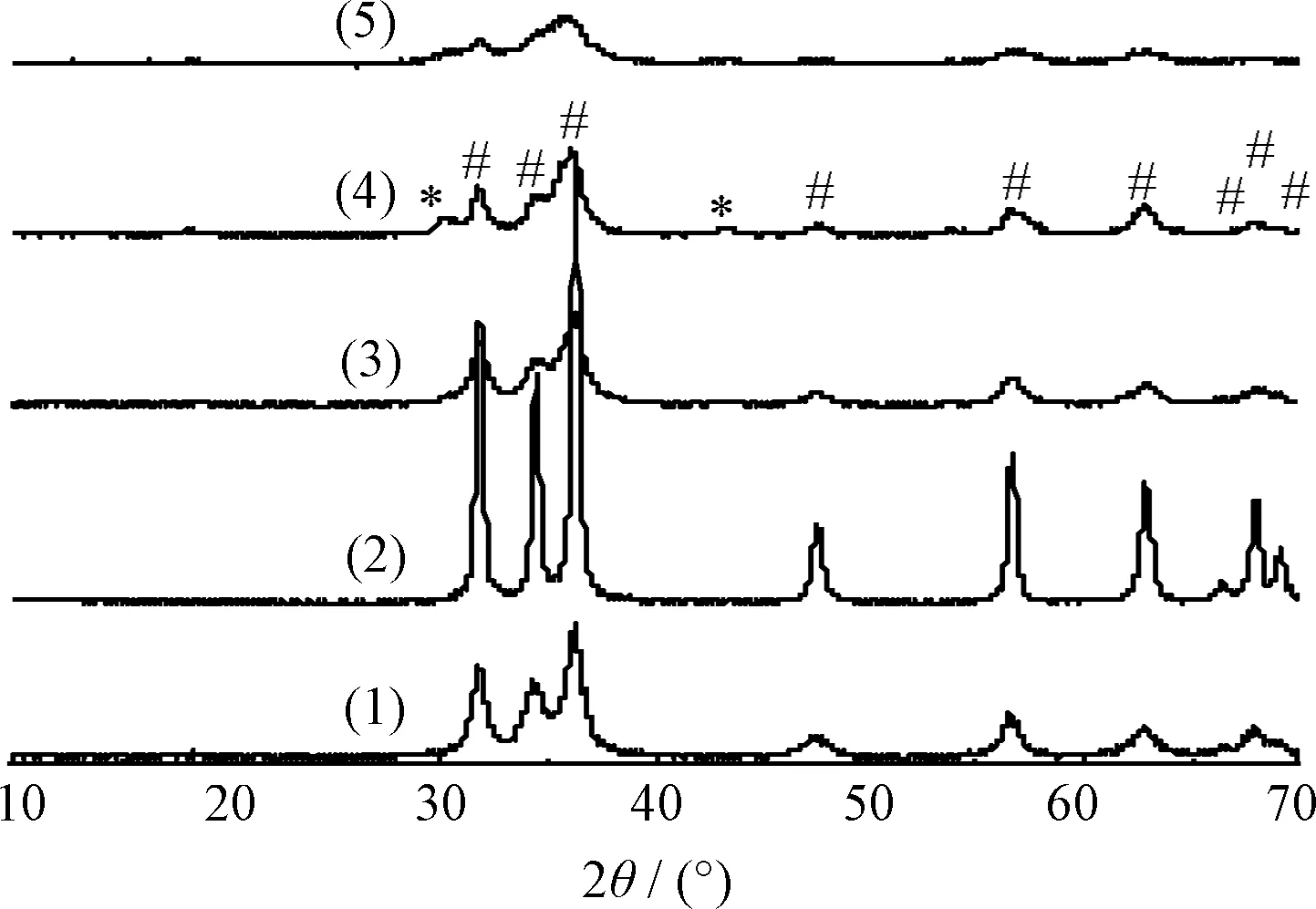
图1 制备的Mn-Zn复合氧化物样品的XRD谱Fig.1 XRD patterns of prepared Mn-Zn composite oxide samples(1) M0Z; (2) M0.1Z; (3) M0.15Z; (4) M0.2Z; (5) M0.25Z ZnMnO3; ZnO

图2 M0.1Z样品的XPS谱Fig.2 XPS profiles of sample M0.1Z(a) M0.1Z; (b) Zn2p; (c) Mn2p3/2; (d) O1s
图2结合能峰值都用C1s的结合能(284.6 eV) 进行校准。图2(a)为M0.1Z样品的全谱,显示出Zn、O、Mn的中心峰。图2(b)为Zn2p的慢扫谱,由图2(b)可见,Zn2p1/2和Zn2p3/2峰位于1043.11 eV和1020.02 eV处,与ZnO的Zn2p1/ 2(1044.8 eV)和Zn2p3/ 2(1021.8 eV)的标准结合能[22]一致,说明未破坏ZnO六方晶系的晶体结构。图2(c)为Mn2p3/2的慢扫谱,Mn2+、Mn3+和 Mn4+对应的2p3/ 2谱峰分别在640.2、641.2 和 642.2 eV处[23-24],从图2(c)可以看出,Mn2p3/2的中心峰值约为642.4 eV,这充分表明了M0.1Z样品中有Mn存在,且Mn离子为+4价。根据XPS结果计算得到M0.1Z样品表面的Mn/Zn原子比约为0.09,比M0.1Z样品的理论原子比低0.11,这说明M0.1Z样品表面的Mn原子个数减少,可以断定,有一部分Mn4+进入ZnO的晶格,且与Zn2+形成ZnMnO3。图2(d)为O1s的慢扫谱,其中心峰值约为529.72 eV,与O2+的标准结合能(529.7 eV)[25]相一致。
2.2n(Mn)/n(Zn)对Mn-Zn复合氧化物比表面积和孔结构的影响
不同n(Mn)/n(Zn)的M0Z、M0.1Z、M0.15Z、M0.2Z、M0.25Z 5个样品的N2吸附-脱附等温线如图3 所示。由图3可见,5个样品对N2的吸附量随吸附压力的变化规律相同,在较低的p/p0下对N2的吸附量都较少,且没有明显的拐点;但是当p/p0较高时,对N2的吸附量均急剧增加,根据IUPAC的分类,呈现典型的Ⅲ型等温线;在p/p0为0.45~0.95时,出现较明显的H3型滞后环,说明样品中有介孔存在,且源自平面狭缝、裂缝和楔形等结构。但是在吸附过程中,5个样品对N2的吸附量不同,添加Mn的样品对N2的吸附量增加。说明Mn的添加改变了样品的孔道结构,增大了样品的比表面积。由BET方法计算出的样品比表面积、由BJH方法计算出的孔体积、平均孔径列于表1。由表1可见,M0.1Z、M0.15Z样品的比表面积接近,均明显高于未掺入Mn元素的ZnO样品的比表面积; M0.2Z样品的比表面积达到最大,同时总孔容和孔径也明显增加;但M0.25Z样品的比表面积下降,同时总孔容和孔径也明显下降,这可能是由于样品中形成了新的物质(见图1),因此影响了样品的表面结构。
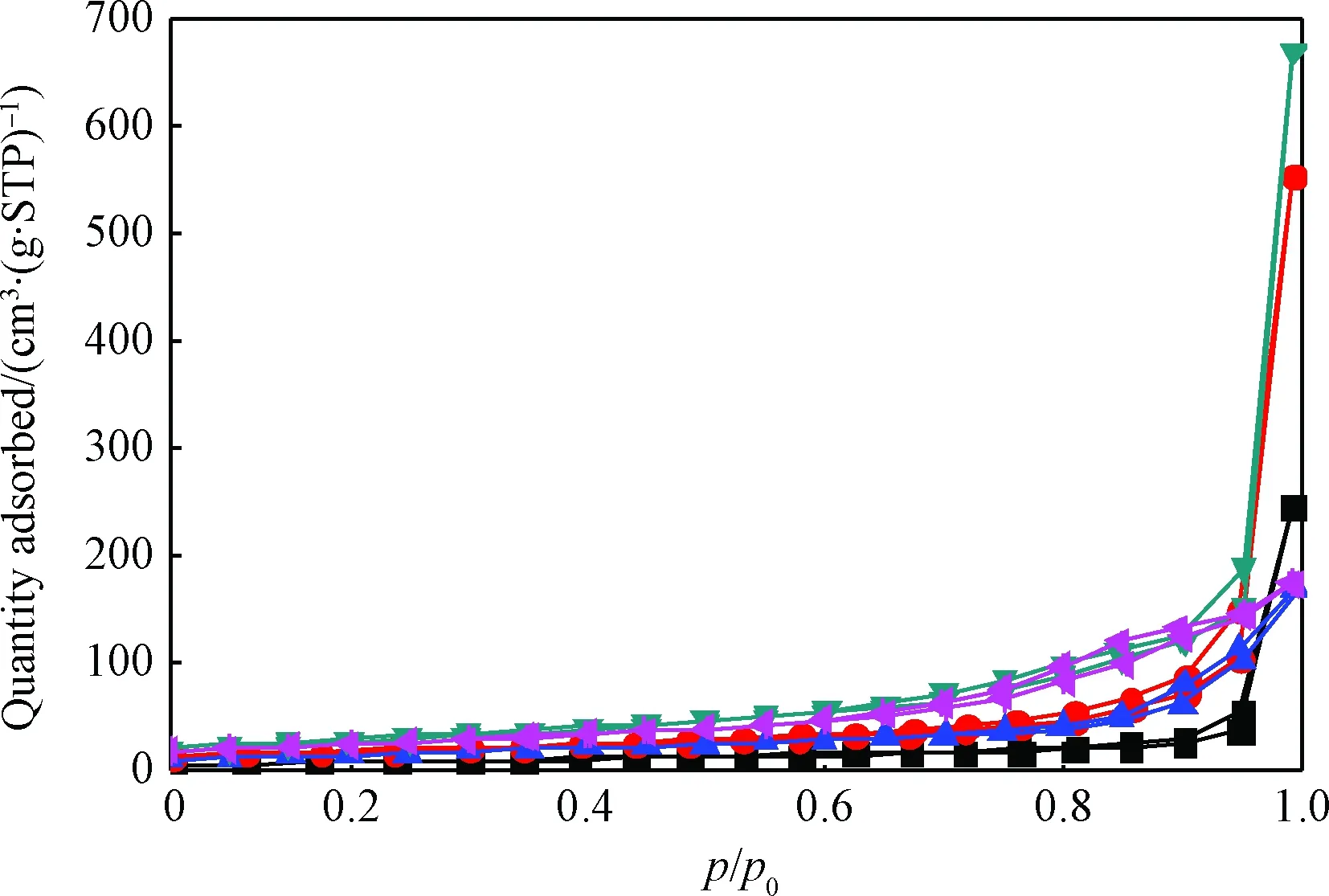
图3 Mn-Zn复合氧化物样品的N2吸附-脱附等温线Fig.3 N2 adsorption-desorption isotherms of Mn-Zn composite oxide samples M0Z; M0.1Z; M0.15Z; M0.2Z; M0.25Z表1 Mn-Zn复合氧化物样品的比表面积、 孔体积和平均孔径Table 1 BET surface area, pore volume and average pore diameter of Mn-Zn composite oxide samples

SampleSBET/(m2·g-1)Porevolume/(cm3·g-1)Diameter/nmM0Z31.320.381316.712M0.1Z67.960.855816.699M0.15Z62.710.760216.610M0.2Z108.401.032038.070M0.25Z94.920.270811.410
2.3n(Mn)/n(Zn)对Mn-Zn复合氧化物负载Ni催化剂脱硫性能的影响
以制得的Mn-Zn复合氧化物负载Ni催化剂NM0Z、NM0.1Z、NM0.15Z、NM0.2Z、NM0.25Z作为脱硫催化剂,在350℃下还原3 h,在进料的体积空速为5 h-1、压力为0.6 MPa、温度为300℃的条件下对模型汽油进行加氢脱硫,结果示于图4。由图4可见,在装置运行10 h后,5个Mn-Zn复合氧化物催化剂样品的脱硫活性基本达到稳定。采用NM0Z时模型汽油的脱硫率为83%,NM0.1Z、NM0.15Z的脱硫性能明显优于NM0Z,脱硫率分别达到89%和91%,采用NM0.2Z时模型汽油的脱硫率在97%左右。由此可见, Mn的添加能够改善脱硫催化剂的脱硫性能,而且Mn的加入量对脱硫性能有重要影响。

图4 采用不同n(Mn)/n(Zn)的Mn-Zn复合氧化物 负载Ni脱硫催化剂时模型汽油的脱硫率Fig.4 The desulfurization ratio of model gasoline over Ni supported on Mn-Zn composite oxides with different n(Mn)/n(Zn)(1) NM0Z; (2) NM0.1Z; (3) NM0.15Z; (4) NM0.2Z; (5) NM0.25Z
根据XRD谱,应用jade软件计算了脱硫效果较好的NM0.2Z催化剂的复合氧化物载体M0.2Z的平均晶粒尺寸和晶胞参数,同时计算了未添加Mn的M0Z样品的相应数据,结果列于表2。可以看出,与M0Z相比,M0.2Z的平均粒径增大,但晶胞参数变小。这是因为当晶粒较大时,在表面上存在的相对原子数目减少,这就增加了它们受力的不对称性。这些原子由于受到晶粒内部较多原子的吸引,其合力较大,且指向晶粒内部,这就使得表面原子向晶粒内移动的倾向变大。为了满足能量最低原理,稳定系统,表面原子要通过减小表面积来达到降低表面能的目的[26]。在这种情况下,产生的附加压力足以使晶格产生大的收缩,使得所有晶面的晶胞参数呈减小的趋势。晶体的晶胞参数变小会引起晶格畸变,O空位和Zn间隙缺陷加强,造成了晶格的多种不规整性。晶体的不规整性对金属离子的化学吸附、催化活性等都起着极为重要的作用,因此NM0.2Z样品的脱硫活性明显高于NM0Z。

表2 M0.2Z和M0Z样品的晶粒尺寸和晶胞参数Table 2 Particle size and crystal cell parameters of M0.2Z and M0Z samples
同时,Mn的添加增大了复合氧化物的比表面积、孔径和孔体积,M0.2Z样品的比表面积达到108.4 m2/g(见表1);大的比表面积有利于分子的吸附、扩散和脱附,因此NM0.2Z的脱硫活性显著增加。
一般认为,Ni/ZnO对噻吩的吸附过程分为两步。首先是噻吩在Ni原子上的氢解过程,然后是H2S在ZnO上的吸附反应的过程[27]。比较ZnO、MnO和ZnMnO3与H2S反应平衡,如式(1)~(3)所示[28],可以发现ZnMnO3吸附H2S的速率明显高于ZnO吸附H2S的速率,因此NM0.2Z催化剂的脱硫活性最高。
ZnO+H2S=ZnS+H2O, k=4.850×104
(1)
MnO2+H2S+H2=MnS+2H2O,
k=1.134×1014
(2)
ZnMnO3+2H2S+H2=ZnS+MnS+3H2O,
k=5.499×1018
(3)
2.4 Mn-Zn复合氧化物脱硫剂的重复使用性能
NM0.2Z 6周期脱硫循环实验的结果列于表3。可以看出,NM0.2Z经过1次再生后,保持产物中硫质量浓度小于5 mg/L,其寿命比新鲜剂缩短了12.5 %;随着再生次数的增加,其寿命逐渐下降;经过6次再生后,其寿命下降幅度较大,降为35 h。

表3 NM0.2Z对模型汽油脱硫的重复使用性能及其织构性质变化Table 3 Reusability of NM0.2Z for the desulfurization of model gasoline and its texture properties changes
ρ(S)<5 mg/L in the product for each generation period
图5为NM0.2Z各次再生后样品的XRD谱。由图5可见,经过1次和2次再生,NM0.2Z样品中的ZnO都保持了其六方铅锌矿的结构,并且没有出现MnO和NiO的特征衍射峰,2次再生后,MnO和NiO仍然高度分散在ZnO表面,并未出现聚集;而且峰型尖锐,说明具有比新鲜剂更好的结晶度。这可能是由于在新鲜剂中存在的ZnMnO3经过反应和再生后转化为ZnO和MnO, 改变了复合氧化物原有的晶体结构。另外,经过1次再生的NM0.2Z并没有出现ZnS的特征衍射峰,而经过2次再生后,在2θ=28.5°处出现了ZnS的特征衍射峰。说明经过多次再生后,在再生过程中有部分ZnS已无法转化成ZnO,因此导致脱硫催化活性的降低;经过6次再生,ZnO六方铅锌矿的结构被破坏,脱硫催化活性大幅度降低。
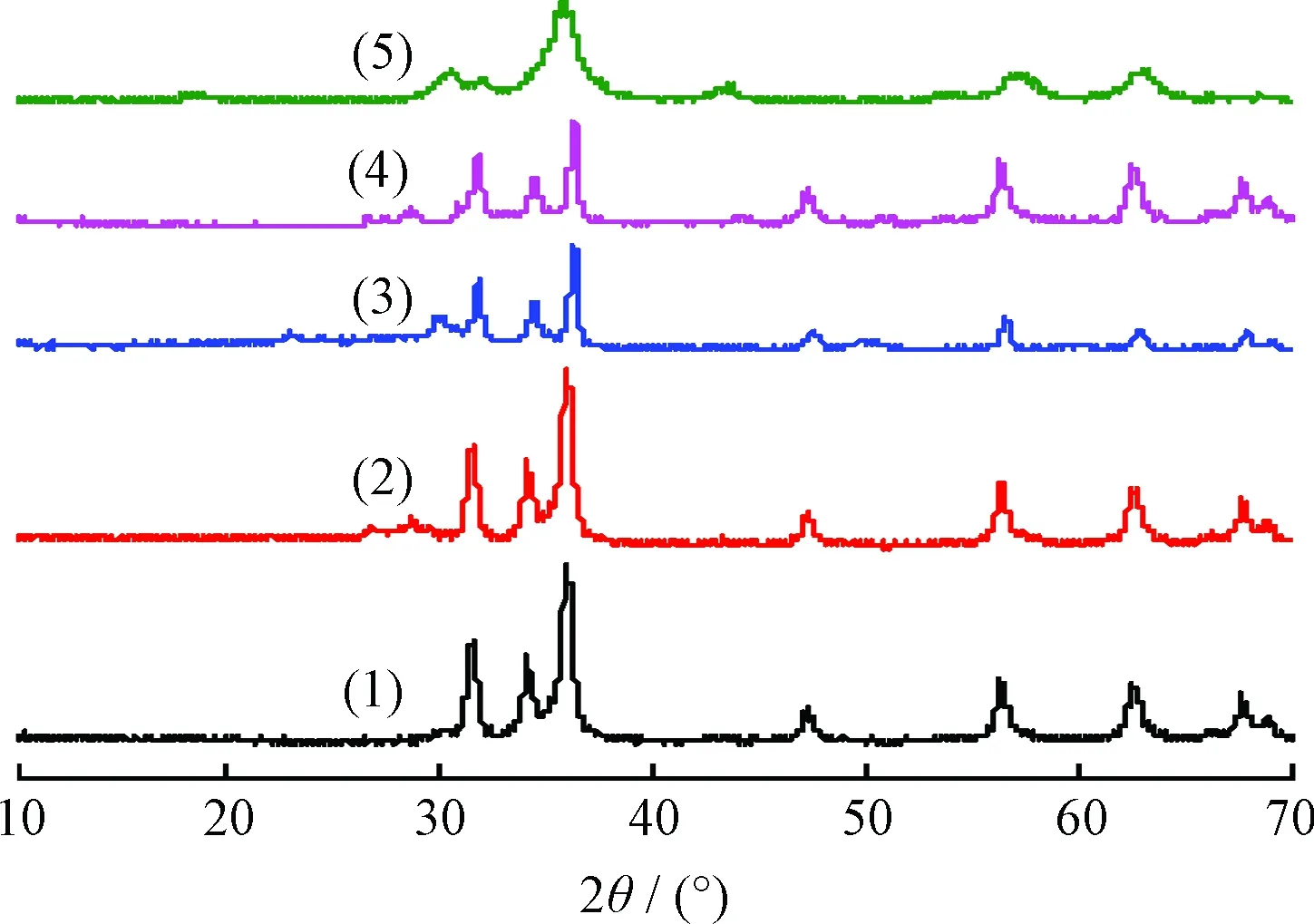
图5 NM0.2Z各次再生后样品的XRD谱Fig.5 XRD patterns of NM0.2Z sample after each regeneration Regeneration: (1) 1 st.; (2) 2 nd.; (3) 3 rd.; (4) 4 th.; (5) 6 th.
NM0.2Z再生后比表面积和孔容的测试结果也列于表3。由表3可见,NM0.2Z再生后的比表面积和孔容都呈减小趋势;1次和3次再生后的比表面积和孔容较接近,与新鲜剂相比减小了20%;但6次再生后,比表面积和孔容明显减小,这与其寿命的缩短趋势一致。可见,比表面积和孔容是影响脱硫剂脱硫活性的重要因素。
3 结 论
(1)Mn-Zn复合氧化物负载金属Ni后制备的NM0.2Z,用于模型汽油的脱硫,脱硫率达到97%以上,比未添加Mn的纯ZnO制备的脱硫剂所得脱硫率高14%。
(2)在Mn-Zn复合氧化物制备过程中产生的ZnMnO3有效地提高了复合氧化物的比表面积和孔容,在吸附脱硫过程中其吸附H2S的速率明显高于ZnO吸附H2S的速率,这是Mn-Zn复合氧化物脱硫性能高于纯ZnO的重要原因。
(3)NM0.2Z经过6次再生后,ZnO六方铅锌矿的结构被破坏,比表面积和孔容明显减小,进而影响到其使用寿命,但再生次数少于5时,表现出了稳定的脱硫催化活性,可满足深度脱硫的要求。
[1] 魏延雨, 李永红, 孔爱华. Ni-Zn复合氧化物用于反应吸附脱除噻吩[J].石油学报(石油加工), 2013, 29(2): 214-221. (WEI Yanyu, LI Yonghong, KONG Aihua. Reactive adsorption desulfurization fir thiophene on adsorbent of Ni-Zn complex oxides[J].Acta Petrolei Sinica (Petroleum Processing Section), 2013, 29(2): 214-221.)
[2] SAMOKHVALOV A, TATARCHUK B J, CATAL R J. Adsorptive removal of hazardous materials using metal-organic frameworks[J].Journal of Hazardous Materials, 2010, 52(3): 381-387.
[3] 林伟. 氧化硅源和氧化锌颗粒大小对S-Zorb吸附剂脱硫活性的影响[J].石油学报(石油加工), 2012, 28(5): 739-743. (LIN Wei. Influence of silica precursor and particle size of zinc oxide on the desulfurization activity of S-Zorb sorbent[J].Acta Petrolei Sinica (Petroleum Processing Section), 2012, 28(5): 739-743.)
[4] YANG R T, HERNANDEZ-MALDONADO A J, YANG F H. Desulfurization of transportation fuels with zeolites under ambient conditions[J].Science, 2003, 34(40): 79-81.
[5] CHICA A, CORMA A, DMINE M E J. Catalytic oxidative desulfurization (ODS) of diesel fuel on a continuous fixed-bed reactor[J].Catal, 2006, 242(10): 299-304.
[6] 徐文清, 熊纯清, 周广林. Ni/Zno吸附剂脱除催化裂化汽油中的硫[J].石油学报(石油加工), 2008, 24(6): 739-742. (XU Wenqing, XIONG Chunqing, ZHOU Guanglin. Remove of sulfur from FCC gasoline by using Ni/ZnO as adsorbent[J].Acta Petrolei Sinica (Petroleum Processing Section), 2008, 24(6): 739-742.)
[7] BABICH I V, MOULIJN J A. Science and technology of novel processes for deep desulfurization of oil refinery streams: A review[J].Fue1, 2003, 82(6): 607-631.
[8] ZHANG Y L,YANG Y X ,HAN H X. Ultra-deep desulfurization via reactive adsorption on Ni/ZnO: The effect of ZnO particle size on the adsorption performance[J].Applied Catalysis B: Environmental, 2012, 119(21): 631-637.
[9] ZHANG J C, LIU Y Q, TIAN S. Reactive adsorption of thiophene on Ni/ZnO adsorbent: Effect of ZnO textural structure on the desulfurization activity [J].Journal of Natural Gas Chemistry, 2010, 19(3): 327-332.
[10] LIU Y Q, SHE N N, ZHAO J C. Fabrication of hierarchical porous ZnO and its performance in Ni/ZnO reactive-adsorption desulfurization[J].Pet Sci, 2013, 10(4): 589-595.
[11] KONG A H, WEI Y Y, LI Y H. Reactive adsorption desulfurization over a Ni/ZnO adsorbent prepared by homogeneous precipitation[J].Front Chem Sci Eng, 2013, 7(2): 170-176.
[12] ANDREY R, IGOR B, BELLAT J P. Reactive adsorption of thiophene on Ni/ZnO: Role of hydrogen pretreatment and nature of the rate determining step[J].Applied Catalysis B: Environmental, 2008, 84(3): 766.
[13] 李芬, 邵纯红, 闫波, 等. 铁掺杂纳米ZnO室温脱硫剂的硫化及再生研究[J].无机化学学报, 2008, 24(10): 15-64. (LI Fen, SHAO Chunhong, YAN Bo, et al. Sulfidation and regeneration of nano-Fe-ZnO desulfurizer at ambient temperature[J].Chinese Journal of Inorganic Chemisitry, 2008, 24(10): 15-64.)
[14] ZHANG Y L,YANG Y X, LIN F. Improvement of adsorptive desulfurization performance of Ni/ZnO adsorbent by doping with Mn additive[J].Chinese Journal of Catalysis, 2013, 34(1): 140-145.
[15] 李治俊, 石秋杰, 李彬, 等. 钕对Ni/ZnO催化剂催化噻吩加氢脱硫的改性研究[J].中国稀土学报, 2008, 26(5): 521-524. (LI Zhijun, SHI Qiujie, LI Ben, et al. Reserch of Ni/ZnO catalyst modificatied by Nd used for thiophene hydrodesulfurization[J].Journal of the Chinese Rare Earth Society, 2008, 26(5): 521-524.)
[16] 于宙, 李祥, 龙雪, 等. Mn掺杂ZnO稀磁半导体材料的制备和磁性研究[J].物理学报, 2008, 57(7): 4539-4544. (YU Zhou, LI Xiang, LONG Xue, et al. The preparation and magnetic studies of Mn doped ZnO dilute magnetic semiconductor materials[J].Acta Physica Sinica, 2008, 57(7): 4539-4544.)
[17] 李彤, 介琼, 张宇, 等. 工作气压对ZnO∶Mn薄膜结构特性的影响. 发光学报, 2013, 34(6): 711- 714. (LI Tong, JIE Qiong, ZHANG Yu, et al. Influence of working pressure on the structural properties of ZnO∶Mn thin film[J].Chinese Journal of Luminescence, 2013, 34(6): 711- 714.)
[18] 位子涵, 孙永娇, 赵振廷, 等. 锰掺杂花状ZnO的合成及其光催化特性研究[J].功能材料, 2015, 46(9): 9081-9085. (WEI Zihan, SUN Yongjiao, ZHAO Zhenting, et al. Research of the synthesis of Mn doped flower ZnO and its photocatalytic properties[J].Functional Materials, 2015, 46(9): 9081-9085.)
[19] 李生娟, 王树林, 徐波. 纳米活性炭/锌锰复合电极材料的制备及性能[J].化工学报, 2010, 61(1): 223-227. (LI Shengjuan, WANG Shulin, XU Bo. Preparation and properties of activated carbon nano-particles/Zn- MnO composite electrode material[J].CIESC Journal, 2010,61(1): 223-227.)
[20] 赵红晓, 王淑敏, 薛登启, 等. Pt-ZnO/C复合材料的合成及对醇类催化活性的研究[J].燃料化学学报, 2011, 39(2): 140-143. (ZHAO Hongxiao, WANG Shumin, XUE Dengqi, et al. Synthesis of Pt-ZnO/C composites and their catalytic activity for alcohols oxidation[J].Journal of Fuel Chemistry and Technology, 2011, 39(2): 140-143.)
[21] 周正有, 罗广圣, 江风益, 等. ZnMnO3及LaZnMnO3的制备及结构特性[J].航空材料学报, 2007, 27(2): 68-73. (ZHOU Zhengyou, LUO Guangsheng, JIANG Fengyi, et al. Preparation and Structure Features of ZnMnO3and LaZnMnO3[J].Journal of Aeronautical Materials, 2007,27(2): 68-73.)
[22] WANG Y, SUN L, KONG L G, et al. Room-temperature ferromagnetism in Co-doped ZnO bulk induced by hydrogenation[J].J Alloy Compd, 2006, 423(1-2): 256-259.
[23] WEI Y J, NAM K W, KIM K B, et al. Spectroscopic studies of the structural properties of Ni substituted spinel LiMn2O4[J].Solid State Ionics, 2006, 177(1-2): 29-35.
[24] SHAJU K M, SUBBA R G V, CHOWDARI B V R. X-ray photoelectron spectroscopy and electrochemical behaviour of 4V cathode, Li(Ni1/2Mn1/2)O2[J].Solid State Ionics, 2003,48(11): 1505-1514.
[25] KHAN S B, RAHMAN M M, MARWANI H M, et al. An assessment of zinc oxide nanosheets as a selective adsorbent for cadmium[J].Nanoscale Research Letters, 2007, 8(9): 377-385.
[26] 刘东亮, 金永中. 纳米镍粉的尺寸效应[J].化工时刊, 2006, 19(8): 7-9. (LIU Dongliang, JIN Yongzhong. The size efiect of nanoscale nickel powder[J].Chemical Industry Times, 2006, 19(8): 7-9.)
[27] RYZHIKOV A, BEZVERKHYY I, BELLAT J P. Reactive adsorption of thiophene on Ni/ZnO—Role of hydrogen pretreatment and nature of the rate determining step[J].Applied Catalysis B: Environmental, 2008, 84(3): 766-772.
[28] ZHANG X Y, ZHENG X R, HAN P, et al. Effects of ultrasound on the desulfurization performance of hot coal gas over Zn-Mn-Cu supported on semi-coke sorbent prepared by high-pressure impregnation method[J].Journal of Energy Chemistry, 2015, (24): 291- 298.
Structure and Desulfurization Performance of Ni Supported on Mn-Zn Mixed Metal Oxide
KANG Lei1,2, WANG Haiyan1,2, GUAN Zongchi2, WANG Yujia2, LIU Dongmei2, YANG Zhanxu2
(1.CollegeofChemicalEngineering,ChinaUniversityofPetroleum,Qingdao266580,China;2.CollegeofChemistry,ChemicalEngineeringandEnvironmentalEngineering,LiaoningUniversityofPetroleum&ChemicalTechnology,Fushun113001,China)
Mn-Zn composit oxide was prepared by hydrothermal method, and Ni was supported on it by the method of equal volume impregnation to prepare the drodesulfurization catalyst, which were characterized by XRD, FT-IR, N2adsorption-desorption and XPS. And then the catalytic drodesulfurization performance of the prepared catalyst was evaluated with thiophene-heptane mixture as model material. The results showed that in the Mn-Zn composit oxide the valence state of Mn was +4, and Mn entered into the lattice of ZnO. The Zn cells were replaced by Mn+4, the crystal cell parameters and particle size of ZnO were changed, with the significant increase of BET surface area, pore volume and pore diameter. The desulfurization rate of the model oil over Mn-Zn composit oxide supported Ni catalyst was increased nearly 14%, compared to ZnO supported Ni catalyst, and the former also possessed better reusability.
hydrothermal method; Mn; ZnO; S-Zorb; desulfurization
2016-03-10
国家自然科学基金项目(21401093)和辽宁省自然科学基金项目(201202126)资助
康蕾,女,讲师,博士研究生;从事清洁燃料生产的研究;E-mail:kllk811003@163.com
王海彦,男,教授,从事清洁燃料生产的研究;E-mail:fswhy@126.com
1001-8719(2017)01-0049-07
TE643
A
10.3969/j.issn.1001-8719.2017.01.007
