肾脏滤过分数对单侧肾动脉狭窄腔内治疗选择的影响
2017-02-08冯琦琛栾景源王昌明李天润
冯琦琛 李 选 栾景源 王昌明 李天润
(北京大学第三医院介入血管外科,北京 100083)
·临床研究·
肾脏滤过分数对单侧肾动脉狭窄腔内治疗选择的影响
冯琦琛 李 选*栾景源 王昌明 李天润
(北京大学第三医院介入血管外科,北京 100083)
目的 探讨肾脏滤过分数(filtration fraction,FF)对单侧肾动脉狭窄腔内治疗的影响。 方法 2014年5月~2015年11月我们对31例单侧肾动脉狭窄行经皮肾动脉成形支架植入术(percutaneous transluminal renal angioplasty and stent,PTRAS),分析患者术前与术后健侧肾脏、患侧肾脏肾小球滤过率(glomerular filtration rate,GFR)、肾有效血浆流量(effective renal plasma flow,ERPF)、FF变化,观察患者血压(收缩压)和服用降压药种类的变化。 结果 31例PTRAS均成功。术前患侧GFR(28.79±12.88)ml/min,明显低于健侧(41.72±14.23)ml/min(t=-3.749,P=0.000);术前患侧ERPF(124.55±49.36)ml/min,明显低于健侧(186.92±43.22)ml/min(t=-5.293,P=0.000)。术后患侧肾脏GFR(30.40±12.85)ml/min,明显高于术前(28.79±12.88)ml/min(t=-2.236,P=0.003);术后患侧肾脏ERPF(137.46±47.00)ml/min,明显高于术前(124.55±49.36)ml/min(t=-5.017,P=0.000);术后患侧FF (22.24±5.52)%较术前(24.93±8.68)%明显降低(更趋近于正常值)(t=2.577,P=0.015)。术后患侧GFR(30.39±12.84)ml/min,仍明显低于健侧(40.31±13.87)ml/min(t=-2.920,P=0.005);术后患侧ERPF(137.46±47.00)ml/min,明显低于健侧(178.25±42.25)ml/min(t=-3.593,P=0.001)。术后患侧FF (22.24±5.52)%与健侧FF (22.52±5.73)%无统计学差异(t=-0.195,P=0.846)。术前FF相对正常的患肾,术后FF (21.45±3.35)%较术前FF (21.77±3.26)%变化较小(t=0.847,P=0.407);术前FF明显升高的患肾,术后FF (27.21±5.34)%较术前FF (36.88±6.00)%明显降低(趋向正常值)(t=3.495,P=0.010)。术前肌酐(96.97±25.81)μmol/L与术后(94.39±22.45)μmol/L无统计学差异(t=0.420,P=0.676)。术后收缩压(144.4±11.1)mm Hg较术前(158.5±13.7)mm Hg明显下降(t=7.804,P=0.000);服用降压药物种类术后(2.6±0.6)种,较术前(3.0±0.5)种明显减少(t=4.655,P=0.000)。 结论 对于肾动脉狭窄患者,分肾FF是了解肾脏缺血病理生理进程的有益指标。对于单侧肾动脉狭窄患者,术前FF显著增高或FF相对正常,应视为肾动脉支架植入术的手术指征。
单侧肾动脉狭窄; 经皮肾动脉成形支架植入术; 肾小球滤过率; 肾有效血浆流量; 滤过分数
肾动脉狭窄是引起继发性高血压、缺血性肾病、终末期肾病的一个潜在原因[1]。经皮肾动脉成形支架植入术(percutaneous transluminal renal angioplasty and stent,PTRAS)治疗肾动脉狭窄已广泛应用于临床,对动脉粥样硬化所致肾动脉狭窄患者,PTRAS有益于高血压的降级[2],改善肾功能或减缓肾功能的恶化[3,4],但是Parikh等[5]多中心临床试验结果并不支持上述观点,因此,PTRAS临床应用仍存在较大争议[6]。Weinberg等[7]认为适应证的选择缺陷可能是导致临床试验研究结果失实的重要原因。评价肾脏缺血,通过测定血肌酐或估算肾小球滤过率(estimated glomerular filtration rate, eGFR)是临床最常用的方法。但对于血肌酐已有升高的缺血性肾病患者,肾功能可能已出现不可逆损伤;对于单侧肾动脉狭窄患者,血肌酐和(或)eGFR在正常水平,常常是健侧肾代偿的假象。以EDTA作为显像剂了解分肾GFR,可以发现缺血性肾病所造成的GFR降低。影响分肾GFR变化的因素较多(如高血压、各种肾炎或肾病等),不能充分反映患肾的功能及支架植入术后肾功能的变化情况。临床经验与临床试验间巨大的反差,提示我们对于肾动脉狭窄患者的治疗,PTRAS可能需要更新适应证,以及新的疗效评价标准。2014年5月~2015年11月我们应用99mTc-EC 测定肾有效血浆流量(effective renal plasma flow,ERPF),结合EDTA核素肾扫描测定GFR,计算肾脏滤过分数(filtration fraction,FF),对比PTRAS术前后的变化规律,旨在探讨PTRAS适应证的客观指标。
1 临床资料与方法
1.1 一般资料
本组31例,男20例,女11例。年龄51~80岁,(65.3±8.5)岁。因近期血压控制不稳定发现肾动脉狭窄17例,因难治性高血压[在改善生活方式的基础上,应用合理可耐受的足量≥3种降压药物(包括利尿剂)治疗>1个月血压仍未达标,或服用≥4种降压药物才能有效控制血压]发现肾动脉狭窄9例,因肾功能不全发现肾动脉狭窄1例,因行其他部位CTA发现肾动脉狭窄4例。均为单侧肾动脉狭窄,左侧14例,右侧17例。均合并原发性高血压,术前血压136~190(158.5±13.7)/68~107(86.3±10.2)mm Hg。所有患者均应用2种以上降压药物控制血压,(3.0±0.5)种,包括钙离子拮抗剂、β-受体阻滞剂、硝酸酯类、α-受体阻滞剂及利尿剂。术前血肌酐63~169 μmol/L,(96.97±25.81)μmol/L。所有患者均通过腹主动脉造影明确诊断肾动脉狭窄,均为动脉粥样硬化性肾动脉狭窄,动脉狭窄部位均位于肾动脉起始端,狭窄率60%~100%,(79.2±11.6)%。合并2型糖尿病24例,冠状动脉硬化性心脏病(冠心病9)例,合并下肢动脉粥样硬化闭塞症5例。
病例选择标准:术前CTA明确单侧肾动脉狭窄,狭窄率>50%,同时合并难治性高血压,或术前CTA明确单侧肾动脉狭窄,狭窄率>70%[5],无介入治疗肾动脉狭窄的禁忌证。排除标准:造影剂过敏、术前明确肾脏长径<7 cm及双侧肾动脉狭窄。
1.2 方法
1.2.1 术前准备 所有患者一经诊断肾动脉狭窄即停用血管紧张素转换酶抑制剂(angiotensin converting enzyme inhibitors,ACEI)或血管紧张素Ⅱ受体拮抗剂(angiotensin Ⅱreceptor blocker,ARB)降压药,换用其他药物控制血压。同时至少术前3 d起服用阿司匹林肠溶片100 mg,qd,波立维75 mg,qd。术前完成99mTc-EC 测定ERPF和EDTA核素肾扫描测定GFR;行血清肌酐检查;测量术前3 d基础血压,计算收缩压平均值;记录术前口服降压药物种类。
1.2.2 手术方法 改良置Seldinger技术穿刺股动脉,置鞘。以“猪尾”导管于肾动脉水平行腹主动脉造影,证实肾动脉狭窄并测量狭窄率、狭窄长度及动脉直径。确认狭窄后,根据血管形态,应用F7肾动脉导引导管配合相应形状导管,利用导丝导管技术通过肾动脉狭窄段。根据血管直径应用球囊(sterling Boston Scientific)预扩张(6 atm,到达压力后立即释放球囊)。于肾动脉狭窄段置入球囊扩张式支架[Express SD, Boston Scientific Corporation,国食药监械(进)字2012第3460118号]。术中持续肝素盐水经Guiding灌注。术后24 h禁食禁水、补液,肝素持续泵入,维持活化部分凝血活酶时间(activated partial thromboplastin time, APTT)于正常值的2~3倍。术后复查腹主动脉造影。术后长期服用阿司匹林肠溶片100 mg,qd,波立维75 mg,qd 6个月。同时控制血压、血糖、血脂。术后1个月嘱患者于心内科根据血压情况调整降压药物。
1.3 随访
嘱患者术后3~6个月复查前3 d自行测量血压3次,记录3次收缩压平均值。随访患者术后降压药物调整情况,记录服用降压药物种类。患者术后3~6个月复查双侧肾脏GFR、ERPF及血肌酐。比较患者术前后收缩压、服用降压药物种类、血肌酐,术后双侧肾脏GFR和ERPF。根据GRF和ERPF计算FF,并比较术前与术后健侧肾脏、患侧肾脏FF的变化。
以术前患侧FF值为依据,以正常值18%~22%为基准,我们定义FF升高超过正常高限的30%(FF>28%)为FF绝对升高(本组8例),FF降低超过正常低限的30%(FF<14%)为FF绝对降低(本组2例),其余为相对正常(本组21例)。观察3种情况下患肾术后FF的变化情况。
1.4 观察指标
支架植入后肾动脉残余狭窄发生率;手术并发症;术后分肾GFR、ERPF、FF;术后血肌酐、血压;术后降压药物种类变化。
1.5 统计学分析
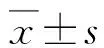
2 结果
PTRAS顺利, 31条肾动脉共植入肾动脉支架
31枚,无手术并发症。术后即刻肾动脉造影,肾动脉残余狭窄均<30%,手术成功率100%。
术前健侧肾GFR、ERPF明显高于患侧,差异有显著性(P<0.05);术前患肾FF高于健侧,但差异无显著性(P>0.05),见表1。患侧肾术后GFR、ERPF较术前明显增加(P<0.05)。健侧肾术后GFR较术前明显降低,术后ERPF较术前明显降低(P<0.05)。患侧肾术后FF较术前明显降低(P<0.05),健侧肾术前后FF无明显变化(表2)。术后患侧肾GFR、ERPF显著低于健侧(P<0.05),两侧肾FF无统计学差异(P>0.05),见表3。对于患侧肾脏,术前FF相对正常21例,术前后FF无统计学差异(P>0.05);术前FF明显升高8例,术后FF较术前明显降低(P<0.05),更接近于正常值(表4);术前FF明显降低2例,FF值分别为7.2%和13.5%,术后FF仍明显减低,分别为8.3%和13%,变化幅度不大。术前后血肌酐水平相当,无统计学差异(P>0.05);术后患者血压较术前明显下降(P<0.05);服用降压药物种类较术前减少,差异有显著性(P<0.05),见表5。


侧别GFR(ml/min)ERPF(ml/min)FF(%)患侧(n=31)28.79±12.88124.55±49.3624.93±8.68健侧(n=31)41.72±14.23186.92±43.2222.22±5.87t值-3.749-5.2931.443P值 0.000 0.0000.154

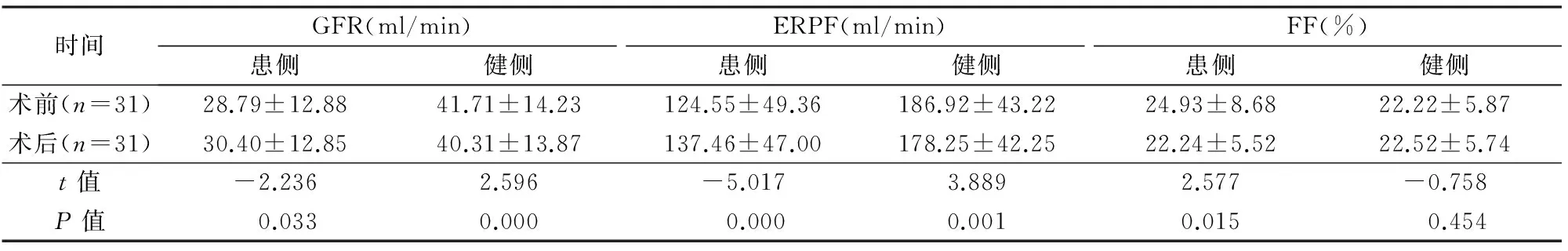
时间GFR(ml/min)ERPF(ml/min)FF(%)患侧健侧患侧健侧患侧健侧术前(n=31)28.79±12.8841.71±14.23124.55±49.36186.92±43.2224.93±8.6822.22±5.87术后(n=31)30.40±12.8540.31±13.87137.46±47.00178.25±42.2522.24±5.5222.52±5.74t值-2.2362.596-5.0173.8892.577-0.758P值 0.0330.000 0.0000.0010.015 0.454

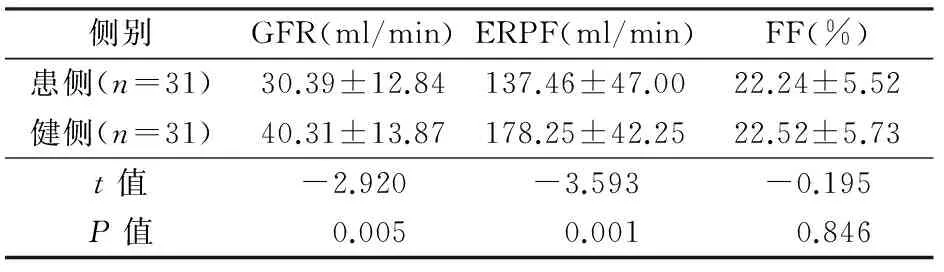
侧别GFR(ml/min)ERPF(ml/min)FF(%)患侧(n=31)30.39±12.84137.46±47.0022.24±5.52健侧(n=31)40.31±13.87178.25±42.2522.52±5.73t值-2.920-3.593-0.195P值 0.005 0.001 0.846


时间FF相对正常(n=21)FF绝对升高(n=8)术前21.77±3.2636.88±6.00术后21.45±3.3527.21±5.34t值0.8473.495P值0.4070.010
3 讨论
肾动脉狭窄临床较为常见,既是继发性高血压

表5 术前后血肌酐、收缩压及服用降压药物
的主要病因,也是导致终末期肾病的重要病因之一。肾动脉狭窄的腔内治疗技术已经广泛应用于临床,肾动脉支架植入术可以有效降低血压或使血压更易控制,停用或减少降压药物的剂量或种类。新版美国肾动脉支架植入术专家共识中,结合临床试验,对肾动脉狭窄支架植入术的手术指征做了进一步的规范,其中缺血性肾病是其主要适应证之一[5]。因此,肾动脉狭窄是否导致肾脏缺血这一问题,需要客观评价方法。
肾脏ERPF主要通过检测肾小管功能,了解肾脏血流灌注情况,是一种能够较好反应肾脏早期缺血的指标[8]。近年来,99mTc 标记的新型肾功能显像剂发展极为迅速,Tc-EC为肾小管分泌型肾功能显像剂,由肾小管主动分泌,其他组织几乎不摄取,在肾内浓集高,靶/本底计数比高,经肾快速排泄,水溶性强,化学稳定性好,可以得出更为精准的检测结果[9]。本研究就是应用99mTc-EC作为显像剂,检测分肾ERPF来评价肾脏血流灌注情况。
FF是GFR/ERPF的比值,是反应肾脏储备能力的一个重要指标,代表流经肾脏的血液被肾小球滤过的百分比,FF正常值为18%~22%。当肾小管功能受损时,FF增高,而肾小球功能受损时FF值下降,故可判断肾脏损害的性质[8]。本研究结果显示单侧肾动脉狭窄患者,患肾GFR和ERPF,较健肾明显降低,说明肾动脉狭窄对肾脏血流灌注及肾功能的影响是明确的。患肾FF高于健肾,提示本组患者以肾小管功能受损为主。
肾动脉支架植入术后,患侧GFR、ERPF较术前明显增加,FF降低更加趋向正常值,是肾脏血流恢复,肾脏功能改善的结果。健侧GFR和ERPF较术前降低,而FF无明显变化,反映双肾血流灌注重新分配,健肾血流量减少。
如上所述,FF是反应肾脏储备能力的一个重要指标,有助于判断肾脏损害的性质。术前患肾的缺血程度及性质不同,肾动脉支架植入术的结果亦不同。术前FF明显升高的患肾,术后FF较术前显著降低,更趋近于正常值。提示我们恢复肾脏血流灌注,有利于改善肾间质的缺血损伤,肾脏功能可以得到有效保存,FF升高的患肾具有改善肾功能的潜力。对于术前FF相对正常的患肾,术后FF较术前无明显变化,这一现象可能与以下原因有关:肾动脉狭窄,肾脏经历了肾血流减少但肾小球率过滤仍然正常的代偿阶段(FF明显升高阶段)后,肾脏的代偿能力逐渐减退,肾脏为维持髓质的血供,部分肾小球功能自动处于休眠状态,肾小球率过滤减低,FF恢复至20%左右,达到能够平衡肾脏灌注和滤过功能的状态。在这种状态下,纠正肾动脉狭窄,肾脏血流能够恢复,在肾髓质血供得到保证的情况下,肾小球的滤过功能也可以得到恢复,肾脏功能可以得到正常维持,术后FF仍维持相对正常水平。我们认为这一现象说明肾缺血,FF值正常反映肾小管和肾小球相对早期功能受损,肾动脉支架植入术对于恢复肾脏功能依然有益。本组2例术前FF明显降低,术后FF直观上均无改善,我们依然有理由相信,由于肾脏缺血时间延长,肾小球逐渐发展为不可逆的病理性损毁,数量逐渐增多,最终造成肾脏滤过功能丧失,FF显著下降,肾动脉支架植入术对恢复肾功能无益。
本组术前后血肌酐未见明显变化。因此,我们认为单纯通过血肌酐水平判断肾功能是否改善,对单侧肾动脉狭窄患者是缺少临床意义的,这现象同样反映肾脏的代偿机制。
对于肾动脉狭窄患者,肾动脉支架植入术后血压和服用降压药物种类的变化,本组结果我们得到了与以往相同的结论[10]。肾动脉支架植入术后患者血压较术前明显下降,服用降压药物种类较术前明显减少。由于本组患者均合并原发性高血压,不除外患者存在高血压所致肾小球硬化对检验结果的影响,但是即使对于存在其他慢性肾病的患者,肾动脉狭窄解除后对于缺血性肾病也是有益的。
综上所述,分肾GFR和ERPF能提示肾脏缺血,但对于肾动脉狭窄患者,分肾FF对判断肾脏早期缺血性损伤和肾脏储备功能有重要的意义。对于单侧肾动脉狭窄患者,术前FF显著增高或FF相对正常,应视为肾动脉支架植入术的手术指征;对于术前FF显著降低的肾动脉狭窄患者,肾动脉支架植入术对于改善肾脏功能可能意义不大。
1 刘 波,吕建峰,粟治洲,等.动脉粥样硬化性肾动脉狭窄传统危险因素的Meta分析.第三军医大学学报,2014,36(19):2037-2043.
2 金仲慧,张 龙,张燕燕,等.肾素-血管紧张素检测在经皮腔内肾动脉成形术中的临床价值.中国微创外科杂志,2014,14(11):1023-1027.
3 White CJ, Olin JW, Diagnosis and management of atherosclerotic renal artery stenosis: improving patient selection and outcomes.Nat Clin Pract Cardiovasc Med,2009,6(3):176-190.
4 George JC, White CJ. Renal artery stenting: lessons from ASTRAL (Angioplasty and Stenting for Renal Artery Lesions). JACC Cardiovasc Interv,2010,3(7):786-787.
5 Parikh MD, Shishehbor DO, Gray BH, et al.SCAI expert consensus statement for renal artery stenting appropriate use. Catheter Cardiovasc Interv,2014,84(7):1163-1171.
6 Cooper CJ, Murphy TP, Cutlip DE, et al.Stenting and medical therapy for atherosclerotic renal-artery stenosis. N Engl J Med,2014,370(1):13-22.
7 Weinberg MD,Olin JW. Stenting for atherosclerotic renal artery stenosis: One poorly designed trial after another. Cleve Clin J Med,2010,77(3):164-171.
8 林 伟,邬恒夫,叶广春,等.99mTc-DTPA与131I-OIH双核素肾动态显像对肾功能的评价.中华核医学杂志,2002,22(4):221-222.
9 饶国辉,李春亿,林增桃,等.99mTc-EC肾动态显像及有效血浆流量测定的临床应用.中国医学影像技术,1996,12(3):169-171.
10 Nordmann AJ, Woo K, Parkes R, et al. Balloon angioplasty or medical therapy for hypertensive patients with atherosclerotic renal artery stenosis? A meta-analysis of randomized controlled trials. Am Med, 2003,114(1):44-50.
(修回日期:2016-10-26)
(责任编辑:李贺琼)
Effects of Renal Filtration Fraction on Endovascular Treatment Selection for Unilateral Renal Artery Stenosis
FengQichen,LiXuan,LuanJingyuan,etal.
DepartmentofInterventionalRadiologyandVascularSurgery,PekingUniversityThirdHospital,Beijing100083,China
LiXuan,E-mail: 13701091788@139.com
Objective To investigate the effects of fraction filtration(FF) on endovascular treatment for patients with unilateral renal artery stenosis. Methods Percutaneous transluminal renal angioplasty and stent (PTRAS) was performed in 31 patients with unilateral renal artery stenosis from May 2014 to November 2015. Preoperative and postoperative glomerular filtration rate (GFR), effective renal plasma flow (ERPF), and renal FF of healthy and diseased kidneys were compared. The blood pressure (SBP) and antihypertensive drugs use were recorded. Results The PTRAS was successfully accomplished in all the 31 cases. Preoperative ipsilateral GFR [(28.79±12.88) ml/min] was significantly lower than that of the contralateral [(41.72±14.23) ml/min,t=-3.749,P=0.000]. Preoperative ipsilateral ERPF [(124.55±49.36) ml/min] was significantly lower than that of the contralateral [(186.92±43.22) ml/min,t=-5.293,P=0.000]. Postoperative ipsilateral renal GFR [(30.40±12.85) ml/min] was significantly higher than that before operation [(28.79±12.88) ml/min,t=-2.236,P=0.003]. Postoperative ipsilateral renal ERPF [(137.46±47.00) ml/min] was significantly higher than of the preoperative [(124.55±49.36) ml/min,t=-5.017,P=0.000]. Postoperative ipsilateral FF (22.24±5.52)% decreased significantly as compared with the preoperative level (24.93±8.68)% (more close to the normal value,t=2.577,P=0.015). Postoperative ipsilateral GFR [(30.39±12.84) ml/min] was still significantly lower than the contralateral [(40.31±13.87) ml/min,t=-2.920,P=0.005]. Postoperative ipsilateral ERPF [(137.46±47.00) ml/min] was significantly lower than that of the contralateral [(178.25±42.25) ml/min,t=-3.593,P=0.001]. No statistical difference was seen between postoperative ipsilateral FF (22.24±5.52)% and contralateral FF (22.52±5.73)% (t=-0.195,P=0.846). In cases with relatively normal preoperative FF, postoperative FF (21.45±3.35)% had small changes compared with the preoperative FF [(21.77±3.26)%,t=0.847,P=0.407]. While in cases with significantly risk-increased preoperative FF, postoperative FF (27.21±5.34)% decreased significantly as compared with the preoperative FF [(36.88±6.00)%,t=3.495,P=0.010]. Preoperative creatinine [(96.97±25.81) μmol/L] and serum creatinine [(94.39±22.45) μmol/L] levels were not statistically significant (t=0.420,P=0.676). Postoperative blood pressure [(144.4±11.1) mm Hg] decreased significantly as compared with preoperative level [(158.5±13.7) mm Hg,t=7.804,P=0.000]. The number of antihypertensive drugs after operation (2.6±0.6) was significantly reduced as compared with before operation [(3.0±0.5),t=4.655,P=0.000]. Conclusions For patients with renal artery stenosis, FF is a useful index to understand the pathophysiological process of renal ischemia. For patients with unilateral renal artery stenosis, significantly increased or relatively normal preoperative FF should be regarded as indications of renal artery stent implantation.
Unilateral renal artery stenosis; Percutaneous transluminal renal angioplasty and stent; Glomerular filtration rate; Effective renal plasma flow; Filtration fraction
A
1009-6604(2017)01-0051-04
10.3969/j.issn.1009-6604.2017.01.014
2016-04-20)
*通讯作者,E-mail:13701091788@139.com
