动态心电心阻抗监测系统的研究
2017-01-21胡欣宇王宇星
胡欣宇++王宇星

摘 要:心血管方面的慢性疾病已成为威胁人类健康的主要疾病,心脏病是造成人类死亡的三大疾病(心脏病、脑血管病和癌症)之一。由于心脏病的发病有很大的偶然性和突发性,开展心脏功能的动态监测非常必要。现有的Holter心电图机只能监测心脏的电学性能,无法对心脏的泵血能力进行动态监测。血流动力学参数是衡量心脏收缩性能和泵血能力的重要指标。为了克服现有系统的不足,文中设计了一种可以动态监测用户心电、心阻抗的传感器系统,本系统能够准确反映用户心脏的电学传导性能和机械泵血性能。
关键词:心电;心阻抗;血流动力学参数;动态监测
中图分类号:TN710;TP393 文献标识码:A 文章编号:2095-1302(2016)12-00-04
0 引 言
由于人们生活方式和膳食结构的改变,因心脏与循环系统不健康而导致的心血管疾病已逐步成为威胁人类健康的多发病症,而且发病率、致残率和死亡率逐年提高,已超越其他疾病高居首位,成为危害人类健康的第一杀手。目前我国城市人口中每5个成年人中就有1个人患有不同程度的心血管方面的疾病。中国每年有100万人死于该类疾病,有更多的人因此致残[1]。由于常规的Holter心电图机只能反映心脏的电学性能,无法反映心脏的机械性能,因此不能对心脏功能做出综合全面的评价,所以心电与血流动力学参数的同时监测变得尤为重要。
血流动力学是研究和衡量循环系统中血液流动循环效率、心脏收缩性能和泵血功能的重要指标,其中心排量和脉搏量是两个最重要的参数。心排量是每分钟心脏泵出血液的总量,是评价心脏收缩功能的重要指标,其变化能够提供机体功能或基础代谢率需求发生重大变化时的早期报警;脉搏量是评价左心室泵血功能的重要指标,其变化是血流量和心肌收缩发生变化的早期信号。它们的监测对于掌握病情、早期发现心血管功能异常,尤其对指导临床针对性用药、抢救血流动力学不稳定的患者以及监测用药疗效十分显著。
心阻抗法(Impedance Cardiography, ICG)又称胸阻抗法,是生物阻抗技术在血流动力学参数监测领域的一个应用。随着心脏的收缩和舒张活动,主动脉内的容积随血流量变化,故其阻抗也随血流量变化。心脏射血时,左心室内的血液迅速流入主动脉,主动脉血容量增加,体积增大,阻抗减小;当心脏舒张时,主动脉弹性回缩血容量减少,体积减小,阻抗增大。由人体的电生理特性可知,血液的电导率要比胸腔中的其他组织高很多,电流在胸部传导时会寻找阻力最小的路径,而胸部的血液主要集中在主动脉处[2],因此胸部阻抗的变化主要来源于主动脉血流的阻抗变化。对这种变化的阻抗信号进行一定的分析处理就可以得到包括心排量在内的血流动力学参数,同时由于其具有简单、无创、安全、易操作、成本低等特点,已被广泛应用于临床,而且该方法便于和心电集成,因此决定采用心阻抗法来进行血流动力学参数的动态监测。
1 心阻抗信号的检测原理
1.1 激励方式
生物阻抗测量的激励方式分为采用幅值恒定的交流电流激励来测量边界点的电位差和采用幅值恒定的交流电压激励,测量流过被测对象的电流两种。
相对而言,在采用电压激励、电流检测的方式时,由于无法预测被测对象的阻抗可能出现的情况,流入被测对象中的电流大小不容易控制,当生物体的阻抗较小时,通过生物体的激励电流就有可能超出生物体所能承受的安全电流范围,影响生物组织的活性,从而危及人身安全,因此需要对注入人体的电流大小加以控制。而采用电流激励、电压检测的方式时,电流源激励模式受未知接触阻抗的影响小,且加到各电极的电流幅值恒定、可控,从而可以保护被测对象的人身安全。而且从检测技术角度看,电压检测比电流检测对检测模块的要求低,更容易实现,因此本文采用电流激励、电压检测的方式来进行心阻抗信号的采集。
1.2 电极配置
常用的生物阻抗测量方法可以分为四电极法和两电极法,如图1(a)和图1(b)所示。四电极法需要4个电极,一对激励电极用于引入恒定的激励电流,一对检测电极用于测量被测对象感应出的电压;而两电极法需要2个电极,这两个电极同时作为激励电极和检测电极使用。
在进行生物阻抗测量时,电极和皮肤之间存在接触阻抗,若使用两电极法测量生物阻抗,由于激励和检测电极为同一对电极,激励电流同时流过接触阻抗和被测对象,接触阻抗将叠加在被测对象的生物阻抗上。由于电极和皮肤的接触阻抗不是一个固定值,会随接触面积而改变,从而使测量结果受到较大的影响。
采用四电极法测量生物阻抗时,因检测电极和激励电极分离,且检测电极位于激励电极之间,激励电流不流经检测电极与皮肤间的接触阻抗,激励电流使被测对象感应的电压信号无衰减的通过检测电极与皮肤之间的接触阻抗[3]。故使用四电极法测量生物阻抗时,电极和皮肤的接触阻抗对测量结果的影响很小,因此本文采用四电极法进行心阻抗信号的测量。
1.3 电极位置分布
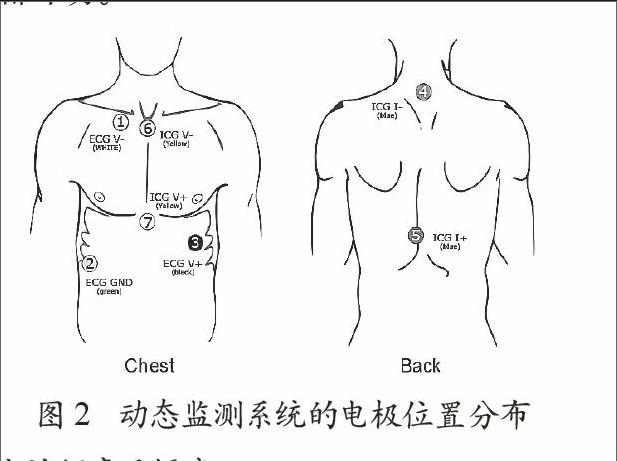
本文采用的心阻抗电极位置分布如图2所示,其背后的4号和5号是激励电极,胸前的6号和7号是检测电极。6号电极位于锁骨之间的胸骨颈静脉切迹,7号电极位于剑突处,在竖直方向上激励电极距离同侧的检测电极至少3 cm。这样的电极位置分布主要有2个优点:
(1)电极被放置在身体的中线处,身体运动时该部位最不容易引起电极移位,可最大程度减小运动伪迹的影响;
(2)在获得最强心阻抗信号的前提下,两个检测电极之间的距离应尽可能短,使噪声最小化,有利于提高信噪比。
由于大部分心阻抗信号来源于胸腔的上三分之一部分,所以本文将检测电极全部置于胸骨上方,一个位于第四肋骨,一个位于颈部。
由于系统用于动态监测,为避免影响到用户的日常活动,心电监测将不使用多导联。标准肢体导联能够比较广泛的反映出心脏的常见疾病,比如心律失常、后壁心肌梗塞等,尤其是在II导联中的波形改变最为明显,所以采用标准II导联进行单导联心电监测。其中1号、2号和3号电极用来监测心电信号,2号电极是右腿驱动。1号电极稍微低于右锁骨,位于胸骨的右侧;2号电极位于身体右侧较低的两根肋骨之间;3号电极位于左侧胸部下方。
1.4 激励电流的频率及幅度
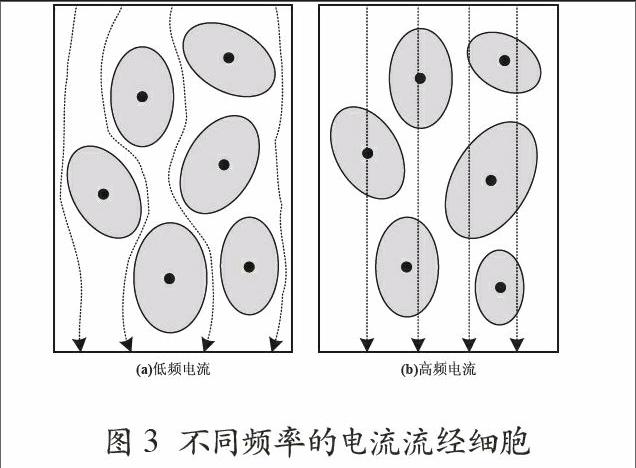
生物组织中含有大量不同形状的细胞,这些细胞由细胞膜、细胞外液和细胞内液组成。从电特性上看,细胞外液和细胞内液可视为电解质,可以将细胞膜等效为电容。因此,当直流或低频电流施加于生物组织时,电流将以任意一种可能的方式绕过细胞,主要流经细胞外液;随着电流频率的提高,细胞膜电容的容抗减小,一部分电流将穿过细胞膜流经细胞内液,如图3所示。所以生物组织的低频电阻抗较大而高频电阻抗较小,电阻抗值由大到小的过渡反映了生物组织细胞膜的电容性质[4]。
生物阻抗或介电特性参数在某个频率范围内有显著的变化,生物组织内存在三个不同的频率散射,分别为、和频散,如图4所示。生物组织的相对介电常数r随频率变化有三个明显的散射区域。
(1)频段主要发生在音频频段(10 Hz10 kHz),是因包围组织内细胞离子层发生变化引起的,主要表现为细胞膜电容发生变化;
(2)频段主要发生在射频频段(10 kHz10 MHz),主要由膜电容的容性短路和生物高分子的旋转松弛所引起。在此频段内,细胞膜电容基本恒定,因而随着频率的增加,膜电容的容抗减小,表现为电导率随频率升高而增大,相对介电常数则随频率升高而减小;
(3)频段主要发生在微波频段(10 MHz以上),是由蛋白质和蛋白质结合产生的水在电场作用下引起分子的偶极转动导致的[5]。
在进行人体阻抗测量时,考虑到人体组织的特征频率在10100 kHz 之间,所以人体阻抗的测量所采用的激励电流频率大都在频段内。如果频率太低,容易产生刺激和激化作用;如果频率太高,又容易使体内产生较多的热量而造成机体灼伤。当频率在50 kHz 以下时,皮肤和电极之间的接触阻抗增加,与电极相关的伪迹信号就会增加,影响测量的准确性[6]。综合以上因素,本文选取频率在50100 kHz之间的激励电流。
对人体而言,安全电压在正常、干燥的环境中为36 V,潮湿环境下为12 V。而能引起人体知觉的直流电流最小为5 mA,交流电流最小为1 mA[7]。测量生物阻抗时一般采取0.11 mA 的交流电流作为激励源,本文采用的激励电流为0.1 mA,远小于1 mA,极大地保证了人身安全。
2 动态心电心阻抗监测电路
基于前文对心阻抗检测原理的分析,本文采用激励电极和检测电极分开的四电极法,电极选用Ag/AgCl材料,通过激励电极在人体胸腔的两端加上一个交变的恒流源,激励电流采用频率为64 kHz,幅度为0.1 mA的方波信号,然后由位于激励电极中间的检测电极来检测主动脉血流感应出的电压信号,该电压信号经开关解调器、高通滤波、交流放大和低通滤波后即可提取出主动脉血流的阻抗变化信号,对该信号进行微分并取负,就可以获得心阻抗信号。
动态心电心阻抗监测系统的电路主要分为信号采集模块、无线通信模块和电源管理模块。
(1)信号采集模块完成心电和心阻抗信号的采集任务;
(2)无线通信模块作为电路的微控制器,通过蓝牙V4.0低功耗协议实现与PC机或者任何支持蓝牙协议的移动设备间的数据通信;
(3)电源管理模块主要完成锂离子电池的充电和电压转换功能。
2.1 信号采集
由于心电和心阻抗信号的微弱特性,分立元器件设计的信号采集电路极易引入空间的电磁干扰,降低信噪比。而集成前端芯片具有功能模块化、低功耗、抗干扰、便携等优点,为生理信号采集提供了新的思路。本文采用TI公司的ADS1292R芯片来完成心电和心阻抗信号的采集。ADS1292R是2通道、同步采样、24位、三角积分的低功耗模数转换器(ADC),此转换器具有内置的低噪声可编程增益放大器、内部参考电压、串行SPI接口、一个内部振荡器和灵活的断电、待机模式。与以往由分立器件组成的电路相比,ADS1292R可在大大减少尺寸、功耗和总体成本的前提下实现可升级医疗仪器系统的创建。此外,可选择输入通道的任一配置生成右腿驱动(RLD) 输出信号。ADS1292R的采样率范围为125 SPS至8 kSPS,其共模抑制比(CMRR)高达-105 dB。ADS1292R还包括一个完全集成的阻抗测量功能,内部有激励电流源和解调模块,可以用来完成心阻抗信号的测量[8]。ADS1292R的通道1采集心阻抗信号,通道2主要采集心电信号,它可与单片机通过SPI接口进行数据通信,由此构成心电和心阻抗信号采集的核心电路。
2.2 无线通信
有线通信方式会妨碍动态监测,所以必须采用无线通信手段来完成数据传输。为了能够实现长时间的连续动态监测,本文采用蓝兆科技公司(Bluegiga Technologies)生产的BLE113芯片作为微控制器和无线传输单元,其内部是TI公司的蓝牙V4.0低功耗协议芯片CC2541。CC2541集成了高性能低功耗的8051内核和2.4 GHz射频收发器,在发送模式和外部中断模式下电流功耗分别为14.3 mA和0.5 A,支持250 Kb/s、500 Kb/s、1 Mb/s、2 Mb/s的数据传输速率,其卓越的性能完全满足动态监测的低功耗需求[9]。BLE113还支持蓝牙V4.0的BLE低功耗协议栈,可以加快下位机程序的开发进度。BLE113几乎不需要外围电路即可实现与外界的蓝牙通信,具体如图5所示,电路中只连接一个用于工作模式和休眠模式切换的按键及两个用于连接蓝牙和发送数据的LED指示灯。
2.3 电源管理
电源管理的首要任务就是提供给各芯片稳定的直流电压,使其能够正常工作。稳压电路要求供电稳定、电压纹波小。动态心电心阻抗监测电路采用锂离子电池进行供电,电路上各芯片正常工作只需要2.1 V和3.0 V两种电压,于是需要采用两种电压转换芯片来完成稳压任务。
本文采用TI公司生产的TPS62730实现2.1 V电压转换,为BLE113供电,电压转换电路如图6所示。TPS62730是一款高频同步降压DC-DC转换器,针对超低功耗无线应用进行了优化。它可提供高达100 mA的输出电流,该芯片的输入电压范围为1.93.9 V。由于锂离子电池在充电过满时,电压会高于3.9 V,因此为了保证输入TPS62730的电压在1.93.9 V范围内,需要在锂离子电池后面串入一个20 Ω的分压电阻来保证TPS62730可以正常工作。
本文采用TI公司生产的TPS73201来实现3.0 V电压转换,为ADS1292R供电,电压转换电路如图7所示。该芯片的电压输入范围为1.75.5 V,即使锂离子电池过冲也不会影响其正常工作。转换电路通过调节R37和R38的阻值以改变输出电压的大小,在此选取R37和R38的阻值分别为46.4 k和30.9 k,使得输出电压能够稳定在3.0 V,以保证ADS1292R能够正常工作。
为了能够给锂离子电池充电,并考虑到充电管理芯片的小尺寸封装及外围电路复杂度等因素,本文选择了MAXIM公司生产的MAX8808型线性充电管理芯片。该芯片的电压输入范围为4.515 V,当电压超过7 V时自动停止充电。同时,该芯片具有单机充电功能,能够自动控制整个充电过程,包括预充、快充、浮充及充满指示等。图8所示为充电管理电路,芯片外围电路简单,仅需很少的电阻和电容。充电电流的大小通过连接芯片第四引脚的R40电阻来调节。在此R40选用2.8 k电阻,充电电流大小为465 mA。充电状态由一个连接芯片第五引脚的蓝色LED灯指示,正在充电时LED灯亮,充电完成时LED灯熄灭。
3 动态心电心阻抗监测软件
动态心电心阻抗监测系统的软件设计主要包括上位机程序和下位机程序,下位机程序以IAR为开发平台,将调试好的C程序通过下载接口下载到BLE113中,单片机负责将采集到的心电和心阻抗信号通过蓝牙V4.0无线发送给PC机,PC机通过USB Dongle来接收单片机发送的数据。上位机程序以LabVIEW为操作平台,通过配置串口实现与单片机的无线通信,完成数据的显示、处理、分析以及存储等操作。
心电和心阻抗信号都是非常微弱的电生理信号,由于人体所处的环境复杂多变,各种外界干扰时常混入心电和心阻抗信号,使得有用信号淹没其中。外界干扰主要来源于工频干扰和基线漂移。工频干扰一般由供电网络引起,其频率固定为50 Hz;基线漂移一般由人体呼吸和电极移动引起,其频率低于10 Hz。工频干扰和基线漂移大大降低了心电和心阻抗信号的信噪比,从而影响心电和心阻抗信号检测的准确率[10],因此工频干扰和基线漂移的滤除显得尤为重要,去噪后的心电和心阻抗信号如图9所示。
4 结 语
该动态心电心阻抗监测系统可动态监测用户心电、心阻抗,能准确反映用户心脏的电学传导性能和机械泵血性能,有效减少因偶然性和突发性心脏病带来的死亡或损伤,具有广阔的应用前景。
参考文献
[1] 赵泽,王玲,潘颂欣,等.心输出量监测技术的原理及发展[J].中国生物医学工程学报, 2010,29(4):619-626.
[2] 蒋黎鹏.基于阻抗法的心功能无创检测系统[D].重庆:重庆大学, 2013.
[3] BH Brown, AJ Wilson, P Bertemes-Filho.Biomedical electronics Bipolar and tetra polar transfer impedance measurements from volume conductor[J]. Electronics Letter, 2001, 36(25): 2060-2062.
[4] Calin CORCIOVA, Dan ZAHARIA. Measuring System of Hemody-namic Parameters Using Electrical Impedance[J]. Annals of the University of Craiova, Electrical Engineering series, 2011(35).
[5] 杨建明,钟胜河,梁妃学,等.基于胸阻抗的人体肺功能参数测量方法[J].南方医科大学学报, 2013,33(9):1352-1356.
[6] 林振衡,黄元庆,杨威.心脏每搏输出量新型Kubicek模型的研究[J].厦门大学学报(自然科学版), 2008,47(5):677-680.
[7] CY Chiang, WC Hu, LY Shyu. Portable Impedance Cardiography System for Real-Time Noninvasive Cardiac Output Measurement[J]. Engineering in Medicine & Biology Society Proceedings of Annual International Conference, 1997, 5(4): 2072-2073.
[8] ADS1292R Datasheet t[Z]. Texas Instruments.
[9] BLE113 Datasheet[Z]. Bluegiga.
[10] 成清清,吴蒙.基于LabVIEW的实时心电信号采集系统的设计[J].计算机技术与发展, 2013,23(4):176-180.
